名校
1 . 下列实验目的、实验操作及现象、结论都正确的是
| 选项 | 实验目的 | 实验及现象 | 结论 |
| A | 验证肉桂醛中含碳碳双键 | 向肉桂醛(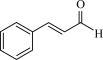 )中加入酸性KMnO4溶液 )中加入酸性KMnO4溶液 | 肉桂醛中含有碳碳双键 |
| B | 比较CuSO4和KMnO4的催化效果 | 向等体积等浓度的H2O2溶液中分别加入5滴等浓度的CuSO4溶液和KMnO4溶液,CuSO4溶液产生气泡速率快 | CuSO4催化H2O2溶液分解效果更好 |
| C | 验证菠菜中含有铁元素 | 将新鲜菠菜剪碎、研磨、溶解、过滤,向滤液中加入几滴KSCN溶液,溶液不变红 | 说明菠菜中不含铁元素 |
| D | 判断强酸和弱酸 | NaHCO3溶液显碱性,NaHSO3溶液显酸性 | 可以确定H2CO3是弱酸,无法判断H2SO3是否为弱酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-19更新
|
803次组卷
|
2卷引用:江西省赣州地区2023-2024学年十大教学能手选拔赛高中化学试题
名校
2 . 常温下, 的溶液A中含有
的溶液A中含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的四种,且溶液中各离子的浓度均为0.1
中的四种,且溶液中各离子的浓度均为0.1 。现取该溶液进行有关实验,实验结果如图所示。下列有关说法正确的是
。现取该溶液进行有关实验,实验结果如图所示。下列有关说法正确的是
 的溶液A中含有
的溶液A中含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的四种,且溶液中各离子的浓度均为0.1
中的四种,且溶液中各离子的浓度均为0.1 。现取该溶液进行有关实验,实验结果如图所示。下列有关说法正确的是
。现取该溶液进行有关实验,实验结果如图所示。下列有关说法正确的是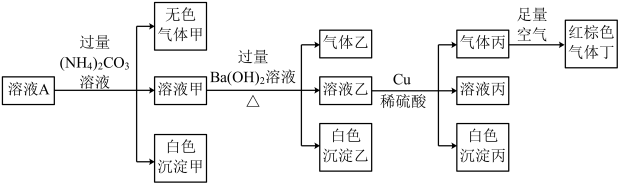
A.溶液A中一定含有 、 、 、 、 、 、 |
B.若实验消耗 14.4g,则生成气体丁的体积为3.36L 14.4g,则生成气体丁的体积为3.36L |
C.沉淀乙中一定有 ,可能有 ,可能有 |
D.溶液A中一定没有 ,但是无法确定是否含有 ,但是无法确定是否含有 |
您最近一年使用:0次
2023-02-08更新
|
241次组卷
|
17卷引用:江西省莲塘一中、临川二中2018届高三上学期第一次联考化学试题
江西省莲塘一中、临川二中2018届高三上学期第一次联考化学试题河南省豫南豫北名校2018届高三精英联赛化学试题1(已下线)黄金30题系列 高三化学 小题易丢分陕西省陕师大附中2018届高三第五次月考化学试题河南省南阳市第一中学校2018届高三第七次考试理综化学试题河北省定州中学2018届高三(承智班)下学期开学考试化学试题河南省豫南豫北名校2018届高三精英联赛化学试题2西藏自治区拉萨中学2018届高三第六次月考理综化学试题湖南省新高考联盟2021届高三下学期3月提升检测化学(A)试题安徽省名校2020-2021学年高二下学期5月第二次联考化学试题陕西省西安中学2021-2022学年高三上学期期中考试化学试题福建省龙岩第一中学2021-2022学年高三上学期第三次月考化学试题(已下线)三轮冲刺卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(辽宁专用)湖南省常德市第一中学 2023届高三7月摸底考试化学试题(已下线)易错点03 离子反应-备战2023年高考化学考试易错题(已下线)学科特色6 离子推断湖南省永州市祁阳县第四中学2023-2024学年高三上学期第三次段考化学试题
3 . 钪(Sc)及其化合物具有许多优良的性能,在宇航、电子、超导等方面有着广泛的应用。钛铁矿中含有TiO2、FeO、Fe2O3、MgO、SiO2和Sc元素,从钛铁矿中提取Sc2O3的流程如图:

下表列出了相关金属离子(离子浓度约0. 01 mol·L-1)在室温下生成氢氧化物沉淀的pH。
回答下列问题:
(1)为了提高“酸浸”的速率,可采取的措施有_______ (任写一点)。
(2)“酸浸”后Ti元素转化为TiOSO4,其水解反应的化学方程式是_______ 。
(3)“洗钛”时H2O2的作用之一是其与 TiO2+反应生成[TiO(H2O2)]2+,该离子为橘黄色的稳定离子,Ti的化合价为_______ 。 ,H2O2还起到的作用是_______ 。
(4)“酸溶”后滤液中存在的金属阳离子Sc3+、TiO2+、Fe3+浓度均约为0.01 mol·L-1,再用氨水调节溶液pH使TiO2+、Fe3+沉淀完全(当离子浓度低于10-5mol· L-1时可认为沉淀完全),而Sc3+不沉淀,则调pH应控制的范围是_______ 。{已知室温下Ksp[Sc(OH)3]=1. 25 × 10-33,lg2≈0. 3,忽略溶液体积变化}
(5)用草酸沉钪时,求在25℃、pH=2的草酸溶液中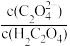 =
=_______ ,写出“沉钪”的离子方程式:_______ 。(已知25℃时,H2C2O4的Ka1=5.0 ×10-2,Ka2=5. 4×10-5)

下表列出了相关金属离子(离子浓度约0. 01 mol·L-1)在室温下生成氢氧化物沉淀的pH。
| 氢氧化物 | TiO2+ | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 1.2 | 2.1 | 6.5 |
| 沉淀完全的pH | 2.8 | 3.3 | 9.7 |
(1)为了提高“酸浸”的速率,可采取的措施有
(2)“酸浸”后Ti元素转化为TiOSO4,其水解反应的化学方程式是
(3)“洗钛”时H2O2的作用之一是其与 TiO2+反应生成[TiO(H2O2)]2+,该离子为橘黄色的稳定离子,Ti的化合价为
(4)“酸溶”后滤液中存在的金属阳离子Sc3+、TiO2+、Fe3+浓度均约为0.01 mol·L-1,再用氨水调节溶液pH使TiO2+、Fe3+沉淀完全(当离子浓度低于10-5mol· L-1时可认为沉淀完全),而Sc3+不沉淀,则调pH应控制的范围是
(5)用草酸沉钪时,求在25℃、pH=2的草酸溶液中
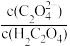 =
=
您最近一年使用:0次
4 . 25℃时,向0.10 元弱酸
元弱酸 溶液逐滴滴入NaOH溶液,溶液中的
溶液逐滴滴入NaOH溶液,溶液中的 、
、 、
、 的物质的量分数
的物质的量分数 随pH的变化如图所示[已知
随pH的变化如图所示[已知 ];
];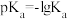 。下列叙述错误的是
。下列叙述错误的是

 元弱酸
元弱酸 溶液逐滴滴入NaOH溶液,溶液中的
溶液逐滴滴入NaOH溶液,溶液中的 、
、 、
、 的物质的量分数
的物质的量分数 随pH的变化如图所示[已知
随pH的变化如图所示[已知 ];
];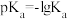 。下列叙述错误的是
。下列叙述错误的是
A. , , |
B. 时, 时,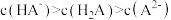 |
C.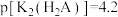 |
D. 时, 时,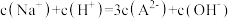 |
您最近一年使用:0次
2021-11-08更新
|
746次组卷
|
5卷引用:江西省新余市第一中学2021-2022学年高三上学期第二次模拟考试化学试题
名校
5 . 下列说法正确的是
| A.常温下反应2Na2SO3(s)+O2(g)=2Na2SO4(s),能自发进行,则△H>0 |
| B.Al2(SO4)3溶液蒸干所得固体产物为Al(OH)3 |
| C.已知工业上常用NH4Cl溶液给金属除锈,则温度降低会使除锈效果减弱 |
| D.pH相同的盐酸和醋酸溶液与足量锌粒反应,产生相同质量的H2,则盐酸溶液的体积小于醋酸溶液的体积 |
您最近一年使用:0次
2021-09-23更新
|
502次组卷
|
4卷引用:江西省吉安市第一中学2021-2022学年高二上学期期中考试(理科)化学试题
解题方法
6 . 为测定某氟化稀土样品中氟元素的质量分数,某化学兴趣小组进行了如下实验。利用高氯酸(高沸点酸)将样品中的氟元素转化为氟化氢(低沸点酸)蒸出,再进行吸收滴定来测定含量。实验装置如图所示。
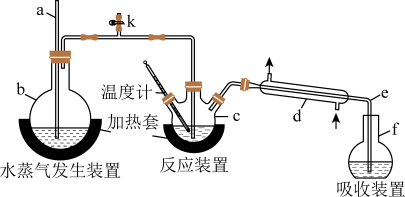
(1)装置c的名称是___________ 。玻璃管a的作用为___________ 。
(2)实验步骤:①连接好实验装置,检查装置气密性;②往c中加入mg氟化稀土样品和 一定体积的高氯酸,f中盛有滴加酚酞的NaOH溶液。加热装置b、c。
①下列物质可代替高氯酸的是___________ 。(填序号)。
A.硫酸B.盐酸C.硝酸D.磷酸
②水蒸气发生装置b的作用是___________ 。
(3)定量测定:将f中得到的馏出液配成100mL溶液,取其中20mL加入V1mL amol·L-1La(NO3)3溶液,得到LaF3沉淀(不考虑其他沉淀的生成),再用cmol·L-1EDTA 标准溶液滴定剩余La3+(La+与 EDTA 按1:1配合),消耗 EDTA 标准溶液 V2mL,则氟化稀土样品中氟的质量分数为___________ 。
(4)问题讨论:
若观察到f中溶液红色褪去,可采用最简单的补救措施是:___________ 。否则会使实验结果偏低。实验中除有HF 气体外,可能还有少量 SiF4(易水解)气体生成。若有SiF4生成,实验结果将_____ 。(填“偏高”“偏低”或“不受影响”)。理由是_____ 。

(1)装置c的名称是
(2)实验步骤:①连接好实验装置,检查装置气密性;②往c中加入mg氟化稀土样品和 一定体积的高氯酸,f中盛有滴加酚酞的NaOH溶液。加热装置b、c。
①下列物质可代替高氯酸的是
A.硫酸B.盐酸C.硝酸D.磷酸
②水蒸气发生装置b的作用是
(3)定量测定:将f中得到的馏出液配成100mL溶液,取其中20mL加入V1mL amol·L-1La(NO3)3溶液,得到LaF3沉淀(不考虑其他沉淀的生成),再用cmol·L-1EDTA 标准溶液滴定剩余La3+(La+与 EDTA 按1:1配合),消耗 EDTA 标准溶液 V2mL,则氟化稀土样品中氟的质量分数为
(4)问题讨论:
若观察到f中溶液红色褪去,可采用最简单的补救措施是:
您最近一年使用:0次
名校
7 . 把下列物质的水溶液加热蒸干后,能得到原溶质的是( )
| A.NaHCO3 | B.AlCl3 | C.NH4HCO3 | D.Fe2(SO4)3 |
您最近一年使用:0次
2021-01-07更新
|
366次组卷
|
3卷引用:江西省新干中学2022-2023学年高三第一次模考化学试题
江西省新干中学2022-2023学年高三第一次模考化学试题陕西省咸阳市实验中学2020-2021学年高二上学期第四次月考化学试题(已下线)第32练 盐类的水解-2023年高考化学一轮复习小题多维练(全国通用)
名校
8 . 在蒸发皿中加热蒸干并灼烧(低于400℃)下列物质的溶液,可以得到该物质固体的是
① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥
①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥
| A.①⑥ | B.②⑤ | C.③④ | D.③⑤ |
您最近一年使用:0次
2020-10-06更新
|
384次组卷
|
2卷引用:江西省吉安县立中学2020-2021学年高二上学期12月月考化学(B班)试题
19-20高二上·江西南昌·阶段练习
解题方法
9 . NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其理由是____ (用必要的化学用语和相关文字说明)。
(2)如图是0.1mol·L-1电解质溶液的pH随温度变化的图象:

①中符合0.1 mol·L-1NH4Al(SO4)2的pH随温度变化的曲线是___ (填写字母)。
②20℃时,0.1mol/L NH4Al(SO4)2中2c(SO4 2−)−c(NH4+)−3c(Al3+)=___ 。
(3)室温时,向100mL 0.1mol/L NH4HSO4溶液中滴加0.1mol/L NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:

试分析图中a、b、c、d四个点,水的电离程度最大的是___ ;在b点,溶液中各离子浓度由大到小的排列顺序是___ 。
(1)NH4Al(SO4)2可作净水剂,其理由是
(2)如图是0.1mol·L-1电解质溶液的pH随温度变化的图象:

①中符合0.1 mol·L-1NH4Al(SO4)2的pH随温度变化的曲线是
②20℃时,0.1mol/L NH4Al(SO4)2中2c(SO4 2−)−c(NH4+)−3c(Al3+)=
(3)室温时,向100mL 0.1mol/L NH4HSO4溶液中滴加0.1mol/L NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:

试分析图中a、b、c、d四个点,水的电离程度最大的是
您最近一年使用:0次
名校
10 . 等物质的量浓度、等体积的下列溶液中(1)H2CO3 (2)Na2CO3 (3)NaHCO3 (4)NH4HCO3 (5)(NH4)2CO3。下列关系或者说法正确的是( )
| A.c(HCO3-)的大小关系为:(4)>(3)>(5)>(2)>(1) |
| B.c(CO32-)的大小关系为:(1)<(4)<(3)<(5)<(2) |
| C.将溶液蒸干后灼烧后只有(1)不能得到对应的固体物质 |
| D.(2)(3)(4)(5)既能与盐酸反应,又能与NaOH溶液反应 |
您最近一年使用:0次
2019-11-24更新
|
338次组卷
|
12卷引用:江西省吉安市省重点中学2020-2021学年高二上学期期中联合考试化学试题
江西省吉安市省重点中学2020-2021学年高二上学期期中联合考试化学试题江西省吉安市2020-2021学年高二上学期期中统考化学试题2016届河北省行唐启明中学高三上学期12月月考化学试卷2017届河北省定州中学高三上学期第二次月考化学卷2016-2017学年吉林省长春市第十一高中高二上学期期初考试化学试卷2016-2017学年河北省邢台一中高二上月考二化学卷2016-2017学年山东省桓台二中高二上学期期中化学试卷苏教版高三单元精练检测八化学试题福建省闽侯第六中学2017-2018学年高二12月月考化学试题山东省枣庄市第八中学南校区2017-2018学年高二上学期第二次月考(12月)化学试题河南省鲁山县第一高级中学2019-2020学年高二11月月考化学试题第3课时 溶液中粒子浓度的大小比较



