名校
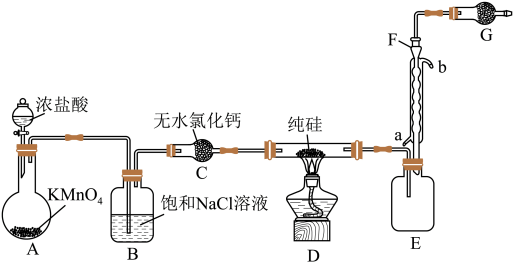
1 . 2023年9月华为推出了举世瞩目的“中国芯”——麒麟芯。“中国芯”的发展离不开单晶硅,四氯化硅是制备高纯硅的原料。某小组拟在实验室用下列装置模拟探究四氯化硅的制备和应用(夹持装置已省略)。
① ,
,
② 遇水剧烈水解,
遇水剧烈水解, 的熔点、沸点分别为―70.0℃、57.7℃。
的熔点、沸点分别为―70.0℃、57.7℃。
③电负性Cl>H>Si, 的沸点为31.8℃,熔点为―126.5℃,在空气中易自燃,遇水会剧烈反应。
的沸点为31.8℃,熔点为―126.5℃,在空气中易自燃,遇水会剧烈反应。
请回答下列问题:
(1)写出A中发生反应的离子方程式:______ 。
(2)装置B的作用是______ 。
(3)仪器F的名称是______ ,冷却水应从______ (填“a”或“b”)口通入。
(4)有同学设计如图装置H、I替代上述E、G装置;______ 。
(5)测定产品纯度。取mg 产品溶于足量蒸馏水中(生成的HCl全部被水吸收),将混合物转入锥形瓶中,滴加甲基橙溶液,用
产品溶于足量蒸馏水中(生成的HCl全部被水吸收),将混合物转入锥形瓶中,滴加甲基橙溶液,用 标准NaOH溶液滴定至终点(终点时硅酸未参加反应),消耗滴定液VmL。则产品的纯度为
标准NaOH溶液滴定至终点(终点时硅酸未参加反应),消耗滴定液VmL。则产品的纯度为______ %(用含m、c和V的代数式表示)。若产品中溶有少量 ,则测定结果
,则测定结果______ (填“偏高”、“偏低”或“无影响”)
(6) 也是制备高纯硅的重要原料,将其通入浓NaOH溶液中,发生反应的化学方程式为
也是制备高纯硅的重要原料,将其通入浓NaOH溶液中,发生反应的化学方程式为______ 。
①
 ,
,
②
 遇水剧烈水解,
遇水剧烈水解, 的熔点、沸点分别为―70.0℃、57.7℃。
的熔点、沸点分别为―70.0℃、57.7℃。③电负性Cl>H>Si,
 的沸点为31.8℃,熔点为―126.5℃,在空气中易自燃,遇水会剧烈反应。
的沸点为31.8℃,熔点为―126.5℃,在空气中易自燃,遇水会剧烈反应。请回答下列问题:
(1)写出A中发生反应的离子方程式:
(2)装置B的作用是
(3)仪器F的名称是
(4)有同学设计如图装置H、I替代上述E、G装置;
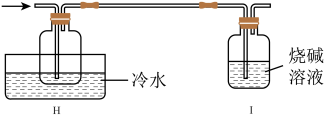
(5)测定产品纯度。取mg
 产品溶于足量蒸馏水中(生成的HCl全部被水吸收),将混合物转入锥形瓶中,滴加甲基橙溶液,用
产品溶于足量蒸馏水中(生成的HCl全部被水吸收),将混合物转入锥形瓶中,滴加甲基橙溶液,用 标准NaOH溶液滴定至终点(终点时硅酸未参加反应),消耗滴定液VmL。则产品的纯度为
标准NaOH溶液滴定至终点(终点时硅酸未参加反应),消耗滴定液VmL。则产品的纯度为 ,则测定结果
,则测定结果(6)
 也是制备高纯硅的重要原料,将其通入浓NaOH溶液中,发生反应的化学方程式为
也是制备高纯硅的重要原料,将其通入浓NaOH溶液中,发生反应的化学方程式为
您最近一年使用:0次
2024-04-19更新
|
217次组卷
|
2卷引用:河南省漯河市高级中学2023-2024学年高三下学期4月月考化学试题
名校
解题方法
2 . 已知液氨的电离类似水的电离,碳酸钠在液氨中完全电离并发生类似水解的氨解。肼( )为二元弱碱,在水中的电离方程式与氨相似。下列说法错误的是
)为二元弱碱,在水中的电离方程式与氨相似。下列说法错误的是
 )为二元弱碱,在水中的电离方程式与氨相似。下列说法错误的是
)为二元弱碱,在水中的电离方程式与氨相似。下列说法错误的是A.元素的电负性: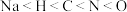 |
B.肼在水中第一步电离的方程式为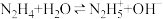 |
C.肼与硫酸反应生成的酸式盐中阳离子的电子式为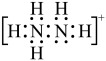 |
D.碳酸钠在液氨中第一步氨解的离子方程式为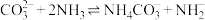 |
您最近一年使用:0次
名校
3 . 镍常作催化剂。以镍废料(主要成分为Ni,含 、NiO、FeO、CaO和
、NiO、FeO、CaO和 )为原料制备纯镍的流程如图所示:
)为原料制备纯镍的流程如图所示:
(1)“酸浸”得到滤渣1的主要成分是 和
和__________ (填化学式)。“酸浸”中镍浸出率与硫酸浓度的关系如图所示。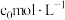 时,镍浸出率降低的可能原因是
时,镍浸出率降低的可能原因是_____________________ (答一条)。
(2)“氧化”中双氧水的作用是______________________ (用离子方程式表示)。
(3)“沉铝”中NiO的作用是________________________________________ 。
(4) 在隔绝空气条件下的热失重曲线如图所示。
在隔绝空气条件下的热失重曲线如图所示。________________________ ,c点对应的氧化物为____________ (填化学式)。
(5)Ni和Nb可组成一种合金材料,其晶胞结构如图所示。 代表阿伏加德罗常数的值,
代表阿伏加德罗常数的值,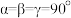 ,该晶胞中Ni、Nb的个数之比为
,该晶胞中Ni、Nb的个数之比为_____________ 。该晶体的密度为_________  (用含a、b、
(用含a、b、 的代数式表示)。
的代数式表示)。
 、NiO、FeO、CaO和
、NiO、FeO、CaO和 )为原料制备纯镍的流程如图所示:
)为原料制备纯镍的流程如图所示: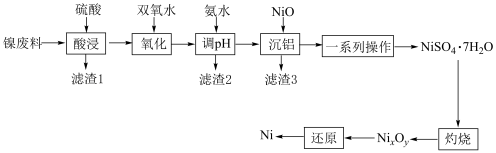
(1)“酸浸”得到滤渣1的主要成分是
 和
和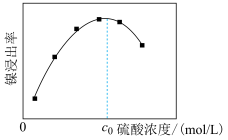
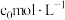 时,镍浸出率降低的可能原因是
时,镍浸出率降低的可能原因是(2)“氧化”中双氧水的作用是
(3)“沉铝”中NiO的作用是
(4)
 在隔绝空气条件下的热失重曲线如图所示。
在隔绝空气条件下的热失重曲线如图所示。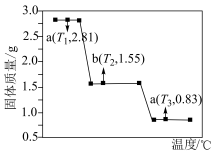
(5)Ni和Nb可组成一种合金材料,其晶胞结构如图所示。
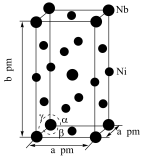
 代表阿伏加德罗常数的值,
代表阿伏加德罗常数的值,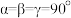 ,该晶胞中Ni、Nb的个数之比为
,该晶胞中Ni、Nb的个数之比为 (用含a、b、
(用含a、b、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
解题方法
4 . 下列图像及对图像的分析结果均正确的是


A.图一中A点应当填写 |
B.图二表示不同温度下发生反应  。实验Ⅱ相比实验Ⅰ、Ⅲ,除温度不同外还可能使用了催化剂 。实验Ⅱ相比实验Ⅰ、Ⅲ,除温度不同外还可能使用了催化剂 |
C.图三为 固体放入水中后,t时刻改变的条件是向溶液中加入KI固体, 固体放入水中后,t时刻改变的条件是向溶液中加入KI固体, 的 的 增大 增大 |
D.图四纵坐标为各粒子分布系数,将均为 的 的 和 和 固体混合物溶于1L水中,所得溶液pH为4.2 固体混合物溶于1L水中,所得溶液pH为4.2 |
您最近一年使用:0次
2023-12-12更新
|
413次组卷
|
2卷引用:辽宁省实验中学2023-2024学年高二上学期第二次月考化学试题
名校
5 . 下列装置(部分夹持仪器省略)能达到实验目的的是
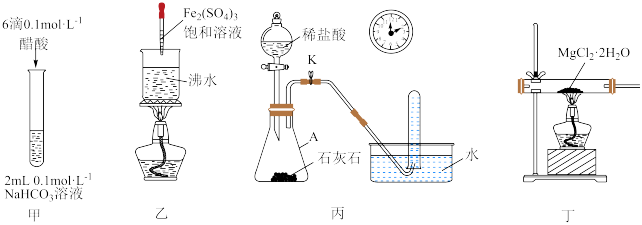

A.用装置甲比较相同温度下醋酸与碳酸的 大小 大小 | B.用装置乙制备 胶体 胶体 |
| C.用装置丙测定石灰石与盐酸反应的速率 | D.用装置丁制取无水 |
您最近一年使用:0次
2023-12-03更新
|
209次组卷
|
2卷引用:山东省新泰市第一中学东校2023-2024学年高二上学期第二次月考化学试题
名校
6 . 某含铬废水中含有一定浓度的 ,同时还含有少量的
,同时还含有少量的 杂质,某研究小组为消除废水污染同时获得
杂质,某研究小组为消除废水污染同时获得 (铬绿),设计如下流程:
(铬绿),设计如下流程:

已知:在酸性环境中 的氧化性强于
的氧化性强于 。
。
(1)“滤渣”的主要成分为___________ (写化学式)。
(2)已知“酸化”调节pH时, 转化为
转化为 。
。
①下列溶液中可以代替“还原”过程中 溶液的是
溶液的是___________ (填标号)。
A.淀粉水解液 B.浓硫酸 C. 溶液 D.
溶液 D. 溶液
溶液
②“还原”步骤中,先加入硫酸酸化,再加入 溶液。若不加
溶液。若不加 酸化,可能造成的后果是
酸化,可能造成的后果是___________ ;若每消耗0.1mol  转移0.4mol
转移0.4mol  ,则加入
,则加入 时发生反应的离子方程式为
时发生反应的离子方程式为___________ 。
(3)已知室温条件下,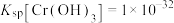 。若“沉铬”后滤液中
。若“沉铬”后滤液中 恰好完全沉淀[
恰好完全沉淀[
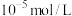 ],则此时溶液的pH=
],则此时溶液的pH=___________ 。
(4)“沉铬”过程所用浓氨水也可换用浓碳酸钠溶液,此时除得到 外,还会有大量气泡生成,试写出反应的离子方程式:
外,还会有大量气泡生成,试写出反应的离子方程式:___________ 。
(5)“滤液”中的 也可利用电解法直接被还原为
也可利用电解法直接被还原为 ,装置如图所示。则该装置的阳极区产生的离子与
,装置如图所示。则该装置的阳极区产生的离子与 反应的离子方程式为
反应的离子方程式为___________ 。

 ,同时还含有少量的
,同时还含有少量的 杂质,某研究小组为消除废水污染同时获得
杂质,某研究小组为消除废水污染同时获得 (铬绿),设计如下流程:
(铬绿),设计如下流程:
已知:在酸性环境中
 的氧化性强于
的氧化性强于 。
。(1)“滤渣”的主要成分为
(2)已知“酸化”调节pH时,
 转化为
转化为 。
。①下列溶液中可以代替“还原”过程中
 溶液的是
溶液的是A.淀粉水解液 B.浓硫酸 C.
 溶液 D.
溶液 D. 溶液
溶液②“还原”步骤中,先加入硫酸酸化,再加入
 溶液。若不加
溶液。若不加 酸化,可能造成的后果是
酸化,可能造成的后果是 转移0.4mol
转移0.4mol  ,则加入
,则加入 时发生反应的离子方程式为
时发生反应的离子方程式为(3)已知室温条件下,
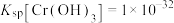 。若“沉铬”后滤液中
。若“沉铬”后滤液中 恰好完全沉淀[
恰好完全沉淀[
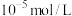 ],则此时溶液的pH=
],则此时溶液的pH=(4)“沉铬”过程所用浓氨水也可换用浓碳酸钠溶液,此时除得到
 外,还会有大量气泡生成,试写出反应的离子方程式:
外,还会有大量气泡生成,试写出反应的离子方程式:(5)“滤液”中的
 也可利用电解法直接被还原为
也可利用电解法直接被还原为 ,装置如图所示。则该装置的阳极区产生的离子与
,装置如图所示。则该装置的阳极区产生的离子与 反应的离子方程式为
反应的离子方程式为
您最近一年使用:0次
2023-11-08更新
|
256次组卷
|
3卷引用:四川省南充市白塔中学2023-2024学年高三上学期第五次考试理科综合试题
名校
7 . 某化学实验小组设计如下实验探究Zn与溶液中Fe3+发生反应的原理。
下列说法错误的是
| 实验 | 试剂 | 现象 |
| I | 2 mL0.1 mol· L-1FeCl3溶液、过量锌粉 | 黄色溶液很快变浅,接着有无色气泡产生,固体中未检出铁单质 |
| Ⅱ | 2 mL1 mol· L-1FeCl3溶液(pH≈0.70)、过量锌粉 | 很快有大量气体产生,出现红褐色浑浊,30 min左右产生红褐色沉淀,溶液颜色变浅,产生少量铁单质 |
| A.实验I说明Fe3+被还原为Fe2+ |
| B.可用酸性高锰酸钾溶液检验实验I得到的溶液中含有Fe2+ |
| C.实验Ⅱ发生了置换反应和复分解反应 |
| D.实验说明Fe3+、H+与Zn的反应与离子浓度有关 |
您最近一年使用:0次
2023-05-23更新
|
1502次组卷
|
11卷引用:辽宁省沈阳市第一二〇中学2023-2024学年高三上学期第一次质量检测化学试题
辽宁省沈阳市第一二〇中学2023-2024学年高三上学期第一次质量检测化学试题吉林省松原市前郭尔罗斯蒙古族自治县第五高级中学(前郭五中)2023-2024学年高三上学期第三次考试 化学试卷 河南省安阳市2023届高三下学期第三次模拟考试理科综合化学试题(已下线)【知识图鉴】单元讲练测必修第一册第三单元02基础练(已下线)第6讲 铁及其重要化合物(已下线)考点14 铁及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题06 元素及其化合物 -2023年高考化学真题题源解密(新高考专用)(已下线)选择题6-10(已下线)热点19 化学微型实验(已下线)2023-2024学年度第二学期高三化学零模试卷北京市师范大学附属实验中学2024届高三零模化学试题
名校
8 . 硫化硅分子式为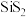 ,遇水会发生水解。下列推测
,遇水会发生水解。下列推测不合理 的是
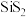 ,遇水会发生水解。下列推测
,遇水会发生水解。下列推测A.与硫化钠作用可生成 |
B.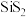 在空气中可以被点燃 在空气中可以被点燃 |
C.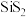 的空间结构名称为V形 的空间结构名称为V形 |
D.水解产物可能为 和 和 |
您最近一年使用:0次
2023-04-21更新
|
378次组卷
|
4卷引用:河南省南阳市第一中学校2022-2023学年高二下学期5月月考化学试题
河南省南阳市第一中学校2022-2023学年高二下学期5月月考化学试题浙江省9+1联盟2022-2023学年高二下学期期中考试化学试题(已下线)【2023】【高二下】【期中考】【9+1联盟】【高中化学】【洪翔峰收集】(已下线)实验05 盐类水解的应用-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)
名校
解题方法
9 . 下列离子能大量存在于指定溶液中的是
A.某中性溶液中: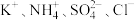 |
B.能使Al粉转化为 的溶液: 的溶液: |
C.能使pH试纸变深蓝色的溶液: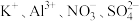 |
D.遇KSCN显红色的溶液: |
您最近一年使用:0次
名校
10 . 常温下, 的溶液A中含有
的溶液A中含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的四种,且溶液中各离子的浓度均为0.1
中的四种,且溶液中各离子的浓度均为0.1 。现取该溶液进行有关实验,实验结果如图所示。下列有关说法正确的是
。现取该溶液进行有关实验,实验结果如图所示。下列有关说法正确的是
 的溶液A中含有
的溶液A中含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的四种,且溶液中各离子的浓度均为0.1
中的四种,且溶液中各离子的浓度均为0.1 。现取该溶液进行有关实验,实验结果如图所示。下列有关说法正确的是
。现取该溶液进行有关实验,实验结果如图所示。下列有关说法正确的是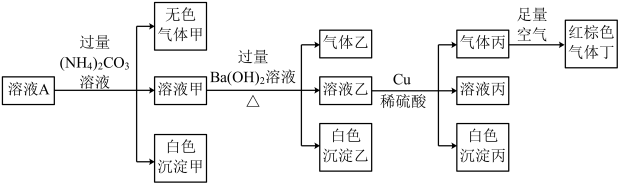
A.溶液A中一定含有 、 、 、 、 、 、 |
B.若实验消耗 14.4g,则生成气体丁的体积为3.36L 14.4g,则生成气体丁的体积为3.36L |
C.沉淀乙中一定有 ,可能有 ,可能有 |
D.溶液A中一定没有 ,但是无法确定是否含有 ,但是无法确定是否含有 |
您最近一年使用:0次
2023-02-08更新
|
241次组卷
|
17卷引用:陕西省陕师大附中2018届高三第五次月考化学试题
陕西省陕师大附中2018届高三第五次月考化学试题西藏自治区拉萨中学2018届高三第六次月考理综化学试题湖南省新高考联盟2021届高三下学期3月提升检测化学(A)试题安徽省名校2020-2021学年高二下学期5月第二次联考化学试题福建省龙岩第一中学2021-2022学年高三上学期第三次月考化学试题湖南省永州市祁阳县第四中学2023-2024学年高三上学期第三次段考化学试题河南省豫南豫北名校2018届高三精英联赛化学试题1江西省莲塘一中、临川二中2018届高三上学期第一次联考化学试题(已下线)黄金30题系列 高三化学 小题易丢分河南省南阳市第一中学校2018届高三第七次考试理综化学试题河北省定州中学2018届高三(承智班)下学期开学考试化学试题河南省豫南豫北名校2018届高三精英联赛化学试题2陕西省西安中学2021-2022学年高三上学期期中考试化学试题(已下线)三轮冲刺卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(辽宁专用)湖南省常德市第一中学 2023届高三7月摸底考试化学试题(已下线)易错点03 离子反应-备战2023年高考化学考试易错题(已下线)学科特色6 离子推断



