名校
解题方法
1 . 水体中的六价铬[Cr(Ⅵ)]对生态环境和人体健康威胁很大。工业废水中[Cr(Ⅵ)]常用还原沉淀法、微生物法等进行处理。
(1)“还原沉淀法”常用Na2SO3、FeSO4等处理Cr(Ⅵ)得到Cr(Ⅲ)。已知溶液中含Cr(Ⅵ)的微粒(H2CrO4、Cr2O 和CrO
和CrO )的物质的量分数随pH的关系如图所示。
)的物质的量分数随pH的关系如图所示。
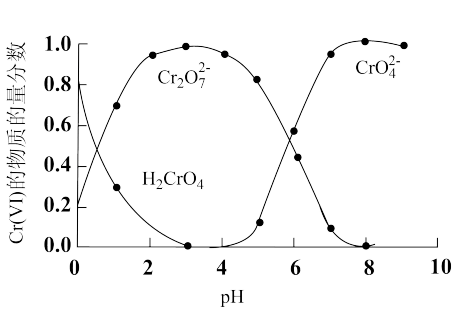
①某含Cr(Ⅵ)废水的pH约为8,写出用Na2SO3处理该废水的主要离子方程式:_______ 。[已知pH=3时,Cr(Ⅲ)以Cr3+形式存在,pH=7.5时,Cr(Ⅲ)开始沉淀]。
②其他条件相同,用Na2SO3处理不同pH含Cr(Ⅵ)的废水,反应相同时间,Cr(Ⅵ)的去除率与pH的关系如图所示。已知酸性条件下Cr(Ⅵ)对Na2SO3具有很强的氧化能力,pH<2时,Cr(Ⅵ)的去除率随pH降低而降低的原因是_______ 。
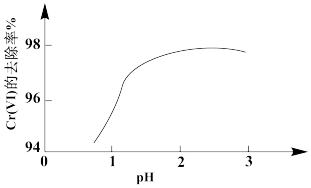
③研究发现,用FeSO4处理pH=3的含Cr(Ⅵ)废水,Cr(Ⅵ)的去除率大于其被FeSO4还原的理论值。Cr(Ⅵ)的去除率大于理论值的原因是_______ 。
(2)“微生物法”处理含Cr(Ⅵ)废水具有效率高、选择性强、吸附容量大等优点。一种微生物法是用硫酸盐还原菌(SRB)处理含Cr(Ⅵ)废水。
①硫酸盐还原菌能将水中的SO 转化为S2-,S2-与CrO
转化为S2-,S2-与CrO 可反应生成Cr2S3和S两种沉淀。写出S2-与CrO
可反应生成Cr2S3和S两种沉淀。写出S2-与CrO 反应的离子方程式:
反应的离子方程式:_______ 。
②用硫酸盐还原菌(SRB)处理含铬废水时,温度常控制在30℃左右,温度过高,Cr(Ⅵ)的去除率低的原因是_______ 。
③硫酸盐还原菌(SRB)常存在于水体中,会腐蚀许多金属及合金。一种Fe合金在硫酸盐还原菌存在条件下腐蚀的机理如图所示。已知溶液中的S2-会完全转化为FeS,则Fe腐蚀后生成Fe(OH)2和FeS的物质的量之比为_______ 。

(1)“还原沉淀法”常用Na2SO3、FeSO4等处理Cr(Ⅵ)得到Cr(Ⅲ)。已知溶液中含Cr(Ⅵ)的微粒(H2CrO4、Cr2O
 和CrO
和CrO )的物质的量分数随pH的关系如图所示。
)的物质的量分数随pH的关系如图所示。
①某含Cr(Ⅵ)废水的pH约为8,写出用Na2SO3处理该废水的主要离子方程式:
②其他条件相同,用Na2SO3处理不同pH含Cr(Ⅵ)的废水,反应相同时间,Cr(Ⅵ)的去除率与pH的关系如图所示。已知酸性条件下Cr(Ⅵ)对Na2SO3具有很强的氧化能力,pH<2时,Cr(Ⅵ)的去除率随pH降低而降低的原因是

③研究发现,用FeSO4处理pH=3的含Cr(Ⅵ)废水,Cr(Ⅵ)的去除率大于其被FeSO4还原的理论值。Cr(Ⅵ)的去除率大于理论值的原因是
(2)“微生物法”处理含Cr(Ⅵ)废水具有效率高、选择性强、吸附容量大等优点。一种微生物法是用硫酸盐还原菌(SRB)处理含Cr(Ⅵ)废水。
①硫酸盐还原菌能将水中的SO
 转化为S2-,S2-与CrO
转化为S2-,S2-与CrO 可反应生成Cr2S3和S两种沉淀。写出S2-与CrO
可反应生成Cr2S3和S两种沉淀。写出S2-与CrO 反应的离子方程式:
反应的离子方程式:②用硫酸盐还原菌(SRB)处理含铬废水时,温度常控制在30℃左右,温度过高,Cr(Ⅵ)的去除率低的原因是
③硫酸盐还原菌(SRB)常存在于水体中,会腐蚀许多金属及合金。一种Fe合金在硫酸盐还原菌存在条件下腐蚀的机理如图所示。已知溶液中的S2-会完全转化为FeS,则Fe腐蚀后生成Fe(OH)2和FeS的物质的量之比为

您最近一年使用:0次
2022-04-19更新
|
372次组卷
|
5卷引用:江苏省泰州中学2022-2023学年高二下学期期中考试化学试题
名校
解题方法
2 . 高炉炼铁的反应为 Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH=-23.5 kJ·mol-1。下列有关说法正确的是
| A.该反应一定能自发进行,则该反应的ΔS>0 |
| B.升高温度使反应物活化分子数增多,能提高反应速率和CO平衡转化率 |
| C.增加炼铁炉高度,延长CO和铁矿石接触时间,能降低平衡时尾气中CO的体积分数 |
| D.制备的生铁中含少量FexC,相同条件下与酸反应放出氢气的速率比纯铁慢 |
您最近一年使用:0次
2022-03-20更新
|
464次组卷
|
5卷引用:江苏省泰州中学2022-2023学年高三上学期期初调研考试 化学试题
江苏省泰州中学2022-2023学年高三上学期期初调研考试 化学试题(已下线)黄金卷6-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(江苏卷)(已下线)第21讲 化学平衡状态 化学平衡的移动(练)-2023年高考化学一轮复习讲练测(全国通用)江苏省扬州市江都区邵伯高级中学2022-2023学年高三10月阶段性测试化学试题(已下线)化学(江苏B卷)-学易金卷:2023年高考第一次模拟考试卷
解题方法
3 . 铁的硫化物被认为是有前景的锂电池材料,但导电性较差,放电时易膨胀。
(1)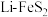 电池是综合性能较好的一种电池。
电池是综合性能较好的一种电池。
①水热法合成 纳米颗粒的方法是将等物质的量的
纳米颗粒的方法是将等物质的量的 、
、 、
、 研磨置于反应釜中,加入蒸馏水加热使之恰好反应,该反应的化学方程式为
研磨置于反应釜中,加入蒸馏水加热使之恰好反应,该反应的化学方程式为___________ 。
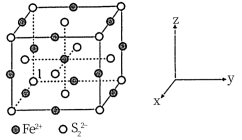
② 晶体的晶胞结构示意图如图所示,离子1的分数坐标是
晶体的晶胞结构示意图如图所示,离子1的分数坐标是 ,则离子1最近的
,则离子1最近的 分数坐标为
分数坐标为___________ (任写一个),每个 周围距离最近且相等的
周围距离最近且相等的 有
有___________ 个。
(2)①将 镶嵌在多孔碳中制成多孔碳/
镶嵌在多孔碳中制成多孔碳/ 复合材料,该电极材料相较
复合材料,该电极材料相较 具有的优势是放电时不易膨胀且
具有的优势是放电时不易膨胀且___________ 。多孔碳/ 复合材料制取方法如下,定性滤纸的作用是提供碳源和
复合材料制取方法如下,定性滤纸的作用是提供碳源和___________ 。
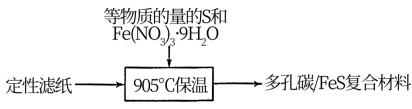
②分别取多孔碳、多孔碳/ 电极在氧气中加热,测得固体残留率随温度变化情况如图所示,多孔碳/
电极在氧气中加热,测得固体残留率随温度变化情况如图所示,多孔碳/ 最终转化为
最终转化为 ,固体残留率为50%。
,固体残留率为50%。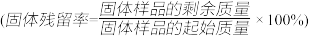
420℃~569℃时,多孔碳/ 固体残留率增大的原因是
固体残留率增大的原因是___________ 。
③ 做为锂电池正极材料,放电时先后发生如下反应:
做为锂电池正极材料,放电时先后发生如下反应: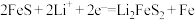
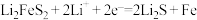
该多孔碳/ 电极质量为4.8g,该电极理论上最多可以得电子
电极质量为4.8g,该电极理论上最多可以得电子___________  。(写出计算过程)
。(写出计算过程)
(1)
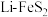 电池是综合性能较好的一种电池。
电池是综合性能较好的一种电池。①水热法合成
 纳米颗粒的方法是将等物质的量的
纳米颗粒的方法是将等物质的量的 、
、 、
、 研磨置于反应釜中,加入蒸馏水加热使之恰好反应,该反应的化学方程式为
研磨置于反应釜中,加入蒸馏水加热使之恰好反应,该反应的化学方程式为②
 晶体的晶胞结构示意图如图所示,离子1的分数坐标是
晶体的晶胞结构示意图如图所示,离子1的分数坐标是 ,则离子1最近的
,则离子1最近的 分数坐标为
分数坐标为 周围距离最近且相等的
周围距离最近且相等的 有
有
(2)①将
 镶嵌在多孔碳中制成多孔碳/
镶嵌在多孔碳中制成多孔碳/ 复合材料,该电极材料相较
复合材料,该电极材料相较 具有的优势是放电时不易膨胀且
具有的优势是放电时不易膨胀且 复合材料制取方法如下,定性滤纸的作用是提供碳源和
复合材料制取方法如下,定性滤纸的作用是提供碳源和
②分别取多孔碳、多孔碳/
 电极在氧气中加热,测得固体残留率随温度变化情况如图所示,多孔碳/
电极在氧气中加热,测得固体残留率随温度变化情况如图所示,多孔碳/ 最终转化为
最终转化为 ,固体残留率为50%。
,固体残留率为50%。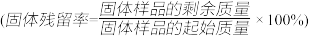

420℃~569℃时,多孔碳/
 固体残留率增大的原因是
固体残留率增大的原因是③
 做为锂电池正极材料,放电时先后发生如下反应:
做为锂电池正极材料,放电时先后发生如下反应: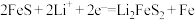
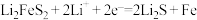
该多孔碳/
 电极质量为4.8g,该电极理论上最多可以得电子
电极质量为4.8g,该电极理论上最多可以得电子 。(写出计算过程)
。(写出计算过程)
您最近一年使用:0次
名校
4 . 三元电池成为2019年我国电动汽车的新能源,其充电时总反应为:LiNixCoyMnzO2+6C(石墨)=Li1-aNixCoyMnzO2+LiaC6,其电池工作原理如图所示,两极之间有一个允许特定的离子X通过的隔膜。下列说法正确的是


| A.允许离子X通过的隔膜属于阴离子交换膜 |
| B.充电时,A为阴极,Li+被氧化 |
| C.可从无法充电的废旧电池的石墨电极中回收金属锂 |
| D.放电时,正极反应式为Li1-aNixCoyMnzO2+aLi++ae-=LiNixCoyMnzO2 |
您最近一年使用:0次
2020-12-30更新
|
185次组卷
|
2卷引用:江苏省泰州中学2020-2021学年高二上学期期中考试化学试题
解题方法
5 . 资料显示: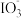 在酸性溶液中能氧化I-,反应为
在酸性溶液中能氧化I-,反应为 +5I-+6H+=3I2+3H2O。为探究Na2SO3溶液和KIO3溶液的反应,甲同学向过量的KIO3酸性溶液中加入Na2SO3溶液,并加入两滴淀粉溶液:开始时无明显现象,t秒后溶液突然变为蓝色。
+5I-+6H+=3I2+3H2O。为探究Na2SO3溶液和KIO3溶液的反应,甲同学向过量的KIO3酸性溶液中加入Na2SO3溶液,并加入两滴淀粉溶液:开始时无明显现象,t秒后溶液突然变为蓝色。
(1)甲同学对这一现象做出如下假设:t秒前生成了I2,但由于存在Na2SO3,I2被消耗,该反应的离子方程式为________ , 的还原性
的还原性________ I-(填“>”“=”或“<”)。
(2)为验证他的猜想,甲同学向反应后的蓝色溶液中加入________ ,蓝色迅速消失,随后再次变蓝。
(3)甲同学设计了如下实验,进一步研究Na2SO3溶液和KIO3溶液反应的过程。
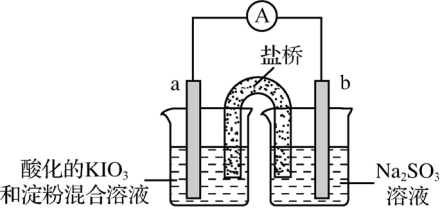
①甲同学在b电极附近的溶液中检测出了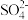
②刚开始放电时,a电极附近溶液未变蓝;取出a电极附近溶液于试管中,溶液变蓝。 在a极放电的产物是
在a极放电的产物是________ 。
③放电一段时间后,a电极附近溶液短暂出现蓝色,随即消失,重复多次后,蓝色不再褪去。电流表显示电路中时而出现电流,时而归零,最终电流消失。电流表短暂归零的原因是________ 。
④下列说法正确的是________ 。
a. a电极附近蓝色不再褪去时, 尚未完全氧化
尚未完全氧化
b. a电极附近短暂出现蓝色,随即消失的原因可能是因为I2被 还原
还原
c. 电流消失后,向b电极附近加入过量Na2SO3溶液,重新产生电流,a电极附近蓝色褪去
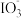 在酸性溶液中能氧化I-,反应为
在酸性溶液中能氧化I-,反应为 +5I-+6H+=3I2+3H2O。为探究Na2SO3溶液和KIO3溶液的反应,甲同学向过量的KIO3酸性溶液中加入Na2SO3溶液,并加入两滴淀粉溶液:开始时无明显现象,t秒后溶液突然变为蓝色。
+5I-+6H+=3I2+3H2O。为探究Na2SO3溶液和KIO3溶液的反应,甲同学向过量的KIO3酸性溶液中加入Na2SO3溶液,并加入两滴淀粉溶液:开始时无明显现象,t秒后溶液突然变为蓝色。(1)甲同学对这一现象做出如下假设:t秒前生成了I2,但由于存在Na2SO3,I2被消耗,该反应的离子方程式为
 的还原性
的还原性(2)为验证他的猜想,甲同学向反应后的蓝色溶液中加入
(3)甲同学设计了如下实验,进一步研究Na2SO3溶液和KIO3溶液反应的过程。

①甲同学在b电极附近的溶液中检测出了
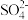
②刚开始放电时,a电极附近溶液未变蓝;取出a电极附近溶液于试管中,溶液变蓝。
 在a极放电的产物是
在a极放电的产物是③放电一段时间后,a电极附近溶液短暂出现蓝色,随即消失,重复多次后,蓝色不再褪去。电流表显示电路中时而出现电流,时而归零,最终电流消失。电流表短暂归零的原因是
④下列说法正确的是
a. a电极附近蓝色不再褪去时,
 尚未完全氧化
尚未完全氧化b. a电极附近短暂出现蓝色,随即消失的原因可能是因为I2被
 还原
还原c. 电流消失后,向b电极附近加入过量Na2SO3溶液,重新产生电流,a电极附近蓝色褪去
您最近一年使用:0次
名校
解题方法
6 . 科学家设计的一种微生物脱盐池的装置如图所示,下列说法正确的是
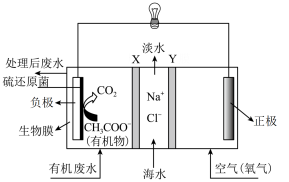

| A.该装置可以在高温下工作 |
| B.X、Y依次为阳离子、阴离子选择性交换膜 |
| C.负极反应为CH3COO− +2H2O − 8e− =2CO2↑+7H+ |
| D.该装置工作时,电能转化为化学能 |
您最近一年使用:0次
2020-11-15更新
|
549次组卷
|
21卷引用:江苏省泰州中学2021届高三上学期第二次月考化学试题
江苏省泰州中学2021届高三上学期第二次月考化学试题【市级联考】江苏省盐城市2019届高三下学期第四次模拟考试化学试题(已下线)专题08 电化学及其应用——2019年高考真题和模拟题化学分项汇编山西大学附中2020届高三上学期第二次模块诊断化学试题山西省祁县第二中学校2020届高三上学期期中考试化学试题吉林省大安一中2019-2020学年高三上学期第四次月考化学试题湖北省武汉市武昌区武汉中学2019-2020学年高二上学期化学(人教版选修4)期末复习试题:专题18 电化学综合训练云南省临沧市凤庆县第一中学2019-2020学年高三上学期期末考试理综化学试题海南省海口市海南中学2020届高三下学期第七次月考化学试题海南省海南中学2020届高三下学期第七次月考化学试题(已下线)考点07 化学能与电能-2020年高考化学命题预测与模拟试题分类精编黑龙江省哈尔滨师范大学附属中学2020届高三6月复课线下考查理综化学试题内蒙古赤峰二中2019-2020学年高一下学期第二次月考(6月)化学试题(已下线)考点09 电化学原理-2020年【衔接教材·暑假作业】新高三一轮复习化学四川省宜宾市叙州区第二中学校2021届高三上学期开学考试理综化学试题河北省唐山市2021届高三上学期第一次摸底考试化学试题广东省佛山市顺德区容山中学2021届高三10月月考化学试题陕西省宝鸡市金台区2021届高三11月检测理综化学试题(已下线)专题05 化学反应与能量——备战2021年高考化学纠错笔记河北省唐山市丰润区第二中学2020-2021学年高二上学期1月月考化学试题(已下线)课时30 新型原电池装置-2022年高考化学一轮复习小题多维练(全国通用)
名校
解题方法
7 . “碳呼吸”电池原理如图所示,(电解质溶液为含C2O 的盐溶液,电池总反应为2A1+ 6CO2=Al2(C2O4)3,下列有关说法正确的是
的盐溶液,电池总反应为2A1+ 6CO2=Al2(C2O4)3,下列有关说法正确的是
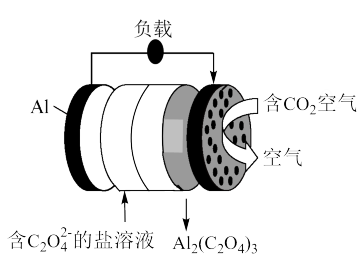
 的盐溶液,电池总反应为2A1+ 6CO2=Al2(C2O4)3,下列有关说法正确的是
的盐溶液,电池总反应为2A1+ 6CO2=Al2(C2O4)3,下列有关说法正确的是
| A.Al作负极 | B.C2O 由负极迁移至正极 由负极迁移至正极 |
| C.该装置将电能转变为化学能 | D.每生成1 mol Al2(C2O4)3,需要消耗134.4L的CO2 |
您最近一年使用:0次
2020-07-22更新
|
377次组卷
|
2卷引用:江苏省泰州市2019-2020学年高一下学期期末考试化学试题
名校
解题方法
8 . 锂二次电池新正极材料的探索和研究对锂电池的发展非常关键。
(1) 锂硒电池具有优异的循环稳定性。
①正极材料Se可由SO2通入亚硒酸(H2SeO3)溶液反应制得,则该反应的化学方程式为__ 。
②一种锂硒电池放电时的工作原理如图1所示,写出正极的电极反应式:________________ 。充电时Li+向________ (填“Se”或“Li”)极迁移。
③ Li2Sex与正极碳基体结合时的能量变化如图2所示,图中3种Li2Sex与碳基体的结合能力由大到小的顺序是________ 。

(2) Li2S电池的理论能量密度高,其正极材料为碳包裹的硫化锂(Li2S)。
① Li2S可由硫酸锂与壳聚糖高温下制得,其中壳聚糖的作用是________ 。
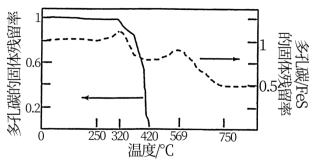
②取一定量Li2S样品在空气中加热,测得样品固体残留率随温度的变化如图3所示。(固体残留率= ×100%)分析300 ℃后,固体残留率变化的原因是
×100%)分析300 ℃后,固体残留率变化的原因是________ 。
(1) 锂硒电池具有优异的循环稳定性。
①正极材料Se可由SO2通入亚硒酸(H2SeO3)溶液反应制得,则该反应的化学方程式为
②一种锂硒电池放电时的工作原理如图1所示,写出正极的电极反应式:
③ Li2Sex与正极碳基体结合时的能量变化如图2所示,图中3种Li2Sex与碳基体的结合能力由大到小的顺序是

(2) Li2S电池的理论能量密度高,其正极材料为碳包裹的硫化锂(Li2S)。
① Li2S可由硫酸锂与壳聚糖高温下制得,其中壳聚糖的作用是
②取一定量Li2S样品在空气中加热,测得样品固体残留率随温度的变化如图3所示。(固体残留率=
 ×100%)分析300 ℃后,固体残留率变化的原因是
×100%)分析300 ℃后,固体残留率变化的原因是
您最近一年使用:0次
2020-05-21更新
|
868次组卷
|
6卷引用:江苏省泰州市2020届高三第二次模拟考试(5月) 化学试题
江苏省泰州市2020届高三第二次模拟考试(5月) 化学试题江苏省扬州市江都区大桥高级中学2020届高三下学期学情调研(三)化学试题江苏省徐州市2019-2020学年高二下学期期末抽测化学试题(已下线)科技热点之几种新型电池(已下线)第18讲 原电池 化学电源(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)4.1.2 化学电源-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)
9 . 将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图所示装置中,进行铁的电化学腐蚀实验。下列有关该实验的说法正确的是


| A.铁被氧化的电极反应式为Fe−3e−=Fe3+ |
| B.铁腐蚀过程中化学能全部转化为电能 |
| C.活性炭的存在会加速铁的腐蚀 |
| D.以水代替NaCl溶液,铁不能发生吸氧腐蚀 |
您最近一年使用:0次
2019-06-10更新
|
10548次组卷
|
76卷引用:江苏省泰州中学2020-2021学年高二上学期第一次月度质量检测化学试题
江苏省泰州中学2020-2021学年高二上学期第一次月度质量检测化学试题江苏省泰州中学2021-2022学年高二上学期第二次质量检测化学试题2019年江苏省高考化学试题(已下线)专题08 电化学及其应用——2019年高考真题和模拟题化学分项汇编河南省南阳市第一中学2018-2019学年高一下学期第六次月考化学试题山东省淄博市第七中学2019-2020学年高三上学期第一次月考化学试题浙江省温州十五校联合体2019-2020学年高二上学期期中联考化学试题福建省莆田四中2019-2020学年高二上学期期中考试化学试题上海交通大学附中2019-2020学年高三上学期期中考试化学试题(已下线)2019年12月10日 《每日一题》化学人教版(选修4)——钢铁的电化学腐蚀贵州省遵义市南白中学2019-2020学年高二上学期第三次月考化学试题2020届人教版高三化学二轮复习选择题专攻练——电化学2020届高三化学知识点强化训练----化学能与电能专题2.4 电化学(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升山西省临汾市2020届高三上学期第二次月考化学试题江苏省常州市田家炳高级中学 2019-2020学年高二上学期12月份阶段调研考试化学试题(已下线)专题十 化学能与电能(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训黑龙江省牡丹江市第一高级中学2020届高三下学期4月线上线下教学检测理综化学试题江苏省南京市南京师I范大学附属中学 2019-2020 学年高二下学期期中考试化学试题上海市长宁区2020届高三第二次模拟化学试题(已下线)专题6.3 电解池 金属的腐蚀与防护(练)——2020年高考化学一轮复习讲练测(已下线)专题6.3 电解池 金属的腐蚀与防护(讲)——2020年高考化学一轮复习讲练测河北省鸡泽县第一中学2019-2020学年高一下学期开学考试化学试题黑龙江省七台河市第一中学2019-2020学年高一下学期期末考试化学试题广东省云浮市2019-2020学年高二上学期期末考试化学试题四川省成都艺术高级中学2020-2021学年高三上学期开学考试化学试题鲁科版(2019)选择性必修1 第1章 化学反应与能量转化 第4节 金属的腐蚀与防护高中必刷题高二选择性必修1第四章 化学反应与电能 第四章素养检测人教版(2019)高二选择性必修第一册 第四章 化学反应与电能 第三节 金属的腐蚀与防护1浙江省苍南县金乡卫城中学2020-2021学年高二上学期第一次月考化学试题江苏省淮安市涟水县第一中学2021届高三上学期10月月考化学试题(已下线)第21讲 电解池 金属的电化学腐蚀与防护 (精讲)——2021年高考化学一轮复习讲练测鲁科版(2019)高二选择性必修第一册第1章 化学反应与能量变化 过高考 3年真题强化闯关人教版(2019)高二化学选择性必修1第四章 化学反应与电能 过高考 3年真题强化闯关福建省福州市八县(市)一中2020-2021学年高二上学期期中联考化学试题福建省福州市八县(市)协作校2020-2021学年高二上学期期中考试化学试题湖南师范大学附属中学2020-2021学年高二上学期第三次大练习化学试题(已下线)高中化学苏教2019版必修第二册-专题6 第三单元综合拔高练(已下线)【浙江新东方】绍兴qw122(已下线)【浙江新东方】高中化学20210304-003(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)【镇江新东方】高二下21心湖期中安徽省淮北市树人高级中学2020-2021学年高一下学期期末考试化学试题(已下线)课时34 金属的腐蚀与防护-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点22 电解池 金属的腐蚀与防护-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点22 电解池 金属的腐蚀与防护-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第17讲 电解池 金属的腐蚀与防护(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)1.3 金属的腐蚀与防护(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)陕西省洛南县洛南中学2022届高三上学期第一次模拟考试化学试题(已下线)4.3 金属的腐蚀和防护-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)天津市和平区2021-2022学年高二上学期线上期末质量检测化学试题(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题06 电化学原理应用—2022年高考化学二轮复习讲练测(全国版)-测试天津市红桥区2020-2021学年高三上学期期末考试化学试题河北省邯郸市大名县第一中学2021-2022学年高一下学期第一次月考化学试题河北省邯郸市永年区第二中学2021-2022学年高一下学期第一次月考化学试题河北省保定市唐县第一中学2021-2022学年高一下学期6月考试化学试题(已下线)考点20 金属的腐蚀与防护-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)专题11 金属的腐蚀与防护-备战2023年高考化学母题题源解密(广东卷)第四章 综合拔高练(已下线)第17讲 电解池 金属的腐蚀与防护 (讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第17讲 电解池 金属的腐蚀与防护 (练)-2023年高考化学一轮复习讲练测(新教材新高考)辽宁省六校2023届高三上学期开学考试化学试题(已下线)专题十一 化学能与电能-实战高考·二轮复习核心突破吉林省吉林市第一中学2022-2023学年高二上学期期末测试化学试题(已下线)专题16 新型电化学装置分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)题型106 金属的腐蚀与防护(已下线)专题六 金属的化学腐蚀与防护(练习)(已下线)专题12 电化学的综合应用广东省惠州市惠东县2022-2023学年高三上学期第二次教学质量检测化学试题(已下线)2019年高考江苏卷化学试题变式题(单选题6-10)(已下线)第25讲电解池与金属的电化学腐蚀(已下线)第4讲 电解池 金属的电化学腐蚀与防护河北省石家庄市辛集市育才中学2023-2024学年高三上学期12月月考化学试题
名校
解题方法
10 . 含硫化物是自然界中最为重要的自然资源之一,在生产生活中应用非常广泛。
(1)燃煤烟气的脱硫(除SO2)技术和脱硝(除NOx)技术是环境科学研究的热点。以下是用硫和氮的氧化物之间的相互转化联合进行的脱硫和脱硝技术反应的热化学方程式。
NO2(g)+SO2(g)+H2O(l)=H2SO4(l) +NO(g) △H=a kJ·mol-1
2NO(g)+O2(g)=2NO2(g) △H=b kJ·mol-1
① 反应2SO2(g)+O2(g)+2H2O(l)=2H2SO4(l) 的△H=_______ KJ/mol-1。
② 将SO2通入硫酸铁溶液也能发生类似的反应。请写出该反应的离子方程式____________ 。
(2)MnSO4是重要的基础锰盐。工业上,生产MnSO4的方法有多种。
①一种较为环保的方法是:利用纤维素水解产物还原软锰矿的方法生产MnSO4,其反应方程式如下:(C6H10O5)n+nH2SO4→n(C6H11O5)HSO4
n(C6H11O5)HSO4 +nH2O →n C6H12O6+nH2SO4
C6H12O6 +12H2SO4+12MnO2→12MnSO4+6CO2↑+18H2O
从理论上讲,每生产1吨MnSO4需要的纤维素的质量为____ 吨。
②软锰矿中都含有一定量的砷的化合物,如果不除砷很难达到饲料级的生产标
准。工业上常用氧化剂来除去其中的砷。可以除去砷的氧化剂有:ClO-、KMnO4、(NH4)2S2O8、O3、H2O2等,但在实际生产中,选用的氧化剂是软锰矿,可能的原因是_________ 。
③在生产MnSO4的浸出渣中常会产生一些硫磺,可以利用四氯乙烯来回收硫磺,
回收硫磺过程中受外界影响较大的因素主要有:萃取温度、液固比等。下图1是上述3种因素对萃取硫磺质量影响的关系图。
请根据以上图表信息,选择最佳的萃取温度和液固比_____________ 。
(3)有人设想用电化学法将SO2转化为H2SO4的原理如图2所示。
① 该电解质溶液中质子的流向是_____ ;(填“从正极流向负极”或“从负极流向正极”)
② 写出该电池负极反应的电极反应方程式:_________
(1)燃煤烟气的脱硫(除SO2)技术和脱硝(除NOx)技术是环境科学研究的热点。以下是用硫和氮的氧化物之间的相互转化联合进行的脱硫和脱硝技术反应的热化学方程式。
NO2(g)+SO2(g)+H2O(l)=H2SO4(l) +NO(g) △H=a kJ·mol-1
2NO(g)+O2(g)=2NO2(g) △H=b kJ·mol-1
① 反应2SO2(g)+O2(g)+2H2O(l)=2H2SO4(l) 的△H=
② 将SO2通入硫酸铁溶液也能发生类似的反应。请写出该反应的离子方程式
(2)MnSO4是重要的基础锰盐。工业上,生产MnSO4的方法有多种。
①一种较为环保的方法是:利用纤维素水解产物还原软锰矿的方法生产MnSO4,其反应方程式如下:(C6H10O5)n+nH2SO4→n(C6H11O5)HSO4
n(C6H11O5)HSO4 +nH2O →n C6H12O6+nH2SO4
C6H12O6 +12H2SO4+12MnO2→12MnSO4+6CO2↑+18H2O
从理论上讲,每生产1吨MnSO4需要的纤维素的质量为
②软锰矿中都含有一定量的砷的化合物,如果不除砷很难达到饲料级的生产标
准。工业上常用氧化剂来除去其中的砷。可以除去砷的氧化剂有:ClO-、KMnO4、(NH4)2S2O8、O3、H2O2等,但在实际生产中,选用的氧化剂是软锰矿,可能的原因是
③在生产MnSO4的浸出渣中常会产生一些硫磺,可以利用四氯乙烯来回收硫磺,
回收硫磺过程中受外界影响较大的因素主要有:萃取温度、液固比等。下图1是上述3种因素对萃取硫磺质量影响的关系图。

请根据以上图表信息,选择最佳的萃取温度和液固比
(3)有人设想用电化学法将SO2转化为H2SO4的原理如图2所示。

① 该电解质溶液中质子的流向是
② 写出该电池负极反应的电极反应方程式:
您最近一年使用:0次



