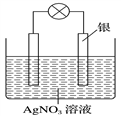
1 . 某学习小组依据氧化还原反应:2Ag++Cu===Cu2++2Ag设计成的原电池如图所示,则负极发生的电极反应为__________________________ ;当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移了的电子数目是___________________ 。

您最近一年使用:0次
名校
2 . 目前,市场上有多种“热敷袋”出售。某一化学研究性学习小组在研究了某种“热敷袋”的构造后,决定自己制造一个一次性“热敷袋”,制造过程如下:①称取15g小颗粒状活性炭,40g还原铁粉,5g细木屑,都放在一只烧杯中,再加入15mL 15%食盐水,用玻璃棒搅拌均匀。②用大头针在小塑料袋上扎几十个针眼 (袋的两层同时扎穿),把烧杯里的混合物全部加入小塑料袋中,封上袋口,再放入大塑料袋中,封上袋口,可长期保存。③使用时将大塑料袋袋口打开,反复搓揉这袋5min~8min,能感觉温度明显上升。回答下列问题:
(1)该一次性“热敷袋”利用了_____________ 原理。
(2)炭粉的作用是________________ 。
(3)将使用过的“热敷袋”打开,发现有大量棕红色粉末生成,该物质主要成分是__________________ 。
(1)该一次性“热敷袋”利用了
(2)炭粉的作用是
(3)将使用过的“热敷袋”打开,发现有大量棕红色粉末生成,该物质主要成分是
您最近一年使用:0次
名校
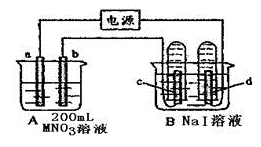
3 . 如下图装置中,b电极用金属 M制成,a、c、d为石墨电极,接通电源,金属M沉积于b极,同时a、d电极上产生气泡。试回答:
(1)a为__________ 极,c极的电极反应式为_________________ 。
(2)电解开始时,在B烧杯的中央,滴几滴淀粉溶液,你能观察到的现象是:__________ ,电解进行一段时间后,罩在c极上的试管中也收集到了气体,此时c极上的电极反应为_________________ 。
(3)当d极上收集到44.8mL气体(标准状况)时停止电解,a极上放出了_____ moL气体,若b电极上沉积金属M的质量为0.432g,则此金属的摩尔质量为_____________ 。
(1)a为
(2)电解开始时,在B烧杯的中央,滴几滴淀粉溶液,你能观察到的现象是:
(3)当d极上收集到44.8mL气体(标准状况)时停止电解,a极上放出了
您最近一年使用:0次
2017-02-25更新
|
740次组卷
|
2卷引用:安徽省六安市第一中学2016-2017学年高二上学期期末考试化学试题
真题
名校
4 . 锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4,溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。 回答下列问题:
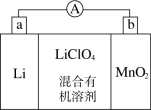
(1)外电路的电流方向是由________ 极流向________ 极(填字母)。
(2)电池正极反应式为___________________________________ 。
(3)是否可用水代替电池中的混合有机溶剂?________ (填“是”或“否”),原因是________________________________________________________________ 。
(4)MnO2可与KOH和KClO3在高温下反应,生成K2MnO4,反应的化学方程式为_______________________________________________ 。K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2的物质的量之比为___________ 。

(1)外电路的电流方向是由
(2)电池正极反应式为
(3)是否可用水代替电池中的混合有机溶剂?
(4)MnO2可与KOH和KClO3在高温下反应,生成K2MnO4,反应的化学方程式为
您最近一年使用:0次
2016-12-09更新
|
4988次组卷
|
15卷引用:2014年全国普通高等学校招生统一考试理科综合能力测试化学(海南卷)
2014年全国普通高等学校招生统一考试理科综合能力测试化学(海南卷)(已下线)2014-2015学年黑龙江省哈尔滨市第六中学高二10月月考化学试卷河北省张家口市第一中学2016-2017学年高一(衔接班)6月月考(理)化学试题福建省惠安惠南中学2017-2018学年高二10月月考(理)化学试题湖北省沙市中学2018届高三上学期第二次双周考试化学试题河南省郑州市第一中学2018-2019学年高二上学期入学测试化学试题(已下线)2019高考备考二轮复习精品资料-专题3 氧化还原反应(教学案)(已下线)2019高考备考二轮复习精品资料-专题10 电化学及其应用(教学案)湖南省双峰县第一中学2018-2019学年高一6月月考化学试题安徽省淮北市第一中学2019-2020学年高一下学期第二次线上学习考试(3月)化学试题山东省德州市齐河县实验中学2019-2020学年高一下学期期中考试化学试题人教版(2019)高二选择性必修第一册 第四章 化学反应与电能 第一节 原电池 教材帮浙江省宁波市北仑中学2020-2021学年高一下学期期中考试化学(1班选考)试题河南省新蔡县第一高级中学2020-2021学年高一下学期5月月考化学试题黑龙江省大兴安岭呼玛县高级中学2021-2022学年高二上学期期末考试化学试题
12-13高二下·河北唐山·期末
解题方法
5 . 电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,除去浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示。
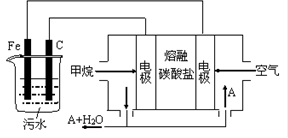
(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,可向污水中加入适量的____________ 。
a.Na2SO4 b.H2SO4 c.NaOH d.CH3COOH e.NaCl
(2)除污过程中污水池中阳离子将移向____ 极(填:“正”或“负”或“阴”或“阳”)。
(3)电解池阳极发生了两个电极反应,电极反应式是
Ⅰ. Fe-2e-=Fe2+ Ⅱ.______________________________________ 。
(4)以上电解过程是以上图右侧的燃料电池为电源,该燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料做电极。
①负极的电极反应是____________________________________________ ;
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环。A物质的电子式为__________ 。
(5)实验过程中,若在阴极产生了44.8 L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况)_________ L。

(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,可向污水中加入适量的
a.Na2SO4 b.H2SO4 c.NaOH d.CH3COOH e.NaCl
(2)除污过程中污水池中阳离子将移向
(3)电解池阳极发生了两个电极反应,电极反应式是
Ⅰ. Fe-2e-=Fe2+ Ⅱ.
(4)以上电解过程是以上图右侧的燃料电池为电源,该燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料做电极。
①负极的电极反应是
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环。A物质的电子式为
(5)实验过程中,若在阴极产生了44.8 L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况)
您最近一年使用:0次
9-10高一下·山东聊城·期末
解题方法
6 . 从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平。下图表示了三种金属被人类开发利用的大致年限。

(1)上述图中的三种常用金属的开发利用之所以有先后,主要取决于____
(填选项序号)
A.金属的导电性强弱B.金属在地壳中的含量多少
C.金属的化合价高低D.金属的活动性大小
(2)早在西汉成书的《淮南万毕术》里,就有"曾青得铁则化为铜"的记载。曾青又有空青、白青、石胆、胆矾等名称其实都是天然的硫酸铜。
①写出"曾青得铁则化为铜"的离子方程式________________ 。
②若根据上述反应设计成原电池,请在方框中画出原电池的装置图,标出正、负极和电解质溶液,并写出电极反应式。

__________________
正极反应___________________________
负极反应___________________________
③设计一个实验方案,使如图装置中的铁棒上析出铜,而铁的质量不变。(可用文字叙述也可用图示意)。

______________________
(3)铁路工人常用铝热反应来焊接钢轨,写出有关的化学方程式_____________ 。教材中引发铝热反应的试剂是__________ 。

(1)上述图中的三种常用金属的开发利用之所以有先后,主要取决于
(填选项序号)
A.金属的导电性强弱B.金属在地壳中的含量多少
C.金属的化合价高低D.金属的活动性大小
(2)早在西汉成书的《淮南万毕术》里,就有"曾青得铁则化为铜"的记载。曾青又有空青、白青、石胆、胆矾等名称其实都是天然的硫酸铜。
①写出"曾青得铁则化为铜"的离子方程式
②若根据上述反应设计成原电池,请在方框中画出原电池的装置图,标出正、负极和电解质溶液,并写出电极反应式。

正极反应
负极反应
③设计一个实验方案,使如图装置中的铁棒上析出铜,而铁的质量不变。(可用文字叙述也可用图示意)。

(3)铁路工人常用铝热反应来焊接钢轨,写出有关的化学方程式
您最近一年使用:0次
7 . 工业制硝酸的主要反应为:4NH3(g)+5O2(g)⇌4NO(g)+6H2O(l)△H
(1)已知氢气的燃烧热为△H=﹣285.8kJ/mol.
N2(g)+3H2(g)═2NH3(g)△H=﹣92.4kJ/mol;
N2(g)+O2(g)═2NO(g)△H=+180.6kJ/mol.
则上述工业制硝酸的主要反应的△H=_____ 。
(2)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如表:
①反应在第2min到第4min时,O2的平均反应速率为_____ 。
②反应在第6min时改变了条件,改变的条件可能是_____ (填序号).
A.使用催化剂 B.升高温度 C.减小压强 D.增加O2的浓度
③下列说法中能说明4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g)达到平衡状态的是_____ (填序号).
A.单位时间内生成n mol NO的同时,生成n mol NH3
B.条件一定,混合气体的平均相对分子质量不再变化
C.百分含量w(NH3)=w(NO)
D.反应速率v(NH3):v(O2):v(NO):v(H2O)=4:5:4:6
E.若在恒温恒压下容积可变的容器中反应,混合气体的密度不再变化
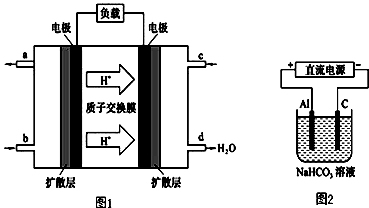
(3)某研究所组装的CH2=CH2﹣O2燃料电池的工作原理如图1所示.
①该电池工作时,b口通入的物质为_____ 。
②该电池负极的电极反应式为:_____ 。
③以此电池作电源,在实验室中模拟铝制品表面“钝化”处理(装置如图2所示)的过程中,发现阳极周围变浑浊并有气泡产生,其原因可能是:_____ (用相关的离子方程式表示)。
(1)已知氢气的燃烧热为△H=﹣285.8kJ/mol.
N2(g)+3H2(g)═2NH3(g)△H=﹣92.4kJ/mol;
N2(g)+O2(g)═2NO(g)△H=+180.6kJ/mol.
则上述工业制硝酸的主要反应的△H=
(2)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如表:
| 浓度 | c(NH3)(mol/L) | c(O2)(mol/L) | c(NO)(mol/L) |
| 起始 | 0.8 | 1.6 | 0 |
| 第2min | 0.6 | a | 0.2 |
| 第4min | 0.3 | 0.975 | 0.5 |
| 第6min | 0.3 | 0.975 | 0.5 |
| 第8min | 0.7 | 1.475 | 0.1 |
①反应在第2min到第4min时,O2的平均反应速率为
②反应在第6min时改变了条件,改变的条件可能是
A.使用催化剂 B.升高温度 C.减小压强 D.增加O2的浓度
③下列说法中能说明4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g)达到平衡状态的是
A.单位时间内生成n mol NO的同时,生成n mol NH3
B.条件一定,混合气体的平均相对分子质量不再变化
C.百分含量w(NH3)=w(NO)
D.反应速率v(NH3):v(O2):v(NO):v(H2O)=4:5:4:6
E.若在恒温恒压下容积可变的容器中反应,混合气体的密度不再变化
(3)某研究所组装的CH2=CH2﹣O2燃料电池的工作原理如图1所示.
①该电池工作时,b口通入的物质为
②该电池负极的电极反应式为:
③以此电池作电源,在实验室中模拟铝制品表面“钝化”处理(装置如图2所示)的过程中,发现阳极周围变浑浊并有气泡产生,其原因可能是:

您最近一年使用:0次
2016-01-14更新
|
138次组卷
|
2卷引用:2016届宁夏银川二中高三上学期统考理综化学试卷
10-11高一下·安徽滁州·期中
8 . 市场上出售的“热敷袋”其主要成分是铁屑、炭粉和少量的NaCl、水等。热敷袋在启用前用塑料袋使之与空气隔绝,启用时,打开塑料袋轻轻揉搓,就会放出热量,使用完后,会发现袋内有许多铁锈生成。回答:
(1)热敷袋放出的热量来源于_________ 放出的热量。
(2)炭粉的作用是________________________ 。
(3)加入NaCl的作用是________________________ 。
(4)写出有关电极反应式和化学方程式________________ 。
(1)热敷袋放出的热量来源于
(2)炭粉的作用是
(3)加入NaCl的作用是
(4)写出有关电极反应式和化学方程式
您最近一年使用:0次



