名校
解题方法
1 . 完成下列问题
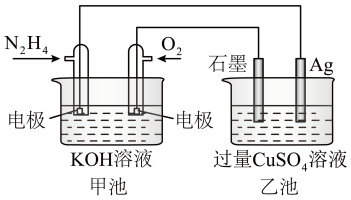
(1)如图所示,甲池的总反应式为 ,
,___________ (填“原电池”或“电解池”),写出通入 一极发生电极反应式
一极发生电极反应式___________ 。
②乙池中电解反应的化学方程式为___________ 。
③当甲池中消耗 时,乙池中
时,乙池中 电极上析出固体的质量是
电极上析出固体的质量是___________ 。
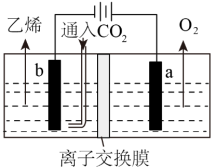
(2)高铁酸钠(Na2FeO4)易溶于水,是一种新型多功能水处理剂,可以用如图所示电解装置制取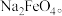 电解一段时间后,
电解一段时间后, 降低的区域在
降低的区域在___________ (填“阴极室”或“阳极室”);阳极电极反应式为:___________ 。 电极上的电极反应式为
电极上的电极反应式为___________ ;
②该装置中使用的是___________ (填“阴”或“阳”)离子交换膜。
(1)如图所示,甲池的总反应式为
 ,
,
 一极发生电极反应式
一极发生电极反应式②乙池中电解反应的化学方程式为
③当甲池中消耗
 时,乙池中
时,乙池中 电极上析出固体的质量是
电极上析出固体的质量是(2)高铁酸钠(Na2FeO4)易溶于水,是一种新型多功能水处理剂,可以用如图所示电解装置制取
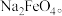 电解一段时间后,
电解一段时间后, 降低的区域在
降低的区域在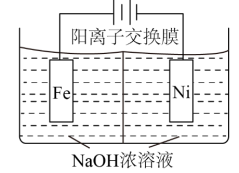
 电极上的电极反应式为
电极上的电极反应式为②该装置中使用的是
您最近半年使用:0次
解题方法
2 . 一种Zn-催化电极(表面锂掺杂了锡纳米粒子)催化制甲酸盐的电化学装置如图所示。下列说法正确的是

| A.放电时,正极电极反应式为:CO2+2e-+H2O=HCOO-+OH- |
| B.充电时,催化电极周围pH升高 |
| C.放电时,锡纳米粒子能提高CO2的平衡转化率 |
| D.充电时,催化电极应与电源的负极相连 |
您最近半年使用:0次
名校
3 . 与锂离子电池相比,有机电池不依赖战略金属、充电速度更快且环境友好。如图是一种可降解的多肽电池。(假设离子交换膜仅允许 通过)下列说法不正确的是
通过)下列说法不正确的是

 通过)下列说法不正确的是
通过)下列说法不正确的是
| A.放电时,电极电势:c>d |
B.放电时,总反应方程式为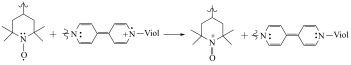 |
| C.充电时,电路中每通过2mol电子,阳极区质量增加298g |
D.充电时,a电极的方程式为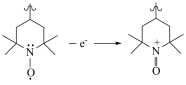 |
您最近半年使用:0次
2024-04-10更新
|
298次组卷
|
2卷引用:重庆市巴蜀中学校2024届高三下学期高考适应性月考(七)化学试卷
4 . 认真观察下列装置,回答下列问题:
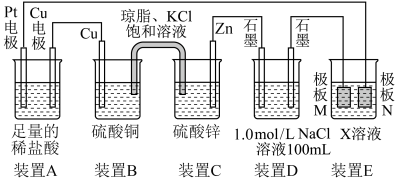
(1)C装置中,Zn电极叫___________ (填“正极”或“负极”);电极方程式为___________ ;盐桥中K+的移动方向___________ (填“向左”、“向右”或“不移动”)。
(2)电池工作初期,A装置中总反应的离子方程式为___________ 。
(3)若装置E中的目的是在Cu材料上镀Ag,则X溶液中的溶质为___________ ,极板M的材料为___________ 。
(4)当装置A中Cu电极质量改变12.8g时,则装置D中产生的气体体积为___________ L(标准状况下)。

(1)C装置中,Zn电极叫
(2)电池工作初期,A装置中总反应的离子方程式为
(3)若装置E中的目的是在Cu材料上镀Ag,则X溶液中的溶质为
(4)当装置A中Cu电极质量改变12.8g时,则装置D中产生的气体体积为
您最近半年使用:0次
名校
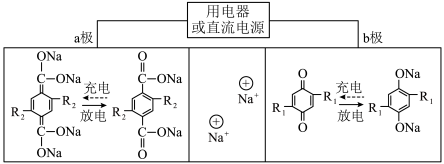
5 . 一种钠离子可充电电池的示意图如下所示。该电池主要依靠钠离子在两极之间移动来工作,其中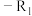 代表没参与反应的
代表没参与反应的 代表没参与反应的—
代表没参与反应的—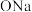 。下列说法正确的是
。下列说法正确的是
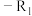 代表没参与反应的
代表没参与反应的 代表没参与反应的—
代表没参与反应的—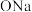 。下列说法正确的是
。下列说法正确的是
A.放电时, 极为正极 极为正极 |
B.充电时, 由 由 极区向 极区向 极区迁移 极区迁移 |
C.充电时,阳极发生的电极反应为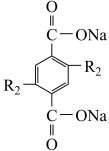 -2e-+2Na+= -2e-+2Na+= |
D.若电池充满电时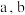 两极室的质量相等,则放电过程中转移 两极室的质量相等,则放电过程中转移 电子时,两极室的质量差为 电子时,两极室的质量差为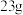 |
您最近半年使用:0次
解题方法
6 . 下图为利用肼(N2H4)-空气燃料电池电解CuSO4溶液的示意图。下列说法正确的是


| A.左图负极反应式为:N2H4-6e-+4OH-=N2↑+4H2O |
| B.铜棒为电解池的阳极 |
| C.一段时间后,左图中电解质溶液的pH不变 |
| D.标况下,当左图中有2.24LO2被还原时,右图阳极上放出2.24L气体 |
您最近半年使用:0次
名校
7 . 某种钠电池的充电、放电过程的工作原理如图所示,下列说法正确的是
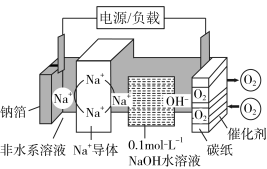

| A.放电时,电子由碳纸电极移向钠箔电极 |
B.放电时,碳纸电极上的反应式为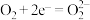 |
| C.充电时,碳纸电极应与电源负极连接 |
| D.充电时,NaOH溶液的物质的量浓度减小 |
您最近半年使用:0次
2024-04-09更新
|
87次组卷
|
3卷引用:河北省沧州市泊头市八县联考2023-2024学年高三下学期3月月考化学试题
名校
解题方法
8 . H2、CO、CH4等都是重要的能源,也是重要的化工原料。
(1)25℃,101kPa时,8.0gCH4完全燃烧生成二氧化碳气体和液态水放出445.1kJ热量。写出该反应的热化学反应方程式:_______ 。
(2)水煤气中的CO和H2在高温下反应可生成甲烷。在体积为2L的恒容密闭容器中,充入1molCO和5molH2,一定温度下发生反应: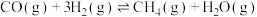 。测得CO和H2的转化率随时间变化如图所示。
。测得CO和H2的转化率随时间变化如图所示。
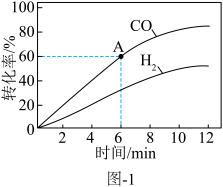
①从反应开始到6min,CO的平均反应速率_________ ,6min时,H2的转化率为________ 。
②下列叙述中能说明上述反应达到化学平衡状态的是___________ 。(填字母)
a.容器中混合气体的密度保持不变
b.容器中混合气体的总压强保持不变
c.容器中CH4的体积分数保持不变
d.单位时间内每消耗1molCO,同时生成1molCH4
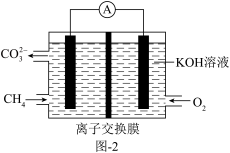
(3)甲烷燃料电池装置如图,电池总反应为 。通入CH4一端电极反应方程式为:
。通入CH4一端电极反应方程式为:__________ ;通入氧气的电极为电池的_________ (填“正极”或“负极”),若通入0.1molCH4充分反应,计算用此燃料电池电解饱和食盐水,理论上得到氢气的体积(标准状况下)__________ 。
(1)25℃,101kPa时,8.0gCH4完全燃烧生成二氧化碳气体和液态水放出445.1kJ热量。写出该反应的热化学反应方程式:
(2)水煤气中的CO和H2在高温下反应可生成甲烷。在体积为2L的恒容密闭容器中,充入1molCO和5molH2,一定温度下发生反应:
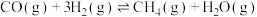 。测得CO和H2的转化率随时间变化如图所示。
。测得CO和H2的转化率随时间变化如图所示。
①从反应开始到6min,CO的平均反应速率
②下列叙述中能说明上述反应达到化学平衡状态的是
a.容器中混合气体的密度保持不变
b.容器中混合气体的总压强保持不变
c.容器中CH4的体积分数保持不变
d.单位时间内每消耗1molCO,同时生成1molCH4
(3)甲烷燃料电池装置如图,电池总反应为
 。通入CH4一端电极反应方程式为:
。通入CH4一端电极反应方程式为:
您最近半年使用:0次
名校
解题方法
9 . 关于下列装置说法正确的是
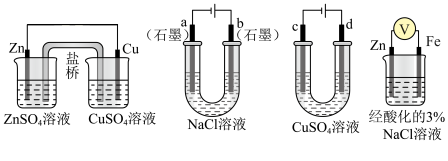

A.装置①中,盐桥中的 移向 移向 溶液 溶液 |
| B.装置②工作一段时间通过0.2mol电子,a极产生的气体体积为2.24L |
C.用装置③精炼铜时,d极为粗铜,电解质溶液中 浓度减小 浓度减小 |
D.装置④中电子由Zn流向Fe,装置中有 生成 生成 |
您最近半年使用:0次
10 . 以浓差电池(电解质溶液浓度不同造成电势差)为电源,用石墨作电极将 转化为高纯
转化为高纯 的装置如图。下列说法错误的是
的装置如图。下列说法错误的是

 转化为高纯
转化为高纯 的装置如图。下列说法错误的是
的装置如图。下列说法错误的是
A.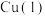 的电极反应式为 的电极反应式为 |
| B.离子交换膜II为阳离子交换膜 |
C.工作时, 电极附近溶液的 电极附近溶液的 降低 降低 |
D.电解停止时,理论上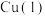 和 和 电极的质量差为 电极的质量差为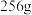 |
您最近半年使用:0次



