名校
1 . X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大。X的s轨道上电子全充满,p轨道上无电子,Y与Z相邻,Z是地壳中含量最丰富的元素,M为非金属性最强的元素,Q是纯碱中的一种元素,下列说法不正确 的是
A.第一电离能: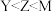 |
B.简单离子半径: |
C.化合物 可能为两性氢氧化物 可能为两性氢氧化物 |
| D.Z与Q形成化合物的化合物中可能含有非极性键 |
您最近一年使用:0次
2024-03-14更新
|
257次组卷
|
3卷引用:四川省绵阳中学2023-2024学年高二下学期4月月考化学试题
名校
2 . X、Y、Z、W、P、Q是元素周期表前四周期的六种常见元素,原子序数依次增大。X在自然界中有多种同素异形体,其中一种是自然界中最硬的单质;Z是地壳中含量最多的元素;W基态原子核外的9个原子轨道上填充了电子,且有1个未成对电子;P是常见的金属元素,其单质能与盐酸反应,不与碱反应,它的某种氧化物可用作红色颜料;Q基态原子的M层全充满,N层没有成对电子,只有一个未成对电子。回答以下问题:
(1)P、Q中位于周期表的d区的是__________ (填元素符号,下同),基态Q原子的价层电子排布式为__________ ;元素X、Y、Z中,电负性最大的是__________ 。
(2)烃 的1个分子中含有
的1个分子中含有__________ 个σ键;X和Y的简单氢化物中沸点更高的是__________ (填化学式),理由是__________ (答2点)。
(3)化合物 可用作杀菌消毒剂和漂白剂,
可用作杀菌消毒剂和漂白剂, 分子的中心原子杂化类型是
分子的中心原子杂化类型是__________ ;工业上可用W的单质与潮湿的碳酸钠反应制取 ,并生成另外两种含钠的化合物,反应中无其它气体生成,写出该反应的化学方程式
,并生成另外两种含钠的化合物,反应中无其它气体生成,写出该反应的化学方程式__________ 。
(1)P、Q中位于周期表的d区的是
(2)烃
 的1个分子中含有
的1个分子中含有(3)化合物
 可用作杀菌消毒剂和漂白剂,
可用作杀菌消毒剂和漂白剂, 分子的中心原子杂化类型是
分子的中心原子杂化类型是 ,并生成另外两种含钠的化合物,反应中无其它气体生成,写出该反应的化学方程式
,并生成另外两种含钠的化合物,反应中无其它气体生成,写出该反应的化学方程式
您最近一年使用:0次
2024-02-22更新
|
160次组卷
|
4卷引用:四川省泸州市2023-2024学年高二上学期1月期末化学试题
名校
3 . 已知A、B、C、D、E、F是原子序数依次增大的前四周期元素。其中A是宇宙中含量最多的元素;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素原子的价层电子排布式为 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是| A.A、B、C三种元素的电负性:B>C>A |
| B.B、C、D、E四种元素的第一电离能:B>C>E>D |
C.B、C形成的化合物 为酸性氧化物 为酸性氧化物 |
D.F的常见离子的核外电子排布图为 |
您最近一年使用:0次
2024-01-08更新
|
314次组卷
|
7卷引用:四川省成都石室中学2023-2024学年高二上学期期中考试化学试卷
四川省成都石室中学2023-2024学年高二上学期期中考试化学试卷山东省济南市历城第二中学2023-2024学年高二上学期期末化学模拟试题(已下线)1.2.2元素周期律-随堂练习甘肃省武威第七中学2023-2024学年高二上学期期末考试化学试题(已下线)名校期中好题汇编-原子结构与性质(选择题)名校期中好题汇编-原子结构与性质(选择题)(已下线)清单01 原子结构与性质(考点清单)(讲+练)-2023-2024学年高二化学下学期期末考点大串讲(人教版2019)
名校
解题方法
4 . 有四种短周期元素,它们的结构、性质等信息如下表所述,请根据表中信息填写:
(1)A原子的核外电子排布式___________ 。
(2)离子半径:B___________ A(填“大于”或“小于”)。
(3)C原子的外围电子轨道式___________ ,其原子核外有 ___________ 个未成对电子,能量最高的电子为___________ 轨道上的电子,其轨道呈___________ 形。
(4)D原子占据最高能层符号为___________ ,能量不同的电子数为___________ ,空间运动状态不同电子数为___________ ,运动状态不同电子数为___________ 。
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
(2)离子半径:B
(3)C原子的外围电子轨道式
(4)D原子占据最高能层符号为
您最近一年使用:0次
名校
解题方法
5 . 已知A、B、C、D、E、F是原子序数依次增大的前四周期元素。其中A是宇宙中含量最多的元素;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素原子的价层电子排布式为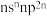 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
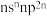 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是| A.A、B、C三种元素的电负性:B>C>A |
| B.B、C、D、E四种元素的第一电离能:B>C>E>D |
| C.B、C、E形成的简单离子半径大小顺序:E离子>C离子>B离子 |
D.F离子的核外电子排布式为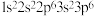 |
您最近一年使用:0次
名校
解题方法
6 . X、Y、Z、Q、R是原子序数依次增大的短周期主族元素,它们原子的最外层电子数之和为24,X是地壳中含量最高的元素,基态Z原子的p轨道上存2个未成对电子,Q的单质为黄色晶体,常存在于火山口附近。下列说法错误的是
| A.QX2分子为极性分子 | B.元素电负性:X>R>Q |
| C.Y位于元素周期表中的s区 | D.Z、Q、R的氧化物对应水化物的酸性依次增强 |
您最近一年使用:0次
2023-10-28更新
|
144次组卷
|
3卷引用:四川省南充市仪陇中学校2023-2024学年高二下学期4月月考化学试题
7 . 碳元素在自然界中分布很广,是存在形式最复杂的元素。实验室可用邻二氮菲(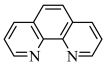 )与
)与 形成的红色配合物(如下图)测定铁的含量。
形成的红色配合物(如下图)测定铁的含量。
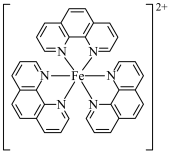
回答下列问题:
(1)基态 原子的价电子占据的能量最高的能级是
原子的价电子占据的能量最高的能级是_______ ,基态 原子核外电子的空间运动状态有
原子核外电子的空间运动状态有_______ 种, 的价电子轨道表达式为
的价电子轨道表达式为_______ 。
(2)红色配离子的中心原子的配位数为_______ ;
(3)邻二氮菲分子中C、N两种元素原子的杂化方式分别为_______ 、_______ ;
(4)红色配合物中H、C、N、Fe四种元素的电负性从大到小的顺序为_______ ;
(5)红色配离子中不存在的作用力有_______ ;
A. 键 B.
键 B. 键 C.离子键 D氢键 E.配位键
键 C.离子键 D氢键 E.配位键
(6)临床建议服用维生素 促进“亚铁”的吸收,避免生成
促进“亚铁”的吸收,避免生成 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是_______ ;
(7)汽车安全气囊产生气体的功臣是叠氮化钠 ,
, 的空间构型为
的空间构型为_______ 。
 )与
)与 形成的红色配合物(如下图)测定铁的含量。
形成的红色配合物(如下图)测定铁的含量。
回答下列问题:
(1)基态
 原子的价电子占据的能量最高的能级是
原子的价电子占据的能量最高的能级是 原子核外电子的空间运动状态有
原子核外电子的空间运动状态有 的价电子轨道表达式为
的价电子轨道表达式为(2)红色配离子的中心原子的配位数为
(3)邻二氮菲分子中C、N两种元素原子的杂化方式分别为
(4)红色配合物中H、C、N、Fe四种元素的电负性从大到小的顺序为
(5)红色配离子中不存在的作用力有
A.
 键 B.
键 B. 键 C.离子键 D氢键 E.配位键
键 C.离子键 D氢键 E.配位键(6)临床建议服用维生素
 促进“亚铁”的吸收,避免生成
促进“亚铁”的吸收,避免生成 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是(7)汽车安全气囊产生气体的功臣是叠氮化钠
 ,
, 的空间构型为
的空间构型为
您最近一年使用:0次
2023-04-01更新
|
166次组卷
|
3卷引用:四川省宜宾市叙州区第一中学校2023-2024学年高二上学期1月期末化学试题
名校
解题方法
8 . 已知A、B、C、D、E、F为周期表前四周期原子序数依次增大的六种元素。其中A是元素周期表中原子半径最小的元素。B原子最外层电子数是内层电子数的2倍。D、E为同主族元素,且E的原子序数为D的2倍。F元素在地壳中的含量位于金属元素的第二位。试回答下列问题:
(1)F元素原子的价电子排布式为___________ 。
(2)下列关于B2A2的说法中正确的是___________(填序号)。
(3)B和D形成的一种三原子分子与C和D形成的一种化合物互为等电子体,则满足上述条件的B和D形成的化合物的结构式为___________ 。
(4)C元素原子的第一电离能比B、D两元素原子的第一电离能高的主要原因是___________ 。
(5)E的氢化物的价电子对互斥理论模型为___________ ,E原子的杂化方式为___________ 杂化。
(1)F元素原子的价电子排布式为
(2)下列关于B2A2的说法中正确的是___________(填序号)。
| A.B2A2中的所有原子都满足8电子结构 |
| B.每个B2A2分子中σ键和π键数目比为1:1 |
| C.B2A2是含极性键和非极性键的非极性分子 |
| D.B2A2分子中的B-A键属于s-sp σ键 |
(4)C元素原子的第一电离能比B、D两元素原子的第一电离能高的主要原因是
(5)E的氢化物的价电子对互斥理论模型为
您最近一年使用:0次
9 . 化合物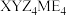 可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为
可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为 ,X与M同周期,E在地壳中含量最多。下列说法正确的是
,X与M同周期,E在地壳中含量最多。下列说法正确的是
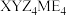 可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为
可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为 ,X与M同周期,E在地壳中含量最多。下列说法正确的是
,X与M同周期,E在地壳中含量最多。下列说法正确的是A.元素电负性: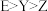 | B.氢化物沸点: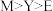 |
C.第一电离能: | D.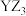 和 和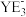 的空间结构均为三角锥形 的空间结构均为三角锥形 |
您最近一年使用:0次
2023-07-04更新
|
8407次组卷
|
16卷引用:四川省南充市阆中中学校2023-2024学年高二下学期3月月考化学试卷
四川省南充市阆中中学校2023-2024学年高二下学期3月月考化学试卷2023年高考广东卷化学真题(已下线)2023年广东卷高考真题变式题(选择题11-16)(已下线)第19讲元素周期律与元素周期表江西省宜春市宜丰中学2023-2024学年高三上学期开学考试化学试题(已下线)考点18 元素周期律与元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)广东省江门市第一中学2023-2024学年高二上学期第一次段考化学试题(已下线)选择题1-5陕西师范大学附属中学2023-2024学年高二上学期期中考试化学试题(已下线)题型20 物质结构与性质基础-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)重庆市第七中学校2023-2024学年高三上学期月考(12月)化学试题河北省石家庄二中教育集团2023-2024学年高二年级上学期期末考试化学试题安徽省合肥市第七中学2023-2024学年高二下学期第一次段考化学试卷 福建省南安市侨光中学2023-2024学年高二下学期4月月考化学试题甘肃省白银市靖远县第四中学2023-2024学年高二下学期4月月考化学试题广东省乐昌市第二中学2023-2024学年高三下学期保温测试(5月模拟)化学试题
名校
解题方法
10 . 铝和硅在地壳中含量丰富,其单质和化合物具有广泛的应用价值。请回答下列问题:
(1)①基态Si原子的价电子排布式为_______ 。
②Si所在周期中的非金属元素(Si、P、S、Cl),其第一电离能由小到大的顺序为_______ 。
③写出一种与SiCl4互为等电子体的离子的化学式_______ 。
(2)AlCl3的相对分子质量为133.5,178℃开始升华,易溶于水、四氯化碳等,熔融时生成可挥发的二聚物(Al2Cl6),结构如图所示:

①二聚物中Al原子的杂化轨道类型为_______
②分子中含有化学键的类型有_______ 。
A、离子键 B、配位键 C、氢键 D、σ键 E、π键 F、非极性键
(3)LiAlH4是一种特殊的还原剂,可将羧酸直接还原成醇。CH3COOH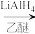 CH3CH2OH
CH3CH2OH
① 的空间构型名称是
的空间构型名称是_______ 。
②CH3COOH分子中π键和σ键的数目之比为_______ 。
(4)铝和白磷在一定条件下可以制备磷化铝(AlP),其晶胞如图所示:

①晶胞中A原子的原子坐标为(0,0,0),B的原子坐标为( ,
, ,
, ),则C的原子坐标为:
),则C的原子坐标为:_______ 。
②晶胞中Al的配位数是_______ ,若该晶胞的密度为ag/cm3,Al的半径为xpm,P的半径为ypm,则该晶体的空间利用率为_______ 。(列出表达式)
(1)①基态Si原子的价电子排布式为
②Si所在周期中的非金属元素(Si、P、S、Cl),其第一电离能由小到大的顺序为
③写出一种与SiCl4互为等电子体的离子的化学式
(2)AlCl3的相对分子质量为133.5,178℃开始升华,易溶于水、四氯化碳等,熔融时生成可挥发的二聚物(Al2Cl6),结构如图所示:

①二聚物中Al原子的杂化轨道类型为
②分子中含有化学键的类型有
A、离子键 B、配位键 C、氢键 D、σ键 E、π键 F、非极性键
(3)LiAlH4是一种特殊的还原剂,可将羧酸直接还原成醇。CH3COOH
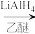 CH3CH2OH
CH3CH2OH①
 的空间构型名称是
的空间构型名称是②CH3COOH分子中π键和σ键的数目之比为
(4)铝和白磷在一定条件下可以制备磷化铝(AlP),其晶胞如图所示:

①晶胞中A原子的原子坐标为(0,0,0),B的原子坐标为(
 ,
, ,
, ),则C的原子坐标为:
),则C的原子坐标为:②晶胞中Al的配位数是
您最近一年使用:0次



