22-23高一下·浙江·期中
1 . 按要求完成下列填空:
(1)①写出乙烯的电子式_______ ;
②黄铁矿主要成分的化学式_______ 。
(2)写出Si元素在元素周期表中的位置_______ 。
(3)在加热条件下木炭与浓硫酸反应的化学方程式为_______ 。
(1)①写出乙烯的电子式
②黄铁矿主要成分的化学式
(2)写出Si元素在元素周期表中的位置
(3)在加热条件下木炭与浓硫酸反应的化学方程式为
您最近一年使用:0次
名校
2 . 下表显示了元素周期表中的一部分。
请回答下列问题。
(1)硫元素的原子序数是_______ 。
(2)氟元素的原子结构示意图为_______ (填写字母)。
A.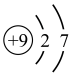 B.
B.
(3)镁元素在元素周期表的第_______ (填“二”或“三”)周期第_______ (填“ⅡA”或“ⅢA”)族。
(4)已知同主族元素从上到下原子半径逐渐增大,原子半径大小:H_______ (填“<”或“>”)Na。
(5)雷雨天闪电时空气中有O3生成,O2转化为O3是_______ (填“物理变化”或“化学变化”)。
(6)SiO2可用于生产光导纤维,SiO2中硅元素的化合价为_______ 。
(7)海水中的重要元素——钠和氯,形成生活中常见调味品的化学式为_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 第一周期 | 1 H 氢 | 2 He 氦 | ||||||
| 第二周期 | 3 Li 锂 | 4 Be 镀 | 5 B 硼 | 6 C 碳 | 7 N 氮 | 8 O 氧 | 9 F 氟 | 10 Ne 氖 |
| 第三周期1 | 1 Na 钠 | 12 Mg 镁 | 33 Al 铝 | 14 Si 硅 | 15 P 磷 | 16 S 硫 | 17 C 氯 | 18 Ar 氩 |
(1)硫元素的原子序数是
(2)氟元素的原子结构示意图为
A.
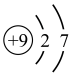 B.
B.
(3)镁元素在元素周期表的第
(4)已知同主族元素从上到下原子半径逐渐增大,原子半径大小:H
(5)雷雨天闪电时空气中有O3生成,O2转化为O3是
(6)SiO2可用于生产光导纤维,SiO2中硅元素的化合价为
(7)海水中的重要元素——钠和氯,形成生活中常见调味品的化学式为
您最近一年使用:0次
2023-05-11更新
|
178次组卷
|
2卷引用:云南省蒙自市第一高级中学2022-2023学年高一下学期5月期中考试化学试题
3 . 元素周期表中锑元素的数据如图。

(1)根据锑的价层电子排布式5s25p3可知,锑在元素周期表中位于第___________ 周期,第___________ 族。
(2)基态锑原子中有___________ 个未成对电子,这些未成对电子具有___________ (填“相同”或“不同”)的自旋状态。
(3)基态锑原子的5s轨道形状为___________ 形,该原子最外层电子占有___________ 个轨道。
(4)Bi在元素周期表中与Sb相邻,位于Sb的正下方。则两种元素的电负性Sb___________ Bi;原子半径Sb___________ Bi (填“>”或“<”)。

(1)根据锑的价层电子排布式5s25p3可知,锑在元素周期表中位于第
(2)基态锑原子中有
(3)基态锑原子的5s轨道形状为
(4)Bi在元素周期表中与Sb相邻,位于Sb的正下方。则两种元素的电负性Sb
您最近一年使用:0次
名校
4 . 下图是尚未完成的元素周期表,其中a、b、c、d、e、f为元素代号。_____
(2)在上图中用斜线阴影 标出过渡元素的范围。
标出过渡元素的范围。________
(3)在上图中用实线画出金属元素与非金属元素的分界线。________
(4)a原子在周期表中的位置是___________ ,写出a原子结构示意图___________ 。
(5)b和e两元素的原子以___________ (填化学键类型)形成化合物。
(6)b、c、d三种元素中,原子半径最大的是___________ (填元素名称),离子半径最大的是___________ (填离子符号)。
(7)写出c、d元素各自所形成的最高价氧化物对应的水化物之间发生的反应的离子方程式___________ 。
(8)b元素与其同主族元素的原子序数之差不可能是___________。
(9)下列有关元素周期表的叙述中,错误的是___________。

(2)在上图中用斜线阴影
 标出过渡元素的范围。
标出过渡元素的范围。(3)在上图中用实线画出金属元素与非金属元素的分界线。
(4)a原子在周期表中的位置是
(5)b和e两元素的原子以
(6)b、c、d三种元素中,原子半径最大的是
(7)写出c、d元素各自所形成的最高价氧化物对应的水化物之间发生的反应的离子方程式
(8)b元素与其同主族元素的原子序数之差不可能是___________。
| A.8 | B.16 | C.26 | D.44 |
| A.位于金属非金属分界线附近的元素既表现出金属的某些性质,又表现出非金属的某些性质 |
| B.人们在金属非金属分界线附近寻找高效催化剂 |
| C.元素b的最高价氧化物对应的水化物的酸性是最强的 |
| D.f是金属性最强的元素 |
您最近一年使用:0次
2023-05-01更新
|
236次组卷
|
2卷引用:上海市控江中学2022-2023学年高一下学期期中考试化学试题
名校
5 .  是高效、广谱、绿色的消毒剂,回答下列问题。
是高效、广谱、绿色的消毒剂,回答下列问题。
(1)氯在元素周期表中的位置是___________ ,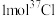 的中子数为
的中子数为___________ 。
(2)下列能判断Cl和O两种元素非金属性强弱的是___________ (填序号)。
a.原子得电子能力
b.与金属钠反应得电子的数目
c.最简单气态氢化物的稳定性
d.单质的沸点
(3)生产生活中含氯物质的排放会加快臭氧层的破坏。该过程的机理如图,总反应化学方程式为___________ 。

(4)化工、冶金行业的废水中存在 ,可用
,可用 气体将其转化为两种无毒气体
气体将其转化为两种无毒气体
① 的电子式为
的电子式为___________ 。
②该反应的离子方程式为___________ 。
(5)X、Y、Z、W四种短周期元素在周期表中的位置关系如图,Y和Z的核外电子数之和为22。将少量X的最高价氧化物通入到硅酸钠溶液中实现现象是___________ ,反应的离子方程式为___________ 。
 是高效、广谱、绿色的消毒剂,回答下列问题。
是高效、广谱、绿色的消毒剂,回答下列问题。(1)氯在元素周期表中的位置是
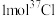 的中子数为
的中子数为(2)下列能判断Cl和O两种元素非金属性强弱的是
a.原子得电子能力
b.与金属钠反应得电子的数目
c.最简单气态氢化物的稳定性
d.单质的沸点
(3)生产生活中含氯物质的排放会加快臭氧层的破坏。该过程的机理如图,总反应化学方程式为

(4)化工、冶金行业的废水中存在
 ,可用
,可用 气体将其转化为两种无毒气体
气体将其转化为两种无毒气体①
 的电子式为
的电子式为②该反应的离子方程式为
(5)X、Y、Z、W四种短周期元素在周期表中的位置关系如图,Y和Z的核外电子数之和为22。将少量X的最高价氧化物通入到硅酸钠溶液中实现现象是
| X | Y | |
| Z | W |
您最近一年使用:0次
名校
解题方法
6 . 2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。中国科学院院士张青莲教授曾主持测定了铟(49In)等9种元素相对原子质量的新值,被采用为国际新标准。
(1)In在周期表中的位置是______ 。
(2)In的最高价氧化物对应的水化物的碱性______ Ba(OH)2的碱性(填“>”或“<”)。
(3)硒(34Se)是动物和人体所必需的微量元素之一,也是重要的工业原料,与氧同族。Se原子电子式可表示为______ 。
(4)下列说法合理的是______ 。
a.SeO2既有氧化性又有还原性 b.热稳定性:H2Se<HCl<H2S
c.酸性:H2SeO4<HBrO4<HClO4 d.Se比S更易与氢气反应
(1)In在周期表中的位置是
(2)In的最高价氧化物对应的水化物的碱性
(3)硒(34Se)是动物和人体所必需的微量元素之一,也是重要的工业原料,与氧同族。Se原子电子式可表示为
(4)下列说法合理的是
a.SeO2既有氧化性又有还原性 b.热稳定性:H2Se<HCl<H2S
c.酸性:H2SeO4<HBrO4<HClO4 d.Se比S更易与氢气反应
您最近一年使用:0次
名校
7 . 下表是元素周期表的一部分。
(1) 和
和 互为
互为___________ ,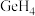 分子的空间结构为
分子的空间结构为___________ 。
(2) 为
为___________ (填“共价”或“离子”)化合物,该物质可作为野外工作的应急燃料,其与水反应的化学方程式为___________ 。
(3)能作为氯、溴、碘元素非金属性递变规律的判断依据是___________。
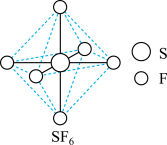
(4) 分子的空间结构为正八面体形,如图所示。
分子的空间结构为正八面体形,如图所示。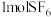 中含有
中含有___________ 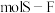 键,它的一氯代物
键,它的一氯代物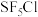 有
有___________ 种。
(5)研究发现,给小鼠喂食适量硒酸钠 可减轻重金属铊引起的中毒。Na、Se、O形成的简单离子的半径由大到小的顺序为
可减轻重金属铊引起的中毒。Na、Se、O形成的简单离子的半径由大到小的顺序为___________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 一 | H | ||||||
| 二 | C | O | F | ||||
| 三 | Na | Si | S | Cl | |||
| 四 | Ca | Ge | Se | Br |
 和
和 互为
互为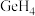 分子的空间结构为
分子的空间结构为(2)
 为
为(3)能作为氯、溴、碘元素非金属性递变规律的判断依据是___________。
A. , , , , 的熔点 的熔点 | B. , , , , 的氧化性 的氧化性 |
C. 、 、 、 、 的热稳定性 的热稳定性 | D. 、 、 、 、 的酸性 的酸性 |
 分子的空间结构为正八面体形,如图所示。
分子的空间结构为正八面体形,如图所示。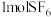 中含有
中含有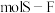 键,它的一氯代物
键,它的一氯代物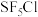 有
有
(5)研究发现,给小鼠喂食适量硒酸钠
 可减轻重金属铊引起的中毒。Na、Se、O形成的简单离子的半径由大到小的顺序为
可减轻重金属铊引起的中毒。Na、Se、O形成的简单离子的半径由大到小的顺序为
您最近一年使用:0次
8 . C、N、O、F等元素的化合物在航天、美容、食品等多领域中有广泛的用途,请回答:
(1)OF2主要用于火箭工程液体助燃剂,该分子的空间结构为______ ;N、O、F的第一电离能由大到小的顺序为_____ (用元素符号表示)。
(2)XeF2是一种选择性很好的氟化试剂,但在室温下易升华,推测XeF2为______ 晶体(填晶体类型)。
(3)FeSO4是一种重要的食品和饲料添加剂:
①Fe在周期表中位于第______ 周期第______ 族。
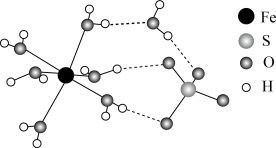
②FeSO4·7H2O的结构示意图如图所示,H2O与Fe2+、SO 的作用类型分别是
的作用类型分别是______ 、______ 。
A.离子键 B.配位键 C.氢键 D.金属键 中键角的大小并解释原因:
中键角的大小并解释原因:______ 。
(1)OF2主要用于火箭工程液体助燃剂,该分子的空间结构为
(2)XeF2是一种选择性很好的氟化试剂,但在室温下易升华,推测XeF2为
(3)FeSO4是一种重要的食品和饲料添加剂:
①Fe在周期表中位于第
②FeSO4·7H2O的结构示意图如图所示,H2O与Fe2+、SO
 的作用类型分别是
的作用类型分别是A.离子键 B.配位键 C.氢键 D.金属键
 中键角的大小并解释原因:
中键角的大小并解释原因:
您最近一年使用:0次
2023-04-20更新
|
197次组卷
|
3卷引用:山西省大同市2022-2023学年高二下学期期中考试化学试题
名校
9 . 下表是元素周期表的一部分,数字①~⑨代表九种常见的短周期元素,请按题目要求回答下列问题:
(1)元素⑨在周期表中的位置___________ 。
(2)在0~⑨元素中,某种元素的氧化物是两性氧化物,请写出该氧化物与氢氧化钠反应的化学方程式___________ 。
(3)请比较④⑨两元素的氢化物的稳定性___________ (用氢化物的分子式表示)。
(4)元素⑨的单质可使湿润的淀粉 试纸变蓝,请写出离子方程式
试纸变蓝,请写出离子方程式___________ 。
(5)将⑤⑥⑦三种元素的离子按半径从大到小排序___________ (用元素符号表示)。
| ① | |||||||
| ② | ③ | ④ | |||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)元素⑨在周期表中的位置
(2)在0~⑨元素中,某种元素的氧化物是两性氧化物,请写出该氧化物与氢氧化钠反应的化学方程式
(3)请比较④⑨两元素的氢化物的稳定性
(4)元素⑨的单质可使湿润的淀粉
 试纸变蓝,请写出离子方程式
试纸变蓝,请写出离子方程式(5)将⑤⑥⑦三种元素的离子按半径从大到小排序
您最近一年使用:0次
名校
10 . 下表是元素周期表的一部分,根据表中的①~⑩种元素,按要求填写下列空白:
(1)在这些元素中,化学性质最不活泼元素的原子结构示意图为___________ 。
(2)①用于考古的一种核素符号为___________ 。①和⑦简单氢化物稳定性较差的是___________ (填化学式)。
(3)元素②和⑥对应的离子半径较小的是___________ (填离子符号)。⑤和⑧最高价氧化物对应水化物酸性较强的是___________ (填化学式)。④和⑥最高价氧化物对应水化物碱性较弱的是___________ (填化学式)。
(4)写出②与④形成原子个数为1:2的化合物的电子式___________ 。
(5)下列关于⑩元素硒(Se)说法推断正确的是___________(填标号)。
(6)④和⑥最高价氧化物对应水化物相互反应的离子方程式为___________ 。
| 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ④ | ⑥ | ⑦ | ⑤ | ⑧ | ⑨ | ||
| 4 | ③ | ⑩ |
(2)①用于考古的一种核素符号为
(3)元素②和⑥对应的离子半径较小的是
(4)写出②与④形成原子个数为1:2的化合物的电子式
(5)下列关于⑩元素硒(Se)说法推断正确的是___________(填标号)。
A. 属于共价化合物,只具有还原性 属于共价化合物,只具有还原性 |
B.Se的最低负化合价是负2价;但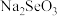 中Se化合价为+4 中Se化合价为+4 |
| C.Se元素非金属性比⑤强 |
| D.Se元素原子半径小于③ |
您最近一年使用:0次



