名校
1 . 如图是元素周期表的一部分,请回答下列问题:

(1)元素④、⑤、⑥的原子半径由大到小的顺序为___________ (用元素符号表示)。
(2)元素②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是___________ (用化学式表示)。
(3)元素①、④、⑤三种元素可形成既含离子键又含极性共价键的化合物,该化合物的电子式为:___________ 。
(4)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

X溶液与Y溶液反应的离子方程式为___________ 。由N产生⑥的单质的化学反应方程式为 ___________ 。

(1)元素④、⑤、⑥的原子半径由大到小的顺序为
(2)元素②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(3)元素①、④、⑤三种元素可形成既含离子键又含极性共价键的化合物,该化合物的电子式为:
(4)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

X溶液与Y溶液反应的离子方程式为
您最近一年使用:0次
名校
解题方法
2 . 钛酸钙是最典型的钙钛矿型化合物,该类化合物具有特殊的理化性质。
(1)基态 的核外电子排布式为
的核外电子排布式为____________ 。
(2)钛酸钙的晶胞如下图所示。
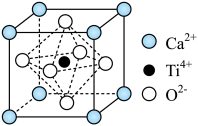
①每个 周围等距且紧邻的
周围等距且紧邻的 有
有______ 个。
②比较 和
和 的离子半径大小并说明理由
的离子半径大小并说明理由____________ 。
(3)钛酸钙的阴、阳离子均可被半径相近的其它离子替代,从而衍生出多种钙钛矿型化合物。
①已知钛酸钙晶胞中距离最近的 和
和 之间的距离为
之间的距离为 ,则钛酸钙晶体密度
,则钛酸钙晶体密度
______  (列出计算式)。
(列出计算式)。
②若忽略离子替代时的体积变化,下列钙钛矿型化合物中,密度大于钛酸钙的是______ (填字母序号)。
a. b.
b.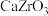 c.
c.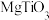
(4)通过离子替代可获得具有优异光电性能的有机钙钛矿型化合物 。其中有机阳离子
。其中有机阳离子 可由甲胺(
可由甲胺( )制得。
)制得。
① 中N的杂化方式为
中N的杂化方式为____________ 。
请从化学键的角度解释由甲胺形成 的过程:
的过程:____________ 。
(1)基态
 的核外电子排布式为
的核外电子排布式为(2)钛酸钙的晶胞如下图所示。

①每个
 周围等距且紧邻的
周围等距且紧邻的 有
有②比较
 和
和 的离子半径大小并说明理由
的离子半径大小并说明理由(3)钛酸钙的阴、阳离子均可被半径相近的其它离子替代,从而衍生出多种钙钛矿型化合物。
①已知钛酸钙晶胞中距离最近的
 和
和 之间的距离为
之间的距离为 ,则钛酸钙晶体密度
,则钛酸钙晶体密度
 (列出计算式)。
(列出计算式)。②若忽略离子替代时的体积变化,下列钙钛矿型化合物中,密度大于钛酸钙的是
a.
 b.
b.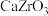 c.
c.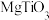
(4)通过离子替代可获得具有优异光电性能的有机钙钛矿型化合物
 。其中有机阳离子
。其中有机阳离子 可由甲胺(
可由甲胺( )制得。
)制得。①
 中N的杂化方式为
中N的杂化方式为请从化学键的角度解释由甲胺形成
 的过程:
的过程:
您最近一年使用:0次
名校
3 . 电气石是一种具有保健作用的天然石材,其中含有的主要元素为 等元素。
等元素。
(1)上述元素中,原子半径最小的是_______ (用元素符号表示),与硫同周期的元素中简单离子半径最小的是_______ (用离子符号表示);
(2)用轨道表示式表示氧元素原子核外电子的运动状态_______ ;氧元素原子核外有_______ 种不同能量的电子;
(3) 分子中
分子中 为
为_______ 杂化,键角等于_______ ,可以判断出 分子为
分子为_______ 分子(选填“极性”或“非极性”); 晶体的熔点比
晶体的熔点比 晶体
晶体_______ (选填“高”、“低”),原因为_______ 。
 等元素。
等元素。(1)上述元素中,原子半径最小的是
(2)用轨道表示式表示氧元素原子核外电子的运动状态
(3)
 分子中
分子中 为
为 分子为
分子为 晶体的熔点比
晶体的熔点比 晶体
晶体
您最近一年使用:0次
4 . 下列表格是元素周期表的一部分,请按要求填空。
(1)写出④⑤⑦的原子半径由大到小的顺序为___________ 。
(2)元素③和⑩形成的化合物中存在的化学键类型为___________ 。
(3)写出由①和⑥形成的化合物的电子式___________ 。
(4)元素⑪在周期表中的位置________ ,其基态原子的核外电子排布式为___________ 。
(5)写出⑧⑫的最高价氧化物的水化物发生反应的化学方程式___________ 。
(6)写出元素②基态原子的核外电子占据的能量最高的原子轨道的形状为___________ ,该基态原子的价层电子轨道表示式为___________ 。
(7)元素④的气态氢化物的VSEPR模型为___________ ,分子的空间结构为___________ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ||||||||||||||
| ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||||||||||||
| ⑪ | ⑫ | ||||||||||||||||
(2)元素③和⑩形成的化合物中存在的化学键类型为
(3)写出由①和⑥形成的化合物的电子式
(4)元素⑪在周期表中的位置
(5)写出⑧⑫的最高价氧化物的水化物发生反应的化学方程式
(6)写出元素②基态原子的核外电子占据的能量最高的原子轨道的形状为
(7)元素④的气态氢化物的VSEPR模型为
您最近一年使用:0次
5 . 下表是元素周期表的部分,表中所列的数字分别代表某一种元素。针对表中①-⑩号元素回答下列问题。
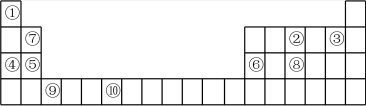
(1)⑩元素的名称是___________ ,⑨元素的原子结构示意图为___________ 。
(2)②、③、④、⑤、⑥五种元素中,原子半径由小到大的顺序是___________ (填元素符号);这五种元素分别形成的简单离子中离子半径最小的是___________ 。(填离子符号)
(3)某些不同族元素的性质也有一定的相似性,如表中元素⑦与元素⑥的氢氧化物有相似的性质,请写出元素⑦的氢氧化物与NaOH溶液反应的化学方程式:___________ 。
(4)元素①和④的单质化合形成的化合物能与水反应生成氢气,向反应后的溶液中滴入酚酞,溶液变红,反应的化学方程式为_________ 。
(5)元素④和⑥相比,金属性较强的是_________ (填元素符号),下列能证明这一事实的有_________ (填序号)。
A.在化合物中④的化合价比⑥的低 B.④的单质能与冷水剧烈反应而⑥的单质不能
C.④的最高价氧化物对应水化物的碱性比⑥强 D.④单质的熔点比⑥单质的低
(6)⑧号元素有多种化合物,次磷酸(H3PO2)和次磷酸钠(NaH2PO2)常为化工生产的还原剂。
I.已知H3PO2是一种一元弱酸,向Ba(H2PO2)2溶液中加入H2SO4制备H3PO2,写出该反应的离子方程式___________ 。
Ⅱ.NaH2PO2可在酸性条件下与Ni2+作用进行“化学镀镍”(如在木材表面生成一层Ni-P合金),反应中磷元素化合价发生的变化是___________ (选填编号)。
a.升高 b.降低 c.既升高又降低

(1)⑩元素的名称是
(2)②、③、④、⑤、⑥五种元素中,原子半径由小到大的顺序是
(3)某些不同族元素的性质也有一定的相似性,如表中元素⑦与元素⑥的氢氧化物有相似的性质,请写出元素⑦的氢氧化物与NaOH溶液反应的化学方程式:
(4)元素①和④的单质化合形成的化合物能与水反应生成氢气,向反应后的溶液中滴入酚酞,溶液变红,反应的化学方程式为
(5)元素④和⑥相比,金属性较强的是
A.在化合物中④的化合价比⑥的低 B.④的单质能与冷水剧烈反应而⑥的单质不能
C.④的最高价氧化物对应水化物的碱性比⑥强 D.④单质的熔点比⑥单质的低
(6)⑧号元素有多种化合物,次磷酸(H3PO2)和次磷酸钠(NaH2PO2)常为化工生产的还原剂。
I.已知H3PO2是一种一元弱酸,向Ba(H2PO2)2溶液中加入H2SO4制备H3PO2,写出该反应的离子方程式
Ⅱ.NaH2PO2可在酸性条件下与Ni2+作用进行“化学镀镍”(如在木材表面生成一层Ni-P合金),反应中磷元素化合价发生的变化是
a.升高 b.降低 c.既升高又降低
您最近一年使用:0次
解题方法
6 . 锂是最轻的活泼金属,其单质及其化合物有广泛的用途。回答下列问题:
(1)在元素周期表中,与
 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是___________ ,该元素基态原子中,占据最高能级电子的电子云轮廓图形状为___________ 。
(2)LiH是一种储氢材料。
(i)Li与H中第一电离能较小的元素是___________ 。
(ii)离子半径:Li+___________ H-(填“>”“=”或“<”)。
(3)已知金属锂晶体为FCC(面心立方晶格),面心立方紧密堆积结构示意图如下:
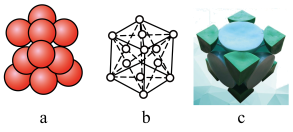
(i)晶胞中锂的配位数为___________ 。
(ii)若锂原子的半径为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则锂晶体密度为
,则锂晶体密度为___________  (列出含有
(列出含有 、
、 的计算式即可)。
的计算式即可)。
(1)在元素周期表中,与
 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是(2)LiH是一种储氢材料。
(i)Li与H中第一电离能较小的元素是
(ii)离子半径:Li+
(3)已知金属锂晶体为FCC(面心立方晶格),面心立方紧密堆积结构示意图如下:

(i)晶胞中锂的配位数为
(ii)若锂原子的半径为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则锂晶体密度为
,则锂晶体密度为 (列出含有
(列出含有 、
、 的计算式即可)。
的计算式即可)。
您最近一年使用:0次
2023-10-28更新
|
93次组卷
|
2卷引用:山西省朔州市怀仁市第九中学高中部2023-2024学年高三上学期11月期中考试化学试题
7 . 以粉煤灰(主要成分:Al2O3、SiO2、少量Fe2O3)为原料,制取Al2O3的部分工艺流程如下:

完成下列填空:
(1)铝原子核外有_______ 种不同能量的电子,最外层电子的轨道式是_______ ,上述流程涉及第二周期元素的原子半径由小到大的顺序是_______ 。
(2)“除铁”是将Fe3+转化为Fe(OH)3沉淀,反应的离子方程式为_______ ,检验溶液中Fe3+是否除尽的方法是_______ 。
(3)解释“结晶”过程中向AlCl3浓溶液中通入HCl气体的原因。_______
(4)上述流程可循环的物质是_______ 。
(5)工业上是通过电解熔化状态下Al2O3,而不是电解熔化状态下AlCl3来获得铝,其原因是_______ 。

完成下列填空:
(1)铝原子核外有
(2)“除铁”是将Fe3+转化为Fe(OH)3沉淀,反应的离子方程式为
(3)解释“结晶”过程中向AlCl3浓溶液中通入HCl气体的原因。
(4)上述流程可循环的物质是
(5)工业上是通过电解熔化状态下Al2O3,而不是电解熔化状态下AlCl3来获得铝,其原因是
您最近一年使用:0次
名校
解题方法
8 . A、B、C、D、E、F是六种短周期主族元素,它们的原子序数依次增大,其中C、F分别是同一主族元素,A、F两种元素的原子核中质子数之和比C、D两种元素原子核中质子数之和少2,F元素的最外层电子数是次外层电子数的0.75倍。又知B元素的最外层电子数是内层电子数的2倍,E元素的最外层电子数等于其电子层数。请回答:
(1)1 mol由E、F二种元素组成的化合物跟由A、C、D三种元素组成的化合物反应生成两种盐和水,完全反应后消耗后者的物质的量为___________ 。
(2)A、C、F间可以形成甲、乙两种负一价双原子阴离子,甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为___________ ;
(3)科学研究证明:化学反应热只与始终态有关,与过程无关。单质B的燃烧热为a kJ/mol。由B、C二种元素组成的化合物BC l4 g完全燃烧放出热量b kJ,写出单质B和单质C反应生成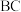 的热化学方程式:
的热化学方程式:___________ ;
(4)用B元素的单质与E元素的单质可以制成电极浸入由A、C、D三种元素组成化合物的溶液中构成电池,则电池负极反应式为___________ 。
(5)C、D、E、F四种元素的离子半径由大到小的顺序___________ (用离子符号表示)
(6)过量B元素的最高价氧化物与D元素的最高价氧化物的水化物反应的离子方程式为___________ 。
(1)1 mol由E、F二种元素组成的化合物跟由A、C、D三种元素组成的化合物反应生成两种盐和水,完全反应后消耗后者的物质的量为
(2)A、C、F间可以形成甲、乙两种负一价双原子阴离子,甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为
(3)科学研究证明:化学反应热只与始终态有关,与过程无关。单质B的燃烧热为a kJ/mol。由B、C二种元素组成的化合物BC l4 g完全燃烧放出热量b kJ,写出单质B和单质C反应生成
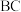 的热化学方程式:
的热化学方程式:(4)用B元素的单质与E元素的单质可以制成电极浸入由A、C、D三种元素组成化合物的溶液中构成电池,则电池负极反应式为
(5)C、D、E、F四种元素的离子半径由大到小的顺序
(6)过量B元素的最高价氧化物与D元素的最高价氧化物的水化物反应的离子方程式为
您最近一年使用:0次
解题方法
9 . A、B、D、E、X是原子序数依次增大的五种短周期元素。A是周期表中相对原子质量最小的元素,A、B能形成两种液态化合物 和
和 。D是短周期中原子半径最大的主族元素,E的周期序数和族序数相等,D、X的原子最外层电子数之和为8。回答下列问题:(用化学用语填空)
。D是短周期中原子半径最大的主族元素,E的周期序数和族序数相等,D、X的原子最外层电子数之和为8。回答下列问题:(用化学用语填空)
(1) 的电子式为
的电子式为__________ ;离子半径D__________ B(填“>”或“<”)。
(2)如图所示,将少量X单质的水溶液分别滴入盛有不同试剂的试管中。

管a中发生反应的化学方程式为__________ ,该反应可用于制备漂白液。
②试管b中的实验现象为__________ ,说明X的非金属性强于碘元素,从原子结构的角度解释其原因是__________ 。
(3)镓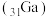 与E为同主族元素,氮化镓
与E为同主族元素,氮化镓 作为第三代半导体材料,具有耐高温、耐高电压等特性。下列相关说法中,正确的是
作为第三代半导体材料,具有耐高温、耐高电压等特性。下列相关说法中,正确的是__________ (填字母序号)。
a. 位于元素周期表的第四周期
位于元素周期表的第四周期
b. 中
中 的化合价为
的化合价为
c. 的离子半径小于
的离子半径小于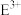 的离子半径
的离子半径
(4)工业上用 处理中性废水中的
处理中性废水中的 ,使其转化为
,使其转化为 沉淀除去,X被还原至最低价,该反应的离子方程式为
沉淀除去,X被还原至最低价,该反应的离子方程式为__________ 。
 和
和 。D是短周期中原子半径最大的主族元素,E的周期序数和族序数相等,D、X的原子最外层电子数之和为8。回答下列问题:(用化学用语填空)
。D是短周期中原子半径最大的主族元素,E的周期序数和族序数相等,D、X的原子最外层电子数之和为8。回答下列问题:(用化学用语填空) (1)
 的电子式为
的电子式为(2)如图所示,将少量X单质的水溶液分别滴入盛有不同试剂的试管中。

管a中发生反应的化学方程式为
②试管b中的实验现象为
(3)镓
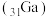 与E为同主族元素,氮化镓
与E为同主族元素,氮化镓 作为第三代半导体材料,具有耐高温、耐高电压等特性。下列相关说法中,正确的是
作为第三代半导体材料,具有耐高温、耐高电压等特性。下列相关说法中,正确的是a.
 位于元素周期表的第四周期
位于元素周期表的第四周期b.
 中
中 的化合价为
的化合价为
c.
 的离子半径小于
的离子半径小于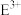 的离子半径
的离子半径(4)工业上用
 处理中性废水中的
处理中性废水中的 ,使其转化为
,使其转化为 沉淀除去,X被还原至最低价,该反应的离子方程式为
沉淀除去,X被还原至最低价,该反应的离子方程式为
您最近一年使用:0次
名校
10 . A、B、C、D、E五种短周期元素,原子序数依次增大,其中只有C为金属元素。A、C原子序数之和等于E的原子序数,D与B同主族且D原子序数是B原子序数的2倍。AB2和DB2溶于水均得到酸性溶液,C2D溶于水得到碱性溶液。
(1)E元素在周期表中的位置为_______________ ;C、D、E的简单离子的离子半径由大到小的顺序是________________ (用离子符号表示)。工业上制取C单质的化学方程式为__________________ 。
(2)C2B2电子式为________________ ,某溶液中含有①NO 、②HCO
、②HCO 、③SO
、③SO 、④CO
、④CO 、⑤SO
、⑤SO 5种阴离子,向其中加入C2B2固体后,溶液中的离子浓度基本保持不变的是(忽略溶液体积变化)
5种阴离子,向其中加入C2B2固体后,溶液中的离子浓度基本保持不变的是(忽略溶液体积变化) ________________ 。
A.① B.①③⑤
C.①④⑤ D.①②④⑤
(3)化合物C2D的水溶液在空气中久置后变质,生成一种单质,所得溶液呈强碱性,用化学方程式表示这一变化过程_________________
(1)E元素在周期表中的位置为
(2)C2B2电子式为
 、②HCO
、②HCO 、③SO
、③SO 、④CO
、④CO 、⑤SO
、⑤SO 5种阴离子,向其中加入C2B2固体后,溶液中的离子浓度基本保持不变的是(忽略溶液体积变化)
5种阴离子,向其中加入C2B2固体后,溶液中的离子浓度基本保持不变的是(忽略溶液体积变化) A.① B.①③⑤
C.①④⑤ D.①②④⑤
(3)化合物C2D的水溶液在空气中久置后变质,生成一种单质,所得溶液呈强碱性,用化学方程式表示这一变化过程
您最近一年使用:0次
2022-11-12更新
|
191次组卷
|
3卷引用:天津市五校2022-2023学年高三上学期期中联考化学试题



