名校
1 . 随着原子序数的递增,8种短周期元素原子半径的相对大小、最高正化合价或最低负化合价如图所示。
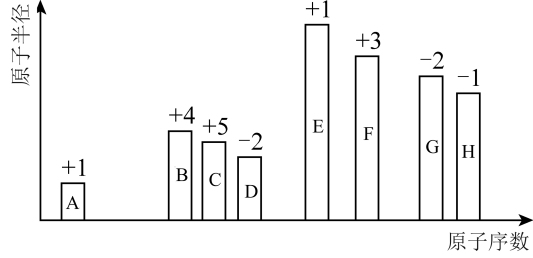
请用相应的化学用语回答下列问题:
(1)元素H在元素周期表中的位置是_______ 。
(2)元素D、G的简单氢化物中,还原性较强的是_______ (填化学式)。元素G、H的最高价氧化物的水化物中,酸性较强的是_______ (填化学式)。
(3)元素D、E、F、G形成的简单离子中,半径最小的离子为_______ (填离子符号)。
(4)化合物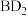 所含的化学键类型是
所含的化学键类型是_______ ,由A、D、H三种元素原子个数比为1∶1∶1形成的化合物的电子式为_______ 。
(5)用电子式表示元素E和H组成的化合物的形成过程:_______ 。
(6)元素F的氧化物与E的最高价氧化物的水化物反应的离子方程式为_______ 。

请用相应的化学用语回答下列问题:
(1)元素H在元素周期表中的位置是
(2)元素D、G的简单氢化物中,还原性较强的是
(3)元素D、E、F、G形成的简单离子中,半径最小的离子为
(4)化合物
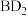 所含的化学键类型是
所含的化学键类型是(5)用电子式表示元素E和H组成的化合物的形成过程:
(6)元素F的氧化物与E的最高价氧化物的水化物反应的离子方程式为
您最近一年使用:0次
2022-01-19更新
|
351次组卷
|
3卷引用:辽宁省抚顺市六校协作体2021-2022学年高一上学期期末考试化学试题
解题方法
2 . U、V、W、X、Y、Z是原子序数依次增大的前四常见元素。Y的单质在 中燃烧的产物可使品红溶液褪色。Z和W元素形成的化合物
中燃烧的产物可使品红溶液褪色。Z和W元素形成的化合物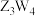 具有磁性。U的单质在
具有磁性。U的单质在 中燃烧可生成UW和
中燃烧可生成UW和 两种气体。X的单质是一种金属,该金属单质在
两种气体。X的单质是一种金属,该金属单质在 中剧烈燃烧生成黑、白两种固体。
中剧烈燃烧生成黑、白两种固体。
请回答下列问题:
(1)X在周期表中的位置:_______ , 的电子式为
的电子式为_______ ;
(2)Z在高温下与水反应的化学方程式_______ ;设计实验方案,检验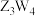 中含
中含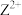 的方法
的方法_______ 。
(3)U、V、W形成的10电子氢化物中,氢化物的稳定性从强到弱的顺序是_______ (写化学式),V的氢化物与空气可以构成一种环保燃料电池,电解质溶液是KOH,其负极的电极反应式为_______ 。
 中燃烧的产物可使品红溶液褪色。Z和W元素形成的化合物
中燃烧的产物可使品红溶液褪色。Z和W元素形成的化合物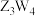 具有磁性。U的单质在
具有磁性。U的单质在 中燃烧可生成UW和
中燃烧可生成UW和 两种气体。X的单质是一种金属,该金属单质在
两种气体。X的单质是一种金属,该金属单质在 中剧烈燃烧生成黑、白两种固体。
中剧烈燃烧生成黑、白两种固体。请回答下列问题:
(1)X在周期表中的位置:
 的电子式为
的电子式为(2)Z在高温下与水反应的化学方程式
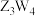 中含
中含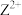 的方法
的方法(3)U、V、W形成的10电子氢化物中,氢化物的稳定性从强到弱的顺序是
您最近一年使用:0次
名校
3 . 下图所示的两种化合物可应用于阻燃材料和生物材料的合成。其中W、X、Y、Z为原子序数依次增大的短周期元素,X和Z同主族,Y原子序数为W原子价电子数的3倍。请回答下列问题:
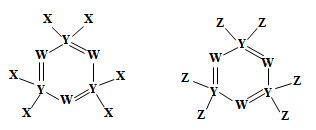
(1)元素Y在周期表中的位置为___________ ,元素Z的最高价氧化物的水化物的化学式为_____ 。
(2)元素W、X、Y、Z的简单阴离子半径由大到小的顺序为_____ 。
(3)Z、W和氢三种元素形成的同时含有离子键和共价键化合物的电子式为_____ 。
(4)研究Y、Z非金属性强弱的方案中不可行的是___________(填序号)。
(5)许多含元素Z的化合物均可作为杀菌消毒剂,将ZO2通入到NaOH和H2O2混合溶液中,可制备NaZO2。
查阅资料:NaZO2晶体易溶于水,难溶于乙醇。NaZO2饱和溶液在温度低于38 ℃时析出NaZO2·3H2O晶体,高于38 ℃时析出NaZO2晶体,高于60 ℃时NaZO2分解成NaZO3和NaZ。
①写出由ZO2制备NaZO2的离子方程式_____ 。
②从上述NaZO2溶液获得干燥的NaZO2晶体的操作步骤为:将溶液在减压和55 ℃条件下蒸发至大量晶体析出后,___________ ,___________ ,低于60℃干燥,得到NaZO2晶体 (补全实验步骤)。

(1)元素Y在周期表中的位置为
(2)元素W、X、Y、Z的简单阴离子半径由大到小的顺序为
(3)Z、W和氢三种元素形成的同时含有离子键和共价键化合物的电子式为
(4)研究Y、Z非金属性强弱的方案中不可行的是___________(填序号)。
| A.比较其简单氢化物的沸点 | B.比较其单质与氢气反应的难易程度 |
| C.比较其简单阴离子的还原性 | D.比较其氧化物的水化物的酸性 |
查阅资料:NaZO2晶体易溶于水,难溶于乙醇。NaZO2饱和溶液在温度低于38 ℃时析出NaZO2·3H2O晶体,高于38 ℃时析出NaZO2晶体,高于60 ℃时NaZO2分解成NaZO3和NaZ。
①写出由ZO2制备NaZO2的离子方程式
②从上述NaZO2溶液获得干燥的NaZO2晶体的操作步骤为:将溶液在减压和55 ℃条件下蒸发至大量晶体析出后,
您最近一年使用:0次
名校
4 . 1869年俄国化学家门捷列夫制出第一张元素周期表,元素周期表体现了元素位置、结构和性质的关系。短周期元素A、B、C、D、E原子序数递增,由它们组成的新型化合物CA4B5D8·4A2D可用于电讯器材、高级玻璃的制造,其受热分解产物中有两种常见的10电子分子,二者反应生成一种弱碱,B、E同主族,E是同周期离子半径最小的。
(1)画出E的离子结构示意图______ ,在元素周期表中的位置为______ 。
(2)100—200℃时只生成一种气体,该气体电子式为______ 。
(3)试比较B、C、E元素所形成最高价氧化物对应水化物的酸性由强到弱的顺序为(写化学式)______ ,并从原子结构角度解释其原因__ 。
(4)请依据推断比较D、E两种元素离子半径的大小______ 。
(5)C的最高价氧化物对应的水化物与E的最高价氧化物对应的水化物反应的离子方程式为______ 。
(6)该化合物500℃热分解后生成的固体氧化物可与Mg单质发生置换反应,写出化学方程式______ 。
(1)画出E的离子结构示意图
(2)100—200℃时只生成一种气体,该气体电子式为
(3)试比较B、C、E元素所形成最高价氧化物对应水化物的酸性由强到弱的顺序为(写化学式)
(4)请依据推断比较D、E两种元素离子半径的大小
(5)C的最高价氧化物对应的水化物与E的最高价氧化物对应的水化物反应的离子方程式为
(6)该化合物500℃热分解后生成的固体氧化物可与Mg单质发生置换反应,写出化学方程式
您最近一年使用:0次
名校
解题方法
5 . W、X、Y、Z、M、G、H七种短周期元素,原子序数依次增大。W、Z同主族,可形成离子化合物ZW;Y、G同主族,可形成GY2、GY3两种分子;X的气态氢化物与其最高价氧化物的水化物能反应;H不是稀有气体元素,W、X、Y、Z、M、G、H的最外层电子数之和等于29。请回答下列问题:
(1)Y在元素周期表中的位置为_______ 。
(2)Y、Z、G三种元素原子半径由大到小的顺序是_______ (用元素符号表示)。
(3)上述元素的最高价氧化物对应水化物的碱性最强的是_______ (填化学式),Z、M最高价氧化物对应的水化物相互反应的离子方程式为_______ ,X的气态氢化物的催化氧化反应的化学方程式为_______ 。
(4)G的非金属性_______ (填“>”或“<”)H的非金属性,下列表述可以作为验证的证据的是_______ (填字母)。
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气化合的难易程度
C.G和H单质分别与Fe反应生成FeG、FeH3
D.比较这两种元素单质与酸或碱反应的难易程度
(1)Y在元素周期表中的位置为
(2)Y、Z、G三种元素原子半径由大到小的顺序是
(3)上述元素的最高价氧化物对应水化物的碱性最强的是
(4)G的非金属性
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气化合的难易程度
C.G和H单质分别与Fe反应生成FeG、FeH3
D.比较这两种元素单质与酸或碱反应的难易程度
您最近一年使用:0次
2023-04-27更新
|
434次组卷
|
2卷引用:广西示范性高中2022-2023学年高一下学期4月期中联合调研测试化学试题
6 . 元素周期表与元素周期律在化学学习研究中有很重要的作用。如表所示是五种元素的相关信息,W、X都位于第三周期。
(1)Q在元素周期表中的位置是________ 。
(2)W的最高价氧化物对应的水化物的化学式是_________ 。
(3)X单质与水反应的离子方程式是__________ 。
(4)金属性 ,用原子结构解释原因:
,用原子结构解释原因:_________ ,失电子能力 ,金属性
,金属性 。
。
(5)下列对于Z及其化合物的推断正确的是________ (填字母)。
A.Z的最低负化合价与W的最低负化合价相同
B.Z的氢化物的稳定性弱于W的氢化物的稳定性
C.Z的单质的氧化性强于W的单质的氧化性
元素 | 信息 |
Q | 地壳中含量最高 |
W | 最高化合价为+7 |
X | 最高价氧化物对应的水化物在第三周期中碱性最强 |
Y | 焰色试验(透过蓝色钴玻璃)火焰呈紫色 |
Z | 原子结构示意图为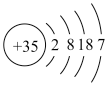 |
(2)W的最高价氧化物对应的水化物的化学式是
(3)X单质与水反应的离子方程式是
(4)金属性
 ,用原子结构解释原因:
,用原子结构解释原因: ,金属性
,金属性 。
。(5)下列对于Z及其化合物的推断正确的是
A.Z的最低负化合价与W的最低负化合价相同
B.Z的氢化物的稳定性弱于W的氢化物的稳定性
C.Z的单质的氧化性强于W的单质的氧化性
您最近一年使用:0次
名校
解题方法
7 . 现有部分从上到下原子序数依次增大的短周期主族元素,它们的元素性质或原子结构如下表所示:
回答下列问题:
(1)写出元素D在元素周期表中的位置:_______ 。
(2)元素A的一种核素可测定文物年代,这种核素是_______ (填核素符号)。B、C、D三种元素的离子半径由大到小的顺序为_______ (填离子符号)。
(3)火箭发动机曾经利用B2H4作燃料、H2C2作助燃剂,产物无污染,写出二者反应的化学方程式:_______ 。
(4)元素C的单质与钠在常温下生成物质X。用电子式表示物质X的形成过程:_______ 。
(5)探寻物质性质的差异性是学习化学的重要方法之一。A、B、E、F四种元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式)。E的最高价氧化物对应的水化物溶液与D的最高价氧化物对应的水化物反应的离子方程式为_______ 。
| 元素编号 | 元素性质或原子结构 |
| A | 该元素的一种同素异形体可用作润滑剂 |
| B | 单质为空气中含量最高的气体 |
| C | 最外层电子数是最内层电子数的3倍 |
| D | 单质为一种银白色金属,通常表面有一层致密的氧化膜,保护金属不被继续腐蚀 |
| E | M层电子数是电子层数的2倍 |
| F | 元素最高正价是+7,最低价是-1 |
(1)写出元素D在元素周期表中的位置:
(2)元素A的一种核素可测定文物年代,这种核素是
(3)火箭发动机曾经利用B2H4作燃料、H2C2作助燃剂,产物无污染,写出二者反应的化学方程式:
(4)元素C的单质与钠在常温下生成物质X。用电子式表示物质X的形成过程:
(5)探寻物质性质的差异性是学习化学的重要方法之一。A、B、E、F四种元素的最高价氧化物对应的水化物中,酸性最强的是
您最近一年使用:0次
2023-10-05更新
|
217次组卷
|
2卷引用:河北省衡水市第二中学2022-2023学年高一下学期4月期中考试化学试题
名校
8 . W、Q、X、Y、Z是原子序数依次增大的短周期主族元素,其最外层电子数之和为19,W只有一个电子层,Q与X、Y、Z位于不同周期,X、Y相邻,Y原子最外层电子数是Q原子内层电子数的2倍,仅由Z元素形成的固体在常温下为淡黄色。回答下列问题:
(1)Y在元素周期表中的位置为_______ 。
(2)最简单氢化物的沸点:Q_______ (填“>”、“<”或“=”)Z。
(3)写出X元素形成的单质与Q的最高价氧化物对应的水化物的稀溶液发生反应的离子方程式:_______ 。
(4)仅由W、Q、Z三种元素可形成化合物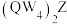 和
和 :
:
①化合物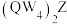 的名称为
的名称为_______ ,该化合物中Q元素的化合价为_______ 价。
②化合物 含有化学键的类型为
含有化学键的类型为_______ (填“离子键”、“共价键”或“离子键与共价键”)。
(5)化合物 与热水反应仅生成X的最高价氧化物对应的水化物和一种具有臭鸡蛋气味的气体,写出其化学方程式:
与热水反应仅生成X的最高价氧化物对应的水化物和一种具有臭鸡蛋气味的气体,写出其化学方程式:_______ 。
(6)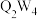 可用作火箭的燃料,1 mol
可用作火箭的燃料,1 mol 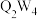 中所含的电子总数为
中所含的电子总数为_______  。
。
(1)Y在元素周期表中的位置为
(2)最简单氢化物的沸点:Q
(3)写出X元素形成的单质与Q的最高价氧化物对应的水化物的稀溶液发生反应的离子方程式:
(4)仅由W、Q、Z三种元素可形成化合物
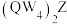 和
和 :
:①化合物
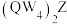 的名称为
的名称为②化合物
 含有化学键的类型为
含有化学键的类型为(5)化合物
 与热水反应仅生成X的最高价氧化物对应的水化物和一种具有臭鸡蛋气味的气体,写出其化学方程式:
与热水反应仅生成X的最高价氧化物对应的水化物和一种具有臭鸡蛋气味的气体,写出其化学方程式:(6)
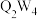 可用作火箭的燃料,1 mol
可用作火箭的燃料,1 mol 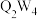 中所含的电子总数为
中所含的电子总数为 。
。
您最近一年使用:0次
2023-03-17更新
|
282次组卷
|
3卷引用:山西省2022-2023学年高一下学期3月联合考试化学试题
名校
解题方法
9 . 原子序数依次增大的A、B、C、D、E五种位于不同短周期的元素,可以两两形成多种原子个数比为 的化合物,其中的甲、乙、丙、丁4种化合物有两种属于离子化合物。A、B的原子序数之和是元素D的一半。B既是蛋白质的重要组成成分,也是某种化肥的组成部分。只有C为金属元素,焰色反应呈黄色。请回答下列问题:
的化合物,其中的甲、乙、丙、丁4种化合物有两种属于离子化合物。A、B的原子序数之和是元素D的一半。B既是蛋白质的重要组成成分,也是某种化肥的组成部分。只有C为金属元素,焰色反应呈黄色。请回答下列问题:
(1)元素E在周期表中的位置是_______ 。
(2)B和D形成原子个数比为 的化合物甲,其相对分子质量在170~190之间,且D的质量分数约为70%,则该化合物的化学式为:
的化合物甲,其相对分子质量在170~190之间,且D的质量分数约为70%,则该化合物的化学式为:_______ 。
(3)A和B形成的化合物乙为 ,在一定条件下可以
,在一定条件下可以 完全电离产生两种离子,其中一种为
完全电离产生两种离子,其中一种为 的离子,该物质在一定条件下的电离方程式为
的离子,该物质在一定条件下的电离方程式为_______ 。
(4)化合物 溶液在空气中长期放置会变质生成丙
溶液在空气中长期放置会变质生成丙 ,用化学方程式表示该过程
,用化学方程式表示该过程_______ 。
(5)D和E以 形成的化合物丁中所有原子均满足
形成的化合物丁中所有原子均满足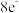 稳定结构,该化合物的电子式为
稳定结构,该化合物的电子式为_______ ;该物质遇水剧烈反应,产生有刺激性气味的混合气体X和Y,同时还有固体单质产生,已知X是能使品红溶液褪色的气体,Y在标准状态下的密度为 ,该上述过程对应的化学方程式为
,该上述过程对应的化学方程式为_______ 。某研究小组同学为确定干燥的X和Y混合气体中Y的存在,设计方案如下:把干燥的X和Y与干燥的 混合,出现白烟,则证明有Y气体,你认为此方案
混合,出现白烟,则证明有Y气体,你认为此方案_______ (填“正确”或“不正确)。
 的化合物,其中的甲、乙、丙、丁4种化合物有两种属于离子化合物。A、B的原子序数之和是元素D的一半。B既是蛋白质的重要组成成分,也是某种化肥的组成部分。只有C为金属元素,焰色反应呈黄色。请回答下列问题:
的化合物,其中的甲、乙、丙、丁4种化合物有两种属于离子化合物。A、B的原子序数之和是元素D的一半。B既是蛋白质的重要组成成分,也是某种化肥的组成部分。只有C为金属元素,焰色反应呈黄色。请回答下列问题:(1)元素E在周期表中的位置是
(2)B和D形成原子个数比为
 的化合物甲,其相对分子质量在170~190之间,且D的质量分数约为70%,则该化合物的化学式为:
的化合物甲,其相对分子质量在170~190之间,且D的质量分数约为70%,则该化合物的化学式为:(3)A和B形成的化合物乙为
 ,在一定条件下可以
,在一定条件下可以 完全电离产生两种离子,其中一种为
完全电离产生两种离子,其中一种为 的离子,该物质在一定条件下的电离方程式为
的离子,该物质在一定条件下的电离方程式为(4)化合物
 溶液在空气中长期放置会变质生成丙
溶液在空气中长期放置会变质生成丙 ,用化学方程式表示该过程
,用化学方程式表示该过程(5)D和E以
 形成的化合物丁中所有原子均满足
形成的化合物丁中所有原子均满足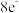 稳定结构,该化合物的电子式为
稳定结构,该化合物的电子式为 ,该上述过程对应的化学方程式为
,该上述过程对应的化学方程式为 混合,出现白烟,则证明有Y气体,你认为此方案
混合,出现白烟,则证明有Y气体,你认为此方案
您最近一年使用:0次
名校
解题方法
10 . 现有部分短周期元素的信息如表所示:
A、B、D三种单质(分别由X、Y、Z元素组成)和甲、乙、丙、丁、戊五种化合物之间的转化关系如图所示(某些条件已略去)。其中丁是一种筒能燃料,分子中含有18个电子,其组成元素与丙相同。
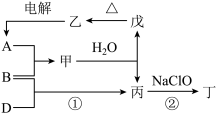
(1)元素X在周期表中的位置是______ ,其简单离子的结构示意图为______ 。
(2)单质B的电子式为______ 。
(3)丙中所含的化学键类型是______ (填序号)。
a.离子键 b.极性共价键 c.非极性共价键
(4)反应②中,0.5 mol 参加反应时转移1 mol电子,该反应的化学方程式为
参加反应时转移1 mol电子,该反应的化学方程式为______ 。
(5)一定条件下,A与 、C(石墨)反应只生成乙和碳化钛(
、C(石墨)反应只生成乙和碳化钛( ),二者均为某些高温结构陶瓷的主要成分,该反应的化学方程式为
),二者均为某些高温结构陶瓷的主要成分,该反应的化学方程式为______ 。
| 元素编号 | 元素性质或原子结构信息 |
| X | 第三周期元素中简单离子半径最小的元素 |
| Y | 其最简单氢化物丙的水溶液呈碱性 |
| Z | 原子核外电子数和所在周期数相等 |

(1)元素X在周期表中的位置是
(2)单质B的电子式为
(3)丙中所含的化学键类型是
a.离子键 b.极性共价键 c.非极性共价键
(4)反应②中,0.5 mol
 参加反应时转移1 mol电子,该反应的化学方程式为
参加反应时转移1 mol电子,该反应的化学方程式为(5)一定条件下,A与
 、C(石墨)反应只生成乙和碳化钛(
、C(石墨)反应只生成乙和碳化钛( ),二者均为某些高温结构陶瓷的主要成分,该反应的化学方程式为
),二者均为某些高温结构陶瓷的主要成分,该反应的化学方程式为
您最近一年使用:0次
2020-03-02更新
|
1103次组卷
|
7卷引用:2016届吉林省东北师范大学附属中学高三上第三次模拟化学试卷



