名校
1 . 短周期元素W、X、Y、Z原子序数依次增大。甲、乙、丙、丁、戊均由上述两种或三种元素组成,甲为淡黄色固体,乙和丁均为分子中含有10个电子的二元化合物,有关物质的转化关系如下图所示。下列说法正确的是
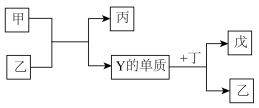

| A.W、X、Y形成的化合物一定为共价化合物 |
| B.简单离子半径:Y>Z>W |
| C.阴离子的还原性:Y>W |
| D.甲中阴阳离子个数比1∶1 |
您最近半年使用:0次
2021-07-12更新
|
284次组卷
|
3卷引用:山东省烟台市2020-2021学年高一下学期期末考试化学试题
2 .  、
、 、
、 、
、 为原子序数依次增大的短周期主族元素,
为原子序数依次增大的短周期主族元素, 的原子半径是所有短周期主族元素中最大的,
的原子半径是所有短周期主族元素中最大的, 的最外层电子是次外层的3倍,
的最外层电子是次外层的3倍, 的单质是一种半导体材料,
的单质是一种半导体材料, 的最外层电子数是
的最外层电子数是 的原子序数的一半,由
的原子序数的一半,由 、
、 、
、 三种元素形成的化合物
三种元素形成的化合物 的结构如图所示。下列叙述错误的是
的结构如图所示。下列叙述错误的是

 、
、 、
、 、
、 为原子序数依次增大的短周期主族元素,
为原子序数依次增大的短周期主族元素, 的原子半径是所有短周期主族元素中最大的,
的原子半径是所有短周期主族元素中最大的, 的最外层电子是次外层的3倍,
的最外层电子是次外层的3倍, 的单质是一种半导体材料,
的单质是一种半导体材料, 的最外层电子数是
的最外层电子数是 的原子序数的一半,由
的原子序数的一半,由 、
、 、
、 三种元素形成的化合物
三种元素形成的化合物 的结构如图所示。下列叙述错误的是
的结构如图所示。下列叙述错误的是
A.简单离子的半径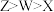 |
B. 单质的熔点高于 单质的熔点高于 单质 单质 |
C.化合物 中 中 都满足8电子稳定结构 都满足8电子稳定结构 |
D. 、 、 、 、 最高价氧化物对应的水化物之间均可以发生反应 最高价氧化物对应的水化物之间均可以发生反应 |
您最近半年使用:0次
名校
解题方法
3 . R、T、U、V、W属于短周期主族元素。R的原子半径在短周期主族元素中最大,T元素的原子最外层电子数是次外层电子数的3倍,U元素的原子L层电子数是M层电子数的2倍,V元素与U元素最外层电子数相同,W元素和T元素可以形成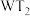 和
和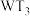 两种化合物。下列叙述正确的是
两种化合物。下列叙述正确的是
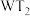 和
和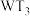 两种化合物。下列叙述正确的是
两种化合物。下列叙述正确的是| A.R与T形成的两种化合物中化学键类型相同 |
B.T、W简单氢化物的稳定性和熔沸点都是 |
C.简单离子半径: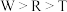 |
| D.这五种元素中电负性最大的是W元素 |
您最近半年使用:0次
4 . 随着原子序数的递增,八种短周期元素(用字母x、y、z……表示)的原子半径相对大小、最高正价或最低负价的变化如下图所示。
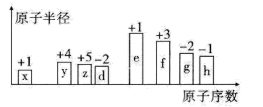
请回答下列问题:
(1)d的简单氢化物的沸点比同主族相邻元素的氢化物沸点___________ (填“高”或“低”),原因是:___________ ;x与e形成的化合物电子式为___________
(2)比较g、h常见离子的半径大小:___________ (填化学式,下同);比较e、f的最高价氧化物对应水化物的碱性强弱:___________ 。
(3)x、y、z、d四种元素能形成多种化合物。
①能形成离子化合物,其中一种x、y、z、d四种原子的个数比为5∶1∶1∶3,其化学式为___________ 。
②能形成共价化合物,写出其中一种的结构简式___________ 。

请回答下列问题:
(1)d的简单氢化物的沸点比同主族相邻元素的氢化物沸点
(2)比较g、h常见离子的半径大小:
(3)x、y、z、d四种元素能形成多种化合物。
①能形成离子化合物,其中一种x、y、z、d四种原子的个数比为5∶1∶1∶3,其化学式为
②能形成共价化合物,写出其中一种的结构简式
您最近半年使用:0次
名校
5 . X、Y、Z、R、W是原子序数依次增大的五种短周期元素。基态Y原子的电子总数是其最高能级电子数的2倍,Y和R同主族,Y和Z最外层电子数之和与W的最外层电子数相同。25℃时,X和W形成化合物的水溶液0.1mol/L时 。下列说法不正确的是
。下列说法不正确的是
 。下列说法不正确的是
。下列说法不正确的是A.电负性: |
| B.Y、Z、W三种元素组成的化合物的水溶液一定显碱性 |
C.简单离子的半径: |
| D.因H-O键的键能大于H-S键的键能,所以X与Y组成的简单分子比X与R组成的简单分子稳定 |
您最近半年使用:0次
2021-07-04更新
|
72次组卷
|
2卷引用:河南省2020-2021学年高二下学期领军考试7月联考化学试题
6 . 化合物A由X、Y、Z三种元素组成,其中X、Y、Z分别属于元素周期表第三、四、五周期中的常见元素。以A为起始物质经过转化后,三种元素分别存在于D、E、F和蓝色溶液ⅱ中。
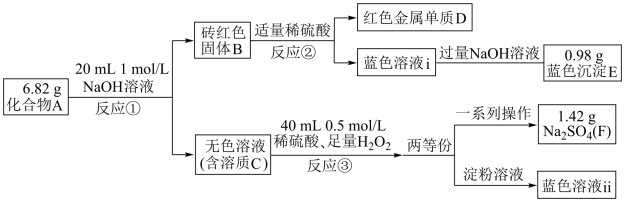
回答下列问题:
(1)实验室检验化合物A中含X元素的常用方法是_______ 。
(2)反应②的离子方程式是_______ 。
(3)蓝色溶液ⅱ说明A中含_______ 元素(填元素符号)。
(4)化合物A的化学式是_______ ,反应①的化学方程式为_______ 。

回答下列问题:
(1)实验室检验化合物A中含X元素的常用方法是
(2)反应②的离子方程式是
(3)蓝色溶液ⅱ说明A中含
(4)化合物A的化学式是
您最近半年使用:0次
解题方法
7 . A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如下图所示。A是短周期中原子半径最小的元素,A、B,C三种元素的原子序数之和等于D元素的原子序数,E是短周期中最活泼的金属元素。下列说法错误的是
| B | C |
| D |
| A.简单离子的半径大小关系:B>C>E |
| B.由A、B两种元素组成的离子化合物BA5中,阴、阳离子个数比为1∶1 |
| C.由C、D、E三种元素组成的某种化合物,其水溶液能与盐酸反应产生沉淀 |
| D.原子序数为116的位(Lv)元素与B元素同族 |
您最近半年使用:0次
8 . 下列实验结果不 能达成相应实验目的的是
| A | B | C | D | |
| 目的 | 探究温度对平衡移动的影响 | 比较元素的非金属性 | 探究△H与反应历程的关系 | 探究气体体积与的分子数的关系 |
| 实验方案 | 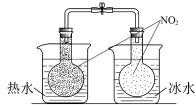 2NO2(g)  N2O4(g) △H<0 N2O4(g) △H<0 | 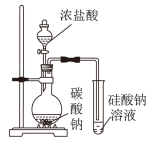 |  | 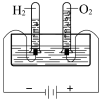 电解水(添加稀硫酸) |
| 结果 | 左侧气体颜色加深,右侧气体颜色变浅 | 烧瓶中产生气泡,试管中出现浑浊 | 测得△H=△H1+△H2 | H2与O2的体积比约为2∶1 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
9 . 下表为元素周期表的一部分,请参照元素①~⑩在表中的位置,回答下列问题:
(1)元素⑩在周期表中的位置是___________ ,⑦的原子结构示意图为___________ 。
(2)④、⑤、⑥的简单离子半径由大到小的顺序为___________ (用离子符号和“>”表示)。
(3)④⑧⑨的气态氢化物中,最稳定的是___________ (用名称表示),最高价氧化物对应水化物中,酸性最强的是___________ (用化学式表示)。
(4)⑤的最高价氧化物对应的水化物与⑦的最高价氧化物对应的水化物发生反应的离子方程式___________ 。
(5)下列五种物质中,①H2O ②CO2 ③Na2O2 ④NaOH ⑤NaBr,
只存在共价键的是___________ ,只存在离子键的是___________ ,既存在离子键又存在共价键的是___________ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||||||||||||
| ⑩ |
(2)④、⑤、⑥的简单离子半径由大到小的顺序为
(3)④⑧⑨的气态氢化物中,最稳定的是
(4)⑤的最高价氧化物对应的水化物与⑦的最高价氧化物对应的水化物发生反应的离子方程式
(5)下列五种物质中,①H2O ②CO2 ③Na2O2 ④NaOH ⑤NaBr,
只存在共价键的是
您最近半年使用:0次
10 . 短周期主族元素A、B、C、D、E常见稳定结构、相关信息、性质如表:
下列说法一定正确的是
| A+ | B2- | C | D的简单氢化物 | E的氢化物的水溶液 |
| 电子数为0 | 离子半径140pm | 常见化合价-2、+4、+6 | 正四面体 | 强酸溶液 |
| A.简单阴离子还原性:E>C |
| B.D与A形成的化合物的沸点低于B与A形成的化合物的沸点 |
| C.B和E形成的其中一种化合物具有强氧化性 |
| D.C的简单离子半径小于140pm |
您最近半年使用:0次



