名校
解题方法
1 . a、b、c、d为短周期元素,原子序数依次增大。a原子最外层电子数等于电子层数的3倍,a和b能组成两种常见的离子化合物,其中一种含两种化学键,d的最高价氧化物对应的水化物和气态氢化物都是强酸。向d的氢化物的水溶液中逐滴加入bca2溶液,开始没有沉淀;随着bca2溶液的不断滴加,逐渐产生白色沉淀。下列推断正确的是
| A.最高价氧化物对应水化物的碱性:b<c |
| B.元素b所在纵列的单质沸点从上到下依次降低 |
| C.工业上电解熔融cd3可得到c的单质 |
| D.b、c、d最高价氧化物对应水化物之间可两两反应 |
您最近半年使用:0次
2021-09-15更新
|
144次组卷
|
2卷引用:河北正定中学2020-2021学年高二上学期开学考试化学试题
解题方法
2 . 四种短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,已知四种元素的原子最外层电子数之和为21,下列说法不正确的是
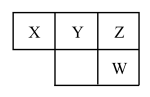

| A.X位于第二周期第ⅣA族 |
B.简单离子半径: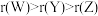 |
| C.W的氧化物对应水化物的酸性一定比Y的强 |
| D.X、Y、W三种元素的最高化合价依次升高 |
您最近半年使用:0次
2021-09-03更新
|
359次组卷
|
5卷引用:浙江省百强校2022届高三上学期开学联考化学试题
浙江省百强校2022届高三上学期开学联考化学试题(已下线)2022年1月浙江省普通高校招生选考科目考试化学仿真模拟试卷C(已下线)解密05 物质结构 元素周期律(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)一轮巩固卷3-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(浙江专用)(已下线)专题卷10 根据元素周期表片段和物质转化关系元素推断-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)
名校
3 . 短周期主族元素A、B、C、D,原子序数依次增大。A、C的原子序数的差为8,A、B、C三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半。下列叙述正确的是
| A.原子半径:A<B<C<D | B.单质B制作的容器可用来盛放浓硝酸 |
| C.A、C形成的物质属于两性氧化物 | D.元素D在周期表中位于第三周期、ⅥA族 |
您最近半年使用:0次
解题方法
4 . 已知W、X、Y、Z均为短周期主族元素,W与X同周期且相邻,W与Y同主族,W、X与Y的原子序数之和为31, Z与其他三种元素既不同周期、也不同主族。下列说法中,正确的是
| A.原子半径大小顺序为Z<Y<W<X |
| B.四种元素中,X元素的非金属性最强 |
| C.常温常压下,四种元素各自形成的单质均为气体 |
| D.W、X、Z三种元素可形成化学式为Z4X2W3型的离子化合物 |
您最近半年使用:0次
名校
解题方法
5 . 短周期主族元素W、X、Y、Z的原子序数依次增大,W与X、Y与Z分别同周期,其中只有Y为金属。W、Y、Z最外层电子数之和为12;X与Z形成的化合物是光导纤维的主要成分。下列说法不正确的是
| A.简单离子半径:W>X>Y |
| B.气态氢化物稳定性:W>X>Z |
| C.Y的简单阳离子和它的含氧酸根离子反应可生成白色沉淀 |
| D.W和Z元素能形成一种新型无机非金属材料,具有硬度大熔点高的特性 |
您最近半年使用:0次
解题方法
6 . 元素W、X、Y、Z在周期表中的相对位置如图所示,且四种元素的原子最外层电子数之和为24。下到说法不正确的是
| W | X | |
| Y | Z |
| A.最高价氧化物对应水化物的酸性:Y>Z |
| B.W的气态氢化物与其最高价氧化物的水化物反应生成离子化合物 |
| C.在元素周期表中,117号元素与Z元素位于同一主族 |
| D.工业上常用YX2漂白纸浆、毛、丝等 |
您最近半年使用:0次
7 . 现有A、B、C、D、E、F六种短周期元素,其相关性质信息如下。请回答下列问题:
(1)元素D在元素周期表中的位置为_______ ,其原子的结构示意图为_______ 。
(2)A、C、D对应的简单离子的半径由大到小的排序是_______ (用离子符号表示)。
(3)B的最简单氢化物的稳定性_______ (填“>”、“<”或“=”) 的稳定性。
的稳定性。
(4) 溶液中存在的化学键类型有
溶液中存在的化学键类型有_______ (填“离子键”、“共价键”或“离子键和共价键”)。A的最高价氧化物的水化物与 溶液反应的离子方程式为
溶液反应的离子方程式为_______ 。
(5)用电子式表示化合物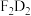 的形成过程
的形成过程_______ 。
(6)已知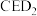 是一种强氧化性漂白剂,它在碱性环境中稳定存在。在碱性条件下,
是一种强氧化性漂白剂,它在碱性环境中稳定存在。在碱性条件下,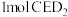 和
和 恰好完全反应,该反应的离子方程式为
恰好完全反应,该反应的离子方程式为_______ 。
| 元素 | 特征 | 元素 | 特征 |
| A | 常见金属,其最高价氧化物对应的水化物可以溶于强碱 | D | 在地壳中含量最多 |
| B | 常见化肥的主要元素,单质常温下呈气态 | E | 单质为黄绿色有毒气体 |
| C | 在短周期主族元素中,原子半径最大 | F | 原子的核外电子只有1个 |
(2)A、C、D对应的简单离子的半径由大到小的排序是
(3)B的最简单氢化物的稳定性
 的稳定性。
的稳定性。(4)
 溶液中存在的化学键类型有
溶液中存在的化学键类型有 溶液反应的离子方程式为
溶液反应的离子方程式为(5)用电子式表示化合物
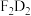 的形成过程
的形成过程(6)已知
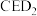 是一种强氧化性漂白剂,它在碱性环境中稳定存在。在碱性条件下,
是一种强氧化性漂白剂,它在碱性环境中稳定存在。在碱性条件下,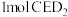 和
和 恰好完全反应,该反应的离子方程式为
恰好完全反应,该反应的离子方程式为
您最近半年使用:0次
8 . 短周期元素X、Y、Z的原子序数依次增加,r与q是由这些元素组成的二元化合物,n、p、m分别是元素X、Y、Z的单质,m通常为黄绿色气体,r与q生成s的反应产生白烟。下列说法正确的是


| A.可用直接加热s的方法制q | B.r的热稳定性比H2S强 |
| C.元素Z的含氧酸均为强酸 | D.q的沸点比PH3低 |
您最近半年使用:0次
填空题
|
适中(0.65)
|
9 . 现有A、B、C、D、E、F、G七种短周期主族元素,其原子序数依次增大。已知A、D位于同一主族,D是短周期中原子半径最大的。B、E最外层电子数是最内层电子数的2倍。C、F的最外层电子数相等,且C、F的原子序数之和为A、D原子序数之和的两倍。
(1)A、C、D、F形成的简单离子半径由大到小的顺序是___________ (用元素符号填写)。
(2)B、E、F、G最高价氧化物对应的水化物酸性最强的是___________ (用化学式填写)。
(3)下列事实能说明G元素的非金属性比F元素的非金属性强的是(填序号)______
A.G单质与Na2S溶液反应溶液变浑浊
B.F的氢化物的酸性比G的氢化物酸性弱
C.G和F两元素的简单氢化物受热分解,前者的分解温度高
(4)A、C、D、F四种元素形成的化合物M和N在溶液中相互反应的离子方程式是___________ 。
(1)A、C、D、F形成的简单离子半径由大到小的顺序是
(2)B、E、F、G最高价氧化物对应的水化物酸性最强的是
(3)下列事实能说明G元素的非金属性比F元素的非金属性强的是(填序号)
A.G单质与Na2S溶液反应溶液变浑浊
B.F的氢化物的酸性比G的氢化物酸性弱
C.G和F两元素的简单氢化物受热分解,前者的分解温度高
(4)A、C、D、F四种元素形成的化合物M和N在溶液中相互反应的离子方程式是
您最近半年使用:0次
名校
10 . 下表为元素周期表的一部分,针对表中①~⑧元素填空,回答相关问题。
(1)化学性质最稳定的是_______ (填元素符号)。
(2)原子半径最大的是_______ (填元素符号);离子半径最大的是_______ (填离子符号);得电子能力最强的是_______ (填元素符号)。
(3)④⑤形成的化合物中,含有非极性共价键的化合物的电子式为_______ 。
(4)⑧单质与⑤最高价氧化物的水化物反应制得84消毒液的离子方程式为_______ 。
(5)③④两种元素组成的某化合物,常温下是一种红棕色气体,该气体与水发生反应的化学方程式为_______ 。
(6)比较②和⑦两种元素得电子能力强弱,其简单实验方案是_______ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 |
| 一 | ① | ||||||
| 二 | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)原子半径最大的是
(3)④⑤形成的化合物中,含有非极性共价键的化合物的电子式为
(4)⑧单质与⑤最高价氧化物的水化物反应制得84消毒液的离子方程式为
(5)③④两种元素组成的某化合物,常温下是一种红棕色气体,该气体与水发生反应的化学方程式为
(6)比较②和⑦两种元素得电子能力强弱,其简单实验方案是
您最近半年使用:0次
2021-07-13更新
|
224次组卷
|
2卷引用:山东省青岛胶州市2020-2021学年高一下学期期末考试化学试题



