解题方法
1 . 根据提供条件推断元素,并按要求填空:
(1)原子核外有3个电子层,其最外层电子数为7,最高价氧化物化学式____ ,最高价氧化物对应水化物化学式____ ,其单质与氢气反应的化学方程式为____ 。
(2)第三周期元素,其最外层电子数与电子层数相同。该元素最高价氧化物的化学式____ ,最高价氧化物对应水化物与氢氧化钠溶液反应的化学方程式为____ 。
(3)原子序数依次递增的同周期4种元素,它们氢化物的质子数与电子数都与Ar相同,这些氢化物的化学式分别为____ 、____ 、____ 、____ 。
(4)某元素的最高正价与最低负价的代数和为4,且最高价氧化物中含氧元素质量分数为60%。则该元素最高价氧化物的化学式为____ 。
(1)原子核外有3个电子层,其最外层电子数为7,最高价氧化物化学式
(2)第三周期元素,其最外层电子数与电子层数相同。该元素最高价氧化物的化学式
(3)原子序数依次递增的同周期4种元素,它们氢化物的质子数与电子数都与Ar相同,这些氢化物的化学式分别为
(4)某元素的最高正价与最低负价的代数和为4,且最高价氧化物中含氧元素质量分数为60%。则该元素最高价氧化物的化学式为
您最近半年使用:0次
解题方法
2 . 现有4种短周期主族元素A、B、C和D,相关信息如表:
下列说法不正确 的是
| 元素 | 相关信息 |
| A | 单质常温下为气体,被人看作理想的“绿色能源” |
| B | 地壳中含量最多的元素 |
| C | 焰色反应呈黄色 |
| D | 与C同周期,且D的简单离子半径是同周期中最小的 |
| A.与B同主族的元素有116号元素 |
| B.原子半径C>D>B>A |
| C.C的氢化物能和B的最简单氢化物反应生成A的单质 |
| D.C和D最高价氧化物对应的水化物之间不可能发生化学反应 |
您最近半年使用:0次
3 . 已知短周期元素X、Y、Z在周期表中的位置如图:

按要求回答下列问题:
(1)若Y的-2价阴离子结构示意图为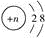 ,则
,则
①Y元素在周期表中位于第___ 周期第___ 族。
②Y与X形成的化合物X2Y2中含有的化学键是___ ,其电子式为___ 。
③用电子式的形式表示X与Z形成化合物的过程:__ 。
(2)若Y元素原子核外最外层电子数是次外层电子数的2倍,则Y元素形成的氢化物的分子空间构型为___ ,其结构式为___ ,最高价氧化物的分子空间构型为___ ,其电子式为__ 。

按要求回答下列问题:
(1)若Y的-2价阴离子结构示意图为
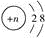 ,则
,则①Y元素在周期表中位于第
②Y与X形成的化合物X2Y2中含有的化学键是
③用电子式的形式表示X与Z形成化合物的过程:
(2)若Y元素原子核外最外层电子数是次外层电子数的2倍,则Y元素形成的氢化物的分子空间构型为
您最近半年使用:0次
名校
4 . 下列为元素周期表中的一部分,用化学式或元素符号回答下列问题。
(1)11种元素中,化学性质最不活泼的是___________ ,原子半径最小的是___________ 。
(2)①②⑤中最高价氧化物的水化物,碱性最强的是___________ 。
(3)②③④中形成的简单离子半径由大到小的顺序是___________ 。
(4)元素⑦的氢化物电子式为___________ ,该氢化物常温下和元素②的单质反应的离子方程式是___________ 。
(5)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为___________ 。
(6)⑧⑨⑪三种元素形成的气态氢化物最稳定的是___________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑦ | ⑪ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)①②⑤中最高价氧化物的水化物,碱性最强的是
(3)②③④中形成的简单离子半径由大到小的顺序是
(4)元素⑦的氢化物电子式为
(5)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为
(6)⑧⑨⑪三种元素形成的气态氢化物最稳定的是
您最近半年使用:0次
2021-06-16更新
|
214次组卷
|
3卷引用:江西省石城中学2020-2021学年高一下学期第二次月考化学试题
名校
5 . X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期,W是短周期主族元素中原子半径最大的,X原子最外层电子数是核外电子层数的3倍,Y的最高正价 与最低负价代数和为6。下列说法正确的是
| A.Y元素最高价氧化物对应的水化物化学式H2YO4 |
| B.X与W形成的两种化合物中,阴.阳离子物质的量之比均为1:2 |
| C.Y.Z两种元素气态氢化物中,Z的气态氢化物最稳定 |
| D.原子半径由小到大的顺序为:X<Z<Y |
您最近半年使用:0次
名校
解题方法
6 . 化合物M的结构如图所示,X、Y、Z、W为原子序数递增的短周期主族元素,Y在自然界中以化合态的形式存在,Z的最外层电子数是其电子层数的3倍。下列说法正确的是
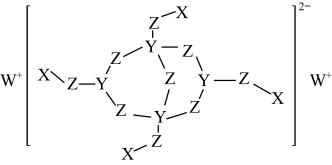

| A.元素Y、元素Z、元素W的单质熔点依次升高 |
| B.X2Z分子间存在氢键,因此X2Z分子稳定性较强 |
| C.W与Z形成的两种常见离子化合物中阴阳离子个数比相同 |
| D.化合物M中各原子或离子均达到2电子或8电子稳定结构 |
您最近半年使用:0次
2021-06-04更新
|
374次组卷
|
2卷引用:湖南师大附中2021届高三第一次模拟考试化学试题
解题方法
7 . 下图是元素周期表的一部分,A、B、C均为短周期元素,A、C两种元素的原子核外电子数之和等于B的质子数,B的原子核内质子数和中子数相等。回答:
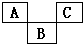
(1)写出元素符号:A___________ ;C___________ 。
(2)A的氢化物的电子式为___________ ;A的氢化物与其最高价氧化物的水化物反应的化学方程式为___________

(1)写出元素符号:A
(2)A的氢化物的电子式为
您最近半年使用:0次
名校
解题方法
8 . 短周期主族元素A,B,C,D,E,F的原子序数依次增大,它们的原子核外电子层数之和为13。B原子的最外层电子数是次外层电子数的2倍,C,D是空气中含量最多的两种元素,D,E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(1)D在周期表中的位置是___ ,写出实验室制备单质F的离子方程式___ 。
(2)化合物甲、乙由A、B、D、E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为:___ 。
(3)由C,D,E,F形成的简单离子的离子半径由大到小的顺序是__ (用元素离子符号表示)。
(4)元素B和F的非金属性强弱,B的非金属性___ 于F(填“强”或“弱”),并用化学方程式证明上述结论__ 。
II.以CA3代替氢气研发燃料电池是当前科研的一个热点。
(5)CA3燃料电池使用的电解质溶液是2mol/L的KOH溶液,电池反应为: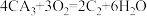 .该电池负极的电极反应式为
.该电池负极的电极反应式为___ ;每消耗3.4gCA3转移的电子数目为___ 。
(1)D在周期表中的位置是
(2)化合物甲、乙由A、B、D、E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为:
(3)由C,D,E,F形成的简单离子的离子半径由大到小的顺序是
(4)元素B和F的非金属性强弱,B的非金属性
II.以CA3代替氢气研发燃料电池是当前科研的一个热点。
(5)CA3燃料电池使用的电解质溶液是2mol/L的KOH溶液,电池反应为:
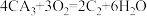 .该电池负极的电极反应式为
.该电池负极的电极反应式为
您最近半年使用:0次
2021-05-27更新
|
249次组卷
|
2卷引用:黑龙江省大庆市铁人中学2020-2021学年高一下学期期中考试化学试题
9 . 短周期主族元素X、Y、Z、W的原子序数依次增大,元素Y是地壳中含量最多的元素,X与Z同主族且二者可形成离子化合物,W的最外层电子数是其电子层数的2倍,下列说法正确的是
| A.非金属性:X<Y<W |
| B.由这四种元素组成的化合物水溶液可呈酸性 |
| C.元素W的简单氢化物为强酸 |
| D.原子半径:Y<Z<W |
您最近半年使用:0次
解题方法
10 . 如表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
(1)元素⑩名称为___ ,在周期表中的位置___ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是___ ,碱性最强的化合物的电子式是:____ 。
(3)元素④的最高价氧化物对应水化物与⑦最高价氧化物对应水化物在溶液中发生反应的化学方程式:___ 。
(4)⑥、⑦、⑨三种元素形成的离子,离子半径由大到小的顺序是(用离子符号表示)___ 。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是
(3)元素④的最高价氧化物对应水化物与⑦最高价氧化物对应水化物在溶液中发生反应的化学方程式:
(4)⑥、⑦、⑨三种元素形成的离子,离子半径由大到小的顺序是(用离子符号表示)
您最近半年使用:0次



