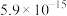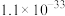1 . 1934年,约里奥—居里夫妇在核反应中用α粒子(氦核 )轰击金属铝,得到磷,开创了人工放射性核素的先河,其核反应为
)轰击金属铝,得到磷,开创了人工放射性核素的先河,其核反应为 。下列化学用语正确的是
。下列化学用语正确的是
 )轰击金属铝,得到磷,开创了人工放射性核素的先河,其核反应为
)轰击金属铝,得到磷,开创了人工放射性核素的先河,其核反应为 。下列化学用语正确的是
。下列化学用语正确的是A.基态A1原子的价层电子轨道表示式为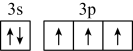 |
| B.He没有共价键,不是非极性分子 |
C.明矾的化学式为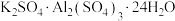 |
| D.基态P原子中p能级的轨道总数为3 |
您最近一年使用:0次
2024-06-02更新
|
269次组卷
|
3卷引用:广东省华南师范大学附属中学2024届高三下学期高考适应性练习(4月)化学试题
广东省华南师范大学附属中学2024届高三下学期高考适应性练习(4月)化学试题(已下线)山东省青岛市2023-2024学年高三下学期第三次模拟考试化学试题甘肃省陇南市部分学校2023-2024学年高三下学期化学押题考试(三模)化学试题
名校
2 . 下列化学用语的表达正确的是
A.H2S的电子式为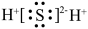 |
B.BaSO4的电离方程式为BaSO4⇌Ba2++ |
| C.中子数为10的氧的同位素为18O |
D.基态O原子核外电子轨道表示式: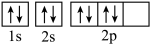 |
您最近一年使用:0次
2024-05-30更新
|
189次组卷
|
2卷引用:广东省梅州市梅江区梅州中学2024届高三下学期5月模拟考试化学试题
名校
解题方法
3 . 下列化学用语或图示表达正确 的是
A.溴的简化电子排布式: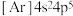 |
B.基态24Cr原子的价层电子轨道表示式为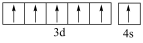 |
C.1-丁醇的键线式: |
D.NH3分子的VSEPR模型为 |
您最近一年使用:0次
4 . 金属钛(Ti)重量轻、强度高、抗腐蚀能力,在航空航天、医疗器械等工业领域有着重要用途。目前生产钛的方法之一是将金红石( )转化为
)转化为 ,再进一步还原得到钛。
,再进一步还原得到钛。
(1)基态Ti原子的价电子轨道表示式:______ 。
(2) 转化为
转化为 有直接氯化法(Ⅰ)和碳氯化法(Ⅱ)。
有直接氯化法(Ⅰ)和碳氯化法(Ⅱ)。
Ⅰ.

Ⅱ.

已知: 的燃烧热为393.5
的燃烧热为393.5 ',
', 的燃烧热为283.0
的燃烧热为283.0
①
______ 。
②碳氯化反应过程中CO和 可以相互转化,如图1所示,下列关于碳氯化反应说法正确的是
可以相互转化,如图1所示,下列关于碳氯化反应说法正确的是______ 。 生成CO反应为放热反应
生成CO反应为放热反应
B.升高温度, 平衡转化率减小
平衡转化率减小
C.增大压强,碳氯化反应平衡向正反应方向移动
D.如图2所示 晶胞中
晶胞中 位于
位于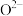 所构成的正八面体的体心,则
所构成的正八面体的体心,则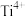 的配位数是6
的配位数是6
③碳氯化法中生成CO比生成 更有利于
更有利于 转化为
转化为 ,从熵变角度分析可能的原因是
,从熵变角度分析可能的原因是______ 。
(3)经光谱分析在碳氯化反应中有光气( )生成,后
)生成,后 继续反应,有理论认为机理如下:
继续反应,有理论认为机理如下: 含有
含有______ 个σ键,决速步骤的反应方程式为______ 。
(4)在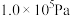 ,将
,将 、C、
、C、 以物质的量比1∶2.2∶2进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。
以物质的量比1∶2.2∶2进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。 的平衡常数
的平衡常数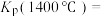
______ Pa。
②图中显示,在200℃平衡时 几乎完全转化为
几乎完全转化为 ,但实际生产中反应温度却远高于此温度,其原因是
,但实际生产中反应温度却远高于此温度,其原因是______ 。
 )转化为
)转化为 ,再进一步还原得到钛。
,再进一步还原得到钛。(1)基态Ti原子的价电子轨道表示式:
(2)
 转化为
转化为 有直接氯化法(Ⅰ)和碳氯化法(Ⅱ)。
有直接氯化法(Ⅰ)和碳氯化法(Ⅱ)。Ⅰ.


Ⅱ.


已知:
 的燃烧热为393.5
的燃烧热为393.5 ',
', 的燃烧热为283.0
的燃烧热为283.0
①

②碳氯化反应过程中CO和
 可以相互转化,如图1所示,下列关于碳氯化反应说法正确的是
可以相互转化,如图1所示,下列关于碳氯化反应说法正确的是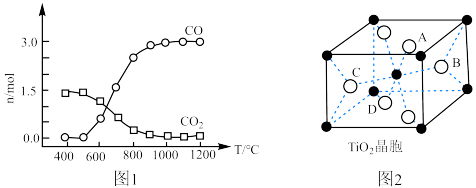
 生成CO反应为放热反应
生成CO反应为放热反应B.升高温度,
 平衡转化率减小
平衡转化率减小C.增大压强,碳氯化反应平衡向正反应方向移动
D.如图2所示
 晶胞中
晶胞中 位于
位于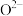 所构成的正八面体的体心,则
所构成的正八面体的体心,则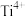 的配位数是6
的配位数是6③碳氯化法中生成CO比生成
 更有利于
更有利于 转化为
转化为 ,从熵变角度分析可能的原因是
,从熵变角度分析可能的原因是(3)经光谱分析在碳氯化反应中有光气(
 )生成,后
)生成,后 继续反应,有理论认为机理如下:
继续反应,有理论认为机理如下: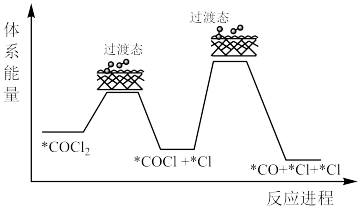
 含有
含有(4)在
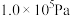 ,将
,将 、C、
、C、 以物质的量比1∶2.2∶2进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。
以物质的量比1∶2.2∶2进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。
 的平衡常数
的平衡常数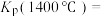
②图中显示,在200℃平衡时
 几乎完全转化为
几乎完全转化为 ,但实际生产中反应温度却远高于此温度,其原因是
,但实际生产中反应温度却远高于此温度,其原因是
您最近一年使用:0次
2024-05-20更新
|
588次组卷
|
2卷引用:广东省汕头市2024届高三二模考试化学试
解题方法
5 . 工业上,处理低品位黄铜矿[二硫化亚铁铜( )]常采用生物堆浸法。堆浸所得的溶液可用于制备绿矾(
)]常采用生物堆浸法。堆浸所得的溶液可用于制备绿矾( )和胆矾(
)和胆矾( )。相关流程如下图。
)。相关流程如下图。 1.0~6.0范围内可保持活性。
1.0~6.0范围内可保持活性。
②金属离子沉淀的pH如下表。
(1)Cu2+价电子轨道表示式为___________ ,生物堆浸前,需先将矿石进行研磨,目的是___________ 。
(2)生物堆浸过程的反应在T。f细菌的作用下进行,主要包括两个阶段,第一阶段的反应为: 。第二阶段反应为
。第二阶段反应为 继续被氧化转变成
继续被氧化转变成 ,反应的离子方程式为
,反应的离子方程式为___________ 。
(3)结合已知推断:生物堆浸过程中,应控制溶液的 在
在___________ 范围内。
(4)过程Ⅰ中,加入 固体还原堆浸液中的
固体还原堆浸液中的 ,得到溶液X。为判断堆浸液中
,得到溶液X。为判断堆浸液中 是否被还原完全,可取少量溶液X,向其中加入
是否被还原完全,可取少量溶液X,向其中加入___________ ,说明Fe3+已被完全还原。
(5)过程Ⅱ中,用 和稀硫酸处理后,
和稀硫酸处理后,
完全溶解 ,用离子方程式表示 的作用是
的作用是___________ 。
(6)绿矾的纯度可通过 滴定法测定。取
滴定法测定。取 绿矾晶体,加适量稀硫酸溶解。用物质的量浓度为cmol/L的
绿矾晶体,加适量稀硫酸溶解。用物质的量浓度为cmol/L的 溶液滴定,滴定终点的判定方法是
溶液滴定,滴定终点的判定方法是___________ 。至恰好完全反应时,消耗 溶液的体积为
溶液的体积为 。绿矾晶体质量分数的计算式为
。绿矾晶体质量分数的计算式为___________ 。
 )]常采用生物堆浸法。堆浸所得的溶液可用于制备绿矾(
)]常采用生物堆浸法。堆浸所得的溶液可用于制备绿矾( )和胆矾(
)和胆矾( )。相关流程如下图。
)。相关流程如下图。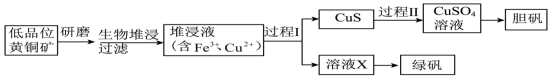
 1.0~6.0范围内可保持活性。
1.0~6.0范围内可保持活性。②金属离子沉淀的pH如下表。
| Fe3+ | Cu2+ | Fe2+ | |
| 开始沉淀时的pH | 1.5 | 4.2 | 6.3 |
| 完全沉淀时的pH | 2.8 | 6.7 | 8.3 |
(2)生物堆浸过程的反应在T。f细菌的作用下进行,主要包括两个阶段,第一阶段的反应为:
 。第二阶段反应为
。第二阶段反应为 继续被氧化转变成
继续被氧化转变成 ,反应的离子方程式为
,反应的离子方程式为(3)结合已知推断:生物堆浸过程中,应控制溶液的
 在
在(4)过程Ⅰ中,加入
 固体还原堆浸液中的
固体还原堆浸液中的 ,得到溶液X。为判断堆浸液中
,得到溶液X。为判断堆浸液中 是否被还原完全,可取少量溶液X,向其中加入
是否被还原完全,可取少量溶液X,向其中加入(5)过程Ⅱ中,用
 和稀硫酸处理后,
和稀硫酸处理后,
 的作用是
的作用是(6)绿矾的纯度可通过
 滴定法测定。取
滴定法测定。取 绿矾晶体,加适量稀硫酸溶解。用物质的量浓度为cmol/L的
绿矾晶体,加适量稀硫酸溶解。用物质的量浓度为cmol/L的 溶液滴定,滴定终点的判定方法是
溶液滴定,滴定终点的判定方法是 溶液的体积为
溶液的体积为 。绿矾晶体质量分数的计算式为
。绿矾晶体质量分数的计算式为
您最近一年使用:0次
解题方法
6 . 某合作学习小组将铜片放进氯化铁溶液中,观察到溶液呈无色,产生红褐色固体,铜片表面有白色物质。
Ⅰ.探究红褐色固体成分
(1)过滤得到红褐色固体,所需的仪器有___________ (填标号)。___________ 溶液,溶液变血红色,证明是氢氧化铁。
②产生氢氧化铁的原因可能是___________ (用化学方程式表示)。
Ⅱ.查阅资料:CuCl是白色难溶物
(3)探究产生白色物质的原因。设计实验方案如下:
①由以上实验可知,产生白色物质的条件是___________ 。
②实验2生成白色物质的化学方程式为:___________ 。
③请你从氧化还原反应规律角度分析实验1中未产生白色物质的原因___________ 。
(4)以石墨为电极电解 溶液,发现在石墨上析出的铜在切断电源后消失。从电化学角度进行分析,铜消失的原因为
溶液,发现在石墨上析出的铜在切断电源后消失。从电化学角度进行分析,铜消失的原因为___________ 。
(5)基于上述分析,用 溶液腐蚀覆铜板效果不理想。查阅资料:工业上常用
溶液腐蚀覆铜板效果不理想。查阅资料:工业上常用 、KCl、盐酸混合物腐蚀覆铜板,原理为:
、KCl、盐酸混合物腐蚀覆铜板,原理为: 。
。
①基态 的价电子轨道表示式为
的价电子轨道表示式为___________ 。
②KCl的作用是___________ 。
(6)氧化还原反应的应用十分广泛。写出一种氧化剂在生活中的应用___________ 。
Ⅰ.探究红褐色固体成分
(1)过滤得到红褐色固体,所需的仪器有
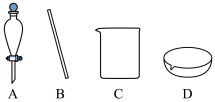
②产生氢氧化铁的原因可能是
Ⅱ.查阅资料:CuCl是白色难溶物
(3)探究产生白色物质的原因。设计实验方案如下:
| 实验 | 铜粉/g | 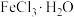 /g /g | 蒸馏水/mL | 实验现象 |
| 1 | 0.1 | 1.8 | 2 | 棕黄色溶液变为墨绿色 |
| 2 | 0.5 | 1.8 | 2 | 棕黄色溶液变为白色浊液 |
②实验2生成白色物质的化学方程式为:
③请你从氧化还原反应规律角度分析实验1中未产生白色物质的原因
(4)以石墨为电极电解
 溶液,发现在石墨上析出的铜在切断电源后消失。从电化学角度进行分析,铜消失的原因为
溶液,发现在石墨上析出的铜在切断电源后消失。从电化学角度进行分析,铜消失的原因为(5)基于上述分析,用
 溶液腐蚀覆铜板效果不理想。查阅资料:工业上常用
溶液腐蚀覆铜板效果不理想。查阅资料:工业上常用 、KCl、盐酸混合物腐蚀覆铜板,原理为:
、KCl、盐酸混合物腐蚀覆铜板,原理为: 。
。①基态
 的价电子轨道表示式为
的价电子轨道表示式为②KCl的作用是
(6)氧化还原反应的应用十分广泛。写出一种氧化剂在生活中的应用
您最近一年使用:0次
解题方法
7 .  是重要的化工原料,在生产和生活中都发挥着重要作用。
是重要的化工原料,在生产和生活中都发挥着重要作用。
(1)配合物广泛存在于自然界,其中 能与
能与 形成深蓝色
形成深蓝色 溶液。
溶液。
①基态 的3d电子轨道表示式为
的3d电子轨道表示式为_______ 。
② 的配位原子是
的配位原子是_______ ,氨气中H—N—H的键角小于配合物中H—N—H的键角,其原因是_______ 。
(2)氨是制取硝酸的重要原料。氨的催化氧化过程主要有以下两个反应:
Ⅰ.

Ⅱ.

①反应

_______ 。
②不同温度下氨催化氧化的平衡常数如下(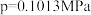 );
);
下列说法正确的是_______ 。
A.如果对反应不加控制,氨和氧气反应的最终产物主要是
B.为使反应有利于向生成更多的NO方向进行,不必关注热力学问题(平衡移动问题),需要关注动力学问题(反应速率问题)
C.在实际生产中,需采用高压氧化,以利于提高NO的产率
D.反应中需控制氨氧比、选择性催化剂的形状、气固相接触时间等
(3)已知可通过下列方法合成尿素:
第一步:
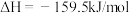
第二步:在体积为5 L的密闭容器中加入1 mol 和4 mol
和4 mol  ,在一定条件下反应进行到10 min时,测得
,在一定条件下反应进行到10 min时,测得 和尿素的物质的量均为0.25 mol,15 min后,测得
和尿素的物质的量均为0.25 mol,15 min后,测得 的物质的量为0.1 mol,如图所示。
的物质的量为0.1 mol,如图所示。
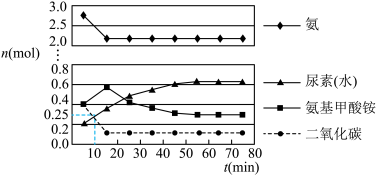
①若用单位时间内物质的量的变化来表示固体或纯液体的反应速率,则10 min内第一步反应中生成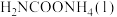 (氨基甲酸铵)的平均反应速率为
(氨基甲酸铵)的平均反应速率为_______ 。
②反应进行15分钟后,随着时间的变化,尿素和氨基甲酸铵的物质的量变化比较明显,但氨气和二氧化碳的物质的量基本不变,其主要原因是_______ ,第一步反应的平衡常数
_______ (列出算式即可)。
 是重要的化工原料,在生产和生活中都发挥着重要作用。
是重要的化工原料,在生产和生活中都发挥着重要作用。(1)配合物广泛存在于自然界,其中
 能与
能与 形成深蓝色
形成深蓝色 溶液。
溶液。①基态
 的3d电子轨道表示式为
的3d电子轨道表示式为②
 的配位原子是
的配位原子是(2)氨是制取硝酸的重要原料。氨的催化氧化过程主要有以下两个反应:
Ⅰ.


Ⅱ.


①反应


②不同温度下氨催化氧化的平衡常数如下(
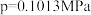 );
);| 温度(℃) | 300 | 500 | 700 | 900 | 1100 |
反应Ⅰ( ) ) | 6.3×1041 | 1.1×1026 | 2.1×1019 | 3.8×1015 | 3.4×1011 |
反应Ⅱ( ) ) | 7.3×1056 | 7.1×1034 | 2.6×1025 | 1.5×1020 | 6.7×1016 |
A.如果对反应不加控制,氨和氧气反应的最终产物主要是

B.为使反应有利于向生成更多的NO方向进行,不必关注热力学问题(平衡移动问题),需要关注动力学问题(反应速率问题)
C.在实际生产中,需采用高压氧化,以利于提高NO的产率
D.反应中需控制氨氧比、选择性催化剂的形状、气固相接触时间等
(3)已知可通过下列方法合成尿素:
第一步:

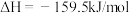
第二步:在体积为5 L的密闭容器中加入1 mol
 和4 mol
和4 mol  ,在一定条件下反应进行到10 min时,测得
,在一定条件下反应进行到10 min时,测得 和尿素的物质的量均为0.25 mol,15 min后,测得
和尿素的物质的量均为0.25 mol,15 min后,测得 的物质的量为0.1 mol,如图所示。
的物质的量为0.1 mol,如图所示。
①若用单位时间内物质的量的变化来表示固体或纯液体的反应速率,则10 min内第一步反应中生成
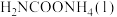 (氨基甲酸铵)的平均反应速率为
(氨基甲酸铵)的平均反应速率为②反应进行15分钟后,随着时间的变化,尿素和氨基甲酸铵的物质的量变化比较明显,但氨气和二氧化碳的物质的量基本不变,其主要原因是

您最近一年使用:0次
解题方法
8 . 化学符号诠释着物质组成的规律。下列化学符号表示正确的是
| A.C2H4的结构简式为CH2CH2 |
B.CO2的电子式为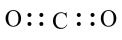 |
C.H2O的球棍模型为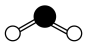 |
D.基态Fe3+价层电子轨道表示式为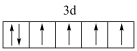 |
您最近一年使用:0次
9 . 用“氧化-萃取法”可从卤水中提取碘,其方法为向酸化的卤水中加入 溶液,再加入萃取剂(R)进行萃取。该过程涉及以下反应:
溶液,再加入萃取剂(R)进行萃取。该过程涉及以下反应:
(ⅰ)

(ⅱ)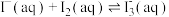
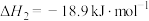
(ⅲ)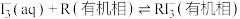
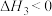
(1)根据盖斯定律,反应

________ 。
(2)基态碘原子价层电子的轨道表示式为________ 。
(3)①反应条件会影响碘的萃取率。其他条件不变时,不同温度下达平衡时碘萃取率
[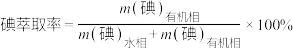 ]曲线如图所示:
]曲线如图所示:_______________ (忽略萃取剂的挥发、 的挥发及
的挥发及 分解产生的影响)。当萃取温度超过320 K时,
分解产生的影响)。当萃取温度超过320 K时, 的分解导致碘萃取率明显下降。
的分解导致碘萃取率明显下降。
②下列说法不正确的是________ (填标号)。
A.增大溶液的pH,碘萃取率降低 B.增大萃取剂用量,碘萃取率升高
C.萃取体系平衡后加水稀释, 变小 D.增大
变小 D.增大 的浓度,反应(ⅰ)的速率增大
的浓度,反应(ⅰ)的速率增大
(4)未加萃取剂时,固定总碘浓度为 ,平衡时溶液中的
,平衡时溶液中的 、
、 、
、 分布系数
分布系数 与溶液中初始
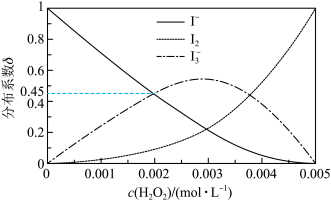
与溶液中初始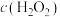 关系如图所示。[总碘浓度
关系如图所示。[总碘浓度 各组分折合为
各组分折合为 后的浓度之和,
后的浓度之和, ,如
,如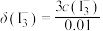 ]
] 、
、 、
、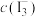 分别为
分别为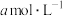 、
、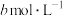 、
、 ,则
,则 、
、 、
、 之间的关系式为
之间的关系式为________ 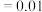 。
。
②计算反应 的平衡常数
的平衡常数
________ (结果保留3位有效数字)。
(5)测定卤水中的 方法:取
方法:取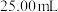 卤水于锥形瓶中,加适量氧化剂恰好将
卤水于锥形瓶中,加适量氧化剂恰好将 全部氧化为
全部氧化为 ;加
;加 溶液酸化后,再加入适量
溶液酸化后,再加入适量 溶液,密闭静置后,用
溶液,密闭静置后,用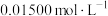
 标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点;平行测定3次,平均消耗
标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点;平行测定3次,平均消耗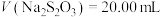 ,则卤水中
,则卤水中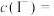
________  。(已知:
。(已知: )
)
 溶液,再加入萃取剂(R)进行萃取。该过程涉及以下反应:
溶液,再加入萃取剂(R)进行萃取。该过程涉及以下反应:(ⅰ)


(ⅱ)
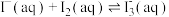
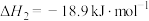
(ⅲ)
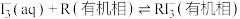
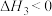
(1)根据盖斯定律,反应


(2)基态碘原子价层电子的轨道表示式为
(3)①反应条件会影响碘的萃取率。其他条件不变时,不同温度下达平衡时碘萃取率
[
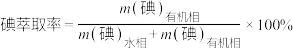 ]曲线如图所示:
]曲线如图所示: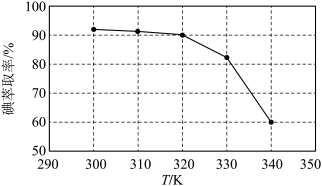
 的挥发及
的挥发及 分解产生的影响)。当萃取温度超过320 K时,
分解产生的影响)。当萃取温度超过320 K时, 的分解导致碘萃取率明显下降。
的分解导致碘萃取率明显下降。②下列说法不正确的是
A.增大溶液的pH,碘萃取率降低 B.增大萃取剂用量,碘萃取率升高
C.萃取体系平衡后加水稀释,
 变小 D.增大
变小 D.增大 的浓度,反应(ⅰ)的速率增大
的浓度,反应(ⅰ)的速率增大(4)未加萃取剂时,固定总碘浓度为
 ,平衡时溶液中的
,平衡时溶液中的 、
、 、
、 分布系数
分布系数 与溶液中初始
与溶液中初始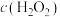 关系如图所示。[总碘浓度
关系如图所示。[总碘浓度 各组分折合为
各组分折合为 后的浓度之和,
后的浓度之和, ,如
,如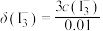 ]
]
 、
、 、
、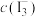 分别为
分别为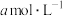 、
、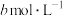 、
、 ,则
,则 、
、 、
、 之间的关系式为
之间的关系式为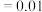 。
。②计算反应
 的平衡常数
的平衡常数
(5)测定卤水中的
 方法:取
方法:取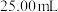 卤水于锥形瓶中,加适量氧化剂恰好将
卤水于锥形瓶中,加适量氧化剂恰好将 全部氧化为
全部氧化为 ;加
;加 溶液酸化后,再加入适量
溶液酸化后,再加入适量 溶液,密闭静置后,用
溶液,密闭静置后,用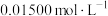
 标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点;平行测定3次,平均消耗
标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点;平行测定3次,平均消耗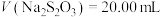 ,则卤水中
,则卤水中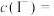
 。(已知:
。(已知: )
)
您最近一年使用:0次
名校
10 . 某化工厂利用废旧锂离子电池正极材料(含有LiCoO2以及少量Ca、Mg、Fe、Al等)制备Co2O3和Li2CO3。工艺流程如下: 如下表:
如下表:
②常温时, 的溶度积
的溶度积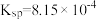 ,该数值随温度升高而减小。
,该数值随温度升高而减小。
(1)LiCoO2中Co元素的化合价为______ ;基态Co原子的价层电子轨道表示式为______ 。
(2)“酸浸”时发生反应: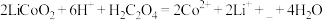 。
。
①补充完整上述离子方程式______ ;
②旧生产工艺用盐酸进行“酸浸”,但易造成环境污染,原因是______ 。
(3)已知滤渣2中含有 ,则常温下滤液2中
,则常温下滤液2中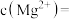
______ mol/L。
(4)滤液3中含金属元素的离子主要是 ,通入空气发生催化氧化反应的离子方程式为
,通入空气发生催化氧化反应的离子方程式为______ 。
(5)沉锂操作过程中的存在反应: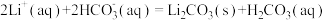 ,该操作中需将温度升高到90℃,原因是
,该操作中需将温度升高到90℃,原因是______ 。
(6)由 进一步制得的
进一步制得的 具有反萤石结构,晶胞如图所示。
具有反萤石结构,晶胞如图所示。 在晶胞中的位置为
在晶胞中的位置为______ ;
②设阿伏加德罗常数的值为 。晶胞
。晶胞 的密度为b
的密度为b ,则晶胞参数(棱长)为
,则晶胞参数(棱长)为______ pm。

 如下表:
如下表:物质 |
|
|
|
|
|
|
|
|
|
 的溶度积
的溶度积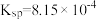 ,该数值随温度升高而减小。
,该数值随温度升高而减小。(1)LiCoO2中Co元素的化合价为
(2)“酸浸”时发生反应:
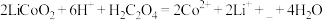 。
。①补充完整上述离子方程式
②旧生产工艺用盐酸进行“酸浸”,但易造成环境污染,原因是
(3)已知滤渣2中含有
 ,则常温下滤液2中
,则常温下滤液2中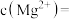
(4)滤液3中含金属元素的离子主要是
 ,通入空气发生催化氧化反应的离子方程式为
,通入空气发生催化氧化反应的离子方程式为(5)沉锂操作过程中的存在反应:
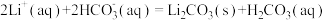 ,该操作中需将温度升高到90℃,原因是
,该操作中需将温度升高到90℃,原因是(6)由
 进一步制得的
进一步制得的 具有反萤石结构,晶胞如图所示。
具有反萤石结构,晶胞如图所示。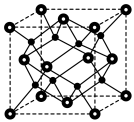
 在晶胞中的位置为
在晶胞中的位置为②设阿伏加德罗常数的值为
 。晶胞
。晶胞 的密度为b
的密度为b ,则晶胞参数(棱长)为
,则晶胞参数(棱长)为
您最近一年使用:0次
2024-03-15更新
|
1002次组卷
|
3卷引用:广东省江门市2023-2024学年高三一模考试化学卷
广东省江门市2023-2024学年高三一模考试化学卷广东省东莞市东华高级中学 东华松山湖高级中学 2024届高三下学期第三次模拟考试 化学试题 (已下线)题型10 工艺流程题(25题)-2024年高考化学常考点必杀300题(新高考通用)