1 . 下列说法正确的是:
A.24Cr原子的核外电子排布式是: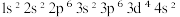 |
| B.最外层电子排布式为ns¹的基态原子所对应元素一定是金属元素 |
| C.原子半径:P>S>Cl |
| D.电负性:Br>Cl>F |
您最近半年使用:0次
2 . 回答下列问题:
(1) 中含有的
中含有的 键数目为
键数目为___________ , 键数目为
键数目为___________ 。
(2)已知CO和 与
与 结构相似,CO分子内
结构相似,CO分子内 键与
键与 键个数之比为
键个数之比为___________ 。 分子中
分子中 键与
键与 键数目之比为
键数目之比为___________ 。
(3)肼 分子可视为
分子可视为 分子中的一个氢原子被
分子中的一个氢原子被 (氨基)取代形成的另一种氮的氢化物。肼可用作火箭燃料,燃烧时发生的反应:
(氨基)取代形成的另一种氮的氢化物。肼可用作火箭燃料,燃烧时发生的反应:
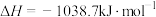 ,若该反应中有
,若该反应中有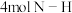 键断裂,则形成的
键断裂,则形成的 键有
键有___________ mol。
(4)Co基态原子核外电子排布式为___________ ; 的价电子轨道表示式为
的价电子轨道表示式为___________ ; 核外电子未成对电子数为
核外电子未成对电子数为___________ 。
(5) 、
、 、
、 、
、 分子中共价键的极性由强到弱的顺序是
分子中共价键的极性由强到弱的顺序是___________ 。
(1)
 中含有的
中含有的 键数目为
键数目为 键数目为
键数目为(2)已知CO和
 与
与 结构相似,CO分子内
结构相似,CO分子内 键与
键与 键个数之比为
键个数之比为 分子中
分子中 键与
键与 键数目之比为
键数目之比为(3)肼
 分子可视为
分子可视为 分子中的一个氢原子被
分子中的一个氢原子被 (氨基)取代形成的另一种氮的氢化物。肼可用作火箭燃料,燃烧时发生的反应:
(氨基)取代形成的另一种氮的氢化物。肼可用作火箭燃料,燃烧时发生的反应:
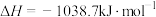 ,若该反应中有
,若该反应中有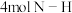 键断裂,则形成的
键断裂,则形成的 键有
键有(4)Co基态原子核外电子排布式为
 的价电子轨道表示式为
的价电子轨道表示式为 核外电子未成对电子数为
核外电子未成对电子数为(5)
 、
、 、
、 、
、 分子中共价键的极性由强到弱的顺序是
分子中共价键的极性由强到弱的顺序是
您最近半年使用:0次
2024-04-27更新
|
47次组卷
|
2卷引用:黑龙江省绥化市绥棱县第一中学2023-2024学年高二上学期1月期末化学试题
解题方法
3 . 镍离子有机配合物可以用在高温润滑油,聚合物添加剂等领域。某芳香类镍离子有机配合物可以通过下列反应过程制备。

| A.该类镍离子有机配合物属于盐类 | B.化合物F分子中 键的数目为61 键的数目为61 |
| C.有关元素的电负性:Cl>S>P | D.配离子G中中心离子的配位数为4 |
您最近半年使用:0次
名校
解题方法
4 . 3-氨基-1-金刚烷醇可用于合成药物维格列汀(治疗2型糖尿病),其分子结构如下图所示。下列说法不正确的是

A.分子中O原子和N原子均为 杂化 杂化 | B.分子中的键角: |
C.电负性: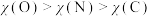 | D.第一电离能: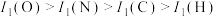 |
您最近半年使用:0次
2024-04-15更新
|
166次组卷
|
2卷引用:江西省新余市2023-2024学年高三上学期第一次调研考试化学试卷
解题方法
5 . 中国科学家团队成功合成了五氮阴离子盐 。五氮阴离子(
。五氮阴离子(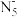 )为环状平面结构,是制备全氮类物质
)为环状平面结构,是制备全氮类物质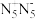 的中间体。
的中间体。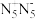 是新一代超高能含能材料下列说法正确的是
是新一代超高能含能材料下列说法正确的是
 。五氮阴离子(
。五氮阴离子(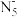 )为环状平面结构,是制备全氮类物质
)为环状平面结构,是制备全氮类物质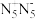 的中间体。
的中间体。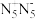 是新一代超高能含能材料下列说法正确的是
是新一代超高能含能材料下列说法正确的是
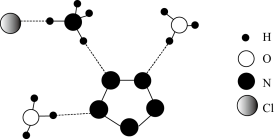
| A.阴阳离子之间作用力只存在离子键 | B.五氮阴离子盐中N、O两种元素均为sp3杂化 |
| C.电负性:N>O>H | D.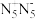 可以作炸药、推进剂 可以作炸药、推进剂 |
您最近半年使用:0次
6 . 下列说法正确的是
A.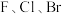 的电负性依次增大 的电负性依次增大 |
B.电子排布不同的两种氮原子: ,能量 ,能量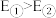 |
| C.太阳光谱中的黑线实质上是太阳中所含元素原子的发射光谱 |
D. 的最外层电子数依次增多 的最外层电子数依次增多 |
您最近半年使用:0次
2024-04-04更新
|
178次组卷
|
2卷引用:浙江省杭州市浙江大学附属中学2023-2024学年高二上学期期末考试化学试题
解题方法
7 . 金属络合物是有机金属催化不对称反应中的一类重要的中间体,M为 (Ⅰ)的络合物单晶结构,如图所示。(
(Ⅰ)的络合物单晶结构,如图所示。(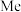 为甲基,
为甲基, 为苯基)
为苯基)
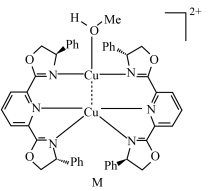
下列叙述正确的是
 (Ⅰ)的络合物单晶结构,如图所示。(
(Ⅰ)的络合物单晶结构,如图所示。(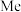 为甲基,
为甲基, 为苯基)
为苯基)
下列叙述正确的是
A.第一电离能: | B.M中只有 与 与 (I)形成配位键 (I)形成配位键 |
C.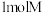 含 含 手性碳原子 手性碳原子 | D.M所含元素中,氮的电负性最大 |
您最近半年使用:0次
解题方法
8 . 火箭推进剂中常使用N2H4(肼,结构式为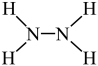 )作为燃烧剂,N2O4作为氧化剂。反应的化学方程式为:2N2H4+N2O4=3N2+4H2O。下列说法
)作为燃烧剂,N2O4作为氧化剂。反应的化学方程式为:2N2H4+N2O4=3N2+4H2O。下列说法不正确 的是
 )作为燃烧剂,N2O4作为氧化剂。反应的化学方程式为:2N2H4+N2O4=3N2+4H2O。下列说法
)作为燃烧剂,N2O4作为氧化剂。反应的化学方程式为:2N2H4+N2O4=3N2+4H2O。下列说法| A.电负性:H<N<O |
| B.肼具有碱性 |
| C.H2O是一种极性分子 |
| D.每生成3molN2时,转移4mol电子 |
您最近半年使用:0次
解题方法
9 . 砷元素(As)广泛分布于自然界中,土壤、水体、矿物和生物体内都含有微量的砷。工业上提取砷的某步反应如下:

(1)砷元素在周期表中的位置是___________ 。
(2)沸点:AsH3___________ NH3,原因是___________ 。
A.> B.<
(3)关于I~Ⅳ四种物质的说法正确的是___________。
(4)已知H3AsO3为三元弱酸,则分子中As原子存在___________ 对孤电子对,AsO 的空间构型为
的空间构型为___________ 。
A.正四面体 B.三角锥形 C.角形
(5)溶解于水中的H3AsO4存在如下平衡:H3AsO4 H2AsO
H2AsO +H+,H2AsO
+H+,H2AsO
 HAsO
HAsO +H+,HAsO
+H+,HAsO
 AsO
AsO +H+。目前常用吸附法消除水中的砷,已知pH越大,吸附剂表面带的负电荷越多。分析吸附剂对砷的吸附量随pH升高而下降的原因
+H+。目前常用吸附法消除水中的砷,已知pH越大,吸附剂表面带的负电荷越多。分析吸附剂对砷的吸附量随pH升高而下降的原因___________ 。
(6)砷和镍(Ni)形成某种晶体的晶胞如图1所示,图2为该晶胞的俯视投影图。
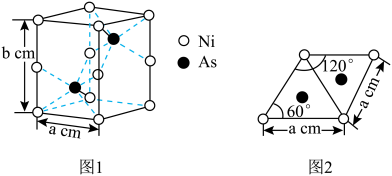
该晶胞中含有___________ 个Ni原子。该晶体的密度 ρ =___________ g·cm-3。(设NA为阿伏加德罗常数,该晶体的摩尔质量为M g·mol-1,用含 a、b、M和NA的代数式表示。)

(1)砷元素在周期表中的位置是
(2)沸点:AsH3
A.> B.<
(3)关于I~Ⅳ四种物质的说法正确的是___________。
| A.I中仅有σ键 | B.Ⅱ中部分元素的第一电离能: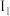 (O)> (O)>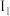 (S) (S) |
| C.Ⅲ中含有的元素中砷的电负性最大 | D.Ⅳ中含有的化学键为离子键、共价键 |
(4)已知H3AsO3为三元弱酸,则分子中As原子存在
 的空间构型为
的空间构型为A.正四面体 B.三角锥形 C.角形
(5)溶解于水中的H3AsO4存在如下平衡:H3AsO4
 H2AsO
H2AsO +H+,H2AsO
+H+,H2AsO
 HAsO
HAsO +H+,HAsO
+H+,HAsO
 AsO
AsO +H+。目前常用吸附法消除水中的砷,已知pH越大,吸附剂表面带的负电荷越多。分析吸附剂对砷的吸附量随pH升高而下降的原因
+H+。目前常用吸附法消除水中的砷,已知pH越大,吸附剂表面带的负电荷越多。分析吸附剂对砷的吸附量随pH升高而下降的原因(6)砷和镍(Ni)形成某种晶体的晶胞如图1所示,图2为该晶胞的俯视投影图。

该晶胞中含有
您最近半年使用:0次
10 . 在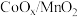 催化下醇的氧化氰化反应如图所示。下列叙述正确的是
催化下醇的氧化氰化反应如图所示。下列叙述正确的是
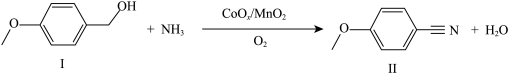
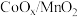 催化下醇的氧化氰化反应如图所示。下列叙述正确的是
催化下醇的氧化氰化反应如图所示。下列叙述正确的是
| A.熔点:Ⅰ>Ⅱ | B.Ⅰ所属类别为酚类 |
| C.Ⅰ和Ⅱ分子中σ键数目相同 | D.Ⅱ含有的元素中 的电负性最大 的电负性最大 |
您最近半年使用:0次



