1 . M、X、Y、Z四种短周期主族元素,M为金属元素,X、Y和Z为非金属元素,原子序数Z<X<M<Y。M在常压下可生成 :
: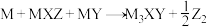 ,其中
,其中 为无色无味气体,反应消耗
为无色无味气体,反应消耗 的同时可获得标准状况下
的同时可获得标准状况下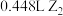 ,
, 可表示成
可表示成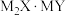 形式。下列说法正确的是
形式。下列说法正确的是
 :
: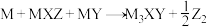 ,其中
,其中 为无色无味气体,反应消耗
为无色无味气体,反应消耗 的同时可获得标准状况下
的同时可获得标准状况下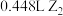 ,
, 可表示成
可表示成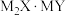 形式。下列说法正确的是
形式。下列说法正确的是| A.基态M原子核外电子空间运动状态有6种 |
| B.电负性:X<Y |
C.Z与X能组合成非极性分子 |
D. 与水反应能得到含有离子键和极性共价键的产物 与水反应能得到含有离子键和极性共价键的产物 |
您最近一年使用:0次
2 . 下列有关说法错误的是
| A.处于最低能量状态的原子叫作基态原子 |
| B.价电子层有2个未成对电子的原子一定属于主族元素 |
| C.玻尔原子结构模型可以较好地解释氢原子的可见光谱线 |
| D.利用电负性可判断化合物中元素化合价的正负及化学键的性质 |
您最近一年使用:0次
3 . 下列有关物质性质说法中,正确的是
| A.s-sσ键与s-p σ键的电子云形状相同 |
| B.热稳定性:HF>HI>HBr>HCl |
| C.具有下列电子排布式的原子中,①1s22s22p63s23p2 ②1s22s22p3 ③1s22s22p2 ④1s22s22p63s23p4,原子半径最大的是① |
| D.某元素气态基态原子的逐级电离能(kJ•mol-1)分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是X2+,其最高正价为+5价 |
您最近一年使用:0次
名校
4 . 硒( )是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(
)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光( )效应以来,
)效应以来, 在发光材料、生物医学等领域引起广泛关注。一种含
在发光材料、生物医学等领域引起广泛关注。一种含 的新型
的新型 分子
分子 的合成路线如下:
的合成路线如下: 与S同族,基态硒原子价电子排布式为
与S同族,基态硒原子价电子排布式为_______ 。
(2) 的沸点低于
的沸点低于 ,其原因是
,其原因是_______ 。
(3)关于I~III三种反应物,下列说法正确的有_______ 。
A.I中仅有 键
键
B.I中的 键为非极性共价键
键为非极性共价键
C.II易溶于水
D.II中原子的杂化轨道类型只有 与
与
E.I~III含有的元素中,O电负性最大
(4)IV中具有孤对电子的原子有_______ 。
(5)硒的两种含氧酸的酸性强弱为
_______  (填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠(
(填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠( )可减轻重金属铊引起的中毒。
)可减轻重金属铊引起的中毒。 的立体构型为
的立体构型为_______ 。
 )是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(
)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光( )效应以来,
)效应以来, 在发光材料、生物医学等领域引起广泛关注。一种含
在发光材料、生物医学等领域引起广泛关注。一种含 的新型
的新型 分子
分子 的合成路线如下:
的合成路线如下: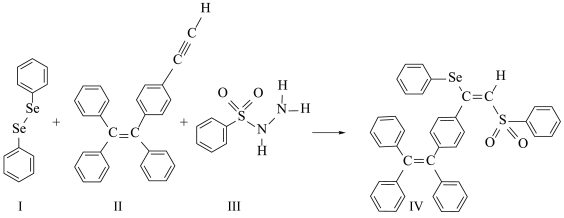
 与S同族,基态硒原子价电子排布式为
与S同族,基态硒原子价电子排布式为(2)
 的沸点低于
的沸点低于 ,其原因是
,其原因是(3)关于I~III三种反应物,下列说法正确的有
A.I中仅有
 键
键B.I中的
 键为非极性共价键
键为非极性共价键C.II易溶于水
D.II中原子的杂化轨道类型只有
 与
与
E.I~III含有的元素中,O电负性最大
(4)IV中具有孤对电子的原子有
(5)硒的两种含氧酸的酸性强弱为

 (填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠(
(填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠( )可减轻重金属铊引起的中毒。
)可减轻重金属铊引起的中毒。 的立体构型为
的立体构型为
您最近一年使用:0次
2022-10-08更新
|
713次组卷
|
6卷引用:山东省乳山市银滩高级中学2021-2022学年高一6月月考化学试题
解题方法
5 . 上海交大郑浩、贾金锋教授,利用低温强磁场扫描隧道显微镜在 体系中成功产生并探测到分段费米面,发表于《Science》杂志。回答下列问题:
体系中成功产生并探测到分段费米面,发表于《Science》杂志。回答下列问题:
(1)Bi与N、P同主族。基态Bi原子的价层电子排布式为_______ ;三者简单氢化物的还原性最强的是_______ (填化学式)。
(2)Se、Te与O同主族,Bi、Te、Se三种元素的电负性由大到小的顺序为_______ , 中心原子的杂化方式为
中心原子的杂化方式为_______ ,Se与O分别与H形成的简单氢化物键角较大的是_______ (填化学式)。
(3)金属铌原子价电子构型为 ,其盐六氟铌酸铵是重要工业原料,结构如图。该盐的阴离子中含有的化学键为
,其盐六氟铌酸铵是重要工业原料,结构如图。该盐的阴离子中含有的化学键为_______ (填标号)。

A. 键 B.
键 B. 键 C.金属键 D.配位键 E.离子键
键 C.金属键 D.配位键 E.离子键
(4)硒化锌是制作高功率 激光器的最佳光学材料,其晶胞结构可看作是金刚石晶胞内部的碳原子被Se原子代替,顶点和面心的碳原子被Zn原子代替。如图为沿y轴投影的硒化锌晶胞中所有原子的分布图。与Zn最近的Se原子构成的立体结构为
激光器的最佳光学材料,其晶胞结构可看作是金刚石晶胞内部的碳原子被Se原子代替,顶点和面心的碳原子被Zn原子代替。如图为沿y轴投影的硒化锌晶胞中所有原子的分布图。与Zn最近的Se原子构成的立体结构为_______ ;若原子1的分数坐标为(0.75,0.25,0.25),则原子2的分数坐标为_______ ;若硒化锌的晶体密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶胞中Se和Zn的最近距离为
,则晶胞中Se和Zn的最近距离为_______ pm(用代数式表示)。

 体系中成功产生并探测到分段费米面,发表于《Science》杂志。回答下列问题:
体系中成功产生并探测到分段费米面,发表于《Science》杂志。回答下列问题:(1)Bi与N、P同主族。基态Bi原子的价层电子排布式为
(2)Se、Te与O同主族,Bi、Te、Se三种元素的电负性由大到小的顺序为
 中心原子的杂化方式为
中心原子的杂化方式为(3)金属铌原子价电子构型为
 ,其盐六氟铌酸铵是重要工业原料,结构如图。该盐的阴离子中含有的化学键为
,其盐六氟铌酸铵是重要工业原料,结构如图。该盐的阴离子中含有的化学键为
A.
 键 B.
键 B. 键 C.金属键 D.配位键 E.离子键
键 C.金属键 D.配位键 E.离子键(4)硒化锌是制作高功率
 激光器的最佳光学材料,其晶胞结构可看作是金刚石晶胞内部的碳原子被Se原子代替,顶点和面心的碳原子被Zn原子代替。如图为沿y轴投影的硒化锌晶胞中所有原子的分布图。与Zn最近的Se原子构成的立体结构为
激光器的最佳光学材料,其晶胞结构可看作是金刚石晶胞内部的碳原子被Se原子代替,顶点和面心的碳原子被Zn原子代替。如图为沿y轴投影的硒化锌晶胞中所有原子的分布图。与Zn最近的Se原子构成的立体结构为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶胞中Se和Zn的最近距离为
,则晶胞中Se和Zn的最近距离为
您最近一年使用:0次
名校
6 . I、如图表示元素周期表中部分元素的某种性质(X值)随原子序数变化的关系示意图。

(1)短周期中原子核外p能级上电子总数与s能级上电子总数相等的元素是_______ (填元素符号)。
(2)预测S元素与 元素x值的大小关系为
元素x值的大小关系为_______ ,x值最小的元素在元素周期表中的位置是_______ (放射性元素除外)。
(3)下列关于元素性质的说法正确的是_______ (填标号)。
a.X值可反映元素最高正化合价的变化规律
b.X值可反映元素在化合物中吸引电子的能力
c.X值的大小可用来判断元素金属性和非金属性的强弱
II、今有① 、②HCl、③
、②HCl、③ 三种溶液,根据要求回答下列问题:
三种溶液,根据要求回答下列问题:
(4)pH相同的三种酸溶液各lmL,加水稀释相同倍数后,溶液中水电离出来的 的关系为
的关系为_______ 。(用序号填空,下同)
(5)当它们pH相同、体积相同时,分别加入足量锌,相同状况下产生气体体积关系为_______ 。
(6)中和等体积相同浓度的烧碱溶液,需同浓度的三种溶液的体积分别为 、
、 、
、 ,则
,则 、
、 、
、 的关系为
的关系为_______ (用等式表示)。
III.平衡思想是化学研究的一个重要观念,在水溶液中存在多种平衡体系。
(7)实验室在保存FeCl3溶液时,常在溶液中加少量的_______ ,以抑制其水解;把 溶液蒸干并灼烧,最后得到的固体主要产物是
溶液蒸干并灼烧,最后得到的固体主要产物是_______ 。
(8)在日常生活中经常用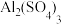 和
和 混合溶液作灭火剂,请用离子方程式表示其灭火原理:
混合溶液作灭火剂,请用离子方程式表示其灭火原理:_______ 。

(1)短周期中原子核外p能级上电子总数与s能级上电子总数相等的元素是
(2)预测S元素与
 元素x值的大小关系为
元素x值的大小关系为(3)下列关于元素性质的说法正确的是
a.X值可反映元素最高正化合价的变化规律
b.X值可反映元素在化合物中吸引电子的能力
c.X值的大小可用来判断元素金属性和非金属性的强弱
II、今有①
 、②HCl、③
、②HCl、③ 三种溶液,根据要求回答下列问题:
三种溶液,根据要求回答下列问题:(4)pH相同的三种酸溶液各lmL,加水稀释相同倍数后,溶液中水电离出来的
 的关系为
的关系为(5)当它们pH相同、体积相同时,分别加入足量锌,相同状况下产生气体体积关系为
(6)中和等体积相同浓度的烧碱溶液,需同浓度的三种溶液的体积分别为
 、
、 、
、 ,则
,则 、
、 、
、 的关系为
的关系为III.平衡思想是化学研究的一个重要观念,在水溶液中存在多种平衡体系。
(7)实验室在保存FeCl3溶液时,常在溶液中加少量的
 溶液蒸干并灼烧,最后得到的固体主要产物是
溶液蒸干并灼烧,最后得到的固体主要产物是(8)在日常生活中经常用
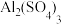 和
和 混合溶液作灭火剂,请用离子方程式表示其灭火原理:
混合溶液作灭火剂,请用离子方程式表示其灭火原理:
您最近一年使用:0次
名校
7 . 短周期元素X、Y、Z、W、E原子核外电子数依次增多。X的原子半径是短周期元素中最小的;Y、Z、W位于同一周期,Z元素基态原子中p轨道所含电子数与s轨道相等;E与W同主族。它们组成的某种分子的结构式如图所示,下列说法正确的是
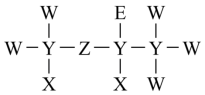
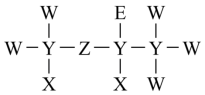
A.简单阴离子半径: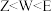 |
| B.同主族元素中E的最高价氧化物对应水化物的酸性最强 |
C.电负性: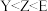 |
D.离子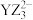 的中心原子的杂化方式是 的中心原子的杂化方式是 杂化 杂化 |
您最近一年使用:0次
2022-01-27更新
|
648次组卷
|
5卷引用:山东省乳山市银滩高级中学2022-2023学年高一4月月考化学试题
解题方法
8 . 下列说法正确的是
| A.元素周期表中周期序数等于核外电子层数,族序数等于最外层电子数 |
B.某基态原子3d轨道电子排布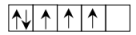 违背了洪特规则 违背了洪特规则 |
| C.在所有元素中,电负性和第一电离能最强的均为氟元素 |
| D.运用玻尔原子结构模型可以解释钠原子光谱中有靠得很近的两条黄色谱线 |
您最近一年使用:0次
9 . 由短周期主族元素组成的化合物如图所示,M、X、Y、Z、W原子序数依次增大,且总和为40,下列有关叙述错误的是

| A.电负性:Z>Y>W |
| B.原子半径:X>Y>Z |
| C.简单氢化物的沸点:X<Y<Z |
| D.Y与W、X都可以形成含极性键的非极性分子 |
您最近一年使用:0次
2021-12-09更新
|
210次组卷
|
3卷引用:山东省威海市文登区2021-2022学年高三上学期期中考试化学试题
名校
解题方法
10 . 短周期元素原子组成的某种分子的结构式如图所示。X原子的核外电子只有一种运动状态;W、Y、Z位于同一周期,Z元素原子中p轨道所含电子数与s轨道相等。E与W有相同数目的价电子。下列说法错误的是


A.电负性: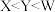 |
B.简单阴离子半径: |
| C.同周期中,第一电离能大于Z的元素有2种 |
| D.同主族元素中,W形成的气态氢化物最稳定 |
您最近一年使用:0次
2021-11-20更新
|
505次组卷
|
5卷引用:山东省威海乳山市2021-2022学年高三上学期期中考试化学试题



