名校
解题方法
1 .  及其化合物在生产和生活中用途广泛,回答下列问题。
及其化合物在生产和生活中用途广泛,回答下列问题。
(1) 的基态原子共有
的基态原子共有_____________ 种不同能级的电子。
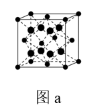
(2) 为只含有离子键的离子化合物,其晶胞结构如图a,距一个
为只含有离子键的离子化合物,其晶胞结构如图a,距一个 最近的所有
最近的所有 为顶点构成的几何形状为
为顶点构成的几何形状为_____________ 。
(3)二茂铁是最重要的金属茂基配合物,结构为一个铁原子处在两个平行的环戊二烯基环之间,结构如图b所示,已知二茂铁的一氯代物只有一种。

①二茂铁的分子式为_____________ 。
②穆斯堡尔谱学数据显示,二茂铁中学铁原子的氧化态为+2,每个茂环带有一个单位负电荷,因此每个环含有_____________ 个 电子。
电子。
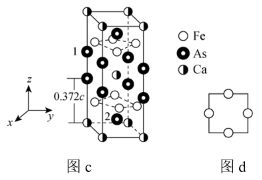
(4)一种铁基超导材料( ,相对分子质量为
,相对分子质量为 )晶胞如图c所示,图d为铁原子沿轴方向的投影图。
)晶胞如图c所示,图d为铁原子沿轴方向的投影图。
① 与
与 位于同一周期、且最外层电子数相等,但
位于同一周期、且最外层电子数相等,但 的熔点、沸点均比
的熔点、沸点均比 高,原因是
高,原因是_____________ 。
② 分子与
分子与 形成配合物后
形成配合物后 键角
键角_____________ (填“变大”“变小”或“不变”)。
③ 、
、 、
、 电负性由大到小的顺序为
电负性由大到小的顺序为_____________ 。
④ 的沸点(319℃,易升华)高于
的沸点(319℃,易升华)高于 的沸点(130.2℃),原因是
的沸点(130.2℃),原因是_____________ 。
⑤已知处于体心与顶点的 原子有着相同的化学环境,晶胞中
原子有着相同的化学环境,晶胞中 原子1的原子坐标为(0,0,0.628),则
原子1的原子坐标为(0,0,0.628),则 原子2的原子坐标为
原子2的原子坐标为_____________ 。
 及其化合物在生产和生活中用途广泛,回答下列问题。
及其化合物在生产和生活中用途广泛,回答下列问题。(1)
 的基态原子共有
的基态原子共有(2)
 为只含有离子键的离子化合物,其晶胞结构如图a,距一个
为只含有离子键的离子化合物,其晶胞结构如图a,距一个 最近的所有
最近的所有 为顶点构成的几何形状为
为顶点构成的几何形状为
(3)二茂铁是最重要的金属茂基配合物,结构为一个铁原子处在两个平行的环戊二烯基环之间,结构如图b所示,已知二茂铁的一氯代物只有一种。

①二茂铁的分子式为
②穆斯堡尔谱学数据显示,二茂铁中学铁原子的氧化态为+2,每个茂环带有一个单位负电荷,因此每个环含有
 电子。
电子。(4)一种铁基超导材料(
 ,相对分子质量为
,相对分子质量为 )晶胞如图c所示,图d为铁原子沿轴方向的投影图。
)晶胞如图c所示,图d为铁原子沿轴方向的投影图。
①
 与
与 位于同一周期、且最外层电子数相等,但
位于同一周期、且最外层电子数相等,但 的熔点、沸点均比
的熔点、沸点均比 高,原因是
高,原因是②
 分子与
分子与 形成配合物后
形成配合物后 键角
键角③
 、
、 、
、 电负性由大到小的顺序为
电负性由大到小的顺序为④
 的沸点(319℃,易升华)高于
的沸点(319℃,易升华)高于 的沸点(130.2℃),原因是
的沸点(130.2℃),原因是⑤已知处于体心与顶点的
 原子有着相同的化学环境,晶胞中
原子有着相同的化学环境,晶胞中 原子1的原子坐标为(0,0,0.628),则
原子1的原子坐标为(0,0,0.628),则 原子2的原子坐标为
原子2的原子坐标为
您最近一年使用:0次
名校
解题方法
2 . A、B、C、D为原子序数依次增大的四种元素,A2﹣和B+具有相同的电子构型:C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是___________ (填元素符号),其中C原子的核外电子排布式为 ___________ 。
(2)单质A有两种同素异形体,其中沸点高的是___________ (填分子式),原因是 ___________ ;B的氢化物的电子式为 ___________ 。
(3)C和D反应可生成组成比为1:3的化合物E,E的立体构型为___________ ,中心原子的杂化轨道类型为 ___________ 。
(4)化合物D2A的立体构型为___________ ,中心原子的价层电子对数为 ___________ 。
(1)四种元素中电负性最大的是
(2)单质A有两种同素异形体,其中沸点高的是
(3)C和D反应可生成组成比为1:3的化合物E,E的立体构型为
(4)化合物D2A的立体构型为
您最近一年使用:0次
解题方法
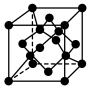
3 . 中国第一辆火星车“祝融号”成功登陆火星,探测发现火星上存在大量橄榄石矿物( ),已知晶体硅的晶胞如图,下列说法错误的是
),已知晶体硅的晶胞如图,下列说法错误的是
 ),已知晶体硅的晶胞如图,下列说法错误的是
),已知晶体硅的晶胞如图,下列说法错误的是
| A.Fe2+价电子排布式为3d6,未成对电子数是4 |
| B.橄榄石中各元素第一电离能和电负性大小顺序均为O>Si>Fe>Mg |
| C.硅的氯化物SiCl4分子是非极性分子,Si的杂化方式是sp3 |
D.若单晶硅晶胞参数是anm,则Si原子的原子半径为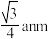 |
您最近一年使用:0次
2023-12-31更新
|
492次组卷
|
2卷引用:河北省石家庄市部分重点高中2023-2024学年高三上学期12月期末化学试题
名校
4 . 短周期主族元素X、Y、Z、W的原子序数依次增大,基态Y原子有3个未成对电子,基态Z原子的价电子数等于其电子层数,这四种元素可形成离子化合物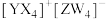 。下列叙述正确的是
。下列叙述正确的是
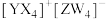 。下列叙述正确的是
。下列叙述正确的是A.氧化性: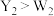 | B.电负性:Y>X>Z |
| C.Y的含氧酸一定是强酸 | D.第一电离能:Y<W |
您最近一年使用:0次
2023-12-30更新
|
480次组卷
|
2卷引用:河北省衡水市武强中学2023-2024学年高二上学期期末考试化学试题
名校
5 . 二硫代磷酸酯的分子结构如图所示。下列说法错误的是
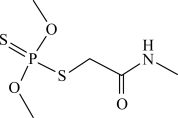
A.电负性: |
B.该分子中含有23个 键 键 |
C.该分子中碳原子的杂化方式为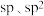 |
D.基态N原子价电子轨道表示式为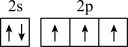 |
您最近一年使用:0次
2023-12-26更新
|
548次组卷
|
5卷引用:2023—2024学年高二上学期化学期末考试模拟试题(一)
名校
解题方法
6 . 下列判断不正确的是
| A.电负性:P<S<Cl | B.沸点:Cl2<Br2<I2 |
| C.微粒半径:Li+<O2-<Na+ | D.键角:BF3>CH4>H2O |
您最近一年使用:0次
2023-12-25更新
|
180次组卷
|
2卷引用:2023-2024学年高二上学期期末化学考试仿真卷(一)2019版选修一、选修二(部分)
2023高三·全国·专题练习
解题方法
7 . 根据要求回答下列问题:
(1)在第二周期主族元素,第一电离能介于B和N之间的元素有___________ 种。
(2)嫦娥五号实现了我国首次地外天体采样返回,带回的月壤中包含了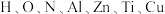 等多种元素,N的第一电离能大于O的,请说明理由:
等多种元素,N的第一电离能大于O的,请说明理由:_______ 。
(3)已知电离能: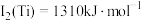 ,
,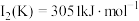 ,
,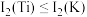 ,其原因为
,其原因为___________ 。
(4)橙红色晶体羰基钴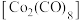 的熔点为
的熔点为 ,可溶于多数有机溶剂。该晶体中三种元素电负性由大到小的顺序为
,可溶于多数有机溶剂。该晶体中三种元素电负性由大到小的顺序为_________ (填元素符号)。配体 中
中 键与
键与 键数目之比是
键数目之比是___________ 。
(5) 中键与键之间的夹角为
中键与键之间的夹角为 ,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为
,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为___________ ,1个分子中含有___________ 个 键。
键。
(6)此后,等电子原理又有所发展。例如,由短周期元素组成的微粒,只要其原子数相同,各原子最外层电子数之和相同,也可互称为等电子体,它们也具有相似的结构特征。在短周期元素组成的物质中,与 互为等电子体的分子有
互为等电子体的分子有___________ 、___________ 。
(1)在第二周期主族元素,第一电离能介于B和N之间的元素有
(2)嫦娥五号实现了我国首次地外天体采样返回,带回的月壤中包含了
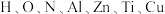 等多种元素,N的第一电离能大于O的,请说明理由:
等多种元素,N的第一电离能大于O的,请说明理由:(3)已知电离能:
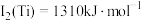 ,
,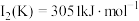 ,
,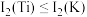 ,其原因为
,其原因为(4)橙红色晶体羰基钴
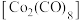 的熔点为
的熔点为 ,可溶于多数有机溶剂。该晶体中三种元素电负性由大到小的顺序为
,可溶于多数有机溶剂。该晶体中三种元素电负性由大到小的顺序为 中
中 键与
键与 键数目之比是
键数目之比是(5)
 中键与键之间的夹角为
中键与键之间的夹角为 ,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为
,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为 键。
键。(6)此后,等电子原理又有所发展。例如,由短周期元素组成的微粒,只要其原子数相同,各原子最外层电子数之和相同,也可互称为等电子体,它们也具有相似的结构特征。在短周期元素组成的物质中,与
 互为等电子体的分子有
互为等电子体的分子有
您最近一年使用:0次
2023-12-15更新
|
370次组卷
|
3卷引用:2023-2024学年高二上学期期末化学考试仿真卷(一)2019版选修一、选修二(部分)
名校
解题方法
8 . X、Y、Z、R、Q是元素周期表中原子序数依次增大的前四周期元素,X是宇宙中含量最多的元素;Y与Z同周期,Y基态原子有3个未成对电子,Z元素原子的价层电子排布为 ;R元素简单离子在同周期离子中半径最小;Q元素最高能层只有1个电子,其余能层均充满电子。下列说法
;R元素简单离子在同周期离子中半径最小;Q元素最高能层只有1个电子,其余能层均充满电子。下列说法不正确 的是
 ;R元素简单离子在同周期离子中半径最小;Q元素最高能层只有1个电子,其余能层均充满电子。下列说法
;R元素简单离子在同周期离子中半径最小;Q元素最高能层只有1个电子,其余能层均充满电子。下列说法A.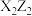 是含有极性键和非极性键的极性分子 是含有极性键和非极性键的极性分子 |
B.第一电离能: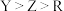 |
| C.Q在周期表的ds区 |
D.电负性: |
您最近一年使用:0次
2023-12-09更新
|
968次组卷
|
5卷引用:广东省深圳实验 湛江一中 珠海一中2023-2024学年高三上学期12月联考化学试题
广东省深圳实验 湛江一中 珠海一中2023-2024学年高三上学期12月联考化学试题浙江省嘉兴市2023-2024学年高三上学期12月月考化学试题卷 (已下线)题型08 元素周期律推断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)专题04 物质结构与性质(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)(已下线)压轴题05 “位-构-性”元素推断(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)
名校
解题方法
9 . 下列有关物质结构与性质说法正确的是
A.酸性: |
B.沸点: |
C.键角: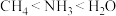 |
D.熔点:对硝基苯酚>邻硝基苯酚(硝基为 ) ) |
您最近一年使用:0次
2023-11-17更新
|
276次组卷
|
2卷引用:2023—2024学年高二上学期化学期末考试模拟试题(一)
名校
10 . X、Y、Z、W四种短周期主族元素,原子序数依次增大。X与Y相邻,X基态原子核外有2个未成对电子;Z是元素周期表中电负性最大的元素。W原子在同周期中原子半径最大。下列说法不正确 的是
A.第一电离能: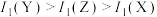 |
| B.最高价氧化物对应水化物的酸性:Y>X |
C.Z、W的简单离子的半径: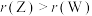 |
| D.简单气态氢化物的热稳定性:Z>Y |
您最近一年使用:0次
2023-11-15更新
|
1195次组卷
|
7卷引用:甘肃省武威第七中学2023-2024学年高二上学期期末考试化学试题



