名校
1 . 下列有关化学用语的表示正确的是
A.中子数为20的氯原子: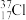 |
| B.CO2的空间结构为V形 |
C.过氧化氢的电子式: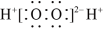 |
| D.HClO的结构式H-Cl-O |
您最近一年使用:0次
2 . 下列叙述中正确的是
| A.NH3、CO、CO2都是极性分子 |
| B.CH4、CCl4都是含有极性键的非极性分子 |
| C.HF、HCl、HBr、HI的稳定性依次增强 |
| D.CS2、H2O、C2H2都是直线形分子 |
您最近一年使用:0次
2022-10-18更新
|
2607次组卷
|
78卷引用:2015-2016学年重庆四十二中高一下期中化学试卷
2015-2016学年重庆四十二中高一下期中化学试卷2015-2016学年重庆市第八中学高二下第三次月考化学试卷高中化学人教版 选修三 第2章 分子结构与性质 键的极性和分子的极性2008年理综全国卷Ⅰ高考试题化学试题(已下线)2012届广西桂林十八中高三第一次月考化学试卷(已下线)2011-2012学年山西大同实验中学高二下学期期中考试化学试卷(已下线)2011-2012学年新疆农七师高级中学高二下学期期末考试试化学试卷(已下线)2011-2012学年福建省漳州立人学校高二下学期期中考试化学试卷(已下线)2012-2013学年山东省济南一中高二下学期期中考试理科化学试卷(已下线)2012-2013学年河北省衡水市第十四中学高二下学期期末考试化学试卷(已下线)2012-2013学年河北省唐山市第一中学高二下学期期末考试化学试卷(已下线)2013届山西省山西大学附中高三9月月考化学试卷2013-2014山东省即墨市高二下学期期中考试化学试卷2015-2016学年陕西西藏民族学院附中高二4月月考化学卷2015-2016学年内蒙古元平煤高中高二实验班下期中化学卷(已下线)同步君 选修3 第二章 第三节 键的极性和分子的极性2016-2017学年宁夏育才中学孔德校区高二下学期第一次(3月)月考化学试卷2016-2017学年山东省淄博市高青一中、淄博实验中学高二下学期期中联考化学试卷新疆生产建设兵团第二中学2016-2017学年高二下学期第二次月考化学试题陕西省黄陵中学2016-2017学年高二(重点班)下学期第三学月考化学试题河南省焦作市博爱一中2016-2017学年高二下学期第一次月考化学试题(已下线)【段考模拟】高二化学下学期第一次月考(3月)原创B卷宁夏银川市唐徕回民中学2017-2018学年高二4月月考化学试题陕西省黄陵中学2017-2018学年高二(重点班)下学期期末考试化学试题云南省双柏县第一中学2018-2019学年高二上学期期中考试化学试题贵州省遵义市正安县第一中学2018-2019学年高二上学期期中考试化学试题云南省元江哈尼族彝族傣族自治县一中2018-2019学年高二上学期12月考试化学试题贵州省剑河县第二高级中学2018-2019学年高二上学期12月份考试化学试题宁夏回族自治区银川市长庆高级中学2018-2019学年高二下学期第二次月考化学试题【全国百强校】新疆维吾尔自治区兵团第二师华山中学2018-2019学年高二下学期第一次调研化学试题(已下线)2019年6月12日 《每日一题》 选修3-物质类别、键的极性及分子的极性之间的关系安徽省淮北师范大学附属实验中学2018-2019学年高二下学期第二次月考化学试题吉林省长春市汽车经济开发区第三中学2018-2019学年高二下学期期中考试化学试题云南省普洱市孟连县一中2018-2019学年高二下学期期末考试化学试题云南省鹤庆三中2018-2019学年高二下学期期末考试化学试题黑龙江省哈尔滨市第三中学校2019-2020学年高二上学期期末考试化学试题上海市青浦二中2016届高三上学期8月摸底考试化学试题山西省运城市永济涑北中学2019-2020学年高二下学期3月月考化学试题黑龙江省哈尔滨市第三中学2019-2020学年高二上学期第一模块(期末)考试化学试题吉林省长春市第二十九中学2019-2020学年高二下学期线上检测化学试题河北省唐山市路北区第十一中学2019-2020学年高二期中考试化学试题辽宁省六校协作体2019-2020高二下学期期初考试化学试卷吉林省舒兰市实验中学2019-2020学年高二下学期期中考试化学试题新疆乌鲁木齐市第四中学2019-2020学年高二下学期期末考试化学试题安徽省六安中学2019-2020学年高二下学期期末考试化学试题新疆昌吉回族自治州呼图壁县第一中学2019-2020学年高二下学期期末考试化学试题福建省龙岩市武平县第一中学2021届高三上学期10月月考化学试题福建省龙海市第二中学2019-2020学年高二下学期期末考试化学试题山东省淄博市般阳中学2020-2021学年高二上学期期中考试化学试题(鲁科版2019)选择性必修2 第2章 微粒间相互作用与物质性质 章末综合检测卷四川省绵阳市江油中学2020-2021学年高二上学期期中考试化学试题辽宁省大连市普兰店区第三十八中学2020-2021学年高二上学期期末考试化学试题辽宁省阜新二高2020-2021学年高二下学期期中考试化学试题云南省通海县一中2020-2021学年高二下学期期中考试化学试题黑龙江省哈尔滨市第三十二中学2019-2020学年高二下学期期中考试化学试题人教2019选择性必修2第二章 分子结构与性质复习与提高黑龙江省绥化市第九中学2021-2022学年高二4月月考化学试题新疆乌鲁木齐市第四中学2021-2022学年高二下学期期中考试化学试题陕西省宝鸡市长岭中学2021-2022学年高二下学期期中考试化学试题福建省南安市侨光中学、昌财实验中学2021-2022学年高二下学期第4次联考(期中)化学试题宁夏贺兰县景博中学2021-2022学年高二下学期第一次月考化学试题四川省绵阳市盐亭中学2022-2023学年高二上学期第一次月考教学质量检测化学试题宁夏吴忠市吴忠中学2022-2023学年高三上学期阶段性测试 化学试题(已下线)【知识图鉴】单元讲练测选择性必修2第二章03单元测山东省威海市文登新一中2021-2022学年高二上学期期中考试化学试题广东省广州市第三中学2022-2023学年高二上学期期末测试化学试题广东省台山市第一中学2022-2023学年高二下学期第一次月考化学试题江西省景德镇市2022-2023学年高二下学期4月期中测试化学试题广东省深圳市观澜中学2022-2023学年高二下学期月考(物质结构)化学试题福建省德化第二中学2022-2023学年高二下学期期中考试化学试题安徽省合肥市第七中学2022-2023学年高二下学期期中检测化学试题广东省珠海市第三中学2023-2024学年高二下学期3月月考化学试卷河北省衡水市枣强中学2023-2024学年高二下学期第一次调研考试化学试题河南省焦作市2022-2023学年第四中学高二下学期期中考试 化学试卷广东省四会中学、广信中学2023-2024学年高二下学期第一次联合考试化学试题四川省富顺一中2023-2024学年高二下学期第一次月考化学试题广东省惠州市华罗庚中学2023-2024学年高二下学期3月月考化学试题广东梅州五华县中英文实验学校2023-2024学年高二下学期3月考试化学试题
3 . 物质世界丰富多彩,物质结构千变万化。回答下列问题:
(1)已知 熔沸点较低,常温下呈液态,易溶于有机溶剂,则
熔沸点较低,常温下呈液态,易溶于有机溶剂,则 晶体为
晶体为_______ (填晶体类型), 中含有
中含有_______  键。
键。
(2)某配合物化学式为 ,取1mol该物质溶解在水中并加热,无刺激性气味气体产生,再向其中加入过量
,取1mol该物质溶解在水中并加热,无刺激性气味气体产生,再向其中加入过量 溶液,产生2mol白色沉淀,则其中Co的化合价为
溶液,产生2mol白色沉淀,则其中Co的化合价为_______ 价,将该配合物溶于水中形成的阳离子化学式为_______ 。
(3)下图表示多硼酸根的一种无限长的链式结构,其化学式可表示为_______ 。
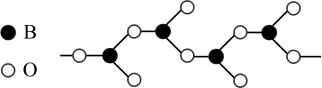
(4)天然硅酸盐组成复杂阴离子的基本结构单元是Si—O四面体,如图(a),通过共用顶角氧离子可形成链状、网状等结构,图(b)为一种无限长双链的多硅酸根,其中Si与O的原子数之比为_______ 。
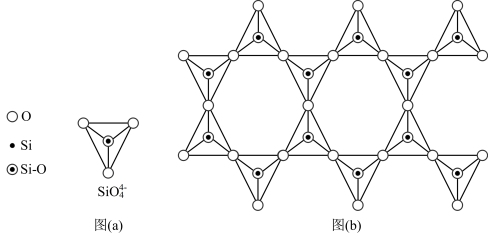
(5)硫和锌可以制备得ZnS晶体,其晶胞结构如图甲所示,晶胞中 和
和 的投影位置如图乙所示。
的投影位置如图乙所示。
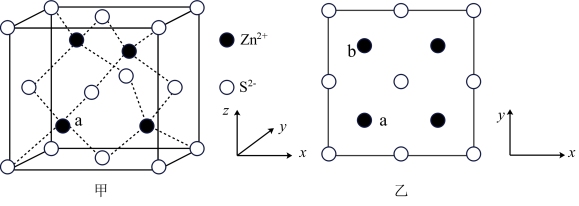
①Zn2+的电子排布式为_______ ,每个Zn2+周围距离最近的 有
有_______ 个。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子分数坐标。例如,a位置的 的坐标为(
的坐标为( ,
, ,
, ),则b位置的
),则b位置的 在图甲中对应的坐标为
在图甲中对应的坐标为_______ 。
③若a、b位置 的空间距离为a pm(核间距),设阿伏加德罗常数的值为
的空间距离为a pm(核间距),设阿伏加德罗常数的值为 ,则ZnS晶体的密度为
,则ZnS晶体的密度为_______  (列出计算表达式)。
(列出计算表达式)。
(1)已知
 熔沸点较低,常温下呈液态,易溶于有机溶剂,则
熔沸点较低,常温下呈液态,易溶于有机溶剂,则 晶体为
晶体为 中含有
中含有 键。
键。(2)某配合物化学式为
 ,取1mol该物质溶解在水中并加热,无刺激性气味气体产生,再向其中加入过量
,取1mol该物质溶解在水中并加热,无刺激性气味气体产生,再向其中加入过量 溶液,产生2mol白色沉淀,则其中Co的化合价为
溶液,产生2mol白色沉淀,则其中Co的化合价为(3)下图表示多硼酸根的一种无限长的链式结构,其化学式可表示为

(4)天然硅酸盐组成复杂阴离子的基本结构单元是Si—O四面体,如图(a),通过共用顶角氧离子可形成链状、网状等结构,图(b)为一种无限长双链的多硅酸根,其中Si与O的原子数之比为

(5)硫和锌可以制备得ZnS晶体,其晶胞结构如图甲所示,晶胞中
 和
和 的投影位置如图乙所示。
的投影位置如图乙所示。
①Zn2+的电子排布式为
 有
有②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子分数坐标。例如,a位置的
 的坐标为(
的坐标为( ,
, ,
, ),则b位置的
),则b位置的 在图甲中对应的坐标为
在图甲中对应的坐标为③若a、b位置
 的空间距离为a pm(核间距),设阿伏加德罗常数的值为
的空间距离为a pm(核间距),设阿伏加德罗常数的值为 ,则ZnS晶体的密度为
,则ZnS晶体的密度为 (列出计算表达式)。
(列出计算表达式)。
您最近一年使用:0次
名校
解题方法
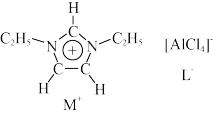
4 . 离子液体是一种由离子构成的很有研究价值的溶剂。某离子液体由如图所示正离子 和负离子
和负离子 构成,已知
构成,已知 中的五元环为平面形结构,该离子有较强的稳定性。
中的五元环为平面形结构,该离子有较强的稳定性。
(1)基态N原子中共有_______ 种运动状态不同的电子,其中占据最高能级的电子云轮廓图为_______ 形。原子中运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为_______ 。
(2) 中的各种元素的电负性由小到大的顺序为
中的各种元素的电负性由小到大的顺序为_______ , 中碳原子的杂化方式为
中碳原子的杂化方式为_______ 。
(3)负离子 的空间构型为
的空间构型为_______ 形,基态氯原子的价层电子轨道表示式为_______ 。
(4)分子中的大 键可用符号
键可用符号 表示,其中m代表形成大
表示,其中m代表形成大 键的原子数,n代表形成大
键的原子数,n代表形成大 键的电子数。如苯(
键的电子数。如苯( )中的大
)中的大 键可表示为
键可表示为 ,则
,则 中的大
中的大 键可表示为
键可表示为_______ 。
(5)碳原子与氮原子还可形成六元环状化合物吡啶(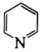 ),其分子中也含有与苯类似的
),其分子中也含有与苯类似的 大
大 键,则吡啶中N原子的孤电子对占据的轨道为
键,则吡啶中N原子的孤电子对占据的轨道为_______ (填标号)。
A.2s轨道 B.2p轨道 C.sp杂化轨道 D. 杂化轨道
杂化轨道
吡啶在水中的溶解度远大于苯,主要原因是①_______ ,②_______ 。
 和负离子
和负离子 构成,已知
构成,已知 中的五元环为平面形结构,该离子有较强的稳定性。
中的五元环为平面形结构,该离子有较强的稳定性。
(1)基态N原子中共有
 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为(2)
 中的各种元素的电负性由小到大的顺序为
中的各种元素的电负性由小到大的顺序为 中碳原子的杂化方式为
中碳原子的杂化方式为(3)负离子
 的空间构型为
的空间构型为(4)分子中的大
 键可用符号
键可用符号 表示,其中m代表形成大
表示,其中m代表形成大 键的原子数,n代表形成大
键的原子数,n代表形成大 键的电子数。如苯(
键的电子数。如苯( )中的大
)中的大 键可表示为
键可表示为 ,则
,则 中的大
中的大 键可表示为
键可表示为(5)碳原子与氮原子还可形成六元环状化合物吡啶(
 ),其分子中也含有与苯类似的
),其分子中也含有与苯类似的 大
大 键,则吡啶中N原子的孤电子对占据的轨道为
键,则吡啶中N原子的孤电子对占据的轨道为A.2s轨道 B.2p轨道 C.sp杂化轨道 D.
 杂化轨道
杂化轨道吡啶在水中的溶解度远大于苯,主要原因是①
您最近一年使用:0次
名校
解题方法
5 . 已知 在一定温度下会发生二聚甚至多聚,如下图所示,下列说法中不正确的是
在一定温度下会发生二聚甚至多聚,如下图所示,下列说法中不正确的是
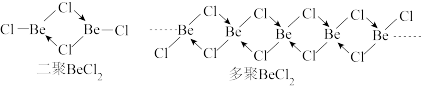
 在一定温度下会发生二聚甚至多聚,如下图所示,下列说法中不正确的是
在一定温度下会发生二聚甚至多聚,如下图所示,下列说法中不正确的是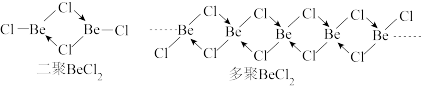
A. 单体(未聚合时)为直线型,中心原子为sp杂化 单体(未聚合时)为直线型,中心原子为sp杂化 |
B. 二聚时中心原子为 二聚时中心原子为 杂化,所有原子在同一平面 杂化,所有原子在同一平面 |
C. 多聚时Be周围的Cl呈正四面体,中心Be原子为 多聚时Be周围的Cl呈正四面体,中心Be原子为 杂化 杂化 |
| D.高温时候更容易呈现二聚或者多聚,低温时候为未聚合的单体 |
您最近一年使用:0次
名校
解题方法
6 . 下列说法中正确的是
A. 和 和 都是正四面体形分子,且键角都为 都是正四面体形分子,且键角都为 |
| B.键长H—F<H—Cl<H—Br<H—I,因此稳定性HF<HCl<HBr<HI |
C. 分子中孤电子对与成键电子对的排斥作用比成键电子对之间的排斥作用弱 分子中孤电子对与成键电子对的排斥作用比成键电子对之间的排斥作用弱 |
| D.金刚石晶体中的最小环为六元环,每个碳原子均被12个六元环共用 |
您最近一年使用:0次
解题方法
7 . LiAlH4是有机合成中常用的还原剂,可在乙醚中制得:4LiH+AlCl3=LiAlH4+3LiCl。下列说法错误的是
| A.Li+半径大于H-半径 |
| B.[AlH4]-空间构型是正四面体 |
| C.LiAlH4中存在离子键、σ键、配位键 |
| D.Al2Cl6为AlCl3的双聚分子,氯原子提供给铝原子孤对电子 |
您最近一年使用:0次
2021-05-19更新
|
163次组卷
|
2卷引用:重庆市缙云联盟2021-2022学年高一10月质量检测化学试题
解题方法
8 . 我国化学家合成的铬的化合物,通过烷基铝和[ph3C]+[B(C6F5)4]-活化后,对乙烯聚合表现出较好的催化活性。合成铭的化合物过程中一步反应如下,该反应涉及H、C、N、O、Cl、Cr等多种元素。
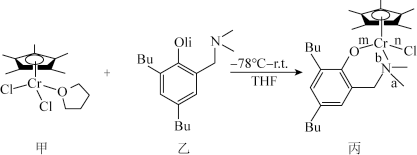
回答下列问题:
(1)下列状态的氯中,电离最外层一个电子所需能量最大的是_____________ (填标号)。
A.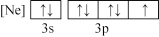 B.
B.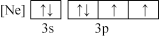
C. D.
D.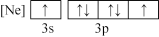
(2)化合物乙中碳原子采取的杂化方式为______ ,化合物丙中a、b、n、m处的化学键是配位键的是______ (填字母)处。
(3)Cr3+具有较强的稳定性,Cr3+的核外电子排布式为______ ;已知没有未成对d电子的过渡金属离子形成的水合离子是无色的,Ti4+、V3+、Ni2+三种离子的水合离子为无颜色的是______ (填离子符号)。
(4)ClO3-的键角小于ClO4-的键角,原因是______ 。
(5)根据结构与性质的关系解释,HNO2的酸性比HNO3弱的原因:______ 。
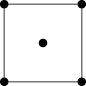
(6)水在合成铬的化合物的过程中作溶剂。研究表明水能凝结成13种类型的结晶体。其中重冰(密度比水大)属于立方晶系,其立方晶胞沿x、y、z轴的投影图如图所示,晶体中的H2O配位数为_____ 晶胞边长为a pm,则重冰的密度为____ g·cm-3(写出数学表达式,NA为阿伏加 德罗常数)。

回答下列问题:
(1)下列状态的氯中,电离最外层一个电子所需能量最大的是
A.
 B.
B.
C.
 D.
D.
(2)化合物乙中碳原子采取的杂化方式为
(3)Cr3+具有较强的稳定性,Cr3+的核外电子排布式为
(4)ClO3-的键角小于ClO4-的键角,原因是
(5)根据结构与性质的关系解释,HNO2的酸性比HNO3弱的原因:
(6)水在合成铬的化合物的过程中作溶剂。研究表明水能凝结成13种类型的结晶体。其中重冰(密度比水大)属于立方晶系,其立方晶胞沿x、y、z轴的投影图如图所示,晶体中的H2O配位数为

您最近一年使用:0次
2020-06-22更新
|
269次组卷
|
2卷引用:重庆市缙云教育联盟2020-2021学年高一下学期期末质量检测化学试题
9-10高一下·重庆·期末
9 . D、E、X、Y、Z是短周期元素,且原子序数逐渐增大,它们的最简单氢化物分子的空间结构依次是正四面体、三角锥形、正四面体、角形(V形)、直线型,回答下列问题:
(1)D和X形成的化合物中的化学键类型是_______________ ;D和Y形成的分子是_________ (填“极性”或“非极性”)分子。
(2)Y和Z的简单离子的半径大小为__________ (用离子符号和“>”、“=”或“<”表示)。
(3)比较元素非金属性的强弱有很多方法,关于D和X的非金属性强弱的研究方案中不可行的是_________ (填序号)。
①比较氢化物的稳定性 ②依据两元素在周期表的位置 ③比较两种单质的颜色
④比较单质与H2化合的难易程度 ⑤比较最高价氧化物对应水化物的酸性
(4)当满足一定比例时,Z的单质可与E的最简单氢化物反应生成一种盐和另一种单质,试写出该反应的化学方程式________________________ 。
(5)写出下列反应的化学方程式:
①工业上用D的单质制X的单质___________________________________ ;
②E的最高价含氧酸的浓溶液与单质D反应__________________________ 。
(6)E有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L甲气体与0.5L氧气混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,则生成的E的含氧酸盐的化学式是__________ 。
(1)D和X形成的化合物中的化学键类型是
(2)Y和Z的简单离子的半径大小为
(3)比较元素非金属性的强弱有很多方法,关于D和X的非金属性强弱的研究方案中不可行的是
①比较氢化物的稳定性 ②依据两元素在周期表的位置 ③比较两种单质的颜色
④比较单质与H2化合的难易程度 ⑤比较最高价氧化物对应水化物的酸性
(4)当满足一定比例时,Z的单质可与E的最简单氢化物反应生成一种盐和另一种单质,试写出该反应的化学方程式
(5)写出下列反应的化学方程式:
①工业上用D的单质制X的单质
②E的最高价含氧酸的浓溶液与单质D反应
(6)E有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L甲气体与0.5L氧气混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,则生成的E的含氧酸盐的化学式是
您最近一年使用:0次



