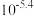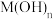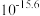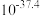名校
1 . 过硫酸钠(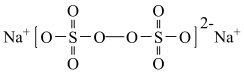 ),易溶于水,加热至65℃分解。作为强氧化剂,广泛应用于蓄电池工业、造纸工业、食品工业等。某化学小组对
),易溶于水,加热至65℃分解。作为强氧化剂,广泛应用于蓄电池工业、造纸工业、食品工业等。某化学小组对 制备和性质及用途进行探究。
制备和性质及用途进行探究。

工业制备过硫酸钠的反应原理:
主反应:

副反应:

实验室设计如图实验装置:
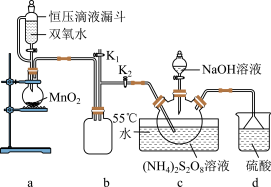
(2)装置b的作用是
(3)上述反应过程中,d装置中主要发生的化学反应方程式为
Ⅱ.探究
 的性质与用途
的性质与用途(4)
 用于废水中苯酚的降解
用于废水中苯酚的降解已知:a.
 具有强氧化性,
具有强氧化性, 浓度较高时会导致
浓度较高时会导致 淬灭。
淬灭。b.
 可将苯酚氧化,但反应速率较慢,加入
可将苯酚氧化,但反应速率较慢,加入 可加快反应。
可加快反应。过程为ⅰ.

ⅱ.
 将苯酚氧化为
将苯酚氧化为 气体
气体①
 氧化苯酚的离子方程式是
氧化苯酚的离子方程式是②将含
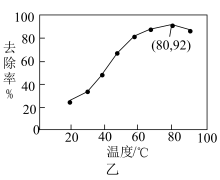
 的溶液稀释后加入苯酚的废水处理器中,调节溶液总体积为1L,pH=1,测得在相同时间内,不同条件下苯酚的降解率如图甲。
的溶液稀释后加入苯酚的废水处理器中,调节溶液总体积为1L,pH=1,测得在相同时间内,不同条件下苯酚的降解率如图甲。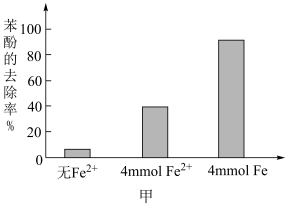
 ,可明显提高苯酚的降解率,主要原因是
,可明显提高苯酚的降解率,主要原因是(5)工业上利用
 能有效处理燃煤锅炉烟气中的NO气体。一定条件下,将含一定浓度NO的烟气以一定的速率通过含
能有效处理燃煤锅炉烟气中的NO气体。一定条件下,将含一定浓度NO的烟气以一定的速率通过含 的处理液中,NO去除率随温度变化的关系如图乙所示,80℃时,NO去除率为92%。若NO初始浓度为
的处理液中,NO去除率随温度变化的关系如图乙所示,80℃时,NO去除率为92%。若NO初始浓度为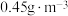 ,
, 达到最大去除率,NO去除的平均反应速率:
达到最大去除率,NO去除的平均反应速率:
 。
。
您最近一年使用:0次
名校
2 . 一种2-甲基色酮内酯(Y)可通过下列反应合成,下列说法正确的是
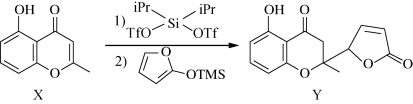
| A.X分子中碳原子的杂化类型都相同 | B.Y分子中所有碳原子均可能处于同平面 |
| C.X、Y均可发生消去反应 | D.1molY与NaOH反应最多消耗2molNaOH |
您最近一年使用:0次
昨日更新
|
107次组卷
|
2卷引用:重庆市名校联盟2023-2024学年高三下学期全真模拟考试化学试题
名校
3 . 下列说法错误的是
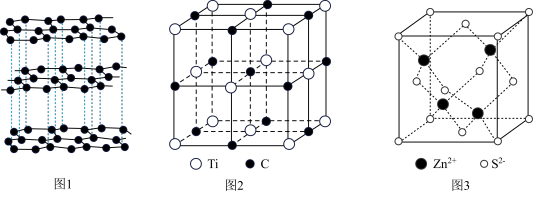
| A.图1晶体中既存在共价键又存在范德华力,属于混合型晶体 |
| B.图2为某气态团簇分子的结构,该气态团簇分子的化学式为TiC |
C.图3为ZnS的晶胞结构, 的配位数为4 的配位数为4 |
D.图3为ZnS的晶胞结构,已知该晶体的密度为 , , 为阿伏加德罗常数的值,则晶胞中 为阿伏加德罗常数的值,则晶胞中 和 和 的最近距离为 的最近距离为 |
您最近一年使用:0次
昨日更新
|
88次组卷
|
2卷引用:重庆市名校联盟2023-2024学年高三下学期全真模拟考试化学试题
名校
4 . 硫酸亚铁铵[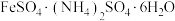 ,相对分子质量为M]为浅绿色晶体,在空气中能稳定存在,不易被氧化,溶于水,不溶于乙醇、实验室制备过程如下:
,相对分子质量为M]为浅绿色晶体,在空气中能稳定存在,不易被氧化,溶于水,不溶于乙醇、实验室制备过程如下:
第一步:在圆底烧瓶中称取mg铁屑,再用量筒量取15mL 的稀硫酸,实验装置如图所示,在80℃条件下电磁搅拌反应3min。
的稀硫酸,实验装置如图所示,在80℃条件下电磁搅拌反应3min。 溶液的蒸发皿中,水浴加热搅拌至硫酸铵全部溶解,停止搅拌,继续蒸发浓缩直至表面有晶膜出现。
溶液的蒸发皿中,水浴加热搅拌至硫酸铵全部溶解,停止搅拌,继续蒸发浓缩直至表面有晶膜出现。
第三步:冷却至室温,待有大量晶体析出时,减压过滤,用试剂N少量多次洗涤,干燥后,称得晶体质量为11.8g。计算产率。
回答下列问题:
(1)硫酸亚铁铵中组成元素的原子半径由大到小的顺序为___________ 。
(2)已知:Cr的3d比4p能量低得多,重铬酸钾具有二聚结构,它由两个通过氧原子键合在一起的铬原子组成,中心Cr为正四面体形,结构为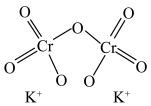 ,其中Cr原子的杂化方式为___________(填标号)。
,其中Cr原子的杂化方式为___________(填标号)。
(3)圆底烧瓶中生成 的离子方程式为
的离子方程式为___________ 。
(4)第二步中需要称量剩余铁屑质量的原因为___________ ,写出制备硫酸亚铁铵晶体的化学方程式:___________ 。
(5)试剂N是___________ 。
(6)准确称取0.8g硫酸亚铁铵晶体三份,分别放入三个250mL锥形瓶中,加入100mL水,20mL 的硫酸。1g氟化铵固体(不参与反应,有利于滴定终点的判断)。6~8滴二苯胺磺酸钠指示剂,用
的硫酸。1g氟化铵固体(不参与反应,有利于滴定终点的判断)。6~8滴二苯胺磺酸钠指示剂,用 重铬酸钾标准液进行滴定。
重铬酸钾标准液进行滴定。
①重铬酸钾在酸性条件下的还原产物为 ,写出该滴定反应的离子方程式:
,写出该滴定反应的离子方程式:___________ 。
②三次实验消耗标准液的体积分别是16.75mL、16.80mL、16.85mL,则硫酸亚铁铵晶体的纯度为___________ (写出含M的表达式)。
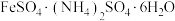 ,相对分子质量为M]为浅绿色晶体,在空气中能稳定存在,不易被氧化,溶于水,不溶于乙醇、实验室制备过程如下:
,相对分子质量为M]为浅绿色晶体,在空气中能稳定存在,不易被氧化,溶于水,不溶于乙醇、实验室制备过程如下:第一步:在圆底烧瓶中称取mg铁屑,再用量筒量取15mL
 的稀硫酸,实验装置如图所示,在80℃条件下电磁搅拌反应3min。
的稀硫酸,实验装置如图所示,在80℃条件下电磁搅拌反应3min。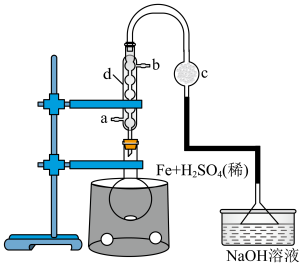
 溶液的蒸发皿中,水浴加热搅拌至硫酸铵全部溶解,停止搅拌,继续蒸发浓缩直至表面有晶膜出现。
溶液的蒸发皿中,水浴加热搅拌至硫酸铵全部溶解,停止搅拌,继续蒸发浓缩直至表面有晶膜出现。第三步:冷却至室温,待有大量晶体析出时,减压过滤,用试剂N少量多次洗涤,干燥后,称得晶体质量为11.8g。计算产率。
回答下列问题:
(1)硫酸亚铁铵中组成元素的原子半径由大到小的顺序为
(2)已知:Cr的3d比4p能量低得多,重铬酸钾具有二聚结构,它由两个通过氧原子键合在一起的铬原子组成,中心Cr为正四面体形,结构为
 ,其中Cr原子的杂化方式为___________(填标号)。
,其中Cr原子的杂化方式为___________(填标号)。A. | B. | C.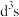 | D.sp |
(3)圆底烧瓶中生成
 的离子方程式为
的离子方程式为(4)第二步中需要称量剩余铁屑质量的原因为
(5)试剂N是
(6)准确称取0.8g硫酸亚铁铵晶体三份,分别放入三个250mL锥形瓶中,加入100mL水,20mL
 的硫酸。1g氟化铵固体(不参与反应,有利于滴定终点的判断)。6~8滴二苯胺磺酸钠指示剂,用
的硫酸。1g氟化铵固体(不参与反应,有利于滴定终点的判断)。6~8滴二苯胺磺酸钠指示剂,用 重铬酸钾标准液进行滴定。
重铬酸钾标准液进行滴定。①重铬酸钾在酸性条件下的还原产物为
 ,写出该滴定反应的离子方程式:
,写出该滴定反应的离子方程式:②三次实验消耗标准液的体积分别是16.75mL、16.80mL、16.85mL,则硫酸亚铁铵晶体的纯度为
您最近一年使用:0次
昨日更新
|
54次组卷
|
2卷引用:2024届重庆市渝西中学高三下学期模拟预测化学试题
5 . 化合物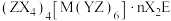 含有4种主族元素,只有M为金属,在地壳中的含量仅次于铝,Y、Z、E同周期。Z的基态原子价层p轨道为半充满状态,X的基态原子价层电子排布式为
含有4种主族元素,只有M为金属,在地壳中的含量仅次于铝,Y、Z、E同周期。Z的基态原子价层p轨道为半充满状态,X的基态原子价层电子排布式为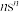 ,E的基态原子p轨道电子数与Y的价层电子数相同。下列说法正确的是
,E的基态原子p轨道电子数与Y的价层电子数相同。下列说法正确的是
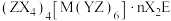 含有4种主族元素,只有M为金属,在地壳中的含量仅次于铝,Y、Z、E同周期。Z的基态原子价层p轨道为半充满状态,X的基态原子价层电子排布式为
含有4种主族元素,只有M为金属,在地壳中的含量仅次于铝,Y、Z、E同周期。Z的基态原子价层p轨道为半充满状态,X的基态原子价层电子排布式为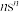 ,E的基态原子p轨道电子数与Y的价层电子数相同。下列说法正确的是
,E的基态原子p轨道电子数与Y的价层电子数相同。下列说法正确的是A.Y、Z、E与X形成的化合物的沸点: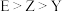 |
B.该化合物的溶液可以与 形成蓝色沉淀 形成蓝色沉淀 |
| C.Y、Z、E元素的第二电离能最大的是E |
D.阴离子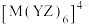 中M的配位数为4 中M的配位数为4 |
您最近一年使用:0次
昨日更新
|
75次组卷
|
2卷引用:2024届重庆市渝西中学高三下学期模拟预测化学试题
名校
6 . 体育锻炼时,大脑会产生5-羟色氨酸(结构如图所示),有益于防止焦虑、抑郁。下列说法正确的是
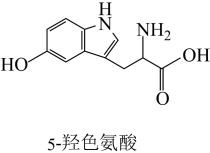
A.分子式为 |
| B.光照下与氯气反应,苯环上可以形成C—Cl键 |
| C.与足量碳酸氢钠溶液反应,所有的O—H键均可断裂 |
| D.环上的碳原子、氮原子的杂化类型相同 |
您最近一年使用:0次
名校
7 . 如图所示的两种化合物可应用于阻燃材料和生物材料的合成。其中W、X、Y、Z为原子序数依次增大的短周期元素,X和Z同主族,Y原子序数为W原子价电子数的3倍。下列说法正确的是
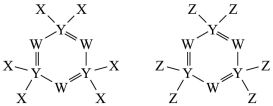
| A.电负性:X>Y>Z |
| B.HZO为弱酸,分子的空间结构为直线型 |
| C.最高价含氧酸酸性:W<Y |
| D.X、W和氢三种元素可形成含阴阳离子都为10电子的化合物 |
您最近一年使用:0次
8 .  是高效、安全的广谱杀菌剂。下列说法错误的是
是高效、安全的广谱杀菌剂。下列说法错误的是
 是高效、安全的广谱杀菌剂。下列说法错误的是
是高效、安全的广谱杀菌剂。下列说法错误的是A.第一电离能: | B. 键角大小; 键角大小;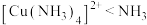 |
C. 中, 中, 提供空轨道, 提供空轨道, 作配体 作配体 | D.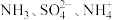 的中心原子的杂化方式相同 的中心原子的杂化方式相同 |
您最近一年使用:0次
名校
9 . 利用高压氨浸法从黄铜矿中提取铜具有提取率高、污染小等优点,被广泛使用。一种由黄铜矿(主要成分为 ,含少量
,含少量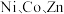 等元素)提取铜的工艺如下:
等元素)提取铜的工艺如下:
I.“固液分离”后溶液中主要离子为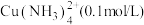 ,杂质离子为
,杂质离子为 、
、 、
、 等阳离子(浓度均为
等阳离子(浓度均为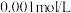 );“电积”时溶液中主要溶质为
);“电积”时溶液中主要溶质为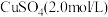 。
。
Ⅱ.不稳定常数对 ,不稳定常数
,不稳定常数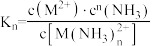
Ⅲ.溶度积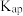
(1)基态 原子的价电子排布式为
原子的价电子排布式为________________ , 中氮原子的杂化方式为
中氮原子的杂化方式为_______________ 。
(2)①浸出前“粉碎磨矿”的目的是_______________ ,②“固液分离”用到的操作是_______________ 。
(3)①“搅拌浸出”主要成分反应的化学方程式为______________ 。(已知:硫元素变成最高价,铁元素变成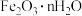 );
);
②铁元素没有以配合物离子存在的原因是__________________ 。
(4)常温下,“沉钴”步骤中,溶液中氨气分子浓度为 ,若要“沉钻”完全[
,若要“沉钻”完全[ 浓度为
浓度为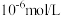 ],需调节
],需调节 至
至___________ ,“萃取”和“反萃取”的作用为________________ 。
 ,含少量
,含少量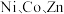 等元素)提取铜的工艺如下:
等元素)提取铜的工艺如下: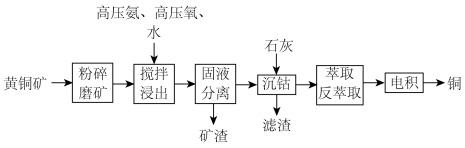
I.“固液分离”后溶液中主要离子为
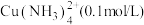 ,杂质离子为
,杂质离子为 、
、 、
、 等阳离子(浓度均为
等阳离子(浓度均为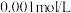 );“电积”时溶液中主要溶质为
);“电积”时溶液中主要溶质为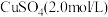 。
。Ⅱ.不稳定常数对
 ,不稳定常数
,不稳定常数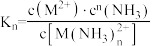
|
|
|
不稳定常数 |
| 0.2 |
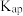
|
|
|
溶度积 |
|
|
(1)基态
 原子的价电子排布式为
原子的价电子排布式为 中氮原子的杂化方式为
中氮原子的杂化方式为(2)①浸出前“粉碎磨矿”的目的是
(3)①“搅拌浸出”主要成分反应的化学方程式为
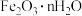 );
);②铁元素没有以配合物离子存在的原因是
(4)常温下,“沉钴”步骤中,溶液中氨气分子浓度为
 ,若要“沉钻”完全[
,若要“沉钻”完全[ 浓度为
浓度为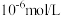 ],需调节
],需调节 至
至
您最近一年使用:0次
名校
解题方法
10 . 下列离子方程式错误的是
A.向氨水中加入少量氯化银: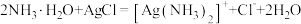 |
B.向明矾溶液中滴加氢氧化钡溶液至沉淀质量最大: |
C.用惰性电极电解硫酸铜溶液: |
D.硝酸铁溶液中通入少量二氧化硫: |
您最近一年使用:0次



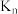 (常温)
(常温)