名校
解题方法
1 . 下列实验操作及现象与对应结论匹配的是
| 选项 | 实验操作及现象 | 结论 |
| A | 取一定量Na2SO3样品,溶解后加入BaCl2溶液,产生白色沉淀。加入浓HNO3,仍有沉淀。 | 此样品中含有SO |
| B | 相同温度下,分别测定相同浓度的NaNO2和CH3COONa溶液pH,NaNO2溶液的pH约为8,CH3COONa溶液的pH约为9 | 相同温度下,Ka(HNO2)<Ka(CH3COOH) |
| C | 向硫酸铜溶液中滴加浓盐酸至过量,溶液由蓝色变为绿色。 | [Cu(H2O)4]2+转化为[CuCl4]2- |
| D | 将Zn(OH)2固体粉末加入过量NaOH溶液中,充分搅拌,溶解得到无色溶液。 | Zn(OH)2既体现碱性又体现酸性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-26更新
|
234次组卷
|
4卷引用:重庆市西南大学附属中学校2024届高三下学期全真模拟集训(二)化学试题
名校
2 . 我国科学家发现一种能用于“点击反应”的新分子,结构如下图所示。其中X、Y、Z和W是原子序数依次增大的短周期主族元素,Y与Z是同一主族元素。下列说法正确的是

| A.简单离子半径:W>Z>Y>X | B.第一电离能:Y>X>Z>W |
| C.简单氢化物的沸点:Y>X>Z | D. 分子中键角均为120° 分子中键角均为120° |
您最近一年使用:0次
2023-12-26更新
|
316次组卷
|
2卷引用:重庆十八中两江实验中学校2023-2024学年高三下学期一诊模拟检测化学试题
名校
3 .  在
在 中可生成硝酰正离子(
中可生成硝酰正离子( ):
):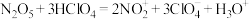 。已知
。已知 的结构如下,下列说法
的结构如下,下列说法错误 的是

 在
在 中可生成硝酰正离子(
中可生成硝酰正离子( ):
):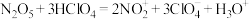 。已知
。已知 的结构如下,下列说法
的结构如下,下列说法
A. 是非极性分子 是非极性分子 | B. 分子间存在氢键 分子间存在氢键 |
C. 空间构型为直线形 空间构型为直线形 | D. 中的O是 中的O是 杂化 杂化 |
您最近一年使用:0次
名校
4 .  与汞共热可得到
与汞共热可得到 和一种汞盐,下列有关说法正确的是
和一种汞盐,下列有关说法正确的是
 与汞共热可得到
与汞共热可得到 和一种汞盐,下列有关说法正确的是
和一种汞盐,下列有关说法正确的是A. 的空间结构为正四面体形 的空间结构为正四面体形 | B. 分子中的 分子中的 原子是 原子是 杂化 杂化 |
C. 的键角大于 的键角大于 的键角 的键角 | D. 分子存在 分子存在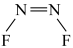 和 和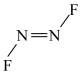 两种结构 两种结构 |
您最近一年使用:0次
5 .  (三氯化六氨合钴)是合成其他含钴配合物的理要原料,实验空中可由金属钴及其他原料制备
(三氯化六氨合钴)是合成其他含钴配合物的理要原料,实验空中可由金属钴及其他原料制备 。
。
已知:(1) 在
在 时恰好完全沉淀为
时恰好完全沉淀为 ;
;
(2)不同温度下 在水中的溶解度如图所示。
在水中的溶解度如图所示。
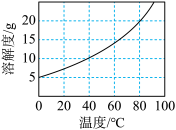
(一) 的制备
的制备
 易潮解,
易潮解,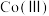 的氧化性强于
的氧化性强于 ,可用金属钴与氯气反应制备
,可用金属钴与氯气反应制备 。实验中利用如图装置(连接用橡胶管省略)进行制备。
。实验中利用如图装置(连接用橡胶管省略)进行制备。
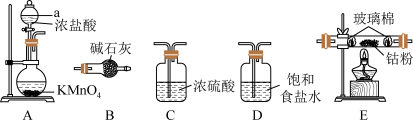
(1)用图中的装置组合制备 ,连接顺序为
,连接顺序为_______ 。装置B的作用是_______ 。
(2)装置A中发生反应的离子方程式为_______ 。
(二) 的制备
的制备
步骤如下:
I.在 锥形瓶内加入
锥形瓶内加入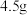 研细的
研细的 ,
, 和
和 水,加热溶解后加入
水,加热溶解后加入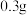 活性炭作催化剂。
活性炭作催化剂。
Ⅱ.冷却后,加入浓氨水混合均匀。控制温度在 以下并缓慢加入
以下并缓慢加入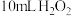 溶液。
溶液。
Ⅲ.在 下反应一段时间后,经过_______、_______、过滤、洗涤、干燥等操作,得到
下反应一段时间后,经过_______、_______、过滤、洗涤、干燥等操作,得到 晶体。
晶体。
(3)在加入浓氨水前,需在步骤I中加入 ,请结合平衡移动原理解释原因
,请结合平衡移动原理解释原因_______ 。
(4)步骤Ⅱ中在加入 浴液时,控制温度在
浴液时,控制温度在 以下并缓慢加入的目的是
以下并缓慢加入的目的是_______ 、_______ 。
(5)制备 的总反应的化学方程式为
的总反应的化学方程式为_______ 。
(6)步骤Ⅲ中的操作名称为_______ 、_______
 (三氯化六氨合钴)是合成其他含钴配合物的理要原料,实验空中可由金属钴及其他原料制备
(三氯化六氨合钴)是合成其他含钴配合物的理要原料,实验空中可由金属钴及其他原料制备 。
。已知:(1)
 在
在 时恰好完全沉淀为
时恰好完全沉淀为 ;
;(2)不同温度下
 在水中的溶解度如图所示。
在水中的溶解度如图所示。
(一)
 的制备
的制备 易潮解,
易潮解,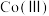 的氧化性强于
的氧化性强于 ,可用金属钴与氯气反应制备
,可用金属钴与氯气反应制备 。实验中利用如图装置(连接用橡胶管省略)进行制备。
。实验中利用如图装置(连接用橡胶管省略)进行制备。
(1)用图中的装置组合制备
 ,连接顺序为
,连接顺序为(2)装置A中发生反应的离子方程式为
(二)
 的制备
的制备步骤如下:
I.在
 锥形瓶内加入
锥形瓶内加入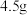 研细的
研细的 ,
, 和
和 水,加热溶解后加入
水,加热溶解后加入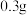 活性炭作催化剂。
活性炭作催化剂。Ⅱ.冷却后,加入浓氨水混合均匀。控制温度在
 以下并缓慢加入
以下并缓慢加入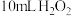 溶液。
溶液。Ⅲ.在
 下反应一段时间后,经过_______、_______、过滤、洗涤、干燥等操作,得到
下反应一段时间后,经过_______、_______、过滤、洗涤、干燥等操作,得到 晶体。
晶体。(3)在加入浓氨水前,需在步骤I中加入
 ,请结合平衡移动原理解释原因
,请结合平衡移动原理解释原因(4)步骤Ⅱ中在加入
 浴液时,控制温度在
浴液时,控制温度在 以下并缓慢加入的目的是
以下并缓慢加入的目的是(5)制备
 的总反应的化学方程式为
的总反应的化学方程式为(6)步骤Ⅲ中的操作名称为
您最近一年使用:0次
名校
6 . 锑白( ,性质类似
,性质类似 )可用作白色颜料和阻燃剂。一种从含锑工业废渣(主要成分是
)可用作白色颜料和阻燃剂。一种从含锑工业废渣(主要成分是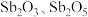 ,含有CuO、
,含有CuO、 和
和 等杂质)中制取
等杂质)中制取 的工业流程如下图所示:
的工业流程如下图所示:
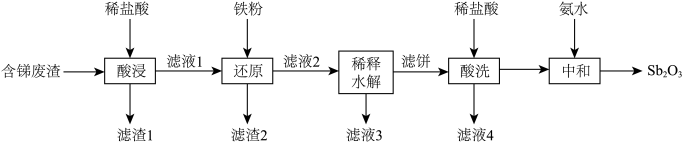
回答下列问题:
(1)锑元素原子序数为51,基态锑原子的价电子轨道表示式为___________ 。
(2)“还原”加入过量铁粉的目的是___________ (填序号)。
a.将 转化为
转化为 b.将
b.将 转化为
转化为 c.将铜离子转化为铜单质
c.将铜离子转化为铜单质
(3)“滤饼”的成分是SbOCl,“稀释水解”主要反应的离子方程式为___________ ;该操作中需要搅拌的原因是___________ 。
(4)“酸洗”后检验沉淀是否洗净的试剂是___________ (填名称)。
(5)“中和”时生成 的化学方程式为
的化学方程式为___________ ,“中和”时不宜将氨水换成氢氧化钠溶液,原因是___________ 。
(6)我国锑的蕴藏量占世界第一位,而锑的化合物也用途广泛。
氟锑酸化学式为 ,酸性比纯硫酸强
,酸性比纯硫酸强 倍,称为超强酸,其与HF作用生成
倍,称为超强酸,其与HF作用生成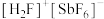 ,则其阳离子的空间结构为
,则其阳离子的空间结构为___________ ,阴离子中心原子的杂化方式合理的是___________ 。
a. b.
b. c.
c. d.
d.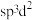
 ,性质类似
,性质类似 )可用作白色颜料和阻燃剂。一种从含锑工业废渣(主要成分是
)可用作白色颜料和阻燃剂。一种从含锑工业废渣(主要成分是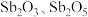 ,含有CuO、
,含有CuO、 和
和 等杂质)中制取
等杂质)中制取 的工业流程如下图所示:
的工业流程如下图所示:
回答下列问题:
(1)锑元素原子序数为51,基态锑原子的价电子轨道表示式为
(2)“还原”加入过量铁粉的目的是
a.将
 转化为
转化为 b.将
b.将 转化为
转化为 c.将铜离子转化为铜单质
c.将铜离子转化为铜单质(3)“滤饼”的成分是SbOCl,“稀释水解”主要反应的离子方程式为
(4)“酸洗”后检验沉淀是否洗净的试剂是
(5)“中和”时生成
 的化学方程式为
的化学方程式为(6)我国锑的蕴藏量占世界第一位,而锑的化合物也用途广泛。
氟锑酸化学式为
 ,酸性比纯硫酸强
,酸性比纯硫酸强 倍,称为超强酸,其与HF作用生成
倍,称为超强酸,其与HF作用生成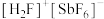 ,则其阳离子的空间结构为
,则其阳离子的空间结构为a.
 b.
b. c.
c. d.
d.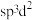
您最近一年使用:0次
名校
7 . 以甲醇为溶剂, 可与色胺酮分子配位结合,形成对DNA具有切割作用的色胺酮钴配合物(合成过程如图所示)。下列说法不正确的是
可与色胺酮分子配位结合,形成对DNA具有切割作用的色胺酮钴配合物(合成过程如图所示)。下列说法不正确的是
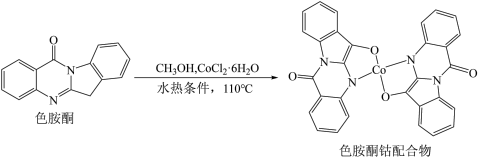
 可与色胺酮分子配位结合,形成对DNA具有切割作用的色胺酮钴配合物(合成过程如图所示)。下列说法不正确的是
可与色胺酮分子配位结合,形成对DNA具有切割作用的色胺酮钴配合物(合成过程如图所示)。下列说法不正确的是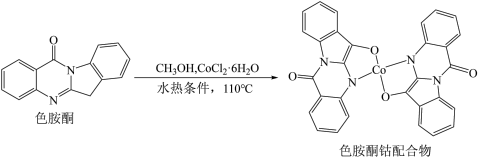
| A.色胺酮分子中所含元素电负性大小关系为:H<C<N<O |
B.色胺酮分子中的碳均采取 杂化 杂化 |
| C.色胺酮钴配合物中钴的配位数为4 |
D.色胺酮钴配合物晶胞中还含有一个 分子, 分子, 通过氢键与色胺酮钴配合物相结合 通过氢键与色胺酮钴配合物相结合 |
您最近一年使用:0次
名校
解题方法
8 . 金粉溶于过氧化氢-浓盐酸可以安全环保的制备氯金酸(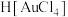 ),其化学方程式为:
),其化学方程式为: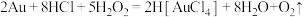 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
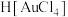 ),其化学方程式为:
),其化学方程式为: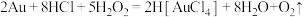 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.消耗1molAu,反应转移的电子数为 |
B.消耗2molHCl生成的 分子数为 分子数为 |
C.消耗85g ,产物中形成的配位键数目为 ,产物中形成的配位键数目为 |
D.2mol液态水中含有的氢键数目为 |
您最近一年使用:0次
2023-05-31更新
|
2024次组卷
|
7卷引用:重庆市南开中学高2023届高三下学期第十次质量检测化学试题
重庆市南开中学高2023届高三下学期第十次质量检测化学试题化学02(15+4模式)2024年1月“九省联考”考前化学猜想卷(已下线)选择题1-52024届湖南省长沙市第一中高三下学期高考适应性演练(一)化学试题(已下线)第9讲 物质的量浓度(已下线)阿伏伽德罗常数的应用(已下线)热点04 有关阿伏加德罗常数的正误判断
名校
解题方法
9 . 2023年5月、神舟十六号载人飞船预计在酒泉卫星发射中心发射。发射航天器的材料、常用的燃料及助燃剂如表所示。下列有关叙述正确的是
| 航天器材料 | 液体燃料 | 固体燃料 | 助燃剂 |
| 钢、钛合金、石墨纤维等 | 液氢、低级醇类、1,2-二甲基肼( ) ) | 硼氢化钠( ) ) | 液氧、五氟化溴( )、高氯酸铵( )、高氯酸铵(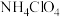 ) ) |
A.基态Fe原子的简化电子排布式为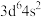 |
B. 的阴离子空间结构为正四面体形 的阴离子空间结构为正四面体形 |
| C.基态N原子核外电子占据的最高能级的电子云轮廓为球形 |
D. 为非极性分子 为非极性分子 |
您最近一年使用:0次
名校
10 . 下列根据实验操作及现象所得出的结论正确的是
实验操作及现象 | 结论 | |
A | 向5mL0.1mol/LKSCN溶液中加入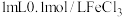 溶液,达平衡后,再加入 溶液,达平衡后,再加入 固体,溶液红色加深 固体,溶液红色加深 | 说明增加反应物浓度,化学平衡正向移动 |
B | 用灼烧后的铂丝蘸取少量某溶液进行焰色试验,观察到火焰呈黄色 | 肯定有钠元素,可能含钾元素 |
C | 向 中分别加入稀盐酸和氨水,沉淀均溶解 中分别加入稀盐酸和氨水,沉淀均溶解 |  是两性氢氧化物 是两性氢氧化物 |
D | 取适量 溶液于试管中,测定pH值,然后加热一段时间,冷却至原温度,再次测定该溶液pH值变小 溶液于试管中,测定pH值,然后加热一段时间,冷却至原温度,再次测定该溶液pH值变小 |  的水解为吸热过程 的水解为吸热过程 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



