解题方法
1 . 硼及其化合物在材料制造、有机合成等方面用途非常广泛,硼的一些化合物表现出缺电子特征。回答下列问题:
(1)基态硼原子的电子排布式为_______ ;B和Al的第一电离能I1(B)_______ I1(Al)(填“>”或“=”或“<”)。
(2)H3BO3(层状结构)的结构示意图如下,在硼酸的层状结构中O的杂化类型是_______ ,层内存在的作用力有_______ 。硼酸显弱酸性与[B(OH)4]-配离子有关,硼酸的电离方程式:_______ 。

(3)自然界中不存在单质硼,硼的氢化物也很少,主要存在的是硼的含氧化合物,根据表中数据分析其原因是_______ 。
(4)已知晶体硼的熔、沸点及硬度数据和基本结构单元(由硼原子组成的正二十面体如图1所示,每个三角形均为正三角形,每个顶点为一个硼原子)如下:

①晶体硼属于原子(共价)晶体,其理由是_______ 。
②每一个硼基本单元由_______ 个原子组成;
③碳化硼,别名黑钻石,是已知最坚硬的三种材料之一,仅次于金刚石和立方氮化硼,图2为碳化硼晶胞,其化学式为_______ ;
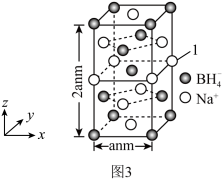
(5)硼氢化钠是一种常用的还原剂。其晶胞结构如图3所示,标注为“1”的Na+坐标参数为_______ 。已知NA代表阿伏加德罗常数的值,则硼氢化钠晶体的密度为ρ=_______ g·cm-3(用含NA的代数式表示)。
(1)基态硼原子的电子排布式为
(2)H3BO3(层状结构)的结构示意图如下,在硼酸的层状结构中O的杂化类型是

(3)自然界中不存在单质硼,硼的氢化物也很少,主要存在的是硼的含氧化合物,根据表中数据分析其原因是
| 化学键 | B-H | B-O | B-B |
| 键能(kJ·mol-1) | 389 | 561 | 293 |
| 晶体 | 金刚石 | 晶体硅 | 晶体硼 |
| 熔点(K) | 3832 | 1683 | 2573 |
| 沸点(K) | 5100 | 2628 | 3823 |
| 硬度 | 10 | 7.0 | 9.6 |

①晶体硼属于原子(共价)晶体,其理由是
②每一个硼基本单元由
③碳化硼,别名黑钻石,是已知最坚硬的三种材料之一,仅次于金刚石和立方氮化硼,图2为碳化硼晶胞,其化学式为
(5)硼氢化钠是一种常用的还原剂。其晶胞结构如图3所示,标注为“1”的Na+坐标参数为

您最近一年使用:0次
2023-03-12更新
|
749次组卷
|
3卷引用:内蒙古呼和浩特市2023届高三第一次质量数据监测理科综合化学试题
解题方法
2 . 镓(Ga)、锗(Ge)、硅(Si)、硒(Se)的单质及某些化合物如砷化镓、磷化镓等都是常用的半导体材料,应用于航空航天测控、光纤通讯等领域。回答下列问题:
(1)科学家常利用___________ ,区分晶体硅和无定形硅。
(2)硒常用作光敏材料,根据元素周期律,原子半径Ga___________ As(填“>”或“<”,后同)。第一电离能Ga___________ As。与硒同周期的p区元素中第一电离能大于硒的元素有___________ 种; 的空间构型是
的空间构型是___________ 。
(3)GaN、GaP、GaAs都是很好的半导体材料,熔点如表所示,分析其变化原因:___________ 。
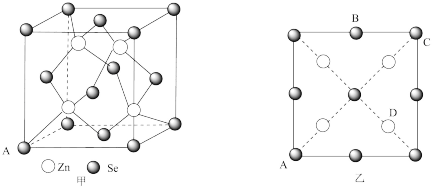
(4)硒化锌( )也是一种重要的半导体材料,其晶胞结构图甲所示,该晶胞中硒原子的配位数是
)也是一种重要的半导体材料,其晶胞结构图甲所示,该晶胞中硒原子的配位数是___________ ;已知晶胞边长为 ,乙图为甲图的俯视图,A点坐标为
,乙图为甲图的俯视图,A点坐标为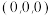 ,B点坐标为
,B点坐标为 ,则D点坐标
,则D点坐标___________ ;若该晶胞密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数 为
为___________  (只列出计算式)。
(只列出计算式)。
(1)科学家常利用
(2)硒常用作光敏材料,根据元素周期律,原子半径Ga
 的空间构型是
的空间构型是(3)GaN、GaP、GaAs都是很好的半导体材料,熔点如表所示,分析其变化原因:
| 物质 |  |  | 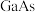 |
| 熔点 |  |  | 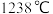 |
 )也是一种重要的半导体材料,其晶胞结构图甲所示,该晶胞中硒原子的配位数是
)也是一种重要的半导体材料,其晶胞结构图甲所示,该晶胞中硒原子的配位数是 ,乙图为甲图的俯视图,A点坐标为
,乙图为甲图的俯视图,A点坐标为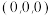 ,B点坐标为
,B点坐标为 ,则D点坐标
,则D点坐标 ,则阿伏加德罗常数
,则阿伏加德罗常数 为
为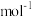 (只列出计算式)。
(只列出计算式)。
您最近一年使用:0次
解题方法
3 . 含铜物质在生产生活中有着广泛应用回答下列问题:
(1)基态Cu原子最高能层的电子排布式为___ 。
(2)CuCl2稀溶液中存[Cu(H2O)6]2+。已知d轨道也可以参与杂化,则[Cu(H2O)6]2+中Cu的杂化方式为___ (填选项字母)。
(3)铜盐属于重金属盐,铜盐中毒可用青霉胺解毒,解毒原理如下:Cu2+能与青霉胺形成环状络合物,该环状络合物无毒、易溶于水,可经尿液排出。
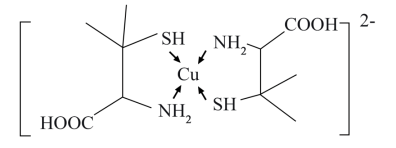
①比较硫化氢与氨气键角的大小:H2S___ NH3(填“>”或“<”) 。
②第二周期元素中,第一电离能大于N的元素有___ (用元素符号表示)。
③请解释该化合物易溶于水的主要原因:___ 。
④该环状络合物中,VSEPR模型为四面体或正四面体的非金属原子共有___ 个。
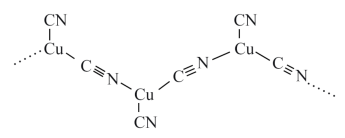
(4)Cu+与CN-形成长链阴离子,其结构片段如图所示,该阴离子中σ键与π键数目之比为___ 。
(5)一种由Cu、In、Te组成的高熵合金具有优良的热电性能,其四方晶胞如图所示:

①In的配位数为___ ;晶体中Te原子填充在Cu、In围成的四面体空隙中,则四面体空隙的占有率为___ 。
②若晶胞底边正方形的边长均为anm,高为cnm,阿伏加德罗常数的值为NA设晶体的最简式的式量为Mr,则该晶体的密度为____ g·cm-3(列出计算式)。
(1)基态Cu原子最高能层的电子排布式为
(2)CuCl2稀溶液中存[Cu(H2O)6]2+。已知d轨道也可以参与杂化,则[Cu(H2O)6]2+中Cu的杂化方式为
| A.sp3 | B.sp3d | C.d2sp3 | D.dsp2 |

①比较硫化氢与氨气键角的大小:H2S
②第二周期元素中,第一电离能大于N的元素有
③请解释该化合物易溶于水的主要原因:
④该环状络合物中,VSEPR模型为四面体或正四面体的非金属原子共有
(4)Cu+与CN-形成长链阴离子,其结构片段如图所示,该阴离子中σ键与π键数目之比为

(5)一种由Cu、In、Te组成的高熵合金具有优良的热电性能,其四方晶胞如图所示:

①In的配位数为
②若晶胞底边正方形的边长均为anm,高为cnm,阿伏加德罗常数的值为NA设晶体的最简式的式量为Mr,则该晶体的密度为
您最近一年使用:0次
解题方法
4 . 在元素周期表中,铜副族(IB族)包括铜、银、金等元素,在生产、生活和科研中都有着广泛用途和重要的研究价值。
(1)Ag元素在元素周期表分区中属于_______ 区,基态Ag原子的价电子排布式为_______ 。
(2)硫代硫酸银(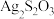 )是微溶于水的白色化合物,它能溶于过量的硫代硫酸钠(
)是微溶于水的白色化合物,它能溶于过量的硫代硫酸钠( )溶液生成
)溶液生成 等络阴离子。
等络阴离子。
①依据 理论推测
理论推测 的空间构型为
的空间构型为_______ ,中心原子S的杂化方式为_______ 。
②在 中配位原子是S原子而非O原子,其原因是
中配位原子是S原子而非O原子,其原因是_______ 。
(3)碘化银常用于做人工增雨剂。其中碘元素形成的最高价氧化物对应水化物有 (偏高碘酸,不稳定)和
(偏高碘酸,不稳定)和 (正高碘酸)等多种形式,它们的酸性
(正高碘酸)等多种形式,它们的酸性
_______  (填“弱于”、“等于”或“强于”)。而
(填“弱于”、“等于”或“强于”)。而 、HBr、HCl的水溶液酸性的排序为由强到弱,其结构原因是
、HBr、HCl的水溶液酸性的排序为由强到弱,其结构原因是_______ 。
(4)在离子晶体中,当 (阳离子)∶r(阴离子)
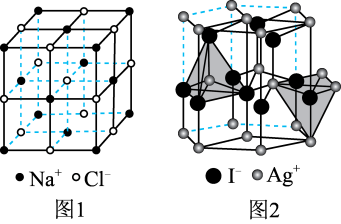
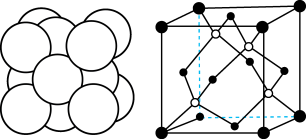
(阳离子)∶r(阴离子) 时,AB型化合物往往采用和NaCl晶体相同的晶体结构(如下图1)。已知
时,AB型化合物往往采用和NaCl晶体相同的晶体结构(如下图1)。已知 ,但在室温下,AgI的晶体结构如下图2所示,称为六方碘化银。I-的配位数为
,但在室温下,AgI的晶体结构如下图2所示,称为六方碘化银。I-的配位数为_______ ,造成AgI晶体结构不同于NaCl晶体结构的原因不可能是_______ (填标号)。
a.几何因素 b.电荷因素 c.键性因素
(5)Cu与Au的某种合金可形成面心立方最密堆积的晶体(密度为 ),在该晶胞中Cu原子处于面心,用NA表示阿伏加德罗常数的值。该晶体具有储氢功能,氢原子可进入到Cu原子与Au原子构成的立方体空隙中,储氢后的晶胞结构与金刚石晶胞结构(如图)相似,该晶体储氢后的化学式为
),在该晶胞中Cu原子处于面心,用NA表示阿伏加德罗常数的值。该晶体具有储氢功能,氢原子可进入到Cu原子与Au原子构成的立方体空隙中,储氢后的晶胞结构与金刚石晶胞结构(如图)相似,该晶体储氢后的化学式为_______ ;若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为_______ (储氢能力 )
)
(1)Ag元素在元素周期表分区中属于
(2)硫代硫酸银(
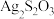 )是微溶于水的白色化合物,它能溶于过量的硫代硫酸钠(
)是微溶于水的白色化合物,它能溶于过量的硫代硫酸钠( )溶液生成
)溶液生成 等络阴离子。
等络阴离子。①依据
 理论推测
理论推测 的空间构型为
的空间构型为②在
 中配位原子是S原子而非O原子,其原因是
中配位原子是S原子而非O原子,其原因是(3)碘化银常用于做人工增雨剂。其中碘元素形成的最高价氧化物对应水化物有
 (偏高碘酸,不稳定)和
(偏高碘酸,不稳定)和 (正高碘酸)等多种形式,它们的酸性
(正高碘酸)等多种形式,它们的酸性
 (填“弱于”、“等于”或“强于”)。而
(填“弱于”、“等于”或“强于”)。而 、HBr、HCl的水溶液酸性的排序为由强到弱,其结构原因是
、HBr、HCl的水溶液酸性的排序为由强到弱,其结构原因是(4)在离子晶体中,当
 (阳离子)∶r(阴离子)
(阳离子)∶r(阴离子) 时,AB型化合物往往采用和NaCl晶体相同的晶体结构(如下图1)。已知
时,AB型化合物往往采用和NaCl晶体相同的晶体结构(如下图1)。已知 ,但在室温下,AgI的晶体结构如下图2所示,称为六方碘化银。I-的配位数为
,但在室温下,AgI的晶体结构如下图2所示,称为六方碘化银。I-的配位数为a.几何因素 b.电荷因素 c.键性因素

(5)Cu与Au的某种合金可形成面心立方最密堆积的晶体(密度为
 ),在该晶胞中Cu原子处于面心,用NA表示阿伏加德罗常数的值。该晶体具有储氢功能,氢原子可进入到Cu原子与Au原子构成的立方体空隙中,储氢后的晶胞结构与金刚石晶胞结构(如图)相似,该晶体储氢后的化学式为
),在该晶胞中Cu原子处于面心,用NA表示阿伏加德罗常数的值。该晶体具有储氢功能,氢原子可进入到Cu原子与Au原子构成的立方体空隙中,储氢后的晶胞结构与金刚石晶胞结构(如图)相似,该晶体储氢后的化学式为 )
)
您最近一年使用:0次
2022-04-25更新
|
1244次组卷
|
4卷引用:内蒙古包头市2022届高三第二次模拟考试理综试卷化学试题
内蒙古包头市2022届高三第二次模拟考试理综试卷化学试题(已下线)押全国卷理综第35题 物质结构与性质-备战2022年高考化学临考题号押题(课标全国卷)(已下线)【直抵名校】01-备战2022年高考化学名校进阶模拟卷(通用版)河南省南阳市2021-2022学年高二下学期期末考试化学试题
解题方法
5 . 铜是人类知道最早的金属之一,也是广泛使用的第一种金属。回答下列问题:
(1)镍白铜(铜镍合金)可用于制作仿银饰品。第二电离能I2(Cu)___________ (填“>”或“<”)I2(Ni),其原因为___________ 。
(2)向[Cu(NH3)2]Cl溶液中通入乙炔(C2H2)气体,可生成红棕色沉淀Cu2C2。
①C2H2分子中σ键与π键的数目之比为___________ ;碳原子的杂化方式为___________ ;
②写出与Cu2C2中阴离子C 互为等电子体的一种分子:
互为等电子体的一种分子:___________ 。
(3)在弱碱性环境中,EDTA( )易与Cu2+形成如图所示配离子,常用于Cu2+的定量测定。
)易与Cu2+形成如图所示配离子,常用于Cu2+的定量测定。
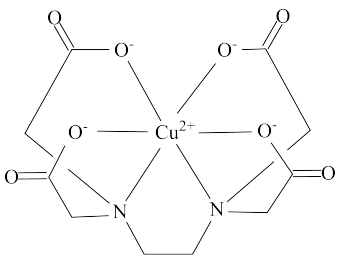
①1mol该配离子中配体数目为___________ (阿伏加德罗常数的值为NA)。
②EDTA能溶于水的原因为___________ 。
(4)铜与氧构成的某种化合物的立方晶胞如图甲所示,图乙是沿晶胞对角面取得的截图,晶胞中所有原子均在对角面上。该化合物的化学式为___________ ,若Cu原子之间最短距离为dpm,阿伏加德罗常数的值为NA,该晶体的密度为___________ g•cm-3(列出计算式即可)。

(1)镍白铜(铜镍合金)可用于制作仿银饰品。第二电离能I2(Cu)
(2)向[Cu(NH3)2]Cl溶液中通入乙炔(C2H2)气体,可生成红棕色沉淀Cu2C2。
①C2H2分子中σ键与π键的数目之比为
②写出与Cu2C2中阴离子C
 互为等电子体的一种分子:
互为等电子体的一种分子:(3)在弱碱性环境中,EDTA(
 )易与Cu2+形成如图所示配离子,常用于Cu2+的定量测定。
)易与Cu2+形成如图所示配离子,常用于Cu2+的定量测定。
①1mol该配离子中配体数目为
②EDTA能溶于水的原因为
(4)铜与氧构成的某种化合物的立方晶胞如图甲所示,图乙是沿晶胞对角面取得的截图,晶胞中所有原子均在对角面上。该化合物的化学式为

您最近一年使用:0次
名校
解题方法
6 . 金属钛(Ti)及化合物在化工、医药、材料等领域具有广泛应用。回答下列问题:
(1)Li4Ti5O12是电池的电极材料。与Li不同族但性质相似的元素是___________ ,其电子占据最高能级的电子云轮廓图是___________
(2)K与Ti位于同一周期,K和Ti的第一电离能(I1)较大的是___________ ,它们的第二电离能(I2)分别为3051kJ/mol、1310kJ/mol,其原因是___________ 。
(3)钛与卤素形成的化合物TiX4熔点如下表
它们熔点差异的原因___________
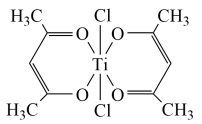
(4)Ti(IV)的某配合物可用于催化环烯烃聚合,其结构如图所示,该配合物中:Ti的配位数为___________ ,与Ti形成配位键的元素是___________ ,碳碳键类型是___________ ;所含非金属元素的含氧酸根离子中心原子杂化轨道类型是sp2的是___________ 、立体构型是V形的是___________
(5)已知N与Ti形成的化合物的晶胞结构如图所示,晶胞中Ti原子与N原子的最近距离为apm;晶胞的密度为p=___________ g/cm3(阿伏加德罗常数值为NA,N、Ti的相对原子质量分别用Ar(N)和Ar(Ti)表示)

(1)Li4Ti5O12是电池的电极材料。与Li不同族但性质相似的元素是
(2)K与Ti位于同一周期,K和Ti的第一电离能(I1)较大的是
(3)钛与卤素形成的化合物TiX4熔点如下表
| TiX4 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点℃ | 377 | -24 | 38.3 | 153 |
(4)Ti(IV)的某配合物可用于催化环烯烃聚合,其结构如图所示,该配合物中:Ti的配位数为

(5)已知N与Ti形成的化合物的晶胞结构如图所示,晶胞中Ti原子与N原子的最近距离为apm;晶胞的密度为p=

您最近一年使用:0次
2021-12-11更新
|
1036次组卷
|
6卷引用:内蒙古自治区霍林郭勒市第一中学2022-203学年高三上学期9月月考化学试题
内蒙古自治区霍林郭勒市第一中学2022-203学年高三上学期9月月考化学试题四川省达州市2021-2022学年高三上学期第一次诊断考试理科综合化学试题(已下线)解密13 物质结构与性质(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)四川省达州市普通高中2022届高三第一次诊断性测试理综化学试题宁夏银川市唐徕中学2022-2023学年高二下学期期中考试化学试题广东省韶关市武江区广东北江实验中学2021-2022学年高三下学期适应性考试(四)化学试题
解题方法
7 . 中国在激光武器研发领域走在了世界的前列,而氟代硼酸钾(KBe2BO3F2)就是制备激光器的核心材料。回答下列问题:
(1)基态氟原子核外电子占据最高能级的电子云形状为___ 形。
(2)氟代硼酸钾中非金属原子的电负性由大到小顺序是___ 。
(3)NaBH4是有机合成中常用的还原剂,其中的阴离子空间构型是___ ,中心原子的杂化形式为___ ;NaBH4中存在___ (填标号)。
a.离子键 b.氢键 C.σ键 d.π键
(4)[H2F][SbF6](氟锑酸)是一种超强酸,写出与[H2F]+具有相同空间构型和键合形式的分子和阴离子分别是___ 、___ (各举一例)。
(5)萤石[CaF2]是一种常用的助溶剂,其晶胞结构如图所示:
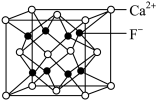
①在晶胞中Ca2+的配位数为___ 。
②若晶胞参数为anm,则CaF2晶胞的密度为___ g•cm-3(设NA为阿伏加德罗常数的值)。
(1)基态氟原子核外电子占据最高能级的电子云形状为
(2)氟代硼酸钾中非金属原子的电负性由大到小顺序是
(3)NaBH4是有机合成中常用的还原剂,其中的阴离子空间构型是
a.离子键 b.氢键 C.σ键 d.π键
(4)[H2F][SbF6](氟锑酸)是一种超强酸,写出与[H2F]+具有相同空间构型和键合形式的分子和阴离子分别是
(5)萤石[CaF2]是一种常用的助溶剂,其晶胞结构如图所示:

①在晶胞中Ca2+的配位数为
②若晶胞参数为anm,则CaF2晶胞的密度为
您最近一年使用:0次
解题方法
8 . 金属铜、铁、铝等在人类文明史上先后被广泛使用。回答下列问题:
(1)基态铜原子价层电子排布式为_________ ;基态Fe原子中未成对电子数为___ ;
基态铝原子电子占据最高能级的电子云轮廓图为_________ 形。
(2)实验测得气态氯化铝分子的结构式为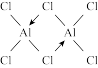 ,氯化铝是
,氯化铝是_________ 晶体,气态氯化铝中存在____ (填字母序号)。
A.离子键 B.配位键 C.氢键 D.范德华力 E.金属键 F.非极性共价键
(3)某些氧化物的熔点数据如表所示:
解释表中氧化物的熔点存在差异的原因:__________ 。
(4)CuCO3可用于制备高温超导体,其3种组成元素中电负性最大的是______ (填元素符号),CO 的空间构型是
的空间构型是_________ ,其中碳原子的杂化方式为_________ 。
(5)氮化铝晶胞结构可看作金刚石晶胞(如图所示)内部的碳原子被N原子代替,顶点和面心的碳原子被铝原子代替。AlN晶体中N和N的原子核间距为apm,AlN摩尔质量为Mg·mol-1,阿伏加德罗常数的值为NA,则AlN晶体的密度为______ g·cm-3(1pm=10-12m)。

(1)基态铜原子价层电子排布式为
基态铝原子电子占据最高能级的电子云轮廓图为
(2)实验测得气态氯化铝分子的结构式为
 ,氯化铝是
,氯化铝是A.离子键 B.配位键 C.氢键 D.范德华力 E.金属键 F.非极性共价键
(3)某些氧化物的熔点数据如表所示:
| 氧化物 | SO3 | K2O | CuO |
| 熔点/℃ | 62.3 | 350 | 1026 |
(4)CuCO3可用于制备高温超导体,其3种组成元素中电负性最大的是
 的空间构型是
的空间构型是(5)氮化铝晶胞结构可看作金刚石晶胞(如图所示)内部的碳原子被N原子代替,顶点和面心的碳原子被铝原子代替。AlN晶体中N和N的原子核间距为apm,AlN摩尔质量为Mg·mol-1,阿伏加德罗常数的值为NA,则AlN晶体的密度为

您最近一年使用:0次
名校
解题方法
9 . 碳、氮和磷元素是几乎所有的生物体中均含有的生命元素。回答下列问题:
(1)叠氮酸(HN3)是一种弱酸,在水中能微弱电离出H+和 ,分子中的大Π键可用符号
,分子中的大Π键可用符号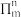 表示,其中m代表参与形成大Π键的原子数,n代表参与形成大Π键的电子数(如苯分子中的大Π键可表示为
表示,其中m代表参与形成大Π键的原子数,n代表参与形成大Π键的电子数(如苯分子中的大Π键可表示为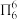 ,则
,则 中的大Π键应表示为
中的大Π键应表示为__________________ 。
(2)2001年德国专家从硫酸铵中检出一种组成为N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以 和
和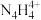 两种离子的形式存在。
两种离子的形式存在。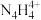 中N原子均为sp3杂化,请推测
中N原子均为sp3杂化,请推测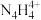 的结构式:
的结构式:_______________________ 。
(3)氨(NH3)和膦(PH3)是两种三角锥形气态氢化物,其键角分别为107°和93.6°,试分析PH3的键角小于NH3的原因:____________________________ 。
(4)ATP(三磷酸腺苷)是一种高能磷酸化合物,在细胞中,它与ADP的相互转化实现贮能和放能,从而保证了细胞各项生命活动的能量供应。ATP的结构简式如图1所示。
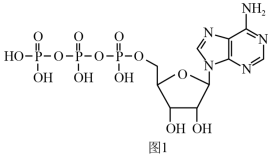 分子中属于sp2杂化的N原子有
分子中属于sp2杂化的N原子有_______________ 个。
(5)某种磁性氮化铁的晶胞结构如图2所示。

①基态Fe原子的电子排布式为______________________ 。
②该化合物的化学式为___________________________ 。
③若晶胞底边长为anm,高为cnm,NA为阿伏加 德罗常数的值,则该磁性氮化铁的晶体密度为__________________ g.cm-3(用含a、c、NA的代数式表示)。
(1)叠氮酸(HN3)是一种弱酸,在水中能微弱电离出H+和
 ,分子中的大Π键可用符号
,分子中的大Π键可用符号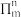 表示,其中m代表参与形成大Π键的原子数,n代表参与形成大Π键的电子数(如苯分子中的大Π键可表示为
表示,其中m代表参与形成大Π键的原子数,n代表参与形成大Π键的电子数(如苯分子中的大Π键可表示为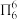 ,则
,则 中的大Π键应表示为
中的大Π键应表示为(2)2001年德国专家从硫酸铵中检出一种组成为N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以
 和
和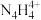 两种离子的形式存在。
两种离子的形式存在。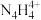 中N原子均为sp3杂化,请推测
中N原子均为sp3杂化,请推测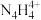 的结构式:
的结构式:(3)氨(NH3)和膦(PH3)是两种三角锥形气态氢化物,其键角分别为107°和93.6°,试分析PH3的键角小于NH3的原因:
(4)ATP(三磷酸腺苷)是一种高能磷酸化合物,在细胞中,它与ADP的相互转化实现贮能和放能,从而保证了细胞各项生命活动的能量供应。ATP的结构简式如图1所示。
 分子中属于sp2杂化的N原子有
分子中属于sp2杂化的N原子有(5)某种磁性氮化铁的晶胞结构如图2所示。

①基态Fe原子的电子排布式为
②该化合物的化学式为
③若晶胞底边长为anm,高为cnm,NA为阿伏加 德罗常数的值,则该磁性氮化铁的晶体密度为
您最近一年使用:0次
解题方法
10 . AA705合金(含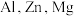 和
和 )几乎与钢一样坚固,但重量仅为钢的三分之一,已被用于飞机机身和机翼、智能手机外壳上等。回答下列问题:
)几乎与钢一样坚固,但重量仅为钢的三分之一,已被用于飞机机身和机翼、智能手机外壳上等。回答下列问题:
(1) 和
和 中阳离子基态核外电子排布式为
中阳离子基态核外电子排布式为_____________________ ,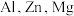 三种元素的第一电离能由大到小为
三种元素的第一电离能由大到小为_____________________ ;
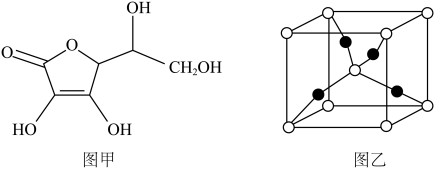
(2)以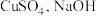 和抗坏血酸为原料,可制备
和抗坏血酸为原料,可制备 。抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为
。抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为_______________ ,推测抗坏血酸在水中的溶解性:_______________ (填“难溶于水”或“易溶于水”),一个 晶胞(见图2)中,
晶胞(见图2)中, 原子的数目为
原子的数目为_______________ ;
(3) 和
和 等配体都能与
等配体都能与 形成配离子。
形成配离子。 含
含______  键,中心离子的配位数为
键,中心离子的配位数为______________ ;
(4) 因杀虫效率高、廉价易得而被广泛应用。已知
因杀虫效率高、廉价易得而被广泛应用。已知 的熔点为2000℃,其晶胞结构如图所示。
的熔点为2000℃,其晶胞结构如图所示。
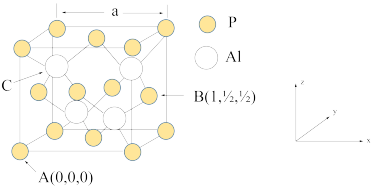
①磷化铝的晶体类型为______________ ,
②A、B点的原子坐标如图所示,则C点的原子坐标为___________ ,
③磷化铝的晶胞参数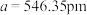 ,其密度为
,其密度为____________  (列出计算式即可,用
(列出计算式即可,用 表示阿伏加 德罗常数的值);
表示阿伏加 德罗常数的值);
(5) 具有对称的立体构型,
具有对称的立体构型, 中的两个
中的两个 被两个
被两个 取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则 的空间构型为
的空间构型为________________ 。
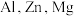 和
和 )几乎与钢一样坚固,但重量仅为钢的三分之一,已被用于飞机机身和机翼、智能手机外壳上等。回答下列问题:
)几乎与钢一样坚固,但重量仅为钢的三分之一,已被用于飞机机身和机翼、智能手机外壳上等。回答下列问题:(1)
 和
和 中阳离子基态核外电子排布式为
中阳离子基态核外电子排布式为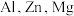 三种元素的第一电离能由大到小为
三种元素的第一电离能由大到小为(2)以
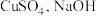 和抗坏血酸为原料,可制备
和抗坏血酸为原料,可制备 。抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为
。抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为 晶胞(见图2)中,
晶胞(见图2)中, 原子的数目为
原子的数目为
(3)
 和
和 等配体都能与
等配体都能与 形成配离子。
形成配离子。 含
含 键,中心离子的配位数为
键,中心离子的配位数为(4)
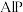 因杀虫效率高、廉价易得而被广泛应用。已知
因杀虫效率高、廉价易得而被广泛应用。已知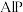 的熔点为2000℃,其晶胞结构如图所示。
的熔点为2000℃,其晶胞结构如图所示。
①磷化铝的晶体类型为
②A、B点的原子坐标如图所示,则C点的原子坐标为
③磷化铝的晶胞参数
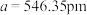 ,其密度为
,其密度为 (列出计算式即可,用
(列出计算式即可,用 表示阿伏加 德罗常数的值);
表示阿伏加 德罗常数的值);(5)
 具有对称的立体构型,
具有对称的立体构型, 中的两个
中的两个 被两个
被两个 取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则 的空间构型为
的空间构型为
您最近一年使用:0次



