名校
1 . 下列对物质性质及解释均正确的是
| 选项 | 性质 | 解释 |
| A | 熔点:Li<Na<K | K+的价电子数多,金属键最强 |
| B | 熔点:晶体硅<碳化硅 | 碳化硅中分子间作用力较大 |
| C | 酸性: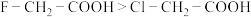 | 电负性:F>Cl,导致羧基中羟基的极性更大 |
| D | H2O的键角比H3O+的键角大 | 中心原子的孤电子对数目H2O>H3O+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . A、B、C、D、E、F、G是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如表所示,请用化学用语回答下列问题。
(1)元素F简单离子的价电子排布式为___________ ;写出元素G在周期表中的位置___________ 。
(2)B与氢元素形成的简单气态氢化物的空间构型为___________ ,C与氢元素形成的简单气态氢化物的VSEPR模型为___________ 。
(3)C、D、E三种元素的简单离子半径由大到小的顺序为___________ (用元素符号表示)。
(4)已知元素A、B形成的 分子中所有原子都满足8电子稳定结构,则
分子中所有原子都满足8电子稳定结构,则 中σ键与π键之比为
中σ键与π键之比为___________ 。
(5)短周期元素M与D同族,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是___________ 化合物(填“离子”或“共价”);M的最高价氧化物对应的水化物与NaOH溶液反应的化学方程式为___________ 。
(6)FC—常用作消毒剂,单质砷(As)在碱性溶液中可被FC—氧化为AsO ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 电离能数据(单位: ):738、1451、7733、10540、13630…… ):738、1451、7733、10540、13630…… |
| E | 基态原子最外层电子排布式为: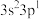 |
| F | 基态原子的最外层p轨道上2个电子的自旋状态与其他电子的自旋状态相反 |
| G | 其中一种氧化物是有磁性的黑色固体 |
(2)B与氢元素形成的简单气态氢化物的空间构型为
(3)C、D、E三种元素的简单离子半径由大到小的顺序为
(4)已知元素A、B形成的
 分子中所有原子都满足8电子稳定结构,则
分子中所有原子都满足8电子稳定结构,则 中σ键与π键之比为
中σ键与π键之比为(5)短周期元素M与D同族,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是
(6)FC—常用作消毒剂,单质砷(As)在碱性溶液中可被FC—氧化为AsO
 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次
名校
解题方法
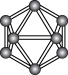
3 . 观察下列模型并结合信息,判断有关说法错误的是
| 晶体硼结构单元(有12个B原子) |  |  分子 分子 | HCN | |
| 结构模型示意图 |
|
|
|
|
A.晶体硼的结构单元中含有30个 键,含20个正三角形 键,含20个正三角形 |
B. 结构中键角1、2、3由大到小的顺序:3>1>2 结构中键角1、2、3由大到小的顺序:3>1>2 |
C.固态硫 中S原子为 中S原子为 杂化 杂化 |
D. 的结构式为 的结构式为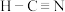 |
您最近一年使用:0次
2024-03-30更新
|
1118次组卷
|
2卷引用:山西省大同市第一中学校2023-2024学年高二下学期3月月考化学试题
名校
4 . 磷酰氯(POCl3)是有机合成的催化剂,可用以下方法制取: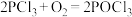 或
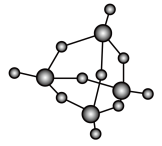
或 ,P4O10的分子空间结构模型如图所示。下列说法不正确的是
,P4O10的分子空间结构模型如图所示。下列说法不正确的是
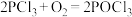 或
或 ,P4O10的分子空间结构模型如图所示。下列说法不正确的是
,P4O10的分子空间结构模型如图所示。下列说法不正确的是
| A.P4O10是非极性分子 |
| B.PCl3的空间构型是三角锥形 |
| C.P4O10分子中所有的键角都相等 |
D.POCl3可与CH3CH2OH反应生成 |
您最近一年使用:0次
解题方法
5 . 连二硫酸锰(MnS2O6,其中Mn为+2价)是一种常用的果蔬保鲜剂,易溶于水,室温下其水溶液在pH为2.8~3.5时最稳定。回答下列问题:
【探究】制备连二硫酸锰(MnS2O6)
某化学小组利用MnO2悬浊液吸收SO2气体制取连二硫酸锰的装置(部分夹持、加热仪器已省略)如图所示。

(1)装置A中装有70%H2SO4的仪器名称为___________ ,装置B的作用是___________ 。
(2)装置C中的反应温度需要控制在0℃左右,控制温度的方法是___________ ,实验时需要向C中通入稍过量的SO2,目的是___________ 。
(3)装置C中反应生成等物质的量的MnS2O6和MnSO4,则反应的化学方程式为___________ ,判断反应完成的现象是___________ 。
(4)连二硫酸结构式为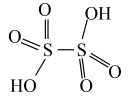 ,推断连二硫酸中S原子上
,推断连二硫酸中S原子上_________ 孤电子对(填“有”或“无”),已知甲磺酸的结构简式为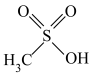 ,连二硫酸H-O的极性
,连二硫酸H-O的极性________ 甲磺酸H-O的极性(填“大于”“小于”或“等于”)。
【探究】制备连二硫酸锰(MnS2O6)
某化学小组利用MnO2悬浊液吸收SO2气体制取连二硫酸锰的装置(部分夹持、加热仪器已省略)如图所示。

(1)装置A中装有70%H2SO4的仪器名称为
(2)装置C中的反应温度需要控制在0℃左右,控制温度的方法是
(3)装置C中反应生成等物质的量的MnS2O6和MnSO4,则反应的化学方程式为
(4)连二硫酸结构式为
 ,推断连二硫酸中S原子上
,推断连二硫酸中S原子上 ,连二硫酸H-O的极性
,连二硫酸H-O的极性
您最近一年使用:0次
解题方法
6 . 磷酸铁锂电池是以磷酸铁锂(LiFePO4)为正极材料的锂离子电池,具有循环寿命长、安全性能好、无环境污染等特点。
(1)磷酸铁锂具有橄榄石结构,空间骨架结构不易发生形变,化学性质稳定。
①基态 的价层电子排布式为
的价层电子排布式为_______ 。
②Li、P、O三种元素的电负性由大到小的顺序是_______ 。
(2)硫酸亚铁(FeSO4)可用于制备磷酸铁锂。
①根据价层电子对互斥理论可知, 的空间结构为
的空间结构为_______ 。
②比较S原子和O原子的第一电离能大小,并从原子结构的角度说明理由:_______ 。
(3)草酸亚铁(FeC2O4)也可用于制备磷酸铁锂。草酸根离子的结构简式为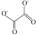 ,其中碳原子的杂化轨道类型为
,其中碳原子的杂化轨道类型为_______ 。
(4)磷酸铁(FePO4)与磷酸铁锂结构相似,其中 围绕
围绕 和
和 分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。充放电过程中,
分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。充放电过程中,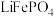 中的
中的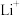 会不断脱嵌或嵌入链之间的孔道内,其结构变化如图所示。
会不断脱嵌或嵌入链之间的孔道内,其结构变化如图所示。
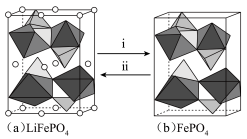
①i表示_______ (填“充电”或“放电”)过程。
②已知Li+的脱嵌率= 。某时刻,若正极材料中Li+的脱嵌率为
。某时刻,若正极材料中Li+的脱嵌率为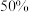 ,则其中
,则其中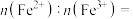
_______ 。
(1)磷酸铁锂具有橄榄石结构,空间骨架结构不易发生形变,化学性质稳定。
①基态
 的价层电子排布式为
的价层电子排布式为②Li、P、O三种元素的电负性由大到小的顺序是
(2)硫酸亚铁(FeSO4)可用于制备磷酸铁锂。
①根据价层电子对互斥理论可知,
 的空间结构为
的空间结构为②比较S原子和O原子的第一电离能大小,并从原子结构的角度说明理由:
(3)草酸亚铁(FeC2O4)也可用于制备磷酸铁锂。草酸根离子的结构简式为
 ,其中碳原子的杂化轨道类型为
,其中碳原子的杂化轨道类型为(4)磷酸铁(FePO4)与磷酸铁锂结构相似,其中
 围绕
围绕 和
和 分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。充放电过程中,
分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。充放电过程中,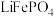 中的
中的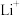 会不断脱嵌或嵌入链之间的孔道内,其结构变化如图所示。
会不断脱嵌或嵌入链之间的孔道内,其结构变化如图所示。
①i表示
②已知Li+的脱嵌率=
 。某时刻,若正极材料中Li+的脱嵌率为
。某时刻,若正极材料中Li+的脱嵌率为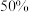 ,则其中
,则其中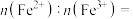
您最近一年使用:0次
名校
解题方法
7 . 偶极矩是电荷量与正、负电荷中心间的距离的乘积。用偶极矩可判断分子的极性:一般来说极性分子的偶极矩不为零;非极性分子的偶极矩为零。下列分子中偶极矩不为零的是
| A.BeCl2 | B.BF3 | C.PCl3 | D.CH4 |
您最近一年使用:0次
名校
解题方法
8 . 我国在新材料领域研究的重大突破,为“天宫”空间站的建设提供了坚实的物质基础。“天宫”空间站使用的材料中含有B、C、N、P、Ni、Fe 等元素。回答下列问题:
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是___________ (填标号,下同),用光谱仪可捕捉到发射光谱的是___________ 。___________ 。
(3)氮化硼(BN)晶体有多种结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,质地软,可作润滑剂。立方相氮化硼与金刚石相似,是超硬材料,有优异的耐磨性。它们的晶体结构及晶胞如图所示。___________ 。
②立方相氮化硼晶体中“一般共价键”与配位键的数目之比为___________ 。
③立方相氮化硼晶胞边长为apm, NA代表阿伏加德罗常数的值,则该晶体的密度为___________ g·cm-3。
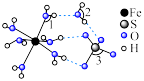
(4)FeSO4·7H2O的结构如图所示,FeSO4·7H2O中∠1、∠2、∠3由大到小的顺序是___________ 。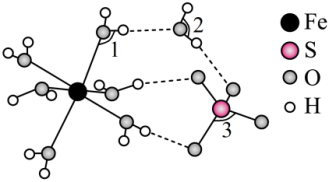
(5)镍的某种氧化物常用作催化剂,其晶胞有如图结构特征:镍离子形成面心立方结构,氧离子填充在镍离子构成的八面体空隙中,填充率为100%。
①从该晶胞中能分割出来的结构图有___________ (填标号)。___________ 个,该距离为___________ pm(用含ρ和NA的代数式表示)。
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是
A.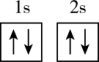 B.
B.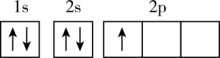 C.
C.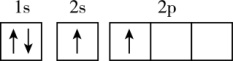 D.
D.
(3)氮化硼(BN)晶体有多种结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,质地软,可作润滑剂。立方相氮化硼与金刚石相似,是超硬材料,有优异的耐磨性。它们的晶体结构及晶胞如图所示。

②立方相氮化硼晶体中“一般共价键”与配位键的数目之比为
③立方相氮化硼晶胞边长为apm, NA代表阿伏加德罗常数的值,则该晶体的密度为
(4)FeSO4·7H2O的结构如图所示,FeSO4·7H2O中∠1、∠2、∠3由大到小的顺序是

(5)镍的某种氧化物常用作催化剂,其晶胞有如图结构特征:镍离子形成面心立方结构,氧离子填充在镍离子构成的八面体空隙中,填充率为100%。
①从该晶胞中能分割出来的结构图有
a.  b.
b.  c.
c. d.
d. 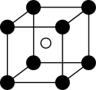 e.
e.
您最近一年使用:0次
2023-07-21更新
|
339次组卷
|
3卷引用:山东省青岛市第二中学2022-2023学年高二5月月考化学试题
名校
解题方法
9 . 铜的单质及其化合物在工农业、国防、科技等领域具有广泛应用。回答下列问题:
(1)基态Cu+的价层电子排布式为_______ 。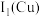
_______ (填“ ”或“
”或“ ”)
”)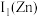 ,原因是
,原因是_______ 。
(2)研究发现,阳离子的颜色与未成对电子数有关。例如:Cu2+、Fe2+、Fe3+等。Cu+呈无色,其原因是_______ 。
(3)合成氨工业中,铜(I)氨溶液常用于除去原料气(N2和H2等)中少量的CO,发生的化学反应为: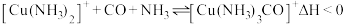 。
。
①NH3分子中N原子的杂化轨道类型是_______ ,NH3和[Cu(NH3)4]2+中H-N-H键角的大小:NH3_______ [Cu(NH3)4]2+ (填“ ”或“
”或“ ”)。
”)。
②铜(Ⅰ)氨液吸收CO适宜的生产条件是_______ (填序号)。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
③[Cu(NH3)3CO]+配离子中配体是_______ 。
(4)CuCl2与乙二胺(H2NCH2CH2NH2)可形成配离子[Cu(En)2]2+ (En是乙二胺的简写),其结构简式如图所示:
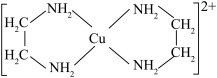
①H2NCH2CH2NH2 (乙二胺)和N(CH3)3(三甲胺)均属于胺,二者相对分子质量相近,但乙二胺的沸点比三甲胺的高得多,原因是_______ 。
②配合物[Cu(En)2]Cl2中不存在的作用力类型有_______ (填选项字母)。
A.配位键 B.极性键 C.离子键 D.非极性键 E.范德华力 F.金属键
(5)金属合金MgCux的结构可看作以Cu4四面体(相互共用顶点)替换立方金刚石结构中的碳原子,形成三维骨架,在晶胞空隙处,有序地放置Mg原子(四面体的4个顶点代表Cu原子,圆球代表Mg原子),结构如图所示。

①
_______ 。
②若Mg原子A的原子坐标为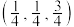 ,则C的原子坐标为
,则C的原子坐标为_______ 。
③晶胞参数为 ,则AB原子之间的距离为
,则AB原子之间的距离为_______ nm。
(1)基态Cu+的价层电子排布式为
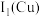
 ”或“
”或“ ”)
”)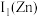 ,原因是
,原因是(2)研究发现,阳离子的颜色与未成对电子数有关。例如:Cu2+、Fe2+、Fe3+等。Cu+呈无色,其原因是
(3)合成氨工业中,铜(I)氨溶液常用于除去原料气(N2和H2等)中少量的CO,发生的化学反应为:
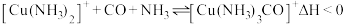 。
。①NH3分子中N原子的杂化轨道类型是
 ”或“
”或“ ”)。
”)。②铜(Ⅰ)氨液吸收CO适宜的生产条件是
A.高温高压 B.高温低压 C.低温高压 D.低温低压
③[Cu(NH3)3CO]+配离子中配体是
(4)CuCl2与乙二胺(H2NCH2CH2NH2)可形成配离子[Cu(En)2]2+ (En是乙二胺的简写),其结构简式如图所示:

①H2NCH2CH2NH2 (乙二胺)和N(CH3)3(三甲胺)均属于胺,二者相对分子质量相近,但乙二胺的沸点比三甲胺的高得多,原因是
②配合物[Cu(En)2]Cl2中不存在的作用力类型有
A.配位键 B.极性键 C.离子键 D.非极性键 E.范德华力 F.金属键
(5)金属合金MgCux的结构可看作以Cu4四面体(相互共用顶点)替换立方金刚石结构中的碳原子,形成三维骨架,在晶胞空隙处,有序地放置Mg原子(四面体的4个顶点代表Cu原子,圆球代表Mg原子),结构如图所示。

①

②若Mg原子A的原子坐标为
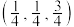 ,则C的原子坐标为
,则C的原子坐标为③晶胞参数为
 ,则AB原子之间的距离为
,则AB原子之间的距离为
您最近一年使用:0次
解题方法
10 . 类比法是一种学习化学的重要方法,下列类比合理的是
| 选项 | 已知 | 类比 |
| A |  与水反应生成乙炔 与水反应生成乙炔 | 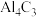 与水反应生成丙炔 与水反应生成丙炔 |
| B |  酸性强于 酸性强于 |  酸性强于 酸性强于 |
| C | 非金属性: | 第一电离能: |
| D |  为V形分子 为V形分子 |  为三角锥形分子 为三角锥形分子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次