名校
1 . 四氮化四硫( ,S为+2价)是重要的硫一氮二元化合物,室温下为橙黄色固体,难溶于水,能溶于
,S为+2价)是重要的硫一氮二元化合物,室温下为橙黄色固体,难溶于水,能溶于 等有机溶剂,可用
等有机溶剂,可用 与
与 (红棕色液体)反应制备,反应装置如图所示(夹持装置略)。
(红棕色液体)反应制备,反应装置如图所示(夹持装置略)。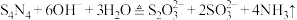 ,回答下列问题:
,回答下列问题:
(1)仪器a的名称为________ ;装置D的作用是________ 。
(2)四氮化四硫( )为双楔形笼状结构,如下图(a)所示。S和N原子交替构成一个假想的八元环,各S-N键长几乎相等。请回答以下问题:
)为双楔形笼状结构,如下图(a)所示。S和N原子交替构成一个假想的八元环,各S-N键长几乎相等。请回答以下问题: 的双楔形笼状结构可通过
的双楔形笼状结构可通过________ 实验测得。
② 分子中正、负电荷的重心完全重合,则为分子
分子中正、负电荷的重心完全重合,则为分子________ (填“极性”或“非极性”)。
③已知:多原子分子中相互平行的多条p轨道,连贯重叠构成一个整体,p电子在多个原子间运动形成大π键,如苯分子存在 型大π键。有研究者提出
型大π键。有研究者提出 的另一种平面八元环结构,如上图(b),S原子的杂化方式为
的另一种平面八元环结构,如上图(b),S原子的杂化方式为________ ;请写出平面 中的大π键类型
中的大π键类型________ 。
(3)装置C中生成 的同时,还生成一种常见固体单质和一种盐,该反应的化学方程式为
的同时,还生成一种常见固体单质和一种盐,该反应的化学方程式为________ ;证明 反应完全的现象是
反应完全的现象是________ 。
(4)分离产物后测定产品纯度:
i.取0.1000g样品加入三颈烧瓶中,再加入足量NaOH溶液并加热蒸出 ;
;
ii.将蒸出的 通入含甲基橙的
通入含甲基橙的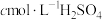 标准溶液中,消耗
标准溶液中,消耗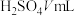 。
。
根据上述实验,计算样品中 的纯度
的纯度________ (列出表达式)。
 ,S为+2价)是重要的硫一氮二元化合物,室温下为橙黄色固体,难溶于水,能溶于
,S为+2价)是重要的硫一氮二元化合物,室温下为橙黄色固体,难溶于水,能溶于 等有机溶剂,可用
等有机溶剂,可用 与
与 (红棕色液体)反应制备,反应装置如图所示(夹持装置略)。
(红棕色液体)反应制备,反应装置如图所示(夹持装置略)。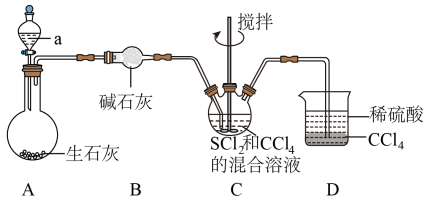
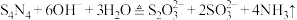 ,回答下列问题:
,回答下列问题:(1)仪器a的名称为
(2)四氮化四硫(
 )为双楔形笼状结构,如下图(a)所示。S和N原子交替构成一个假想的八元环,各S-N键长几乎相等。请回答以下问题:
)为双楔形笼状结构,如下图(a)所示。S和N原子交替构成一个假想的八元环,各S-N键长几乎相等。请回答以下问题: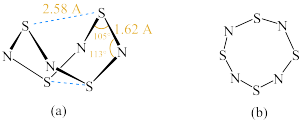
 的双楔形笼状结构可通过
的双楔形笼状结构可通过②
 分子中正、负电荷的重心完全重合,则为分子
分子中正、负电荷的重心完全重合,则为分子③已知:多原子分子中相互平行的多条p轨道,连贯重叠构成一个整体,p电子在多个原子间运动形成大π键,如苯分子存在
 型大π键。有研究者提出
型大π键。有研究者提出 的另一种平面八元环结构,如上图(b),S原子的杂化方式为
的另一种平面八元环结构,如上图(b),S原子的杂化方式为 中的大π键类型
中的大π键类型(3)装置C中生成
 的同时,还生成一种常见固体单质和一种盐,该反应的化学方程式为
的同时,还生成一种常见固体单质和一种盐,该反应的化学方程式为 反应完全的现象是
反应完全的现象是(4)分离产物后测定产品纯度:
i.取0.1000g样品加入三颈烧瓶中,再加入足量NaOH溶液并加热蒸出
 ;
;ii.将蒸出的
 通入含甲基橙的
通入含甲基橙的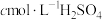 标准溶液中,消耗
标准溶液中,消耗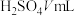 。
。根据上述实验,计算样品中
 的纯度
的纯度
您最近一年使用:0次
2024-04-11更新
|
124次组卷
|
2卷引用:浙江省舟山中学2023-2024学年高二下学期4月月考化学试题
名校
2 . 工业上氮氧化物( :NO和
:NO和 混合气)废气吸收利用的某流程如下:
混合气)废气吸收利用的某流程如下:
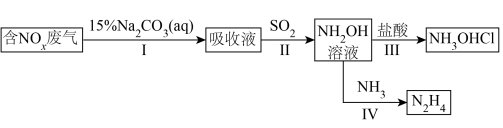
已知:氧化度 ;吸收液含有的产物有
;吸收液含有的产物有 和
和 ;
; 在碱性条件下受热分解产物之一为
在碱性条件下受热分解产物之一为 。
。
请回答:
(1)过程Ⅳ以“肼合成酶”催化 与
与 转化为肼(
转化为肼(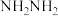 )的反应历程如下所示:
)的反应历程如下所示:
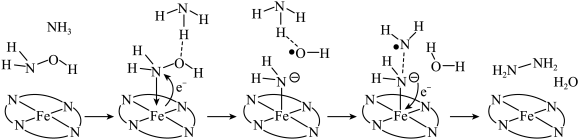
该反应历程中Fe元素的化合价___________ (填“变化”或“不变”)。若将 替换为
替换为 ,反应制得的肼的结构简式为
,反应制得的肼的结构简式为___________ 。
(2)写出过程Ⅰ中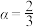 时反应的离子方程式
时反应的离子方程式___________ 。
(3)下列说法正确的是___________。
(4) 是一种理想还原剂,氧化产物对环境友好,写出
是一种理想还原剂,氧化产物对环境友好,写出 还原
还原 的化学方程式
的化学方程式___________ 。
(5)设计实验证明 中存在N元素
中存在N元素___________ 。
 :NO和
:NO和 混合气)废气吸收利用的某流程如下:
混合气)废气吸收利用的某流程如下:
已知:氧化度
 ;吸收液含有的产物有
;吸收液含有的产物有 和
和 ;
; 在碱性条件下受热分解产物之一为
在碱性条件下受热分解产物之一为 。
。请回答:
(1)过程Ⅳ以“肼合成酶”催化
 与
与 转化为肼(
转化为肼(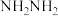 )的反应历程如下所示:
)的反应历程如下所示:
该反应历程中Fe元素的化合价
 替换为
替换为 ,反应制得的肼的结构简式为
,反应制得的肼的结构简式为(2)写出过程Ⅰ中
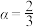 时反应的离子方程式
时反应的离子方程式(3)下列说法正确的是___________。
A.过程Ⅰ采用气、液逆流的方式可提高 的吸收效率 的吸收效率 |
B. 的键角小于 的键角小于 |
C. 可作为配体,与 可作为配体,与 等金属离子形成配合物 等金属离子形成配合物 |
D. 的水溶液显弱碱性,且 的水溶液显弱碱性,且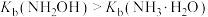 |
(4)
 是一种理想还原剂,氧化产物对环境友好,写出
是一种理想还原剂,氧化产物对环境友好,写出 还原
还原 的化学方程式
的化学方程式(5)设计实验证明
 中存在N元素
中存在N元素
您最近一年使用:0次
2023-11-15更新
|
415次组卷
|
3卷引用:浙江省宁波市2023-2024学年高三上学期选考模拟考试化学试题
浙江省宁波市2023-2024学年高三上学期选考模拟考试化学试题(已下线)专题08 工艺流程综合题(浙江专用)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)新疆乌鲁木齐市第六十八中学2023-2024学年高三上学期1月月考化学试题
解题方法
3 . 氯喹类药物可用于治疗新冠肺炎。氯喹和羟基氯喹的结构分别如图1和图2所示,对这两种化合物的描述不正确 的是
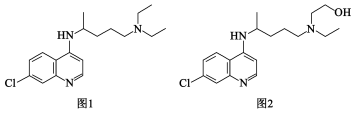

| A.氯喹的分子式和羟基氯喹的分子式仅相差一个O原子 |
B.与足量的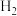 发生加成反应后,两分子中的手性碳原子数相等,且碳原子均为 发生加成反应后,两分子中的手性碳原子数相等,且碳原子均为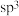 杂化 杂化 |
C.加入 溶液并加热,再加入 溶液并加热,再加入 溶液后生成白色沉淀,可证明氯喹或羟基氯喹中含有氯原子 溶液后生成白色沉淀,可证明氯喹或羟基氯喹中含有氯原子 |
| D.为增大溶解度,易于被人体吸收,常把氯喹或羟基氯喹与硫酸、盐酸反应制成盐类 |
您最近一年使用:0次
解题方法
4 . 短周期元素W、X、Y和Z的原子序数依次增大。W是宇宙中最丰富的元素,W2X是维持生命过程的必需物质,WY可用于玻璃的刻蚀,ZX2是酸雨的主要形成原因之一,室温下化合物ZY4是气体。下列说法不正确 的是
| A.Y的第一电离能在四种元素中最大 |
| B.W2X和ZX2的中心原子分别为sp3和sp2杂化,而ZY6的中心原子为sp3d2杂化 |
| C.W2X的沸点高于W2Z的沸点 |
| D.分子的极性:W2Z<Y2Z |
您最近一年使用:0次
名校
解题方法
5 . 卤素单质及其化合物在科研和工农业生产中有着广泛的应用。请回答:
(1)基态F原子核外电子的空间运动状态有_______ 种。下列属于氯原子激发态且能量较低的是_______ 。(填标号)
a. b.
b.
c. d.
d.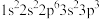
(2)下列说法不正确的是_______
(3)固态氟化氢中存在 形式,画出
形式,画出 的链状结构
的链状结构_______ 。
(4)已知键能: ,请说明理由:
,请说明理由:_______ 。
(5)已知某晶体的结构,其晶胞中阴离子(阳离子未画出)的位置如图1所示,其晶胞中的阳离子(隐去阴离子)在xz、yz和xy平面投影均如图2所示。
①其化学式为_______ ;
②每个 的配位数(紧邻的F原子数)为
的配位数(紧邻的F原子数)为_______ 。
(1)基态F原子核外电子的空间运动状态有
a.
 b.
b.
c.
 d.
d.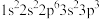
(2)下列说法不正确的是_______
A.熔点 | B.化学键中离子键成分的百分数 |
C.第三电离能: | D.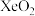 与 与 中心原子的杂化方式相同 中心原子的杂化方式相同 |
(3)固态氟化氢中存在
 形式,画出
形式,画出 的链状结构
的链状结构(4)已知键能:
 ,请说明理由:
,请说明理由:(5)已知某晶体的结构,其晶胞中阴离子(阳离子未画出)的位置如图1所示,其晶胞中的阳离子(隐去阴离子)在xz、yz和xy平面投影均如图2所示。

①其化学式为
②每个
 的配位数(紧邻的F原子数)为
的配位数(紧邻的F原子数)为
您最近一年使用:0次
解题方法
6 . 下列说法不正确 的是
| A.氯气可用于自来水的杀菌、消毒,利用了氯气的漂白性 |
| B.节日燃放的五彩缤纷的烟花是利用了锂、钠、钾、钡等金属元素的焰色 |
| C.聚乙炔中的C原子采取sp2杂化,其中未杂化的p轨道相互平行且重叠,可用于制备导电高分子材料 |
| D.壳聚糖具有生物可降解性,可制成药物载体、手术缝合线、环保包装袋 |
您最近一年使用:0次
7 . F可用于制造人工角膜,具有良好的生物相容性,化学性质稳定,合成路线如下:
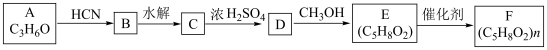
| A.由A生成B发生加成反应 |
B.E分子中 杂化的C原子数多于 杂化的C原子数多于 杂化的C原子数 杂化的C原子数 |
| C.C易溶于水,分子中含有两种亲水基团 |
D.D的结构简式可能为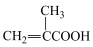 |
您最近一年使用:0次
解题方法
8 . 由CO2合成环状碳酸酯的一种反应机理如图所示。不正确 的是

| A.转化过程中涉及极性键的断裂与形成 |
| B.根据杂化轨道理论,上述转化过程中的含碳化合物碳原子的杂化方式为sp2和sp3 |
| C.化合物1的阳离子体积大,所含离子键较弱,其常温下可能为液态 |
D.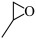 可按照该反应机理与CO2反应生成 可按照该反应机理与CO2反应生成 |
您最近一年使用:0次
名校
解题方法
9 . 3-氨基-1-金刚烷醇可用于合成药物维格列汀(治疗2型糖尿病),其分子结构如图所示。下列说法不正确 的是
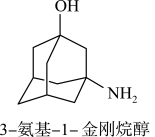
A.分子中O原子和N原子均为 杂化 杂化 |
B.分子中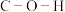 的键角大于 的键角大于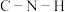 的键角 的键角 |
C.分子中 的极性大于 的极性大于 的极性 的极性 |
D.分子式为 |
您最近一年使用:0次
2024-04-11更新
|
180次组卷
|
2卷引用:浙江省舟山中学2023-2024学年高二下学期4月月考化学试题
名校
解题方法
10 . 有机金属氯化物由原子序数依次增大的短周期主族元素X、Y、Z、M、N组成,部分结构如图所示,基态原子M核外电子所占据原子轨道全充满,N元素的价层电子排布式为 ,下列说法
,下列说法不正确 的是
 ,下列说法
,下列说法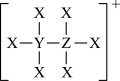
A.Z与N可形成化合物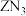 、 、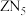 |
B.最简单氢化物的沸点: |
| C.M元素的第一电离能比同周期相邻元素的大 |
D. 离子中Y发生 离子中Y发生 杂化 杂化 |
您最近一年使用:0次
2024-03-21更新
|
428次组卷
|
3卷引用:浙江省宁波市十校2024届高三二模联考化学试题
浙江省宁波市十校2024届高三二模联考化学试题(已下线)压轴题05 “位-构-性”元素推断(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)山东省枣庄市第十六中学等校2023-2024学年高三下学期5月(一模)考试化学试题



