名校
1 . 下列关于C、Si及其化合物的说法正确的是
| A.C和Si的价电子数均为4,推测CO2中的C和SiO2中的Si均为sp杂化 |
| B.CH4的相对分子质量小于SiH4,推测CH4的热稳定性比SiH4小 |
| C.C还原SiO2生成CO和硅单质,可证明C的非金属性强于Si |
D.CH 的键角>CH 的键角>CH 的键角 的键角 |
您最近一年使用:0次
名校
2 . 某些金属和非金属在现代工农业、科技及国防建设等领域中都有着广泛的应用。回答下列问题:
(1)磷原子在成键时,能将一个3s电子激发进入3d能级而参与成键,写出该激发态磷原子的电子排布式_______ ,PH3分子的空间构型是_______ 。
(2)已知偏二甲肼[(CH3)2NNH2]、肼(N2H4)均可做运载火箭的主体燃料,其熔沸点见表。
偏二甲肼中氮原子的杂化方式为_______ ,二者熔沸点存在差异的主要原因是_______ 。
(3)N4H 只有一种化学环境的氢原子,结构如下图所示,其中的大π键可表示为
只有一种化学环境的氢原子,结构如下图所示,其中的大π键可表示为_______ (分子中的大π键可用符号Π 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数,如苯分子中的大π键可表示为Π
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数,如苯分子中的大π键可表示为Π )。
)。

(4)Au的原子序数为79,则其在元素周期表中的位置为_______ 。
(5)经X射线衍射实验证明在碲酸(H6TeO6)分子内的6个羟基排列在碲原子的周围,呈八面体结构,碲酸中碲原子的价层电子对数为_______ 。
(6) FeCoOx是一种新型光电催化剂。第四电离能大小关系是I4(Co) <I4(Fe) ,原因是_______ 。
(7)二硒键和二硫键是重要的光响应动态共价键,其光响应原理可用如图表示,已知光的波长与其能量成反比,则图中实现光响应的波长:λ1_______ λ2(填“>”或“<”或“=”),其原因是_______ 。

(1)磷原子在成键时,能将一个3s电子激发进入3d能级而参与成键,写出该激发态磷原子的电子排布式
(2)已知偏二甲肼[(CH3)2NNH2]、肼(N2H4)均可做运载火箭的主体燃料,其熔沸点见表。
| 物质 | 熔点 | 沸点 |
| 偏二甲肼 | -58℃ | 63.9℃ |
| 肼 | 1.4℃ | 113.5℃ |
偏二甲肼中氮原子的杂化方式为
(3)N4H
 只有一种化学环境的氢原子,结构如下图所示,其中的大π键可表示为
只有一种化学环境的氢原子,结构如下图所示,其中的大π键可表示为 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数,如苯分子中的大π键可表示为Π
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数,如苯分子中的大π键可表示为Π )。
)。
(4)Au的原子序数为79,则其在元素周期表中的位置为
(5)经X射线衍射实验证明在碲酸(H6TeO6)分子内的6个羟基排列在碲原子的周围,呈八面体结构,碲酸中碲原子的价层电子对数为
(6) FeCoOx是一种新型光电催化剂。第四电离能大小关系是I4(Co) <I4(Fe) ,原因是
(7)二硒键和二硫键是重要的光响应动态共价键,其光响应原理可用如图表示,已知光的波长与其能量成反比,则图中实现光响应的波长:λ1

您最近一年使用:0次
3 . 在金属(如:Cu、Co、Be、K等)的湿法冶炼中,某些含氮(如: )、磷[如:磷酸丁基酯(C4H9O)3P=O]等有机物作萃取剂,可将金属萃取出来,从而实现在温和条件下金属冶炼。
)、磷[如:磷酸丁基酯(C4H9O)3P=O]等有机物作萃取剂,可将金属萃取出来,从而实现在温和条件下金属冶炼。
回答下列问题:
(1)基态Co原子核外电子排布式为[Ar]_______ ,有_______ 个 运动状态不同的电子。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 号表示,与之相反的用-
号表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为_______ 。
(3)科学家证实,BeCl2是共价化合物,请设计一个简 单实验证明该结论:_______ ;Be的杂化轨道类型为_______ 。
(4)在N 、 NH3、N2H4、NH
、 NH3、N2H4、NH 、N2H
、N2H 五种微粒中,同种微粒间能形成氢键的有
五种微粒中,同种微粒间能形成氢键的有_______ ;不能作为配位体的有_______ ;空间构型为直线形的是_______ 。
(5)氮原子的第一电离能_______ (填“大于”“小于”或“等 于”)磷原子的第一电离能。
(6)分别用 、
、 表示H2PO
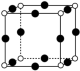
表示H2PO 和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO
和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO 、K+在晶胞xz面、yz面上的位置。若晶胞底边的边长均为a pm、高为c pm,阿伏加德罗常数的值为NA,晶体的密度为
、K+在晶胞xz面、yz面上的位置。若晶胞底边的边长均为a pm、高为c pm,阿伏加德罗常数的值为NA,晶体的密度为 _______ g·cm-3(写出表达式即可)。

 )、磷[如:磷酸丁基酯(C4H9O)3P=O]等有机物作萃取剂,可将金属萃取出来,从而实现在温和条件下金属冶炼。
)、磷[如:磷酸丁基酯(C4H9O)3P=O]等有机物作萃取剂,可将金属萃取出来,从而实现在温和条件下金属冶炼。回答下列问题:
(1)基态Co原子核外电子排布式为[Ar]
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+
 号表示,与之相反的用-
号表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为(3)科学家证实,BeCl2是共价化合物,请设计一个简 单实验证明该结论:
(4)在N
 、 NH3、N2H4、NH
、 NH3、N2H4、NH 、N2H
、N2H 五种微粒中,同种微粒间能形成氢键的有
五种微粒中,同种微粒间能形成氢键的有(5)氮原子的第一电离能
(6)分别用
 、
、 表示H2PO
表示H2PO 和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO
和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO 、K+在晶胞xz面、yz面上的位置。若晶胞底边的边长均为a pm、高为c pm,阿伏加德罗常数的值为NA,晶体的密度为
、K+在晶胞xz面、yz面上的位置。若晶胞底边的边长均为a pm、高为c pm,阿伏加德罗常数的值为NA,晶体的密度为 
您最近一年使用:0次
2022-05-02更新
|
259次组卷
|
3卷引用:黑龙江省齐齐哈尔市2022届高三第二次模拟考试理科综合化学试题
黑龙江省齐齐哈尔市2022届高三第二次模拟考试理科综合化学试题(已下线)专项17 物质结构与性质综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)陕西省安康市重点名校2024届高三上学期10联考化学试题
4 . 点击化学(click chemistry)是一种能够让分子的构建模块快速、高效地结合在一起的化学反应。2022年诺贝尔化学奖授予对点击化学做出贡献的三位化学家。下图是利用点击化学方法设计的一种新型的1,2,3—三唑类杀菌剂的合成路线。下列有关说法正确的是
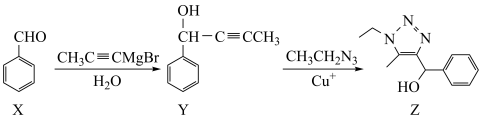
| A.有机物X中的碳原子为sp2杂化 |
| B.有机物Y中所有碳原子一定共平面 |
| C.X生成Y的反应分两步,则第一步属于取代反应 |
| D.有机物Z一定条件下能与H2、Cl2、HNO3发生反应,不能与Na、NaOH反应 |
您最近一年使用:0次
2024-05-13更新
|
142次组卷
|
2卷引用:东北三省四市教研联合体2024届高三下学期高考模拟(二)化学试题
名校
5 . 一种可吸附甲醇的材料,其化学式为 ,部分晶体结构如图所示,其中
,部分晶体结构如图所示,其中 为平面结构。
为平面结构。
 ,部分晶体结构如图所示,其中
,部分晶体结构如图所示,其中 为平面结构。
为平面结构。
A.该晶体中存在 氢键 氢键 |
B. 中C原子为 中C原子为 杂化 杂化 |
C.基态原子的未成对电子数: |
D.基态原子的第一电离能: |
您最近一年使用:0次
2024-05-03更新
|
225次组卷
|
2卷引用:黑龙江省哈三中2023-2024学年高二下学期第一次验收考试化学试卷
解题方法
6 . 化合物M是一种制造压塑粉的原料,结构简式如图所示,其组成元素X、Y、Z、W位于短周期,原子序数依次增大且满足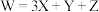 。下列说法错误的是
。下列说法错误的是
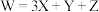 。下列说法错误的是
。下列说法错误的是
A.原子半径: | B.氧化物对应水化物的酸性: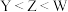 |
C.M中Y原子的杂化方式为 | D.W、Z分别与X形成的简单化合物可发生反应 |
您最近一年使用:0次
名校
解题方法
7 . 含硒(Se)化合物在材料药物领域有重要应用。
(1)Se与S同族,基态Se原子的简化电子排布式为___________ ,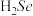 的沸点高于
的沸点高于 ,原因是
,原因是___________ 。
(2)一种含硒的新型 (聚集诱导发光)分子Ⅳ的合成路线如下,下列关于路线中I~Ⅳ的说法正确的有___________。
(聚集诱导发光)分子Ⅳ的合成路线如下,下列关于路线中I~Ⅳ的说法正确的有___________。
(3)硒的两种含氧酸的酸性强弱为
___________  (填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠
(填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠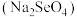 可减轻重金属铊(
可减轻重金属铊( )引起的中毒,
)引起的中毒, 的空间结构为
的空间结构为___________ 。
(4)铊( )与
)与 同族,第一电离能
同族,第一电离能
___________  (填“>”或“<”)。
(填“>”或“<”)。
(5)根据下表中元素的电负性数值判断, 为
为___________ (填“离子化合物”或“共价化合物”,下同), 为
为___________ 。
(6)气态 通常以二聚体
通常以二聚体 的形式存在,其空间结构如图a所示,二聚体中
的形式存在,其空间结构如图a所示,二聚体中 的轨道杂化类型为
的轨道杂化类型为___________ 。 结构如图b所示,若晶胞参数(立方体棱长)为
结构如图b所示,若晶胞参数(立方体棱长)为 ,则晶体密度
,则晶体密度
___________  (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
(1)Se与S同族,基态Se原子的简化电子排布式为
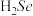 的沸点高于
的沸点高于 ,原因是
,原因是(2)一种含硒的新型
 (聚集诱导发光)分子Ⅳ的合成路线如下,下列关于路线中I~Ⅳ的说法正确的有___________。
(聚集诱导发光)分子Ⅳ的合成路线如下,下列关于路线中I~Ⅳ的说法正确的有___________。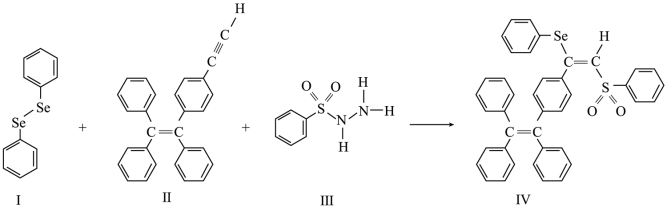
A.Ⅰ中含有两种元素, 键为非极性键 键为非极性键 |
B.Ⅱ中C原子的杂化轨道类型有 与 与 |
| C.Ⅲ中含有的元素中,O的电负性最大 |
D.Ⅳ中 原子的杂化轨道类型为 原子的杂化轨道类型为 |
(3)硒的两种含氧酸的酸性强弱为

 (填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠
(填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠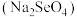 可减轻重金属铊(
可减轻重金属铊( )引起的中毒,
)引起的中毒, 的空间结构为
的空间结构为(4)铊(
 )与
)与 同族,第一电离能
同族,第一电离能
 (填“>”或“<”)。
(填“>”或“<”)。(5)根据下表中元素的电负性数值判断,
 为
为 为
为| 元素 | F |  |  |
| 电负性 | 4.0 | 1.5 | 3.0 |
(6)气态
 通常以二聚体
通常以二聚体 的形式存在,其空间结构如图a所示,二聚体中
的形式存在,其空间结构如图a所示,二聚体中 的轨道杂化类型为
的轨道杂化类型为 结构如图b所示,若晶胞参数(立方体棱长)为
结构如图b所示,若晶胞参数(立方体棱长)为 ,则晶体密度
,则晶体密度
 (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
|
|
| 图a | 图b |
您最近一年使用:0次
名校
8 . 在光照下,螺吡喃发生开、闭环转换而变色,过程如下。下列关于开环螺吡喃和闭环螺吡喃的说法正确的是

| A.开环螺吡喃分子中含有手性碳原子 | B.闭环螺吡喃分子中含有手性碳原子 |
| C.闭环螺吡喃在水中溶解性很好 | D.二者中碳原子数不等,但杂化方式相同 |
您最近一年使用:0次
名校
9 . X、Y、Z为原子序数依次增大的第三周期主族元素,可形成一种如图所示的离子,下列说法错误的是

A.气态氢化物的稳定性: |
| B.该微粒中X和Y的杂化方式相同 |
| C.基态Y原子核外电子的运动状态有9种 |
| D.与Z同主族的元素中,Z的最高价氧化物对应水化物的酸性最强 |
您最近一年使用:0次
名校
10 .  和
和 均可发生水解反应,其中
均可发生水解反应,其中 的水解机理示意图如下:
的水解机理示意图如下:
 和
和 均可发生水解反应,其中
均可发生水解反应,其中 的水解机理示意图如下:
的水解机理示意图如下: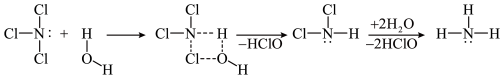
A. 为极性键形成的非极性分子 为极性键形成的非极性分子 | B. 的 的 模型为三角锥形 模型为三角锥形 |
C. 和 和 中的N均为 中的N均为 杂化 杂化 | D.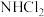 和 和 均能与 均能与 形成氢键 形成氢键 |
您最近一年使用:0次