名校
解题方法
1 . 铱( )属于铂系金属,铂系金属包括钌(
)属于铂系金属,铂系金属包括钌( )、锇(
)、锇( )、铑(
)、铑( )、铱(
)、铱( )、钯(
)、钯( )、铂(
)、铂( )六种金属。其中铑、铱、钯、铂在周期表中的相对位置如图所示。
)六种金属。其中铑、铱、钯、铂在周期表中的相对位置如图所示。
回答下列问题:
(1)基态铱原子的价层电子排布式为_____ 。
(2)实验室常用氯化钯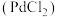 溶液检验
溶液检验 ,发生反应为
,发生反应为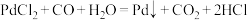 。
。
①在标准状况下,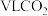 含
含 键数目为
键数目为_____ ( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
② 分子中
分子中 键类型是
键类型是_____ (填字母)。
A. B.
B. C.
C. D.
D.
(3)实验证明,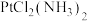 的结构有两种:
的结构有两种: 呈棕黄色,有极性,有抗癌活性,在水中的溶解度为
呈棕黄色,有极性,有抗癌活性,在水中的溶解度为 ,水解后能与草酸
,水解后能与草酸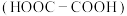 反应生成
反应生成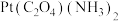 ;B呈淡黄色,无极性,无抗癌活性,在水中的溶解度为
;B呈淡黄色,无极性,无抗癌活性,在水中的溶解度为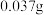 ,水解后不能与草酸反应。
,水解后不能与草酸反应。
①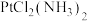 的空间构型是
的空间构型是_____ (填“四面体形”或“平面四边形”)。
②画出A的结构图示:_____ 。
③ 中碳原子的杂化类型是
中碳原子的杂化类型是_____ ,提供孤电子对的原子是_____ (填元素符号)。
 )属于铂系金属,铂系金属包括钌(
)属于铂系金属,铂系金属包括钌( )、锇(
)、锇( )、铑(
)、铑( )、铱(
)、铱( )、钯(
)、钯( )、铂(
)、铂( )六种金属。其中铑、铱、钯、铂在周期表中的相对位置如图所示。
)六种金属。其中铑、铱、钯、铂在周期表中的相对位置如图所示。 |  |
 |  |
 |  |
(1)基态铱原子的价层电子排布式为
(2)实验室常用氯化钯
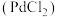 溶液检验
溶液检验 ,发生反应为
,发生反应为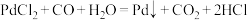 。
。①在标准状况下,
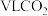 含
含 键数目为
键数目为 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。②
 分子中
分子中 键类型是
键类型是A.
 B.
B. C.
C. D.
D.
(3)实验证明,
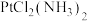 的结构有两种:
的结构有两种: 呈棕黄色,有极性,有抗癌活性,在水中的溶解度为
呈棕黄色,有极性,有抗癌活性,在水中的溶解度为 ,水解后能与草酸
,水解后能与草酸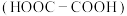 反应生成
反应生成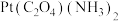 ;B呈淡黄色,无极性,无抗癌活性,在水中的溶解度为
;B呈淡黄色,无极性,无抗癌活性,在水中的溶解度为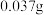 ,水解后不能与草酸反应。
,水解后不能与草酸反应。①
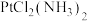 的空间构型是
的空间构型是②画出A的结构图示:
③
 中碳原子的杂化类型是
中碳原子的杂化类型是
您最近一年使用:0次
11-12高三下·上海浦东新·阶段练习
2 . 人体中含量位于前6名的元素依次是:氧、碳、X、氮、钙、磷。根据要求用以上元素完成下列填空:
(1)X是_______ (写元素符号,下同)。能量最高的亚层电子云呈球形的元素有________ 。
(2)形成化合物种类最多的元素的最简氢化物的电子式为_________ ;该分子为非极性分子的原因是________________________________ 。
(3)能证明C、N、O非金属性递变规律的事实是____________ 。
a.最高价氧化物对应水化物的酸性 b.单质与H2反应的难易程度
c.NO2、CO2和C3N4中元素的化合价 d.气态氢化物的稳定性
(4)氮元素的另一种气态氢化物肼可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的。肼燃烧时的能量变化如图所示,则该反应的热化学方程式为_____________ 。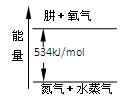
(1)X是
(2)形成化合物种类最多的元素的最简氢化物的电子式为
(3)能证明C、N、O非金属性递变规律的事实是
a.最高价氧化物对应水化物的酸性 b.单质与H2反应的难易程度
c.NO2、CO2和C3N4中元素的化合价 d.气态氢化物的稳定性
(4)氮元素的另一种气态氢化物肼可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的。肼燃烧时的能量变化如图所示,则该反应的热化学方程式为

您最近一年使用:0次
3 . ZnO和硫脲[CS(NH2)2]在一定条件可制备纳米ZnS(粒径8-15nm)。
(1)基态硫原子的价电子排布式为_____ 。
(2)金属Zn在元素周期表的_____ 。
A. s区 B. p区 C. ds区 D. f区
(3)下列说法中正确的是_____ 。
A. 电负性:S<N B. 第一电离能:Zn>S
C. 硫脲[CS(NH2)2]属于分子晶体 D. 硫脲[CS(NH2)2]中所有原子共面
(4)将该纳米ZnS均匀分散于水中,可利用_____ 将该分散系与NaCl溶液进行鉴别。
A. 渗析 B. 丁达尔现象 C. 萃取 D. 盐析
(1)基态硫原子的价电子排布式为
(2)金属Zn在元素周期表的
A. s区 B. p区 C. ds区 D. f区
(3)下列说法中正确的是
A. 电负性:S<N B. 第一电离能:Zn>S
C. 硫脲[CS(NH2)2]属于分子晶体 D. 硫脲[CS(NH2)2]中所有原子共面
(4)将该纳米ZnS均匀分散于水中,可利用
A. 渗析 B. 丁达尔现象 C. 萃取 D. 盐析
您最近一年使用:0次
解题方法
4 . 硅材料在生活中占有重要地位。
(1)太阳能电池板主要材料为单晶硅或多晶硅。硅原子核外未成对电子数为___________ 。单晶硅的晶体类型为___________ 。
A.离子晶体 B.分子晶体 C.共价晶体 D.金属晶体
(2)由硅原子核形成的三种微粒,电子排布式分别为:① 、②
、②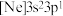 、③
、③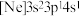 ,有关这些微粒的叙述,正确的是___________。
,有关这些微粒的叙述,正确的是___________。
(3)硅和卤素单质反应可以得到 ,
, 的熔沸点如下表:
的熔沸点如下表:
①气态 分子的空间构型是
分子的空间构型是___________ 。
A.正四面体形 B.三角锥形 C.角形 D.直线形
②0℃时, 、
、 、
、 、
、 呈液态的是
呈液态的是___________ 。
A. B.
B. C.
C. D.
D.
③比较上述 的熔沸点,分析其变化规律及原因
的熔沸点,分析其变化规律及原因___________ 。
(4) 与N-甲基咪唑
与N-甲基咪唑 反应可以得到
反应可以得到 ,其结构如下图所示:
,其结构如下图所示:___________ 。
(5)硅合金具有良好的性能。
①下列关于合金的说法错误的是___________ 。
A.熔点高于组成金属 B.可能含有非金属
C.硬度通常比组成金属大 D.一般比单一金属用途更广
②白铜是我国使用最早的合金之一,白铜晶胞结构如图所示(Cu位于面心),该晶胞含有的Cu原子和Ni原子个数分别为___________ 、___________ 。已知晶体密度为dg·cm-3,设NA为阿伏加德罗常数的值。Ni和Ni之间的最短距离为___________ nm。
(1)太阳能电池板主要材料为单晶硅或多晶硅。硅原子核外未成对电子数为
A.离子晶体 B.分子晶体 C.共价晶体 D.金属晶体
(2)由硅原子核形成的三种微粒,电子排布式分别为:①
 、②
、②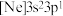 、③
、③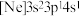 ,有关这些微粒的叙述,正确的是___________。
,有关这些微粒的叙述,正确的是___________。| A.得电子能力:①>② |
| B.微粒半径:③>①>② |
| C.电离一个电子所需最低能量:①>②>③ |
| D.电子排布属于基态原子(或离子)的是:①② |
 ,
, 的熔沸点如下表:
的熔沸点如下表: |  |  |  | |
| 熔点/℃ | -90.0 | -69.8 | 5.6 | 120.7 |
| 沸点/℃ | -85.8 | 57.8 | 154.2 | 287.7 |
 分子的空间构型是
分子的空间构型是A.正四面体形 B.三角锥形 C.角形 D.直线形
②0℃时,
 、
、 、
、 、
、 呈液态的是
呈液态的是A.
 B.
B. C.
C. D.
D.
③比较上述
 的熔沸点,分析其变化规律及原因
的熔沸点,分析其变化规律及原因(4)
 与N-甲基咪唑
与N-甲基咪唑 反应可以得到
反应可以得到 ,其结构如下图所示:
,其结构如下图所示:
(5)硅合金具有良好的性能。
①下列关于合金的说法错误的是
A.熔点高于组成金属 B.可能含有非金属
C.硬度通常比组成金属大 D.一般比单一金属用途更广
②白铜是我国使用最早的合金之一,白铜晶胞结构如图所示(Cu位于面心),该晶胞含有的Cu原子和Ni原子个数分别为

您最近一年使用:0次
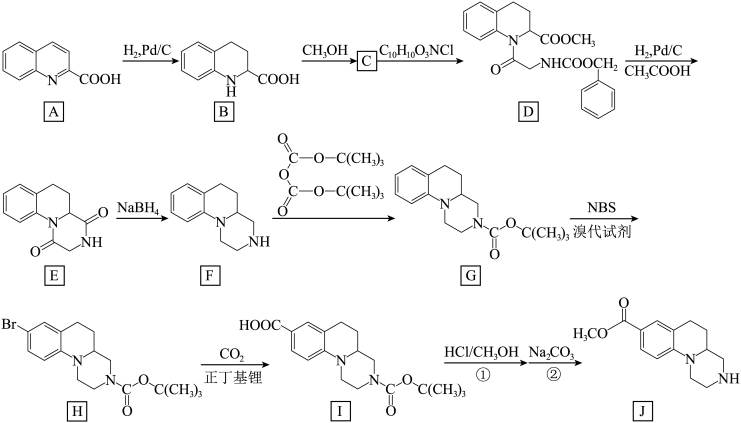
5 . 物质J是合成BCL-2和BCL-XL家族蛋白抑制剂的重要中间体。物质J的某种路线如下所示(部分条件未标出):___________ ,___________ 。
(2)C中含有的官能团为___________ 。
(3)写出C→D转化中反应物 的结构简式
的结构简式___________ 。
(4)写出物质E在碱性(NaOH溶液)、加热条件下水解的化学方程式___________ 。
(5)有关蛋白质说法错误的是___________。
(6)关于物质J说法正确的是___________。
(7)写出一种符合下列条件的B的同分异构体的结构简式___________ 。
ⅰ)属于α-氨基酸类
ⅱ)能使 的
的 溶液褪色
溶液褪色
ⅲ)苯环上仅有两个取代基,且苯环上一溴代物有两种
(8)合成路线中设计F→G,I→J步骤①的目的是___________ 。
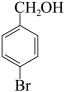
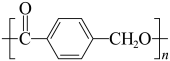
(9)结合以上合成信息,在括号内补全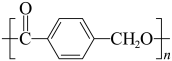 的合成路线。
的合成路线。___________
(2)C中含有的官能团为
(3)写出C→D转化中反应物
 的结构简式
的结构简式(4)写出物质E在碱性(NaOH溶液)、加热条件下水解的化学方程式
(5)有关蛋白质说法错误的是___________。
| A.蛋白质溶液能形成丁达尔现象 |
B.蛋白质中加入 溶液产生盐析现象 溶液产生盐析现象 |
| C.蛋白质水解的最终产物能形成两性离子 |
| D.蛋白质水解的最终产物与茚三酮水溶液在加热条件下发生显色反应 |
(6)关于物质J说法正确的是___________。
| A.分子中含1个不对称碳原子 |
| B.发生水解反应得到3种产物 |
| C.苯环上的一溴代物有3种 |
D.分子中碳原子的杂化类型有 、 、 、sp 、sp |
(7)写出一种符合下列条件的B的同分异构体的结构简式
ⅰ)属于α-氨基酸类
ⅱ)能使
 的
的 溶液褪色
溶液褪色ⅲ)苯环上仅有两个取代基,且苯环上一溴代物有两种
(8)合成路线中设计F→G,I→J步骤①的目的是
(9)结合以上合成信息,在括号内补全
 的合成路线。
的合成路线。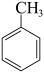
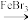 ( )
( )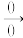 ( )
( )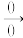
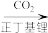 ( )
( )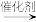
您最近一年使用:0次
解题方法
6 . 下列关于肼的说法正确的是
A.电子式为 | B.既含极性键,又含非极性键 |
| C.属于极性分子 | D.N原子为sp2杂化 |
您最近一年使用:0次
名校
解题方法
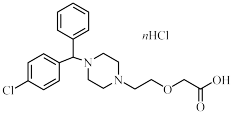
7 . 盐酸左西替利嗪是一种用于治疗荨麻疹的药物。其部分说明书如下:
(1)在左西替利嗪中添加盐酸的目的是___________ ;药品成分中n的值为___________ 。
(2)市售的普通盐酸西替利嗪片也能治疗荨麻疹,而本品仍对西替利嗪的对映体进行分离,其可能原因是___________ 。请在下图中用:“·”标出具有手性的碳原子。___________
| 盐酸左西替利嗪说明书 【成分】本品为西替利嗪的R型对映体,在过量盐酸中结晶制得。 【性状】本品外观是白色或类白色的片剂,易溶于水。
|
(2)市售的普通盐酸西替利嗪片也能治疗荨麻疹,而本品仍对西替利嗪的对映体进行分离,其可能原因是

| A.西替利嗪中,有9个碳原子与氮原子的杂化方式相同 |
| B.将西替利嗪溶于水,形成内盐 |
| C.两个苯环上的12个碳原子共平面 |
| D.分子内含有羧基和酯基 |
您最近一年使用:0次
解题方法
8 . Ⅰ.立方氮化硼(BN)、立方金刚石、碳化硅(SiC)等都是莫氏硬度高的超硬材料,在工业上有广泛应用。
(1)C、N、O三种元素中第一电离能最大的是_____ ,电负性最大的是_____ 。
A.碳元素 B.氮元素 C.氧元素
(2)下列有关Si说法正确的有___________。
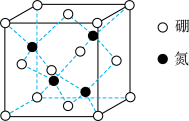
Ⅱ.立方氮化硼(BN)可由硼酸(H3BO3)和尿素[CO(NH2)2]反应制得,下图是立方氮化硼(BN)的晶胞示意图,立方金刚石、碳化硅(SiC)结构均与其相似,三者晶体中键长数据如下表。
(3)已知尿素[CO(NH2)2]结构中,碳、氮、氧原子均在同一平面,判断碳原子的杂化方式___________
(4)依据相关数据,比较上述三种晶体的莫氏硬度,并说明原因___________ 。
(5)立方氮化硼 (BN)晶胞中含有___________ 个硼原子,距离硼原子最近的氮原子有___________ 个。已知立方氮化硼晶体的密度为3.20g·cm−3,NA为阿伏加德罗常数,则该晶体晶胞边长的表达式为___________ cm。(用含NA的式子表达)已知:M(B) =10.8 g·mol−1,M(N) =14.0 g·mol−1
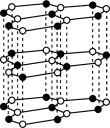
(6)六方氮化硼(BN)的结构与石墨相似,俗称“白石墨”,其结构如下图所示,若要区分某BN样品是六方氮化硼(BN)还是立方氮化硼(BN)下列方法可行的是___________。
(1)C、N、O三种元素中第一电离能最大的是
A.碳元素 B.氮元素 C.氧元素
(2)下列有关Si说法正确的有___________。
| A.基态Si原子核外有3种能量的电子 |
| B.Si原子由基态变为激发态时会释放能量 |
| C.基态Si原子的价层电子排布式为3p2 |
| D.Si在元素周期表中属于p区元素 |
Ⅱ.立方氮化硼(BN)可由硼酸(H3BO3)和尿素[CO(NH2)2]反应制得,下图是立方氮化硼(BN)的晶胞示意图,立方金刚石、碳化硅(SiC)结构均与其相似,三者晶体中键长数据如下表。

| 晶体 | 键长(pm) |
| 立方氮化硼(BN) | 157 |
| 立方金刚石 | 154 |
| 碳化硅(SiC) | 184 |
(3)已知尿素[CO(NH2)2]结构中,碳、氮、氧原子均在同一平面,判断碳原子的杂化方式
(4)依据相关数据,比较上述三种晶体的莫氏硬度,并说明原因
(5)立方氮化硼 (BN)晶胞中含有
(6)六方氮化硼(BN)的结构与石墨相似,俗称“白石墨”,其结构如下图所示,若要区分某BN样品是六方氮化硼(BN)还是立方氮化硼(BN)下列方法可行的是___________。

| A.晶体X射线衍射 | B.原子发射光谱 |
| C.质谱 | D.测定晶体的莫氏硬度 |
您最近一年使用:0次
名校
解题方法
9 . 卤素互化物、拟卤素与卤素单质的结构,性质相似。常见的卤素互化物有ICl、IBr等,拟卤素有(CN)2、(SCN)2等。
(1)卤族元素位于元素周期表的_______ 。
(2)79Br和81Br这两种核素的中子数之差的绝对值为_______ 。
(3)①Cl2;②ICl;③IBr三种物质熔点由高到低的顺序为_______ 。
(4)①已知CN-与N2结构相似,CN-的电子式为______ 。
②推算HCN分子中σ键与π键数目之比为_______ 。
③关于氨基氰(N≡C-NH2)分子的说法中正确的是_______ 。
A.C原子采用sp3杂化
B.N原子的杂化形式有sp与sp3杂化
C.C≡N键的键长大于C-N键
D.所有原子满足8电子稳定结构
开采的金矿可用氰化法提取,步骤如下:
i.将金矿砂溶于pH为10.5~11的KCN溶液,并鼓入空气,过滤除去矿渣,得含K[Au(CN)2]的滤液;
ii.向滤液中加入足量金属锌,得单质金。Zn+2K[Au(CN)2]=2Au+K2[Zn(CN)4]
(5)K[Au(CN)2]中Au+的配体为______ 。
(6)K2[Zn(CN)4]中Au+的配位数为______ 。
(7)i中反应的离子方程式为:_______ 。
 Au+
Au+ CN-+
CN-+ _______+
_______+ _______=
_______= [Au(CN)2]-+
[Au(CN)2]-+ _______
_______
(8)已知Ka(HCN)=4.0×10-10。i中,pH<10.5会导致相同时间内Au的浸取率下降,原因_______ 。
(1)卤族元素位于元素周期表的
| A.s区 | B.p区 | C.d区 | D.f区 |
(3)①Cl2;②ICl;③IBr三种物质熔点由高到低的顺序为
| A.①>②>③ | B.③>②>① | C.②>①>③ | D.③>①>② |
②推算HCN分子中σ键与π键数目之比为
③关于氨基氰(N≡C-NH2)分子的说法中正确的是
A.C原子采用sp3杂化
B.N原子的杂化形式有sp与sp3杂化
C.C≡N键的键长大于C-N键
D.所有原子满足8电子稳定结构
开采的金矿可用氰化法提取,步骤如下:
i.将金矿砂溶于pH为10.5~11的KCN溶液,并鼓入空气,过滤除去矿渣,得含K[Au(CN)2]的滤液;
ii.向滤液中加入足量金属锌,得单质金。Zn+2K[Au(CN)2]=2Au+K2[Zn(CN)4]
(5)K[Au(CN)2]中Au+的配体为
(6)K2[Zn(CN)4]中Au+的配位数为
(7)i中反应的离子方程式为:
 Au+
Au+ CN-+
CN-+ _______+
_______+ _______=
_______= [Au(CN)2]-+
[Au(CN)2]-+ _______
_______(8)已知Ka(HCN)=4.0×10-10。i中,pH<10.5会导致相同时间内Au的浸取率下降,原因
您最近一年使用:0次
10 . 立方烷(分子式为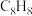 )是具有高度对称性的立方体结构分子,与游戏用的骰子十分类似。立方烷的核磁共振氢谱图如下所示。
)是具有高度对称性的立方体结构分子,与游戏用的骰子十分类似。立方烷的核磁共振氢谱图如下所示。
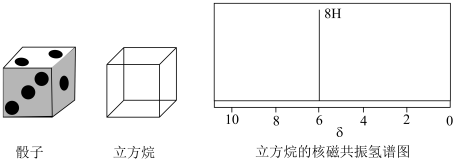
(1)从烃的分类角度看,立方烷属于_____ 。
A.脂肪烃 B.烯烃 C.芳香烃
(2)关于立方烷的说法正确的是_____。
(3)立方烷的二氯代物有_____种。
科学家首次制备立方烷的合成路线如下:
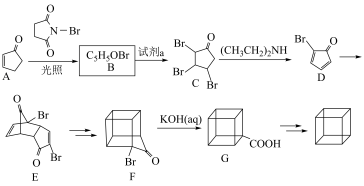
已知: 表示多步反应。
表示多步反应。
(4)A的分子式为_____ ,1molA与氢气加成时,最多消耗_____ mol氢气。
(5)试剂a为_____ 。
(6)C中含有_____个手性碳原子。
(7)C→D的反应类型为_____。
(8)D中所含官能团的名称为碳碳双键、_____ 、_____ 。
(9)芳香族化合物H与G互为同分异构体,写出一种满足下列条件H的结构简式_____ 。
a.能与 溶液反应 b.存在顺反异构体 c.所有碳原子均为
溶液反应 b.存在顺反异构体 c.所有碳原子均为 杂化
杂化
(10)设计一条由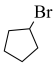 制备
制备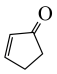 的合成路线。(无机试剂任选)
的合成路线。(无机试剂任选)_____ 。
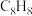 )是具有高度对称性的立方体结构分子,与游戏用的骰子十分类似。立方烷的核磁共振氢谱图如下所示。
)是具有高度对称性的立方体结构分子,与游戏用的骰子十分类似。立方烷的核磁共振氢谱图如下所示。
(1)从烃的分类角度看,立方烷属于
A.脂肪烃 B.烯烃 C.芳香烃
(2)关于立方烷的说法正确的是_____。
| A.易溶于水 | B.只含 键 键 | C.属于极性分子 | D.能使酸性 溶液褪色 溶液褪色 |
(3)立方烷的二氯代物有_____种。
| A.2 | B.3 | C.4 | D.5 |
科学家首次制备立方烷的合成路线如下:

已知:
 表示多步反应。
表示多步反应。(4)A的分子式为
(5)试剂a为
(6)C中含有_____个手性碳原子。
| A.2 | B.3 | C.4 | D.5 |
(7)C→D的反应类型为_____。
| A.取代反应 | B.加成反应 | C.消去反应 | D.氧化反应 |
(8)D中所含官能团的名称为碳碳双键、
(9)芳香族化合物H与G互为同分异构体,写出一种满足下列条件H的结构简式
a.能与
 溶液反应 b.存在顺反异构体 c.所有碳原子均为
溶液反应 b.存在顺反异构体 c.所有碳原子均为 杂化
杂化(10)设计一条由
 制备
制备 的合成路线。(无机试剂任选)
的合成路线。(无机试剂任选)
您最近一年使用:0次