名校
解题方法
1 . 磷的单质及其化合物用途非常广泛。回答下列问题:
(1)白磷晶胞属于面心立方最密堆积,每个 周围距离最近的
周围距离最近的 个数为
个数为___________ ;白磷隔绝空气加热转化为红磷,红磷是巨型分子,无定型结构,能证明白磷是晶体的实验验证方法是___________ 。
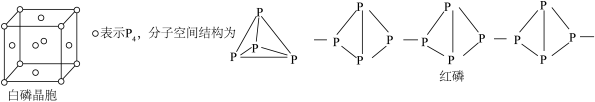
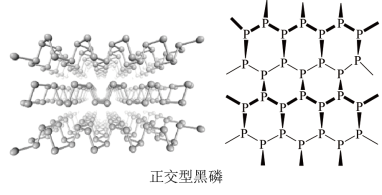
(2)黑磷晶体是一种新型材料,其中正交型黑磷具有类似石墨的片层结构。正交型黑磷中P原子的杂化方式为___________ 。白磷和正交型黑磷相比,熔点较高的是___________ ,原因是___________ 。
(3)BP是一种超硬耐磨涂层材料,晶胞结构与金刚石晶胞相似,其晶胞可看作金刚石晶胞内部的C原子被B原子替代,顶点和面心的C原子被P原子替代,晶胞参数为apm。沿z轴从上往下俯视的晶胞投影图如下所示。
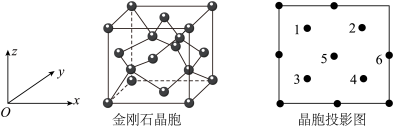
①投影图中原子5代表原子___________ (填“P”或“B”)。
②若投影图中原子6的分数坐标是(1,0.5,0.5),则原子1的分数坐标是___________ ,原子1、6之间的距离为___________ pm。
(1)白磷晶胞属于面心立方最密堆积,每个
 周围距离最近的
周围距离最近的 个数为
个数为
(2)黑磷晶体是一种新型材料,其中正交型黑磷具有类似石墨的片层结构。正交型黑磷中P原子的杂化方式为

(3)BP是一种超硬耐磨涂层材料,晶胞结构与金刚石晶胞相似,其晶胞可看作金刚石晶胞内部的C原子被B原子替代,顶点和面心的C原子被P原子替代,晶胞参数为apm。沿z轴从上往下俯视的晶胞投影图如下所示。

①投影图中原子5代表原子
②若投影图中原子6的分数坐标是(1,0.5,0.5),则原子1的分数坐标是
您最近一年使用:0次
名校
2 . 在金属(如:Cu、Co、Be、K等)的湿法冶炼中,某些含氮(如: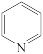 )、磷[如:磷酸丁基酯(C4H9O)3P=O]等有机物作萃取剂,可将金属萃取出来,从而实现在温和条件下金属冶炼。回答下列问题:
)、磷[如:磷酸丁基酯(C4H9O)3P=O]等有机物作萃取剂,可将金属萃取出来,从而实现在温和条件下金属冶炼。回答下列问题:
(1)基态Co原子核外电子排布式为[Ar]____ ,有____ 个未成对电子。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反的用-
表示,与之相反的用- 文表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为
文表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为____ 。
(3)科学家证实,BeCl2是共价化合物,请设计一个简单实验证明该结论:____ ;Be的杂化轨道类型为____ 。
(4)在N 、NH3、N2H4、NH
、NH3、N2H4、NH 、N2H
、N2H 五种微粒中,同种微粒间能形成氢键的有
五种微粒中,同种微粒间能形成氢键的有____ ;不能作为配位体的有____ ;空间构型为直线形的是____ 。
(5)氮原子的第一电离能____ (填“大于”“小于”或“等于”)磷原子的第一电离能。
(6)分别用 、
、 表示H2PO
表示H2PO 和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO
和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO 、K+在晶胞xx面、yz面上的位置。若晶胞底边的边长均为apm,高为cpm,阿伏加德罗常数的值为NA,晶体的密度为
、K+在晶胞xx面、yz面上的位置。若晶胞底边的边长均为apm,高为cpm,阿伏加德罗常数的值为NA,晶体的密度为____ g·cm-3(写出表达式即可)。

 )、磷[如:磷酸丁基酯(C4H9O)3P=O]等有机物作萃取剂,可将金属萃取出来,从而实现在温和条件下金属冶炼。回答下列问题:
)、磷[如:磷酸丁基酯(C4H9O)3P=O]等有机物作萃取剂,可将金属萃取出来,从而实现在温和条件下金属冶炼。回答下列问题:(1)基态Co原子核外电子排布式为[Ar]
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+
 表示,与之相反的用-
表示,与之相反的用- 文表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为
文表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为(3)科学家证实,BeCl2是共价化合物,请设计一个简单实验证明该结论:
(4)在N
 、NH3、N2H4、NH
、NH3、N2H4、NH 、N2H
、N2H 五种微粒中,同种微粒间能形成氢键的有
五种微粒中,同种微粒间能形成氢键的有(5)氮原子的第一电离能
(6)分别用
 、
、 表示H2PO
表示H2PO 和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO
和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO 、K+在晶胞xx面、yz面上的位置。若晶胞底边的边长均为apm,高为cpm,阿伏加德罗常数的值为NA,晶体的密度为
、K+在晶胞xx面、yz面上的位置。若晶胞底边的边长均为apm,高为cpm,阿伏加德罗常数的值为NA,晶体的密度为
您最近一年使用:0次
2022-06-15更新
|
480次组卷
|
3卷引用:江西省名校2022届高三下学期第三次模拟理科综合化学试题
江西省名校2022届高三下学期第三次模拟理科综合化学试题(已下线)专题17 物质结构与性质综合题-备战2023年高考化学母题题源解密(全国通用)2024届四川省宜宾市第四中学校高三上学期一诊模拟考试理综试题
2014高三·全国·专题练习
名校
3 . 已知A、B、C、D、E都是元素周期表中的前四周期元素,它们原子序数的大小关系为A<C<B<D<E。又知A原子的p轨道为半充满,其形成的简单氢化物的沸点是同主族非金属元素的氢化物中最高的。D原子得到一个电子后其3p轨道将全充满。B+离子比D原子形成的离子少一个电子层。C与B可形成BC型的离子化合物。E的原子序数为29。
请回答下列问题:
(1) 元素A简单氢化物中A原子的杂化类型是________ ,B、C、D的电负性由小到大的顺序为______ (用所对应的元素符号表示)。C的气态氢化物易溶于水的原因是____________________ 。
(2)E原子的基态电子排布式为________ 。元素E的单质晶体在不同温度下可有两种堆积方式,晶胞分别如图a和b所示,则其面心立方堆积的晶胞与体心立方堆积的晶胞中实际含有的E原子的个数之比为____________ 。

(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是:________ 。
(4)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是________ 。
(5)温室效应,科学家设计反应:CO2+4H2—→CH4+2H2O以减小空气中CO2。若有1 mol CH4生成,则有________ mol σ键和________ mol π键断裂。
请回答下列问题:
(1) 元素A简单氢化物中A原子的杂化类型是
(2)E原子的基态电子排布式为

(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是:
(4)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是
(5)温室效应,科学家设计反应:CO2+4H2—→CH4+2H2O以减小空气中CO2。若有1 mol CH4生成,则有
您最近一年使用:0次
解题方法
4 . 羟醛缩合反应是一种常用的增长碳链的方法。一种合成目标产物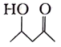 (图中物质⑦)的反应机理如图所示。下列说法错误的是
(图中物质⑦)的反应机理如图所示。下列说法错误的是
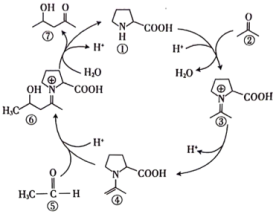
| A.物质②和⑤均易溶于水 |
| B.物质③→④的过程中,N的杂化方式未发生改变 |
| C.⑥→⑦的过程中没有非极性键的断裂和生成 |
D.化合物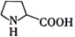 为该反应的催化剂,能降低反应的活化能 为该反应的催化剂,能降低反应的活化能 |
您最近一年使用:0次
2024-06-02更新
|
66次组卷
|
2卷引用:江西省九校联考2023-2024学年高三下学期3月月考化学试题
5 . 由四种短周期主族元素形成的某有机物甲的结构如图所示,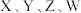 的原子序数依次增大,
的原子序数依次增大,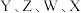 的原子半径依次减小。下列说法错误的是
的原子半径依次减小。下列说法错误的是
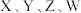 的原子序数依次增大,
的原子序数依次增大,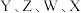 的原子半径依次减小。下列说法错误的是
的原子半径依次减小。下列说法错误的是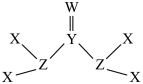
| A.通常状况下,由于甲分子间形成氢键使甲呈固态 |
B.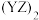 为直线形分子,其中2个Y原子均采取 为直线形分子,其中2个Y原子均采取 杂化 杂化 |
C. 电负性: 电负性: |
D.第一电离能: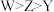 |
您最近一年使用:0次
名校
解题方法
6 . NH4NO3、Pb(N3)2、N5AsF6、2,4,6-三硝基甲苯均可用作炸药。下列关于它们的说法正确的是
A.NH4NO3是一种常见的炸药,其分解反应为2NH4NO3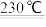 2N2↑+O2↑+4H2O↑,上述反应中,每生成0.15molO2转移电子数为0.6NA 2N2↑+O2↑+4H2O↑,上述反应中,每生成0.15molO2转移电子数为0.6NA |
B. 的中心原子N的杂化方式为sp杂化 的中心原子N的杂化方式为sp杂化 |
| C.基态As原子的价层电子中成对电子数与未成对电子数的比值为12∶3 |
| D.NH4NO3、Pb(N3)2、N5AsF6、2,4,6-三硝基甲苯形成的晶体均为离子晶体 |
您最近一年使用:0次
解题方法
7 . 一种含 催化剂活化甲烷中碳氢键的反应机理如图所示。下列说法错误的是
催化剂活化甲烷中碳氢键的反应机理如图所示。下列说法错误的是
 催化剂活化甲烷中碳氢键的反应机理如图所示。下列说法错误的是
催化剂活化甲烷中碳氢键的反应机理如图所示。下列说法错误的是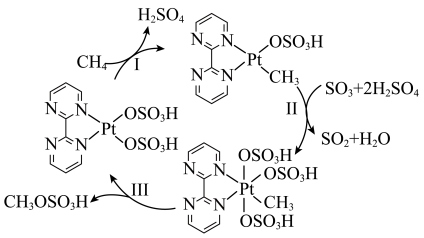
A.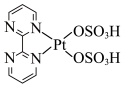 是该反应是催化剂 是该反应是催化剂 |
B. 为含极性键的非极性分子 为含极性键的非极性分子 |
C.配位键 强于配位键 强于配位键 键 键 |
D.上述过程的总反应: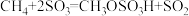 |
您最近一年使用:0次
名校
8 . 己二酸是一种重要的化工原料,在现有工业路线基础上,研究提出了“绿色”合成路线:
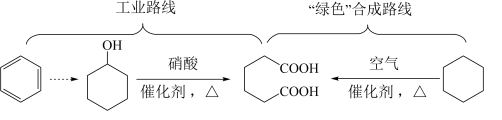
A.苯环中含有C—C键和 键 键 |
| B.—COOH是亲水基团,—OH是疏水基团 |
| C.图中“绿色”合成路线的原子利用率小于100% |
| D.己二酸、环己醇中碳原子杂化方式完全相同 |
您最近一年使用:0次
2024-04-15更新
|
135次组卷
|
2卷引用:江西省九江市同文中学多校联考2024届高三下学期3月月考化学试题
名校
9 . 氢叠氮酸( )属于叠氮化物,是一种弱酸,其酸性类似于醋酸,能微弱电离出
)属于叠氮化物,是一种弱酸,其酸性类似于醋酸,能微弱电离出 和
和 。分子结构示意图如图所示。回答下列问题:
。分子结构示意图如图所示。回答下列问题:

(1)下列有关说法正确的是___________(填字母符号)。
(2)叠氮酸根可作为一种配体,在 中钴显
中钴显___________ 价,基态钴原子的价电子排布式为___________ 。 空间形状为
空间形状为___________ 。
(3) 与
与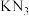 结构类似,前者熔点比后者
结构类似,前者熔点比后者___________ (填“大”或“小”), 中氮原子的第一电离能比氧原子
中氮原子的第一电离能比氧原子___________ (填“大”或“小”)。
(4)人造立方氮化硼是超硬材料,其晶胞如图所示。

①晶体中硼原子的配位数为___________ 。
②设该晶体的摩尔质量为 ,晶体的密度为ρ
,晶体的密度为ρ ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶体中的距离最近的硼原子之间的距离为
,则晶体中的距离最近的硼原子之间的距离为___________ cm。
 )属于叠氮化物,是一种弱酸,其酸性类似于醋酸,能微弱电离出
)属于叠氮化物,是一种弱酸,其酸性类似于醋酸,能微弱电离出 和
和 。分子结构示意图如图所示。回答下列问题:
。分子结构示意图如图所示。回答下列问题:
(1)下列有关说法正确的是___________(填字母符号)。
A. 中含有5个 中含有5个 键 键 | B. 中三个氮原子采用的都是sp2杂化 中三个氮原子采用的都是sp2杂化 |
C. 、 、 都是极性分子 都是极性分子 | D. 、 、 、 、 分子间都可以形成氢键 分子间都可以形成氢键 |
 中钴显
中钴显 空间形状为
空间形状为(3)
 与
与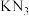 结构类似,前者熔点比后者
结构类似,前者熔点比后者 中氮原子的第一电离能比氧原子
中氮原子的第一电离能比氧原子(4)人造立方氮化硼是超硬材料,其晶胞如图所示。

①晶体中硼原子的配位数为
②设该晶体的摩尔质量为
 ,晶体的密度为ρ
,晶体的密度为ρ ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶体中的距离最近的硼原子之间的距离为
,则晶体中的距离最近的硼原子之间的距离为
您最近一年使用:0次
名校
解题方法
10 . 短周期主族元素X、Y、Z、W原子序数依次增大,四种元素组成的一种食品添加剂结构如图所示。Z的原子半径在短周期中最大,W基态原子的s能级电子总数是p能级电子总数的2/3。下列说法不正确的是
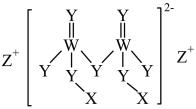
| A.电负性:Y>W>Z |
| B.简单离子半径:W>Y>Z |
| C.简单氢化物沸点:Y>W |
| D.WX3、X3Y+中W、Y两种原子的杂化轨道类型不同 |
您最近一年使用:0次
2024-03-13更新
|
233次组卷
|
2卷引用:江西省南昌市第十九中学2023-2024学年高二下学期3月月考化学试题



