1 . 盐酸和草酸是生活中常见的酸,回答下列问题:
Ⅰ.某学生用0.2000mol/L的标准NaOH溶液滴定未知浓度的盐酸,操作如下:
a.用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
b.固定好滴定管并使滴定管尖嘴处充满液体;
c.调节液面至“0”或“0”刻度线以下,并记下读数;
d.移取20.00L待测液注入洁净的存有少量蒸馏水的锥形瓶中,并加入3滴酚酞溶液;
e.用标准液滴定至终点,记下滴定管液面读数。
(1)以上步骤中有错误的是___________ (填字母)。
(2)该同学将中和滴定原理应用到葡萄酒中抗氧化剂残留量(以游离 计算)的测定中:
计算)的测定中:
准确量取100.00L葡萄酒样品,加酸蒸馏出抗氧化剂成分,取馏分于锥形瓶中,滴加少量淀粉溶液,用0.0100mo/L标准 溶液滴定至终点,重复操作三次,平均消耗标准溶液22.50mL。(已知滴定过程中所发生的反应是
溶液滴定至终点,重复操作三次,平均消耗标准溶液22.50mL。(已知滴定过程中所发生的反应是 )
)
①滴定前需排放装有标准溶液的滴定管尖嘴处的气泡,其正确的图示为___________ (填字母)。
A. B.
B. 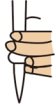 C.
C. 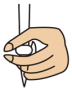 D.
D.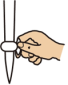
②判断达到滴定终点的依据是___________ ;所测100.00mL葡萄酒样品中抗氧化剂的残留量为___________ mg/L。
Ⅱ.已知常温下的电离平衡常数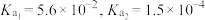 ,某化学小组研究草酸
,某化学小组研究草酸 及其盐的性质。
及其盐的性质。
(3) 中
中 的杂化类型是
的杂化类型是___________ 。
(4)常温下,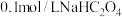 溶液中各离子浓度由大到小的顺序为
溶液中各离子浓度由大到小的顺序为___________ 。
(5)下列 溶液中离子浓度的关系不正确的是
溶液中离子浓度的关系不正确的是___________ (填字母)。
A.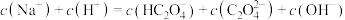
B.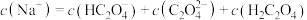
C.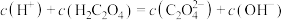
(6)探究 和
和 在溶液中的反应。
在溶液中的反应。
【资料】i.三水三草酸合铁酸钾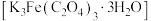 为翠绿色晶体,光照易分解,其水溶液中存在:
为翠绿色晶体,光照易分解,其水溶液中存在: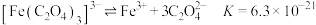 。
。
ii.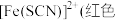
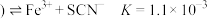 。
。
进行如下实验:
经检验,上述实验中 和
和 未发生氧化还原反应。
未发生氧化还原反应。
取实验中少量晶体洗净,配成溶液波,滴加 溶液,不变红,原因是
溶液,不变红,原因是___________ (结合资料,用必要的化学用语和数据解释原因),继续加入硫酸,溶液变红,说明加入硫酸, 与
与 结合使反应
结合使反应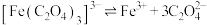 平衡
平衡___________ (填“正向”或“逆向”)移动。
(7)设计实验证明草酸的酸性比碳酸强:___________ 。
Ⅰ.某学生用0.2000mol/L的标准NaOH溶液滴定未知浓度的盐酸,操作如下:
a.用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
b.固定好滴定管并使滴定管尖嘴处充满液体;
c.调节液面至“0”或“0”刻度线以下,并记下读数;
d.移取20.00L待测液注入洁净的存有少量蒸馏水的锥形瓶中,并加入3滴酚酞溶液;
e.用标准液滴定至终点,记下滴定管液面读数。
(1)以上步骤中有错误的是
(2)该同学将中和滴定原理应用到葡萄酒中抗氧化剂残留量(以游离
 计算)的测定中:
计算)的测定中:准确量取100.00L葡萄酒样品,加酸蒸馏出抗氧化剂成分,取馏分于锥形瓶中,滴加少量淀粉溶液,用0.0100mo/L标准
 溶液滴定至终点,重复操作三次,平均消耗标准溶液22.50mL。(已知滴定过程中所发生的反应是
溶液滴定至终点,重复操作三次,平均消耗标准溶液22.50mL。(已知滴定过程中所发生的反应是 )
)①滴定前需排放装有标准溶液的滴定管尖嘴处的气泡,其正确的图示为
A.
 B.
B.  C.
C.  D.
D.
②判断达到滴定终点的依据是
Ⅱ.已知常温下的电离平衡常数
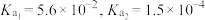 ,某化学小组研究草酸
,某化学小组研究草酸 及其盐的性质。
及其盐的性质。(3)
 中
中 的杂化类型是
的杂化类型是(4)常温下,
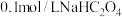 溶液中各离子浓度由大到小的顺序为
溶液中各离子浓度由大到小的顺序为(5)下列
 溶液中离子浓度的关系不正确的是
溶液中离子浓度的关系不正确的是A.
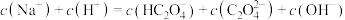
B.
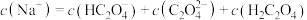
C.
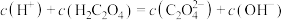
(6)探究
 和
和 在溶液中的反应。
在溶液中的反应。【资料】i.三水三草酸合铁酸钾
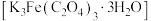 为翠绿色晶体,光照易分解,其水溶液中存在:
为翠绿色晶体,光照易分解,其水溶液中存在: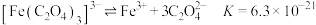 。
。ii.
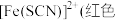
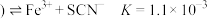 。
。进行如下实验:
| 操作 | 现象 |
在避光处,向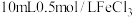 溶液中缓慢加入 溶液中缓慢加入  溶液至过量,搅拌,充分反应后,冰水浴冷却,过滤 溶液至过量,搅拌,充分反应后,冰水浴冷却,过滤 | 得到翠绿色溶液和翠绿色晶体 |
 和
和 未发生氧化还原反应。
未发生氧化还原反应。取实验中少量晶体洗净,配成溶液波,滴加
 溶液,不变红,原因是
溶液,不变红,原因是 与
与 结合使反应
结合使反应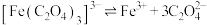 平衡
平衡(7)设计实验证明草酸的酸性比碳酸强:
您最近一年使用:0次
解题方法
2 . 2020年12月17日,我国“嫦娥五号”返回器携月壤成功着陆。研究发现,月壤中存在天然的铁、金、银、铅、锌、铜、锑、铼等矿物颗粒。
(1)要证明月壤中含有这些元素,可采用的方法是___________ 。
(2)写出铜的基态原子的电子排布式:___________ 。
(3)月球表面的月海玄武岩中富含钛和铁,将月海玄武岩用硝酸溶解,所得溶液用 检验,溶液呈红色。
检验,溶液呈红色。 中K、C、N的电负性从大到小的顺序是
中K、C、N的电负性从大到小的顺序是___________ ,C原子的杂化轨道类型是___________ , 的空间构型是
的空间构型是___________ 形,1
 中含有的
中含有的 键数目是
键数目是___________ 。
(4)嫦娥五号采样机中的钻杆是由中国科学院科学家研制的碳化硅增强铝基复合材料制成,具有轻质、高刚度、高强度和耐磨损等特点。
①铝基复合材料中有一种重要的物质氮化铝( ,熔点为2249℃),氮化铝属类金刚石氮化物,则它属于
,熔点为2249℃),氮化铝属类金刚石氮化物,则它属于___________ (填晶体类型)。氮化铝可用氧化铝(熔点为2054℃)为原料来制取,从晶体类型角度分析 的熔点比氧化铝高的原因是
的熔点比氧化铝高的原因是___________ 。
②氮化铝的晶体结构如图所示,其中铝原子的配位数是___________ , 与N原子最近的距离为a
与N原子最近的距离为a ,则该晶体的密度为
,则该晶体的密度为___________  。(
。( 为阿伏加德罗常数的值,列出表达式即可)
为阿伏加德罗常数的值,列出表达式即可)

(1)要证明月壤中含有这些元素,可采用的方法是
(2)写出铜的基态原子的电子排布式:
(3)月球表面的月海玄武岩中富含钛和铁,将月海玄武岩用硝酸溶解,所得溶液用
 检验,溶液呈红色。
检验,溶液呈红色。 中K、C、N的电负性从大到小的顺序是
中K、C、N的电负性从大到小的顺序是 的空间构型是
的空间构型是
 中含有的
中含有的 键数目是
键数目是(4)嫦娥五号采样机中的钻杆是由中国科学院科学家研制的碳化硅增强铝基复合材料制成,具有轻质、高刚度、高强度和耐磨损等特点。
①铝基复合材料中有一种重要的物质氮化铝(
 ,熔点为2249℃),氮化铝属类金刚石氮化物,则它属于
,熔点为2249℃),氮化铝属类金刚石氮化物,则它属于 的熔点比氧化铝高的原因是
的熔点比氧化铝高的原因是②氮化铝的晶体结构如图所示,其中铝原子的配位数是
 与N原子最近的距离为a
与N原子最近的距离为a ,则该晶体的密度为
,则该晶体的密度为 。(
。( 为阿伏加德罗常数的值,列出表达式即可)
为阿伏加德罗常数的值,列出表达式即可)
您最近一年使用:0次
3 . 在金属(如:Cu、Co、Be、K等)的湿法冶炼中,某些含氮(如: )、磷[如:磷酸丁基酯(C4H9O)3P=O]等有机物作萃取剂,可将金属萃取出来,从而实现在温和条件下金属冶炼。
)、磷[如:磷酸丁基酯(C4H9O)3P=O]等有机物作萃取剂,可将金属萃取出来,从而实现在温和条件下金属冶炼。
回答下列问题:
(1)基态Co原子核外电子排布式为[Ar]_______ ,有_______ 个 运动状态不同的电子。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 号表示,与之相反的用-
号表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为_______ 。
(3)科学家证实,BeCl2是共价化合物,请设计一个简 单实验证明该结论:_______ ;Be的杂化轨道类型为_______ 。
(4)在N 、 NH3、N2H4、NH
、 NH3、N2H4、NH 、N2H
、N2H 五种微粒中,同种微粒间能形成氢键的有
五种微粒中,同种微粒间能形成氢键的有_______ ;不能作为配位体的有_______ ;空间构型为直线形的是_______ 。
(5)氮原子的第一电离能_______ (填“大于”“小于”或“等 于”)磷原子的第一电离能。
(6)分别用 、
、 表示H2PO
表示H2PO 和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO
和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO 、K+在晶胞xz面、yz面上的位置。若晶胞底边的边长均为a pm、高为c pm,阿伏加德罗常数的值为NA,晶体的密度为
、K+在晶胞xz面、yz面上的位置。若晶胞底边的边长均为a pm、高为c pm,阿伏加德罗常数的值为NA,晶体的密度为 _______ g·cm-3(写出表达式即可)。

 )、磷[如:磷酸丁基酯(C4H9O)3P=O]等有机物作萃取剂,可将金属萃取出来,从而实现在温和条件下金属冶炼。
)、磷[如:磷酸丁基酯(C4H9O)3P=O]等有机物作萃取剂,可将金属萃取出来,从而实现在温和条件下金属冶炼。回答下列问题:
(1)基态Co原子核外电子排布式为[Ar]
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+
 号表示,与之相反的用-
号表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为(3)科学家证实,BeCl2是共价化合物,请设计一个简 单实验证明该结论:
(4)在N
 、 NH3、N2H4、NH
、 NH3、N2H4、NH 、N2H
、N2H 五种微粒中,同种微粒间能形成氢键的有
五种微粒中,同种微粒间能形成氢键的有(5)氮原子的第一电离能
(6)分别用
 、
、 表示H2PO
表示H2PO 和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO
和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO 、K+在晶胞xz面、yz面上的位置。若晶胞底边的边长均为a pm、高为c pm,阿伏加德罗常数的值为NA,晶体的密度为
、K+在晶胞xz面、yz面上的位置。若晶胞底边的边长均为a pm、高为c pm,阿伏加德罗常数的值为NA,晶体的密度为 
您最近一年使用:0次
2022-05-02更新
|
259次组卷
|
3卷引用:陕西省安康市重点名校2024届高三上学期10联考化学试题
陕西省安康市重点名校2024届高三上学期10联考化学试题黑龙江省齐齐哈尔市2022届高三第二次模拟考试理科综合化学试题(已下线)专项17 物质结构与性质综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)
名校
解题方法
4 . X、Y、Z、Q、R、W均为前四周期原子序数依次增大的六种元素,其中前4种为同周期相邻元素。Q的基态原子2p能级有1个未成对电子,R是周期表中族序数最大但核电荷数最小的,W原子核内有29个质子。请回答(用相应元素符号表示):
(1)2021年3月20日三星堆考古揭晓了最新发掘的大量珍贵文物,考古学家可利用 的一种核素来鉴定其年代,该核素的符号为
的一种核素来鉴定其年代,该核素的符号为_______ 。
(2)与Z同周期的所有元素中,第一电离能大于Z的有_______ 种。
(3)请写一个能证明非金属性Q强于Z的化学反应方程式_______ 。
(4)Y的一种氢化物分子中共有18个电子,其电子式是_______ 。
(5) 离子的空间结构是
离子的空间结构是_______ ,与其互为等电子体的有_______ 、_______ 。(任写一种分子和一种阳离子)
(6)向W的硫酸盐中加入过量氨水,再加入一定乙醇,析出晶体的化学式是_______ 。
(7)R元素位于周期表的_______ 区,基态 的价层电子轨道表示式是
的价层电子轨道表示式是_______ 。化合物 中与直接结合的原子是X而不是Z的可能原因是
中与直接结合的原子是X而不是Z的可能原因是_______ , 含有的
含有的 键数目是
键数目是_______ 。
(1)2021年3月20日三星堆考古揭晓了最新发掘的大量珍贵文物,考古学家可利用
 的一种核素来鉴定其年代,该核素的符号为
的一种核素来鉴定其年代,该核素的符号为(2)与Z同周期的所有元素中,第一电离能大于Z的有
(3)请写一个能证明非金属性Q强于Z的化学反应方程式
(4)Y的一种氢化物分子中共有18个电子,其电子式是
(5)
 离子的空间结构是
离子的空间结构是(6)向W的硫酸盐中加入过量氨水,再加入一定乙醇,析出晶体的化学式是
(7)R元素位于周期表的
 的价层电子轨道表示式是
的价层电子轨道表示式是 中与直接结合的原子是X而不是Z的可能原因是
中与直接结合的原子是X而不是Z的可能原因是 含有的
含有的 键数目是
键数目是
您最近一年使用:0次
名校
解题方法
5 . 超高能含能材料被视为可影响国家安全的战略性技术材料,其组成元素通常含碳、氮、过渡金属元素等。回答下列问题:
(1)在现代化学中,常利用_______ 来鉴定元素。
(2)[Co(NH3)5CO3]NO3是一种制备超高能含能材料的原料。基态Co3+中有_______ 个未成对电子,CO 的空间立体构型为
的空间立体构型为_______ ,该物质中所含有的第二周期元素的电负性由大到小的顺序为_______ ,配离子中的配位数为_______ 。正丁醇和正己烷是含有该物质中部分元素的有机化合物,已知物质在单位时间内挥发得越快,温度下降得就越快。用温度传感器进行数字化实验,测得这两种有机化合物在挥发过程中的温度变化曲线如图所示。则该数字化实验证明_______ (填物质名称)更难挥发,从物质结构角度分析原因为_______ 。

(3)叠氮化铅[Pb(N3)2]是一种各国都纳入军事标准和民用标准的引爆药,与N 互为等电子体的一种分子的分子式是
互为等电子体的一种分子的分子式是_______ 。科学家制得一 种高氮化合物BN17,结构组成为N [B(N3)4]- ,该化合物的晶体类型为
[B(N3)4]- ,该化合物的晶体类型为_______ 晶体,其中B原子的杂化方式为_______ 。
(4)2,4-二硝基间苯酚是火工品制造业常用的重要中间体,其摩尔质量为200g·mol-1,分子结构可简化为图1所示,分子在晶体中的堆积方式如图2所示。该晶体属于正交晶系结构,晶胞参数分别为apm、bpm、cpm,α=β=γ=90°。则该晶体的密度ρ=_______ g·cm-3(列出计算式,设NA为阿伏加德罗常数的值)。

(1)在现代化学中,常利用
(2)[Co(NH3)5CO3]NO3是一种制备超高能含能材料的原料。基态Co3+中有
 的空间立体构型为
的空间立体构型为
(3)叠氮化铅[Pb(N3)2]是一种各国都纳入军事标准和民用标准的引爆药,与N
 互为等电子体的一种分子的分子式是
互为等电子体的一种分子的分子式是 [B(N3)4]- ,该化合物的晶体类型为
[B(N3)4]- ,该化合物的晶体类型为(4)2,4-二硝基间苯酚是火工品制造业常用的重要中间体,其摩尔质量为200g·mol-1,分子结构可简化为图1所示,分子在晶体中的堆积方式如图2所示。该晶体属于正交晶系结构,晶胞参数分别为apm、bpm、cpm,α=β=γ=90°。则该晶体的密度ρ=

您最近一年使用:0次
2021-01-26更新
|
289次组卷
|
2卷引用:陕西省西安中学2021届高三第七次模拟考试化学试题
名校
解题方法
6 . 氢能被视为21世纪最具发展潜力的清洁能源,开发高效储氢材料是氢能利用的重要研究方向。
(1)H3BNH3是一种潜在的储氢材料,其中N原子的价电子轨道表达式为____ 。
(2)制备H3BNH3的化学原料为(HB=NH)3,为六元环状物质,与其互为等电子体的有机物分子式为__ ,CH4、H2O、CO2的键角由大到小的顺序为____ ,B、C、N、O的第一电离能由大到小的顺序为_ 。
(3)C16S8是新型环烯类储氢材料,研究证明其分子呈平面结构(如图所示)。

①C16S8分子中C原子和S原子的杂化轨道类型分别为____ 。
②测得C16S8中碳硫键的键长介于C─S和C=S之间,其原因可能是______ 。
(4)某种铜银合金晶体具有储氢功能,它是面心立方最密堆积结构,Cu原子位于面心,Ag原子位于顶点,H原子可进入由Cu原子和Ag原子构成的四面体空隙中。若将Cu、Ag原子等同看待,该晶体储氢后的晶胞结构与CaF2(如图)相似,该晶体储氢后的化学式为_____ 。

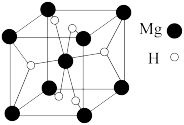
(5)MgH2是金属氢化物储氢材料,其晶胞如图所示,该晶体的密度为 ρ g/cm3,则该晶胞的体积为_____ 。(用含ρ、NA的代数式表示即可)
(1)H3BNH3是一种潜在的储氢材料,其中N原子的价电子轨道表达式为
(2)制备H3BNH3的化学原料为(HB=NH)3,为六元环状物质,与其互为等电子体的有机物分子式为
(3)C16S8是新型环烯类储氢材料,研究证明其分子呈平面结构(如图所示)。

①C16S8分子中C原子和S原子的杂化轨道类型分别为
②测得C16S8中碳硫键的键长介于C─S和C=S之间,其原因可能是
(4)某种铜银合金晶体具有储氢功能,它是面心立方最密堆积结构,Cu原子位于面心,Ag原子位于顶点,H原子可进入由Cu原子和Ag原子构成的四面体空隙中。若将Cu、Ag原子等同看待,该晶体储氢后的晶胞结构与CaF2(如图)相似,该晶体储氢后的化学式为

(5)MgH2是金属氢化物储氢材料,其晶胞如图所示,该晶体的密度为 ρ g/cm3,则该晶胞的体积为

您最近一年使用:0次
2020-09-01更新
|
275次组卷
|
5卷引用:陕西省西安中学2021届高三上学期第四次月考化学试题
名校
解题方法
7 . 氢能被视为21世纪最具发展潜力的清洁能源,开发高效储氢材料是氢能利用的重要研究方向。
(1)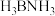 是一种潜在的储氢材料,其中N原子的价电子排布式为
是一种潜在的储氢材料,其中N原子的价电子排布式为________________ 。
(2) 的键角由大到小的顺序为
的键角由大到小的顺序为________________________ , 的第一电离能由大到小的顺序为
的第一电离能由大到小的顺序为_______________________________ 。
(3) 是新型环烯类储氢材料,研究证明其分子呈平面结构(如图所示)。
是新型环烯类储氢材料,研究证明其分子呈平面结构(如图所示)。

① 分子中
分子中 原子和
原子和 原子的杂化轨道类型分别为
原子的杂化轨道类型分别为_________________________ 。
②测得 中碳硫键的键长介于C-S键和C=S键之间,其原因可能是
中碳硫键的键长介于C-S键和C=S键之间,其原因可能是________________________________________________ 。
(4)某种铜银合金晶体具有储氢功能,它是面心立方最密堆积结构, 原子位于面心,Ag原子位于顶点,H原子可进入由Cu原子和Ag原子构成的四面体空隙中。若将
原子位于面心,Ag原子位于顶点,H原子可进入由Cu原子和Ag原子构成的四面体空隙中。若将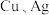 原子等同看待,该晶体储氢后的晶胞结构与
原子等同看待,该晶体储氢后的晶胞结构与 (如图)相似,该晶体储氢后的化学式为
(如图)相似,该晶体储氢后的化学式为_________________________ 。


(5) 是金属氢化物储氢材料,其晶胞如图所示,该晶体的密度为
是金属氢化物储氢材料,其晶胞如图所示,该晶体的密度为 ,则该晶胞的体积为
,则该晶胞的体积为___________  (用含
(用含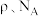 的代数式表示)。
的代数式表示)。
(1)
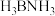 是一种潜在的储氢材料,其中N原子的价电子排布式为
是一种潜在的储氢材料,其中N原子的价电子排布式为(2)
 的键角由大到小的顺序为
的键角由大到小的顺序为 的第一电离能由大到小的顺序为
的第一电离能由大到小的顺序为(3)
 是新型环烯类储氢材料,研究证明其分子呈平面结构(如图所示)。
是新型环烯类储氢材料,研究证明其分子呈平面结构(如图所示)。
①
 分子中
分子中 原子和
原子和 原子的杂化轨道类型分别为
原子的杂化轨道类型分别为②测得
 中碳硫键的键长介于C-S键和C=S键之间,其原因可能是
中碳硫键的键长介于C-S键和C=S键之间,其原因可能是(4)某种铜银合金晶体具有储氢功能,它是面心立方最密堆积结构,
 原子位于面心,Ag原子位于顶点,H原子可进入由Cu原子和Ag原子构成的四面体空隙中。若将
原子位于面心,Ag原子位于顶点,H原子可进入由Cu原子和Ag原子构成的四面体空隙中。若将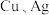 原子等同看待,该晶体储氢后的晶胞结构与
原子等同看待,该晶体储氢后的晶胞结构与 (如图)相似,该晶体储氢后的化学式为
(如图)相似,该晶体储氢后的化学式为

(5)
 是金属氢化物储氢材料,其晶胞如图所示,该晶体的密度为
是金属氢化物储氢材料,其晶胞如图所示,该晶体的密度为 ,则该晶胞的体积为
,则该晶胞的体积为 (用含
(用含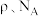 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2020-03-26更新
|
223次组卷
|
2卷引用:陕西省西安中学2020届高三第三次模拟考试化学试题
解题方法
8 . 近年来,科学家们对高压下富氢化物高温超导体研究方兴未艾。科学家利用氨硼烷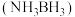 为氢源合成了多种具有高温超导性的富氢化物如
为氢源合成了多种具有高温超导性的富氢化物如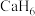 、
、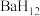 、
、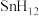 。回答下列问题:
。回答下列问题:
(1)氨硼烷中,元素的电负性:B_______ N(填“>”或“<”),上述6种元素中,位于元素周期表p区的是_______ 。
(2)基态Sn原子的价电子排布图为_______ , 的熔点(963℃)远高于
的熔点(963℃)远高于 (
(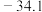 ℃),原因是
℃),原因是_______ 。
(3)乙硼烷与氨硼烷组成相似,但分子结构不同,其成键情况如图所示,每个B原子均以 杂化轨道成键,水平面上下是两个3中心2电子“氢桥键”。
杂化轨道成键,水平面上下是两个3中心2电子“氢桥键”。_______ (填标号)。
a.N-B键为配位键,可自由旋转
b.氢桥键为非极性键,不能自由旋转
c.乙硼烷分子中既有 键,又有
键,又有 键
键
d.氨硼烷为极性分子,熔点比乙硼烷高
②乙硼烷水解释放 ,生成
,生成 。
。 具有层状结构,与
具有层状结构,与 溶液反应生成
溶液反应生成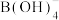 。
。 和
和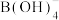 中B的轨道杂化类型分别为
中B的轨道杂化类型分别为_______ 和_______ 。
(4)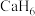 是第一个理论预测具有独特的“氢笼”结构的富氢化物。
是第一个理论预测具有独特的“氢笼”结构的富氢化物。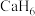 属于立方晶系,晶胞结构及原子投影位置如图所示:
属于立方晶系,晶胞结构及原子投影位置如图所示: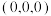 ;b处H为
;b处H为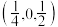 。则Ca的配位数为
。则Ca的配位数为_______ ,H原子之间最短距离为_______ pm(列出计算式),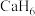 单位体积含氢质量的计算式为
单位体积含氢质量的计算式为_______  (阿伏加德罗常数的值为
(阿伏加德罗常数的值为 )。
)。
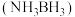 为氢源合成了多种具有高温超导性的富氢化物如
为氢源合成了多种具有高温超导性的富氢化物如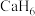 、
、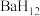 、
、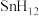 。回答下列问题:
。回答下列问题:(1)氨硼烷中,元素的电负性:B
(2)基态Sn原子的价电子排布图为
 的熔点(963℃)远高于
的熔点(963℃)远高于 (
(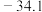 ℃),原因是
℃),原因是(3)乙硼烷与氨硼烷组成相似,但分子结构不同,其成键情况如图所示,每个B原子均以
 杂化轨道成键,水平面上下是两个3中心2电子“氢桥键”。
杂化轨道成键,水平面上下是两个3中心2电子“氢桥键”。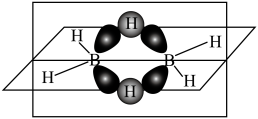
a.N-B键为配位键,可自由旋转
b.氢桥键为非极性键,不能自由旋转
c.乙硼烷分子中既有
 键,又有
键,又有 键
键 d.氨硼烷为极性分子,熔点比乙硼烷高
②乙硼烷水解释放
 ,生成
,生成 。
。 具有层状结构,与
具有层状结构,与 溶液反应生成
溶液反应生成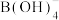 。
。 和
和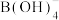 中B的轨道杂化类型分别为
中B的轨道杂化类型分别为(4)
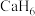 是第一个理论预测具有独特的“氢笼”结构的富氢化物。
是第一个理论预测具有独特的“氢笼”结构的富氢化物。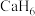 属于立方晶系,晶胞结构及原子投影位置如图所示:
属于立方晶系,晶胞结构及原子投影位置如图所示: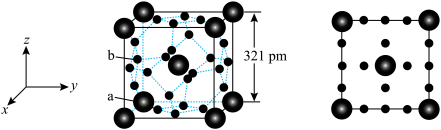
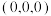 ;b处H为
;b处H为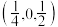 。则Ca的配位数为
。则Ca的配位数为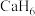 单位体积含氢质量的计算式为
单位体积含氢质量的计算式为 (阿伏加德罗常数的值为
(阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
9 . 下列有关甲醛(HCHO)分子的说法正确的是
| A.其中C原子采取sp即杂化 |
| B.是三角锥形 |
| C.其中H-C-O键的键角大于H-C-H键的键角 |
| D.是手性分子 |
您最近一年使用:0次
10 . 1828年,德国化学家弗里德里希 维勒首次使用无机物质氰酸铵与硫酸铵人工合成了尿素,揭开了人工合成有机物的序幕。尿素在农业生产中扮演者重要的角色,其结构如图所示。下列有关说法错误的是
维勒首次使用无机物质氰酸铵与硫酸铵人工合成了尿素,揭开了人工合成有机物的序幕。尿素在农业生产中扮演者重要的角色,其结构如图所示。下列有关说法错误的是
 维勒首次使用无机物质氰酸铵与硫酸铵人工合成了尿素,揭开了人工合成有机物的序幕。尿素在农业生产中扮演者重要的角色,其结构如图所示。下列有关说法错误的是
维勒首次使用无机物质氰酸铵与硫酸铵人工合成了尿素,揭开了人工合成有机物的序幕。尿素在农业生产中扮演者重要的角色,其结构如图所示。下列有关说法错误的是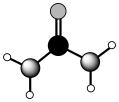
A.结构中元素第一电离能由大到小: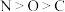 |
| B.分子中N原子与C原子的杂化不同 |
| C.该物质在水中溶解度较大 |
| D.基态碳原子核外有6种不同空间运动状态的电子 |
您最近一年使用:0次



