1 . 钒、钨、锌在工业上用途广泛。
(1)基态钒(V)元素在周期表中的位置为_______ ,其最高化合价为_______ ,与其同周期且未成对电子数相同的元素符号为_______ ;
(2)钒能形成多种配合物。钒的两种配合物X、Y化学式均为V(NH3)3ClSO4,取X、Y的溶液进行如下实验(已知配体难电离出来),所用试剂及所得现象如表所示:
则X的配离子为_______ ,Y的配体为_______ 。
(3)NaxWO3是一类色彩丰富的非整比化合物,其晶体结构如图2所示,若Na+无空缺,化学式为NaWO3,完全空缺则为WO3,每填入1个Na+,相应有1个W6+还原为W5+。NaxWO3的颜色与x值的对应关系如图1所示,已知NaxWO3晶体中n(W6+):n(W5+)=2:3,则其颜色为_______ 色。

(4)如图3是金属钨晶体中的一个晶胞的结构模型(原子间实际是相互接触的)。其中心的原子位于立方体的体心。实验测得金属钨的半径为rcm,假定金属钨为等直径的刚性球,请回答以下各题:

①每一个晶胞中分摊到_______ 个钨原子。
②计算晶胞的空间利用率_______ (写出表达式,不计算具体数值)。
(1)基态钒(V)元素在周期表中的位置为
(2)钒能形成多种配合物。钒的两种配合物X、Y化学式均为V(NH3)3ClSO4,取X、Y的溶液进行如下实验(已知配体难电离出来),所用试剂及所得现象如表所示:
| 原溶液 | X溶液 | X溶液 | Y溶液 | Y溶液 |
| 所加试剂 | BaCl2溶液 | AgNO3溶液 | BaCl2溶液 | AgNO3溶液 |
| 现象 | 白色沉淀 | 无明显变化 | 无明显变化 | 白色沉淀 |
则X的配离子为
(3)NaxWO3是一类色彩丰富的非整比化合物,其晶体结构如图2所示,若Na+无空缺,化学式为NaWO3,完全空缺则为WO3,每填入1个Na+,相应有1个W6+还原为W5+。NaxWO3的颜色与x值的对应关系如图1所示,已知NaxWO3晶体中n(W6+):n(W5+)=2:3,则其颜色为

(4)如图3是金属钨晶体中的一个晶胞的结构模型(原子间实际是相互接触的)。其中心的原子位于立方体的体心。实验测得金属钨的半径为rcm,假定金属钨为等直径的刚性球,请回答以下各题:

①每一个晶胞中分摊到
②计算晶胞的空间利用率
您最近一年使用:0次
2 . 盐酸氯丙嗪是一种多巴胺受体的阻断剂,临床有多种用途。化合物 是盐酸氯丙嗪制备的原料,可由化合物
是盐酸氯丙嗪制备的原料,可由化合物 和
和 在铜作催化剂条件下反应制得。
在铜作催化剂条件下反应制得。___________ 。
(2)1mol化合物 分子中含有σ键数目为
分子中含有σ键数目为___________ 。
(3)化合物 分子中sp3方式杂化的原子数目是
分子中sp3方式杂化的原子数目是___________ 。
(4)已知[Cu(NH3)4]SO4中[Cu(NH3)4]2+具有对称的空间构型,且当两个NH3被两个Cl-取代时,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为___________ (填序号)。
a.平面正方形 b.正四面体 c.三角锥型 d.V型
(5)已知在[Cu(NH3)4]SO4中溶液中加入少量NiSO4,会立即转化为[Ni(NH3)6]SO4中,由此可知Ni2+与NH3之间形成的化学键键能___________ (填“大于”或“小于”)Cu2+与NH3之间形成的化学键键能。[Cu(NH3)4]2+中存在的化学键类型有___________ 。
 是盐酸氯丙嗪制备的原料,可由化合物
是盐酸氯丙嗪制备的原料,可由化合物 和
和 在铜作催化剂条件下反应制得。
在铜作催化剂条件下反应制得。 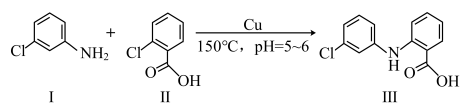
(2)1mol化合物
 分子中含有σ键数目为
分子中含有σ键数目为(3)化合物
 分子中sp3方式杂化的原子数目是
分子中sp3方式杂化的原子数目是(4)已知[Cu(NH3)4]SO4中[Cu(NH3)4]2+具有对称的空间构型,且当两个NH3被两个Cl-取代时,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为
a.平面正方形 b.正四面体 c.三角锥型 d.V型
(5)已知在[Cu(NH3)4]SO4中溶液中加入少量NiSO4,会立即转化为[Ni(NH3)6]SO4中,由此可知Ni2+与NH3之间形成的化学键键能
您最近一年使用:0次
名校
解题方法
3 . 铜是常见的、用途广泛的金属元素之一、
(1)基态Cu原子核外未成对电子所在的原子轨道是_______ 。
(2)一价铜离子某配合物的结构如图所示:_______ 。
②上述配合物中所含元素电负性由大到小的顺序为_______ (用元素符号表示)。
(3)常见的铜的氧化物有CuO和 两种。已知:CuO晶胞中
两种。已知:CuO晶胞中 的位置如图1所示;两种晶胞中
的位置如图1所示;两种晶胞中 和
和 的位置相同,其在晶胞侧视图中的位置相同(如图2),假设两种晶胞的参数相同,CuO晶体的密度是
的位置相同,其在晶胞侧视图中的位置相同(如图2),假设两种晶胞的参数相同,CuO晶体的密度是 。
。 、
、 、
、_______ 和_______ 。
② 晶体的密度是
晶体的密度是_______  (用含
(用含 的代数式表示)。
的代数式表示)。
(1)基态Cu原子核外未成对电子所在的原子轨道是
(2)一价铜离子某配合物的结构如图所示:

②上述配合物中所含元素电负性由大到小的顺序为
(3)常见的铜的氧化物有CuO和
 两种。已知:CuO晶胞中
两种。已知:CuO晶胞中 的位置如图1所示;两种晶胞中
的位置如图1所示;两种晶胞中 和
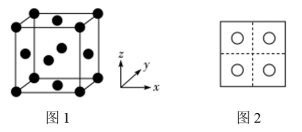
和 的位置相同,其在晶胞侧视图中的位置相同(如图2),假设两种晶胞的参数相同,CuO晶体的密度是
的位置相同,其在晶胞侧视图中的位置相同(如图2),假设两种晶胞的参数相同,CuO晶体的密度是 。
。
 、
、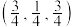 、
、②
 晶体的密度是
晶体的密度是 (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
4 . 硫酸四氨合铜晶体( )常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。实验室制备
)常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。实验室制备 的流程如下:
的流程如下:
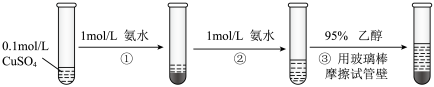
请回答:
(1)写出过程②发生反应的离子方程式_______ 。
(2)过程③加入95%乙醇的作用是_______ 。
(3)根据①→②→③的现象,给出相应微粒与 结合由弱到强的排序
结合由弱到强的排序_______ 。
(4) 具有对称的空间构型,若其中两个
具有对称的空间构型,若其中两个 被两个
被两个 取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则 的空间构型为
的空间构型为_______ 。
(5)下列说法正确的是_______。
 )常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。实验室制备
)常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。实验室制备 的流程如下:
的流程如下:
请回答:
(1)写出过程②发生反应的离子方程式
(2)过程③加入95%乙醇的作用是
(3)根据①→②→③的现象,给出相应微粒与
 结合由弱到强的排序
结合由弱到强的排序(4)
 具有对称的空间构型,若其中两个
具有对称的空间构型,若其中两个 被两个
被两个 取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则 的空间构型为
的空间构型为(5)下列说法正确的是_______。
A.③中发生反应的离子方程式为: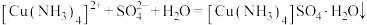 |
| B.③中用玻璃棒摩擦器壁可以促进晶体析出 |
C. 晶体中存在共价键、配位键、离子键和氢键 晶体中存在共价键、配位键、离子键和氢键 |
D.硫酸四氨合铜晶体在水中的电离方程式为: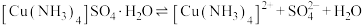 |
您最近一年使用:0次
解题方法
5 . 铜是常见的、用途广泛的金属元素之一。
(1)基态Cu原子核外未成对电子所在的原子轨道是_______ 。
(2)一价铜离子配合物的结构如图所示:
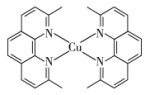
①上述配合物中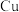 (Ⅰ)的配位数是
(Ⅰ)的配位数是_______ 。
②上述配合物分子中碳原子的杂化方式为_______ 。
③上述配合物中所含元素电负性由大到小的顺序为_______ (用元素符号表示)。
(3)常见的铜的氧化物有CuO和 两种。已知:CuO晶胞中
两种。已知:CuO晶胞中 的位置如图1所示;两种晶胞中
的位置如图1所示;两种晶胞中 和
和 的位置相同,其在晶胞侧视图中的位置相同(如图2)。假设两种晶胞的参数相同,CuO晶体的密度是
的位置相同,其在晶胞侧视图中的位置相同(如图2)。假设两种晶胞的参数相同,CuO晶体的密度是 。
。
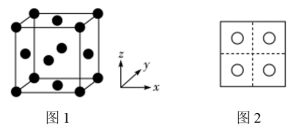
①CuO晶胞中,铜离子的坐标参数是 、
、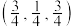 、
、_______ 和_______ 。
② 晶体的密度是
晶体的密度是_______  (用含
(用含 的代数式表示)。
的代数式表示)。
(1)基态Cu原子核外未成对电子所在的原子轨道是
(2)一价铜离子配合物的结构如图所示:

①上述配合物中
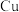 (Ⅰ)的配位数是
(Ⅰ)的配位数是②上述配合物分子中碳原子的杂化方式为
③上述配合物中所含元素电负性由大到小的顺序为
(3)常见的铜的氧化物有CuO和
 两种。已知:CuO晶胞中
两种。已知:CuO晶胞中 的位置如图1所示;两种晶胞中
的位置如图1所示;两种晶胞中 和
和 的位置相同,其在晶胞侧视图中的位置相同(如图2)。假设两种晶胞的参数相同,CuO晶体的密度是
的位置相同,其在晶胞侧视图中的位置相同(如图2)。假设两种晶胞的参数相同,CuO晶体的密度是 。
。
①CuO晶胞中,铜离子的坐标参数是
 、
、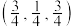 、
、②
 晶体的密度是
晶体的密度是 (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2024-03-18更新
|
102次组卷
|
2卷引用:湖南省岳阳市湘阴县知源高级中学等多校2023-2024学年高三上学期11月月考化学试题
名校
6 . 硫酸四氨合铜晶体{[Cu(NH3)4]SO4∙H2O}在工业上用途广泛,常温下该物质在空气中不稳定,受热时易发生分解。现以铜粉、3mol/L的硫酸、浓氨水、10%NaOH溶液、95%的乙醇溶液、0.500mol/L稀盐酸、0.500mol/L的NaOH溶液来合成硫酸四氨合铜晶体并测定其纯度。(已知:CuSO4在水中的溶解度随温度的升高而增大。)
I.CuSO4溶液的制备
①称取4g铜粉,在A仪器中灼烧10分钟并不断搅拌,放置冷却。
②在蒸发皿中加入30mL 3mol/L的硫酸,将A中固体慢慢放入其中,加热并不断搅拌。
③趁热过滤得蓝色溶液。
(1)A仪器的名称为___________ 。
(2)第③步中,趁热过滤的目的是___________ 。
Ⅱ.晶体的制备
将上述制备的CuSO4溶液按如图所示进行操作___________ 。
(4)析出晶体时采用加入乙醇的方法,请结合物质结构与性质知识解释乙醇的作用:___________ ,此处不采用浓缩结晶的原因是___________ 。
Ⅲ.氨含量的测定
精确称取w g晶体,加适量水溶解,注入如图所示的三颈烧瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,并用蒸馏水冲洗导管内壁,用V1 mL 0.5mol/L的盐酸标准溶液完全吸收。取下接收瓶,用0.5mol/L NaOH标准溶液滴定过剩的HCl,到终点时消耗V2 mL NaOH溶液。___________ 。
(6)为了减少误差,用NaOH标准溶液滴定过剩的HCl溶液时最好使用___________ (填“酚酞”或“甲基橙”)作指示剂。
(7)样品中氨的质量分数的表达式为___________ (用含w、V1、V2的代数式表式)。
(8)下列实验操作可能使氨含量的测定结果偏高的是___________(填标号)。
I.CuSO4溶液的制备
①称取4g铜粉,在A仪器中灼烧10分钟并不断搅拌,放置冷却。
②在蒸发皿中加入30mL 3mol/L的硫酸,将A中固体慢慢放入其中,加热并不断搅拌。
③趁热过滤得蓝色溶液。
(1)A仪器的名称为
(2)第③步中,趁热过滤的目的是
Ⅱ.晶体的制备
将上述制备的CuSO4溶液按如图所示进行操作

(4)析出晶体时采用加入乙醇的方法,请结合物质结构与性质知识解释乙醇的作用:
Ⅲ.氨含量的测定
精确称取w g晶体,加适量水溶解,注入如图所示的三颈烧瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,并用蒸馏水冲洗导管内壁,用V1 mL 0.5mol/L的盐酸标准溶液完全吸收。取下接收瓶,用0.5mol/L NaOH标准溶液滴定过剩的HCl,到终点时消耗V2 mL NaOH溶液。

(6)为了减少误差,用NaOH标准溶液滴定过剩的HCl溶液时最好使用
(7)样品中氨的质量分数的表达式为
(8)下列实验操作可能使氨含量的测定结果偏高的是___________(填标号)。
| A.滴定时未用NaOH标准溶液润洗滴定管 |
| B.读数时,滴定前平视,滴定后俯视 |
| C.将样品液中的氨全部蒸出后,未用蒸馏水冲洗导管内壁 |
| D.取下接收瓶前,未用蒸馏水冲洗插入接收瓶中的导管外壁 |
您最近一年使用:0次
解题方法
7 . 硫酸四氨合铜晶体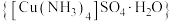 常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。实验室制备
常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。实验室制备 的流程如图。
的流程如图。 的空间结构为平面四边形。下列说法正确的是
的空间结构为平面四边形。下列说法正确的是
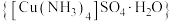 常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。实验室制备
常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。实验室制备 的流程如图。
的流程如图。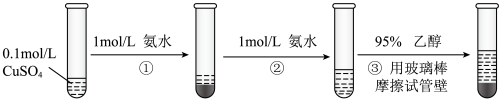
 的空间结构为平面四边形。下列说法正确的是
的空间结构为平面四边形。下列说法正确的是A. 晶体中存在的化学键有共价键、配位键、离子键和氢键 晶体中存在的化学键有共价键、配位键、离子键和氢键 |
| B.过程③加入95%乙醇的作用是增大溶剂极性,减小硫酸四氨合铜的溶解度 |
C.根据上述实验现象可知,与 结合能力由弱到强的顺序为 结合能力由弱到强的顺序为 |
D.若 中两个 中两个 被两个 被两个 取代,只有一种结构 取代,只有一种结构 |
您最近一年使用:0次
2024-05-14更新
|
186次组卷
|
3卷引用:河南省新乡市2024届高三第三次模拟考试理综-化学试题
8 . 配合物在许多方面有着广泛的用途,目前我国科学家利用配合物在能源转化与储存方面有着杰出的贡献,请根据题意回答下列问题:
(1)将 1 mol TiCl3·4H2O 溶于水,加入足量 AgNO3 溶液,得到 1 mol AgCl 沉淀,已知Ti3+的配位数为6,TiCl3·4H2O的化学式用配合物的形式表示为___ 。
(2)有下列实验:___ 。深蓝色晶体的化学式为___ 。
②写出蓝色沉淀溶解成深蓝色溶液的离子方程式___ 。
③[Cu(NH3)4]2+中H−N−H键角比NH3分子中H−N−H键角___ (填“大”或“小”)。[Cu(NH3)4]SO4中存在的化学键类型有___ (填标号)。
A.离子键 B.共价键 C.氢键 D.配位键
④物质在外磁场的作用下会发生磁化现象,在磁场中物质的磁性可分为顺磁性、反磁性和铁磁性,中心离子或原子上含有未成对电子的物质具有顺磁性,下列配离子中具有顺磁性的是___ (填标号)。
A.[Cr(OH)4] − B.[Cu(CN)4]3− C.[ZnCl4]2− D.[Fe(CN)6]4−
画出[Cu(CN)4]2−的结构:___ (用“→”或“—”将配位键表示出来)。
(1)将 1 mol TiCl3·4H2O 溶于水,加入足量 AgNO3 溶液,得到 1 mol AgCl 沉淀,已知Ti3+的配位数为6,TiCl3·4H2O的化学式用配合物的形式表示为
(2)有下列实验:

②写出蓝色沉淀溶解成深蓝色溶液的离子方程式
③[Cu(NH3)4]2+中H−N−H键角比NH3分子中H−N−H键角
A.离子键 B.共价键 C.氢键 D.配位键
④物质在外磁场的作用下会发生磁化现象,在磁场中物质的磁性可分为顺磁性、反磁性和铁磁性,中心离子或原子上含有未成对电子的物质具有顺磁性,下列配离子中具有顺磁性的是
A.[Cr(OH)4] − B.[Cu(CN)4]3− C.[ZnCl4]2− D.[Fe(CN)6]4−
画出[Cu(CN)4]2−的结构:
您最近一年使用:0次
名校
解题方法
9 . 金属锰的用途非常广泛,涉及人类生产生活的方方面面,用含锰废料(主要成分为MnO2,含有少量Al2O3、Fe2O3、MgO、SiO2等)制备锰的流程如下:
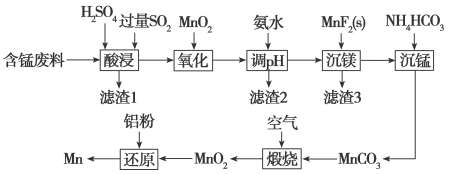
已知:Ⅰ.25 ℃时几种难溶物的溶度积常数见下表:
Ⅱ.当溶液中某离子浓度≤10-5mol·L-1时,认为该离子沉淀完全。
回答下列问题:
(1)基态Mn原子的核外电子排布式为___________ ,Mn2+能形成配离子为八面体的配合物MnCl2·nNH3,在该配合物的配离子中,Mn2+位于八面体的中心。若含1 mol该配合物的溶液与足量AgNO3溶液作用可生成1 mol AgCl沉淀,则该配离子化学式为___________ 。比较Fe和Mn的第三电离能,I3(Fe)___________ I3(Mn)(填“大于”或“小于”),原因是___________
(2)“滤渣1”的主要成分为___________ (填化学式)。
(3)写出“酸浸”过程中Fe2O3和SO2反应的化学方程式___________ 。
(4)“氧化”过程中,被MnO2氧化的物质有___________ (写化学式)。
(5)若“调pH”后所得溶液中c(Mn2+)=0.2 mol·L-1,则调pH的范围是4.7≤pH<___________ (保留两位有效数字)。
(6)分别写出“沉镁”和“沉锰”的离子方程式___________ ,___________ 。
(7)生成的MnCO3沉淀需经充分洗涤,检验沉淀是否洗净的方法是___________ 。

已知:Ⅰ.25 ℃时几种难溶物的溶度积常数见下表:
| 难溶物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 | Mn(OH)2 | MnF2 | MgF2 |
| 溶度积(Ksp) | 2.8×10-39 | 1×10-33 | 5.6×10-12 | 2.0×10-13 | 5.3×10-3 | 5.2×10-11 |
回答下列问题:
(1)基态Mn原子的核外电子排布式为
(2)“滤渣1”的主要成分为
(3)写出“酸浸”过程中Fe2O3和SO2反应的化学方程式
(4)“氧化”过程中,被MnO2氧化的物质有
(5)若“调pH”后所得溶液中c(Mn2+)=0.2 mol·L-1,则调pH的范围是4.7≤pH<
(6)分别写出“沉镁”和“沉锰”的离子方程式
(7)生成的MnCO3沉淀需经充分洗涤,检验沉淀是否洗净的方法是
您最近一年使用:0次
10 . 近年来,人们发现 不仅在颜料、防腐工业等方面具有广泛的用途,而且
不仅在颜料、防腐工业等方面具有广泛的用途,而且 的大单晶体是一种很重要的电光调制晶体,也是有机合成中性能优良的催化剂。研究发现一种利用低品位铜矿(含
的大单晶体是一种很重要的电光调制晶体,也是有机合成中性能优良的催化剂。研究发现一种利用低品位铜矿(含 、
、 和
和 等)为原料制取
等)为原料制取 的工艺流程如下:
的工艺流程如下:
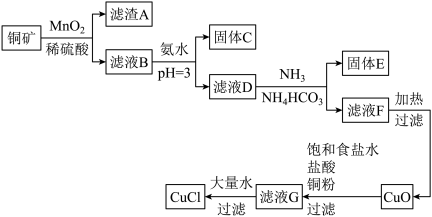
已知:i.水溶液中不存在碳酸铜,碳酸铜遇水立即水解为碱式碳酸铜和氢氧化铜。
ii.室温时, 的溶度积常数
的溶度积常数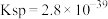 。
。
(1)铜矿中未被 氧化的物质有
氧化的物质有___________ 。
(2)滤液D中铁离子的浓度约为___________ 。
(3)向滤液D中先通氨气的目的是___________。
(4)固体E主要是 ,生成
,生成 的离子方程式是
的离子方程式是___________ 。
(5)滤液F加热生成 、
、 和
和 ,反应的化学方程式是
,反应的化学方程式是___________ 。
(6)若要制取99.5g ,理论上至少需要质量分数为25%的
,理论上至少需要质量分数为25%的 的铜矿粉的质量为
的铜矿粉的质量为___________ g。
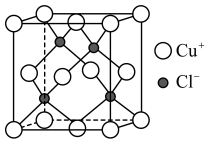
(7)查阅资料: 立方晶胞结构如下图所示,其晶胞参数为apm,
立方晶胞结构如下图所示,其晶胞参数为apm, 以配位键与
以配位键与 相结合,其中
相结合,其中 的配位数为
的配位数为___________ , 晶体密度为
晶体密度为___________  。
。
 不仅在颜料、防腐工业等方面具有广泛的用途,而且
不仅在颜料、防腐工业等方面具有广泛的用途,而且 的大单晶体是一种很重要的电光调制晶体,也是有机合成中性能优良的催化剂。研究发现一种利用低品位铜矿(含
的大单晶体是一种很重要的电光调制晶体,也是有机合成中性能优良的催化剂。研究发现一种利用低品位铜矿(含 、
、 和
和 等)为原料制取
等)为原料制取 的工艺流程如下:
的工艺流程如下:
已知:i.水溶液中不存在碳酸铜,碳酸铜遇水立即水解为碱式碳酸铜和氢氧化铜。
ii.室温时,
 的溶度积常数
的溶度积常数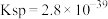 。
。(1)铜矿中未被
 氧化的物质有
氧化的物质有(2)滤液D中铁离子的浓度约为
(3)向滤液D中先通氨气的目的是___________。
A.中和溶液中的 | B.调节溶液 值,生成 值,生成 沉淀 沉淀 |
C.有利于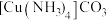 的生成 的生成 | D.增加 的溶解度 的溶解度 |
(4)固体E主要是
 ,生成
,生成 的离子方程式是
的离子方程式是(5)滤液F加热生成
 、
、 和
和 ,反应的化学方程式是
,反应的化学方程式是(6)若要制取99.5g
 ,理论上至少需要质量分数为25%的
,理论上至少需要质量分数为25%的 的铜矿粉的质量为
的铜矿粉的质量为(7)查阅资料:
 立方晶胞结构如下图所示,其晶胞参数为apm,
立方晶胞结构如下图所示,其晶胞参数为apm, 以配位键与
以配位键与 相结合,其中
相结合,其中 的配位数为
的配位数为 晶体密度为
晶体密度为 。
。
您最近一年使用:0次



