名校
解题方法
1 . 下列叙述中正确的有句
①离子键没有方向性和饱和性,而共价键有方向性和饱和性
②配位键在形成时,是由成键双方各提供一个电子形成共用电子对
③金属键的实质是金属中的“自由电子”与金属阳离子形成的一种强烈的相互作用
④在冰晶体中,既有极性键、非极性键,又有氢键
⑤化合物NH4Cl和CuSO4·5H2O都存在配位键
⑥NaCl、HF、CH3CH2OH、SO2都易溶于水,但原因不完全相同
①离子键没有方向性和饱和性,而共价键有方向性和饱和性
②配位键在形成时,是由成键双方各提供一个电子形成共用电子对
③金属键的实质是金属中的“自由电子”与金属阳离子形成的一种强烈的相互作用
④在冰晶体中,既有极性键、非极性键,又有氢键
⑤化合物NH4Cl和CuSO4·5H2O都存在配位键
⑥NaCl、HF、CH3CH2OH、SO2都易溶于水,但原因不完全相同
| A.2句 | B.3句 | C.4句 | D.5句 |
您最近一年使用:0次
2024-05-02更新
|
115次组卷
|
2卷引用:河南省南阳市第一中学校2023-2024学年高二下学期第一次月考化学试题
名校
2 . 已知 、
、 分别在850℃、300℃能大量分解,对此事实解释合理的是
分别在850℃、300℃能大量分解,对此事实解释合理的是
 、
、 分别在850℃、300℃能大量分解,对此事实解释合理的是
分别在850℃、300℃能大量分解,对此事实解释合理的是A. 能形成氢键而 能形成氢键而 不能 不能 | B.As—H键的键能小于N—H键的键能 |
C. 是极性分子而 是极性分子而 是非极性分子 是非极性分子 | D. 极易溶于水而 极易溶于水而 不能 不能 |
您最近一年使用:0次
解题方法
3 . 回答下列问题:
(1)在下列表格中填写各物质的中心原子杂化轨道类型和空间构型:
(2)一定压强下,将HF和HCl混合气体降温时,首先液化的物质是__________ 。
(1)在下列表格中填写各物质的中心原子杂化轨道类型和空间构型:
|
|
|
|
| |
杂化方式 | |||||
空间构型 |
您最近一年使用:0次
2024-04-08更新
|
68次组卷
|
2卷引用:河南省南阳市六校联考2023-2024学年高二下学期3月月考化学试卷
4 . 下列有关物质熔沸点的叙述错误的是
A.因为碳氢键键能小于碳氧键,所以 熔点低于 熔点低于 |
B. 的沸点高于 的沸点高于 |
C.F、Cl、O三种元素的简单氢化物沸点由高到低的顺序为 |
D.对羟基苯甲醛(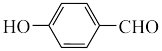 )的熔沸点高于邻羟基苯甲醛( )的熔沸点高于邻羟基苯甲醛(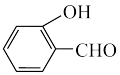 ) ) |
您最近一年使用:0次
2024-04-08更新
|
80次组卷
|
2卷引用:河南省南阳市六校联考2023-2024学年高二下学期3月月考化学试卷
名校
解题方法
5 . 下列对有关事实的解释不正确的是
| 选项 | 事实 | 解释 |
| A | 水的沸点比硫化氢的沸点高 | 水分子间形成氢键 |
| B | 在CS2中的溶解度:CCl4>H2O | CS2、CCl4为非极性分子,而H2O为极性分子 |
| C | 用质谱仪检测乙酸时,谱图出现了质荷比为120的峰 | 两个乙酸分子通过范德华力形成了二聚体 |
| D | 稳定性:[Cu(H2O)4]2+<[Cu(NH3)4]2+ | N的电负性小于O的电负性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-19更新
|
310次组卷
|
3卷引用:河南省南阳市华龙高中2023-2024学年高二下学期3月月考化学试题
名校
解题方法
6 . 回答下列问题
(1)钛在元素周期表中的位置___________ ,基态钛原子的价层电子轨道表示式为___________ ,与Ti同周期的所有过渡元素的基态原子中,最外层电子数与钛不同的元素有___________ 种。下列状态的钛元素形成得微粒中,电离其最外层的一个电子所需能量最小的是___________ (填序号)。
A.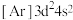 B.
B.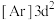 C.
C.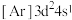 D.
D.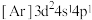
(2)第三周期元素中第一电离能介于Al和P的元素有___________ 种。与Co同周期,基态原子有1个未成对电子的元素有___________ 种。
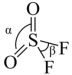
(3) 分子结构如图所示,已知键角
分子结构如图所示,已知键角 为124°,
为124°, 为96°,则
为96°,则 的原因主要是
的原因主要是___________ 。
(4) 、
、 、
、 沸点由高到低的顺序为
沸点由高到低的顺序为___________ ,其主要原因是___________ 。
(5)铜离子的一种配合物化学式为 ,该配合物中铜离子的配位数为
,该配合物中铜离子的配位数为___________ 。
(6)醋酸 中C原子的杂化类型为
中C原子的杂化类型为___________ 。
(7)等物质的量的 和
和 中,σ键数目之比
中,σ键数目之比___________ 。
(1)钛在元素周期表中的位置
A.
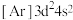 B.
B.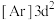 C.
C.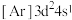 D.
D.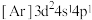
(2)第三周期元素中第一电离能介于Al和P的元素有
(3)
 分子结构如图所示,已知键角
分子结构如图所示,已知键角 为124°,
为124°, 为96°,则
为96°,则 的原因主要是
的原因主要是
(4)
 、
、 、
、 沸点由高到低的顺序为
沸点由高到低的顺序为(5)铜离子的一种配合物化学式为
 ,该配合物中铜离子的配位数为
,该配合物中铜离子的配位数为(6)醋酸
 中C原子的杂化类型为
中C原子的杂化类型为(7)等物质的量的
 和
和 中,σ键数目之比
中,σ键数目之比
您最近一年使用:0次
解题方法
7 . 化合物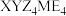 可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为
可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为 ,X与M同周期,E元素原子最外层电子数是次外层的3倍。下列说法正确的是
,X与M同周期,E元素原子最外层电子数是次外层的3倍。下列说法正确的是
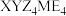 可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为
可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为 ,X与M同周期,E元素原子最外层电子数是次外层的3倍。下列说法正确的是
,X与M同周期,E元素原子最外层电子数是次外层的3倍。下列说法正确的是A.元素电负性: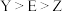 |
B.最简单氢化物沸点: |
C.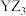 和 和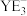 的空间结构均为三角锥形 的空间结构均为三角锥形 |
D.第一电离能: |
您最近一年使用:0次
名校
解题方法
8 . 分铜液净化渣主要含铜、碲(Te)、锑(Sb)、砷(As)等元素的化合物,一种回收工艺流程如图所示:

已知:①“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有Na2TeO3、Na3AsO4
②“酸浸”时,锑元素反应生成难溶的Sb2O(SO4)4浸渣。
回答下列问题:
(1)基态As的价层电子排布式为_______ 。
(2)“碱浸”时,TeO2与NaOH反应的离子方程式为_______ 。
(3)向碱浸液加入盐酸调节pH=4,有TeO2析出,分离出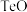 2的操作是
2的操作是_______ 。滤液中As元素最主要的存在形式为_______ (常温下,H3AsO4的各级电离常数为:K 。
。
A.H3AsO4 B.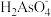 C.
C.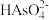 D.
D.
(4)①Sb2O(SO4)4中,Sb的化合价为_______ 。
②“氯盐酸浸”时,通入SO2的目的是_______ 。
(5)“水解”时,生成SbOCl的化学方程式为_______ 。
(6)碲(Te)所在的主族中,简单气态氢化物沸点最低的是_______ (填化学式);该族元素硒的某种氧化物为链状聚合结构(如图所示),该氧化物的化学式为_______ 。

(7)设 中H-N-H键角大小分别为a、b、c,则a、b、c的由大到小的关系为
中H-N-H键角大小分别为a、b、c,则a、b、c的由大到小的关系为_______ 。

已知:①“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有Na2TeO3、Na3AsO4

②“酸浸”时,锑元素反应生成难溶的Sb2O(SO4)4浸渣。
回答下列问题:
(1)基态As的价层电子排布式为
(2)“碱浸”时,TeO2与NaOH反应的离子方程式为
(3)向碱浸液加入盐酸调节pH=4,有TeO2析出,分离出
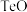 2的操作是
2的操作是 。
。A.H3AsO4 B.
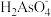 C.
C.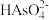 D.
D.
(4)①Sb2O(SO4)4中,Sb的化合价为
②“氯盐酸浸”时,通入SO2的目的是
(5)“水解”时,生成SbOCl的化学方程式为
(6)碲(Te)所在的主族中,简单气态氢化物沸点最低的是

(7)设
 中H-N-H键角大小分别为a、b、c,则a、b、c的由大到小的关系为
中H-N-H键角大小分别为a、b、c,则a、b、c的由大到小的关系为
您最近一年使用:0次
9 . 下列说法中正确的是
①原子光谱的特征谱线用于鉴定元素,从 2
2 s2
s2 1跃迁至
1跃迁至 2
2 s2
s2 4时释放能量
4时释放能量
②Cl2分子中,Cl-Cl键是p-pσ键
③铍原子最外层原子轨道的电子云图:
④ ,该电子排布图违背了泡利原理
,该电子排布图违背了泡利原理
⑤键能N-N>P-P、N-H>P-H,因此N2H4的沸点大于P2H4的沸点
⑥碘易溶于浓碘化钾溶液,甲烷难溶于水都可用“相似相溶”原理解释
⑦氟的电负性大于氯的电负性,导致三氟乙酸的酸性大于三氯乙酸的酸性
⑧三氧化硫有单分子气体和三聚分子固体(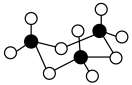 )两种存在形式,两种形式中S原子的杂化轨道类型不同
)两种存在形式,两种形式中S原子的杂化轨道类型不同
①原子光谱的特征谱线用于鉴定元素,从
 2
2 s2
s2 1跃迁至
1跃迁至 2
2 s2
s2 4时释放能量
4时释放能量②Cl2分子中,Cl-Cl键是p-pσ键
③铍原子最外层原子轨道的电子云图:

④
 ,该电子排布图违背了泡利原理
,该电子排布图违背了泡利原理⑤键能N-N>P-P、N-H>P-H,因此N2H4的沸点大于P2H4的沸点
⑥碘易溶于浓碘化钾溶液,甲烷难溶于水都可用“相似相溶”原理解释
⑦氟的电负性大于氯的电负性,导致三氟乙酸的酸性大于三氯乙酸的酸性
⑧三氧化硫有单分子气体和三聚分子固体(
 )两种存在形式,两种形式中S原子的杂化轨道类型不同
)两种存在形式,两种形式中S原子的杂化轨道类型不同| A.①②④⑦ | B.①②⑤⑦ | C.①②⑦⑧ | D.①④⑥⑦ |
您最近一年使用:0次
名校
10 . 下列说法不正确的是
| A.邻羟基苯甲酸的沸点低于对羟基苯甲酸的沸点 |
| B.棉花的葡萄糖结构单元中含有羟基,具有一定的吸湿性 |
| C.苯酚在浓氨水作用下与甲醛反应生成线型热塑性高分子化合物 |
D.18-冠-6(空腔直径260~320pm)能与 (276pm)通过某种相互作用力形成超分子 (276pm)通过某种相互作用力形成超分子 |
您最近一年使用:0次
2023-12-31更新
|
278次组卷
|
3卷引用:河南省南阳市新野县第一高级中学校2023-2024学年高三上学期12月月考化学试题
河南省南阳市新野县第一高级中学校2023-2024学年高三上学期12月月考化学试题浙江省北斗星盟2024届高三上学期12月联考-化学试题 (已下线)压轴题08 有机物的结构与性质(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)