1 . 钒、钨、锌在工业上用途广泛。
(1)基态钒(V)元素在周期表中的位置为_______ ,其最高化合价为_______ ,与其同周期且未成对电子数相同的元素符号为_______ ;
(2)钒能形成多种配合物。钒的两种配合物X、Y化学式均为V(NH3)3ClSO4,取X、Y的溶液进行如下实验(已知配体难电离出来),所用试剂及所得现象如表所示:
则X的配离子为_______ ,Y的配体为_______ 。
(3)NaxWO3是一类色彩丰富的非整比化合物,其晶体结构如图2所示,若Na+无空缺,化学式为NaWO3,完全空缺则为WO3,每填入1个Na+,相应有1个W6+还原为W5+。NaxWO3的颜色与x值的对应关系如图1所示,已知NaxWO3晶体中n(W6+):n(W5+)=2:3,则其颜色为_______ 色。

(4)如图3是金属钨晶体中的一个晶胞的结构模型(原子间实际是相互接触的)。其中心的原子位于立方体的体心。实验测得金属钨的半径为rcm,假定金属钨为等直径的刚性球,请回答以下各题:

①每一个晶胞中分摊到_______ 个钨原子。
②计算晶胞的空间利用率_______ (写出表达式,不计算具体数值)。
(1)基态钒(V)元素在周期表中的位置为
(2)钒能形成多种配合物。钒的两种配合物X、Y化学式均为V(NH3)3ClSO4,取X、Y的溶液进行如下实验(已知配体难电离出来),所用试剂及所得现象如表所示:
| 原溶液 | X溶液 | X溶液 | Y溶液 | Y溶液 |
| 所加试剂 | BaCl2溶液 | AgNO3溶液 | BaCl2溶液 | AgNO3溶液 |
| 现象 | 白色沉淀 | 无明显变化 | 无明显变化 | 白色沉淀 |
则X的配离子为
(3)NaxWO3是一类色彩丰富的非整比化合物,其晶体结构如图2所示,若Na+无空缺,化学式为NaWO3,完全空缺则为WO3,每填入1个Na+,相应有1个W6+还原为W5+。NaxWO3的颜色与x值的对应关系如图1所示,已知NaxWO3晶体中n(W6+):n(W5+)=2:3,则其颜色为

(4)如图3是金属钨晶体中的一个晶胞的结构模型(原子间实际是相互接触的)。其中心的原子位于立方体的体心。实验测得金属钨的半径为rcm,假定金属钨为等直径的刚性球,请回答以下各题:

①每一个晶胞中分摊到
②计算晶胞的空间利用率
您最近一年使用:0次
2 . I.次磷酸( )是一种精细化工产品。
)是一种精细化工产品。
(1) 溶液中的含磷微粒只有
溶液中的含磷微粒只有 和
和 ,则该溶液呈
,则该溶液呈_______ 性(填“酸”“碱”或“中”)。
(2)25℃时, 溶液和盐酸的物质的量浓度相同。加水稀释至相同的pH,此时加入
溶液和盐酸的物质的量浓度相同。加水稀释至相同的pH,此时加入 溶液中水的体积
溶液中水的体积_______ (填“大于”“小于”或“等于”)加入盐酸中水的体积。
II.
(3)硅元素可形成多种晶体。
①硅与氯、溴结合能形成 、
、 ,沸点较高的是
,沸点较高的是_______ 。
②晶体Si和晶体SiC结构相似,熔点较低的是_______ 。
(4)某化合物具有超导性,其晶胞结构如图所示,则该化合物的化学式为_______ ,1个Mg与_______ 个Ni等距离且最近。

III.为了达到碳中和,研发二氧化碳、烃类等物质的利用技术已成为科研热点。
(5)



则

_______ (用 、
、 表示)。
表示)。
(6)已知反应:
 。将1molCO和2mol
。将1molCO和2mol 充入1L恒容密闭容器中,在一定条件下合成甲醇,相同时间(2min)内测得CO的转化率与温度的对应关系如图所示:
充入1L恒容密闭容器中,在一定条件下合成甲醇,相同时间(2min)内测得CO的转化率与温度的对应关系如图所示:
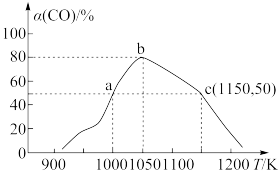
①试求温度为1000K条件下,反应开始至2min时,
_______ 。
②已知c点时容器内的压强为p,则在1150K温度下该反应的压强平衡常数 为
为_______ ( 是用各气体物质的分压替代浓度来计算的平衡常数)。
是用各气体物质的分压替代浓度来计算的平衡常数)。
 )是一种精细化工产品。
)是一种精细化工产品。(1)
 溶液中的含磷微粒只有
溶液中的含磷微粒只有 和
和 ,则该溶液呈
,则该溶液呈(2)25℃时,
 溶液和盐酸的物质的量浓度相同。加水稀释至相同的pH,此时加入
溶液和盐酸的物质的量浓度相同。加水稀释至相同的pH,此时加入 溶液中水的体积
溶液中水的体积II.
(3)硅元素可形成多种晶体。
①硅与氯、溴结合能形成
 、
、 ,沸点较高的是
,沸点较高的是②晶体Si和晶体SiC结构相似,熔点较低的是
(4)某化合物具有超导性,其晶胞结构如图所示,则该化合物的化学式为

III.为了达到碳中和,研发二氧化碳、烃类等物质的利用技术已成为科研热点。
(5)




则


 、
、 表示)。
表示)。(6)已知反应:

 。将1molCO和2mol
。将1molCO和2mol 充入1L恒容密闭容器中,在一定条件下合成甲醇,相同时间(2min)内测得CO的转化率与温度的对应关系如图所示:
充入1L恒容密闭容器中,在一定条件下合成甲醇,相同时间(2min)内测得CO的转化率与温度的对应关系如图所示:
①试求温度为1000K条件下,反应开始至2min时,

②已知c点时容器内的压强为p,则在1150K温度下该反应的压强平衡常数
 为
为 是用各气体物质的分压替代浓度来计算的平衡常数)。
是用各气体物质的分压替代浓度来计算的平衡常数)。
您最近一年使用:0次
名校
解题方法
3 .  及其化合物在生产生活方面都有重要的用途.回答下列问题:
及其化合物在生产生活方面都有重要的用途.回答下列问题:
(1)基态铁原子的核外电子排布式为:______ , 比
比 更稳定的原因是:
更稳定的原因是:______ 。
(2) 中铁元素的配位数是
中铁元素的配位数是______ ,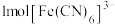 中含有的
中含有的 键的数目为
键的数目为______ , 中C原子的杂化方式为
中C原子的杂化方式为______ 。
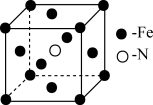
(3)铁和氨在 可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式:
可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式:______ 。
(4)血红素铁用作铁强化剂,其吸收率比一般铁剂高3倍,图中画出 与N原子间的化学键(若是配位键,需要用箭头加以表示)
与N原子间的化学键(若是配位键,需要用箭头加以表示)______ 。

 及其化合物在生产生活方面都有重要的用途.回答下列问题:
及其化合物在生产生活方面都有重要的用途.回答下列问题:(1)基态铁原子的核外电子排布式为:
 比
比 更稳定的原因是:
更稳定的原因是:(2)
 中铁元素的配位数是
中铁元素的配位数是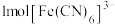 中含有的
中含有的 键的数目为
键的数目为 中C原子的杂化方式为
中C原子的杂化方式为(3)铁和氨在
 可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式:
可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式:
(4)血红素铁用作铁强化剂,其吸收率比一般铁剂高3倍,图中画出
 与N原子间的化学键(若是配位键,需要用箭头加以表示)
与N原子间的化学键(若是配位键,需要用箭头加以表示)
您最近一年使用:0次
4 . 某工业废渣的主要成分为NiO、CuO、 、ZnO,一种综合回收利用的工艺流程如图所示:
、ZnO,一种综合回收利用的工艺流程如图所示:

回答下列问题:
(1)写出浸渣主要成分的一种用途:_______ 。
(2)浸取液含有的配离子有 、
、 、
、 ,
, 的中心离子为
的中心离子为_______ ,配位数为_______ ; 能作配体的原因是
能作配体的原因是_______ 。
(3)“还原”得到Cu时发生反应的氧化剂和还原剂的物质的量之比为_______ ;该反应温度不宜过高,原因是_______ 。
(4)“沉锌镍”后得到的滤液中可循环利用的物质有_______ (填化学式)。
(5)“脱锌”时反应的化学方程式为_______ 。
(6)NiO为绿色固体,常用作搪瓷的着色剂,其晶胞结构如图所示:

①测定晶体结构最常用的方法是_______ (填选项字母)。
A.核磁共振氢谱 B.红外光谱 C.X射线衍射实验 D.称重法
②若晶胞中 之间的最短距离为a nm,阿伏加德罗常数的值为
之间的最短距离为a nm,阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为_______  (用含
(用含 、a的代数式表示)。
、a的代数式表示)。
 、ZnO,一种综合回收利用的工艺流程如图所示:
、ZnO,一种综合回收利用的工艺流程如图所示:
回答下列问题:
(1)写出浸渣主要成分的一种用途:
(2)浸取液含有的配离子有
 、
、 、
、 ,
, 的中心离子为
的中心离子为 能作配体的原因是
能作配体的原因是(3)“还原”得到Cu时发生反应的氧化剂和还原剂的物质的量之比为
(4)“沉锌镍”后得到的滤液中可循环利用的物质有
(5)“脱锌”时反应的化学方程式为
(6)NiO为绿色固体,常用作搪瓷的着色剂,其晶胞结构如图所示:

①测定晶体结构最常用的方法是
A.核磁共振氢谱 B.红外光谱 C.X射线衍射实验 D.称重法
②若晶胞中
 之间的最短距离为a nm,阿伏加德罗常数的值为
之间的最短距离为a nm,阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为 (用含
(用含 、a的代数式表示)。
、a的代数式表示)。
您最近一年使用:0次
解题方法
5 . 氧族元素包括氧、硫、硒等,这些元素的单质及其化合物在工农业生产和科学研究中具有广泛的用途。回答下列问题:
(1)下列属于氧原子激发态的轨道表示式的有___________ (填字母,下同),其中失去最外层上一个电子所需能量最低的是___________ 。
a. b.
b.
c.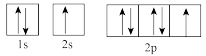 d.
d.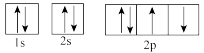
(2)科学研究表明,过硫化氢(也叫二硫化氢)加入烯烃中可制备硫醇,其熔沸点及制备方法如下表所示:
① 的结构为
的结构为 ,其中2个S原子的
,其中2个S原子的___________ 杂化轨道形成S—S___________ (填“ ”或“
”或“ ”)共价键。
”)共价键。
② 分子结构中H—O—O键角为
分子结构中H—O—O键角为 ,则
,则 分子结构中H—S—S键角
分子结构中H—S—S键角___________ (填“=”“>”或“<”) 。
。
③ 的熔沸点比
的熔沸点比 的熔沸点低的原因是
的熔沸点低的原因是___________ 。
(3)在能源逐渐匮乏的形势下,超导材料显得尤为重要。Li、Fe、Se三种元素组成的某新型超导材料的晶胞结构如图所示:
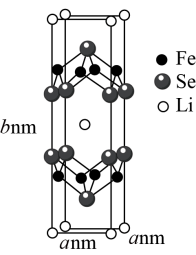
1个晶胞中的Se原子数为___________ 。晶胞的部分参数如图所示,且晶胞棱边夹角均为90°,晶体密度为 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为___________ (列式表示)。
(1)下列属于氧原子激发态的轨道表示式的有
a.
 b.
b.
c.
 d.
d.
(2)科学研究表明,过硫化氢(也叫二硫化氢)加入烯烃中可制备硫醇,其熔沸点及制备方法如下表所示:
| 物质 | 熔点/℃ | 沸点/℃ |  制备方法 制备方法 |
 | -90.0 | 71.0 | 加热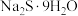 至熔融,再把硫溶入其中,得多硫化钠溶液。在263K下,将该溶液注入稀硫酸中,得多硫化氢混合物,分离、干燥、真空蒸馏,即得 至熔融,再把硫溶入其中,得多硫化钠溶液。在263K下,将该溶液注入稀硫酸中,得多硫化氢混合物,分离、干燥、真空蒸馏,即得 |
 | -0.4 | 150.0 |
 的结构为
的结构为 ,其中2个S原子的
,其中2个S原子的 ”或“
”或“ ”)共价键。
”)共价键。②
 分子结构中H—O—O键角为
分子结构中H—O—O键角为 ,则
,则 分子结构中H—S—S键角
分子结构中H—S—S键角 。
。③
 的熔沸点比
的熔沸点比 的熔沸点低的原因是
的熔沸点低的原因是(3)在能源逐渐匮乏的形势下,超导材料显得尤为重要。Li、Fe、Se三种元素组成的某新型超导材料的晶胞结构如图所示:

1个晶胞中的Se原子数为
 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为
您最近一年使用:0次
6 . 硼及其化合物在新材料、工农业生产等方面用途、广泛。
(1)写出基态B原子的轨道表达式___________ 。
(2)已知:硼酸的电离方程式可表示为H3BO3+H2O⇌[B(OH)4]-+H+。
①根据以上信息,下列说法正确的是_________ 。(填序号)
a.硼酸是一元酸
b.硼酸在电离的过程中,B原子的杂化类型发生了变化
c.硼酸与过量NaOH反应,能观察到白色沉淀逐渐消失
②从化学键的角度表述由H3BO3,形成[B(OH)4]-的过程__________ 。
(3)B与N可以形成不同类型的晶体,如六方氮化硼、立方氮化硼等,其结构如图。
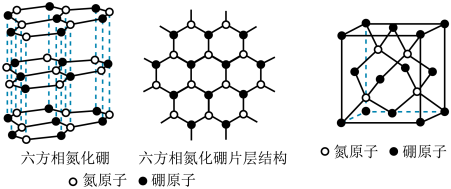
①六方氮化硼的晶体结构类似石墨,每一个B或N的杂化类型是__________ 。
②立方氮化硼因其硬度高、耐磨性好,在机械加工行业广泛用作切削工具。立方氮化硼可在高温高压的条件下由六方氮化硼转化而成。如图,立方氮化硼的晶体类型为___________ ,立方氮化硼的密度为dg⋅cm-3,阿伏加德罗常数为NA,B与N的相对原子质量分别为m和n,则立方晶胞边长a=______________ cm。

(1)写出基态B原子的轨道表达式
(2)已知:硼酸的电离方程式可表示为H3BO3+H2O⇌[B(OH)4]-+H+。
①根据以上信息,下列说法正确的是
a.硼酸是一元酸
b.硼酸在电离的过程中,B原子的杂化类型发生了变化
c.硼酸与过量NaOH反应,能观察到白色沉淀逐渐消失
②从化学键的角度表述由H3BO3,形成[B(OH)4]-的过程
(3)B与N可以形成不同类型的晶体,如六方氮化硼、立方氮化硼等,其结构如图。

①六方氮化硼的晶体结构类似石墨,每一个B或N的杂化类型是
②立方氮化硼因其硬度高、耐磨性好,在机械加工行业广泛用作切削工具。立方氮化硼可在高温高压的条件下由六方氮化硼转化而成。如图,立方氮化硼的晶体类型为
您最近一年使用:0次
名校
解题方法
7 . 硼元素从发现之初就有着重要用途,古埃及制造玻璃使用硼砂作溶剂,古代炼丹家也使用过硼砂。晶态硼的熔沸点高、硬度大。工业上可用碱法制备单质硼,制备流程如下:

(1)B在元素周期表中的位置是_______ 。 是有机化学中的常用试剂,其电子式为
是有机化学中的常用试剂,其电子式为_______ 。
(2)滤渣1是_______ (填化学式),通入 的目的是
的目的是_______ 。
(3)以 和Mg为原料制备硼单质,用化学反应方程式表示其制备过程:
和Mg为原料制备硼单质,用化学反应方程式表示其制备过程:_______ 。
(4) 是潜在的储氢材料,为白色晶体,稳定无毒。
是潜在的储氢材料,为白色晶体,稳定无毒。
① 在催化剂作用下与水反应释放氢气,另一产物的阴离子
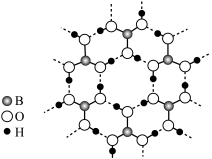
在催化剂作用下与水反应释放氢气,另一产物的阴离子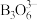 具有环状结构,写出
具有环状结构,写出 与水反应的化学方程式:
与水反应的化学方程式:_______ 。
②熔化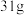
 可缓慢释放2g氢气,并转变为化合物A;A在高于500℃时释放氢气,转变为BN。A不稳定,容易形成聚合物,请写出聚合物的结构式:
可缓慢释放2g氢气,并转变为化合物A;A在高于500℃时释放氢气,转变为BN。A不稳定,容易形成聚合物,请写出聚合物的结构式:_______ 。
(5)氮化硼(BN)有多种晶形。它可以和碳一样形成与石墨相似的平面六边形的层状结构,如题图1,层中 共价键的键长比
共价键的键长比 单键的键长短,其原因是
单键的键长短,其原因是_______ 。

(6)已知立方氮化硼晶胞(图2)边长为apm,阿伏加德罗常数的值为 ,则晶体的密度为
,则晶体的密度为_______  。
。


(1)B在元素周期表中的位置是
 是有机化学中的常用试剂,其电子式为
是有机化学中的常用试剂,其电子式为(2)滤渣1是
 的目的是
的目的是(3)以
 和Mg为原料制备硼单质,用化学反应方程式表示其制备过程:
和Mg为原料制备硼单质,用化学反应方程式表示其制备过程:(4)
 是潜在的储氢材料,为白色晶体,稳定无毒。
是潜在的储氢材料,为白色晶体,稳定无毒。①
 在催化剂作用下与水反应释放氢气,另一产物的阴离子
在催化剂作用下与水反应释放氢气,另一产物的阴离子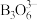 具有环状结构,写出
具有环状结构,写出 与水反应的化学方程式:
与水反应的化学方程式:②熔化
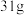
 可缓慢释放2g氢气,并转变为化合物A;A在高于500℃时释放氢气,转变为BN。A不稳定,容易形成聚合物,请写出聚合物的结构式:
可缓慢释放2g氢气,并转变为化合物A;A在高于500℃时释放氢气,转变为BN。A不稳定,容易形成聚合物,请写出聚合物的结构式:(5)氮化硼(BN)有多种晶形。它可以和碳一样形成与石墨相似的平面六边形的层状结构,如题图1,层中
 共价键的键长比
共价键的键长比 单键的键长短,其原因是
单键的键长短,其原因是
(6)已知立方氮化硼晶胞(图2)边长为apm,阿伏加德罗常数的值为
 ,则晶体的密度为
,则晶体的密度为 。
。
您最近一年使用:0次
2022-12-03更新
|
262次组卷
|
2卷引用:重庆市南开中学校2022-2023学年高三上学期第四次月考化学试题
名校
8 . 氮元素在农药生产及工业制造业等领域用途非常广泛。回答下列问题:
(1)NH3是重要的配体,其中H—N—H的键角为107.3°。
①NH3分子的VSEPR模型为___________ 。
②[Cu(NH3)4]2+中H—N—H的键角_____ 107.3°(填“大于”“小于”或“等于”)。
③甲基胺离子(CH3NH3+)的电子式为______________ 。
(2)已知氨在一定条件下可形成一种立方晶系,其立方晶胞沿x、y或z轴投影图均如图所示。已知晶胞的棱长为a pm,则该晶体的密度为______ g/cm3。(写出数学表达式,设NA为阿伏加德罗常数的值)。

(3)CO和H2可以合成简单有机物,已知CO、H2合成CH3OH、HCOOCH3的能量变化如图所示,计算:2CH3OH(g) HCOOCH3(g)+2H2(g) △H=
HCOOCH3(g)+2H2(g) △H=_____ 。

已知键能数据如下表,则C≡O的键能为__________ kJ•mol-1。
(4)利用电解原理,可将氨气转化为高纯氢气,其装置如图所示。
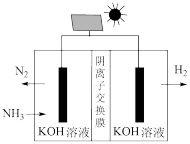
电解过程中OH—的移动方向为____ (填“从左往右”或“从右往左”);阳极的电极反应式为______________ 。
(1)NH3是重要的配体,其中H—N—H的键角为107.3°。
①NH3分子的VSEPR模型为
②[Cu(NH3)4]2+中H—N—H的键角
③甲基胺离子(CH3NH3+)的电子式为
(2)已知氨在一定条件下可形成一种立方晶系,其立方晶胞沿x、y或z轴投影图均如图所示。已知晶胞的棱长为a pm,则该晶体的密度为

(3)CO和H2可以合成简单有机物,已知CO、H2合成CH3OH、HCOOCH3的能量变化如图所示,计算:2CH3OH(g)
 HCOOCH3(g)+2H2(g) △H=
HCOOCH3(g)+2H2(g) △H=
已知键能数据如下表,则C≡O的键能为
化学键 | H-H | C-O | C≡O | H-O | C-H |
键能/(kJ•mol-1) | 436 | 326 | A | 464 | 414 |

电解过程中OH—的移动方向为
您最近一年使用:0次
名校
解题方法
9 . 过渡元素用途广泛。回答下列问题:
(1)基态 的价电子排布式为
的价电子排布式为_______ 。
(2)Co与Ca位于同一周期、且最外层电子数相等,但Co的熔点、沸点均比Ca高,原因是_______ 。
(3) 1mol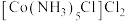 中含有的σ键数目为
中含有的σ键数目为_______ , 分子与
分子与 形成配合物后
形成配合物后 键角
键角_______ (填“变大”“变小”或“不变”)。
(4) 中配体
中配体 的空间结构为
的空间结构为_______ ,N、O原子相比,第二电离能与第一电离能差值更大的是_______ (填元素符号)。
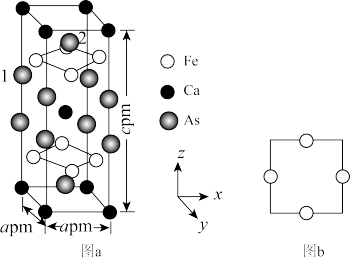
(5)一种铁基超导材料晶胞结构如图a所示,铁原子沿z轴方向的投影如图b所示。该材料的化学式为_______ ,已知体心与顶点的Ca原子有着相同的化学环境,晶胞中As原子1分数坐标为(0,0,0.628),则As原子2的分数坐标为_______ ,体心Ca原子与As原子1之间的距离为_______ pm。
(1)基态
 的价电子排布式为
的价电子排布式为(2)Co与Ca位于同一周期、且最外层电子数相等,但Co的熔点、沸点均比Ca高,原因是
(3) 1mol
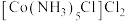 中含有的σ键数目为
中含有的σ键数目为 分子与
分子与 形成配合物后
形成配合物后 键角
键角(4)
 中配体
中配体 的空间结构为
的空间结构为(5)一种铁基超导材料晶胞结构如图a所示,铁原子沿z轴方向的投影如图b所示。该材料的化学式为

您最近一年使用:0次
2022-12-18更新
|
480次组卷
|
2卷引用:山东省淄博市2022-2023学年高三上学期12月月考化学试题
10 . 碳族化合物在研究和生产中有许多重要用途,请回答下列问题:
(1)已知 中硅元素为+4价,则H、Si、O、C的电负性由大到小的顺序为
中硅元素为+4价,则H、Si、O、C的电负性由大到小的顺序为_______ 。
(2)基态锗原子(Ge)价层电子的轨道表示式为_______ 。
(3)邻羟基苯甲酸的沸点比对羟基苯甲酸的沸点低;请解释其原因_______ 。
(4)氮化硅( )是一种耐磨损、耐高温的结构陶瓷材料,其部分空间结构如图所示,其结构中每个原子杂化类型相同且均达到8电子稳定结构,请比较晶体结构中键角大小:N—Si—N
)是一种耐磨损、耐高温的结构陶瓷材料,其部分空间结构如图所示,其结构中每个原子杂化类型相同且均达到8电子稳定结构,请比较晶体结构中键角大小:N—Si—N_______ Si—N—Si(填“>”“<”“=”)。
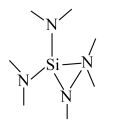
(5)某锂电池的负极材料是将锂原子嵌入到两层石墨烯层中间,其晶体结构如图。已知该晶体中最近的两个碳原子核间距离为a nm,石墨烯层间距离为b nm,则该晶体的密度为_______  (用
(用 表示阿伏加德罗常数,列式即可)。
表示阿伏加德罗常数,列式即可)。
(1)已知
 中硅元素为+4价,则H、Si、O、C的电负性由大到小的顺序为
中硅元素为+4价,则H、Si、O、C的电负性由大到小的顺序为(2)基态锗原子(Ge)价层电子的轨道表示式为
(3)邻羟基苯甲酸的沸点比对羟基苯甲酸的沸点低;请解释其原因
(4)氮化硅(
 )是一种耐磨损、耐高温的结构陶瓷材料,其部分空间结构如图所示,其结构中每个原子杂化类型相同且均达到8电子稳定结构,请比较晶体结构中键角大小:N—Si—N
)是一种耐磨损、耐高温的结构陶瓷材料,其部分空间结构如图所示,其结构中每个原子杂化类型相同且均达到8电子稳定结构,请比较晶体结构中键角大小:N—Si—N
(5)某锂电池的负极材料是将锂原子嵌入到两层石墨烯层中间,其晶体结构如图。已知该晶体中最近的两个碳原子核间距离为a nm,石墨烯层间距离为b nm,则该晶体的密度为
 (用
(用 表示阿伏加德罗常数,列式即可)。
表示阿伏加德罗常数,列式即可)。
您最近一年使用:0次



