真题
名校
1 . 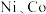 均是重要的战略性金属。从处理后的矿石硝酸浸取液(含
均是重要的战略性金属。从处理后的矿石硝酸浸取液(含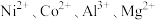 )中,利用氨浸工艺可提取
)中,利用氨浸工艺可提取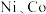 ,并获得高附加值化工产品。工艺流程如下:
,并获得高附加值化工产品。工艺流程如下:
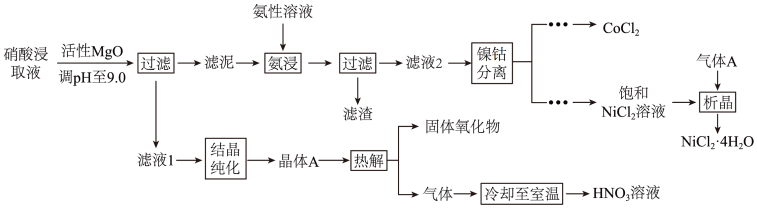
已知:氨性溶液由 、
、 和
和 配制。常温下,
配制。常温下,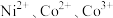 与
与 形成可溶于水的配离子:
形成可溶于水的配离子: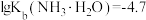 ;
; 易被空气氧化为
易被空气氧化为 ;部分氢氧化物的
;部分氢氧化物的 如下表。
如下表。
回答下列问题:
(1)活性 可与水反应,化学方程式为
可与水反应,化学方程式为___________ 。
(2)常温下, 的氨性溶液中,
的氨性溶液中,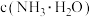
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3)“氨浸”时,由 转化为
转化为 的离子方程式为
的离子方程式为___________ 。
(4) 会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物。滤渣的X射线衍射图谱中,出现了
会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物。滤渣的X射线衍射图谱中,出现了 的明锐衍射峰。
的明锐衍射峰。
① 属于
属于___________ (填“晶体”或“非晶体”)。
② 提高了
提高了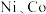 的浸取速率,其原因是
的浸取速率,其原因是___________ 。
(5)①“析晶”过程中通入的酸性气体A为___________ 。
②由 可制备
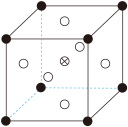
可制备 晶体,其立方晶胞如图。
晶体,其立方晶胞如图。 与O最小间距大于
与O最小间距大于 与O最小间距,x、y为整数,则
与O最小间距,x、y为整数,则 在晶胞中的位置为
在晶胞中的位置为___________ ;晶体中一个 周围与其最近的O的个数为
周围与其最近的O的个数为___________ 。
(6)①“结晶纯化”过程中,没有引入新物质。晶体A含6个结晶水,则所得 溶液中
溶液中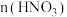 与
与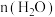 的比值,理论上最高为
的比值,理论上最高为___________ 。
②“热解”对于从矿石提取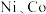 工艺的意义,在于可重复利用
工艺的意义,在于可重复利用 和
和___________ (填化学式)。
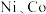 均是重要的战略性金属。从处理后的矿石硝酸浸取液(含
均是重要的战略性金属。从处理后的矿石硝酸浸取液(含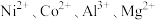 )中,利用氨浸工艺可提取
)中,利用氨浸工艺可提取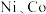 ,并获得高附加值化工产品。工艺流程如下:
,并获得高附加值化工产品。工艺流程如下:
已知:氨性溶液由
 、
、 和
和 配制。常温下,
配制。常温下,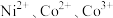 与
与 形成可溶于水的配离子:
形成可溶于水的配离子: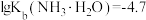 ;
; 易被空气氧化为
易被空气氧化为 ;部分氢氧化物的
;部分氢氧化物的 如下表。
如下表。| 氢氧化物 |  |  |  |  |  |
 | 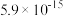 |  |  | 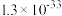 | 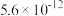 |
(1)活性
 可与水反应,化学方程式为
可与水反应,化学方程式为(2)常温下,
 的氨性溶液中,
的氨性溶液中,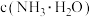
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(3)“氨浸”时,由
 转化为
转化为 的离子方程式为
的离子方程式为(4)
 会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物。滤渣的X射线衍射图谱中,出现了
会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物。滤渣的X射线衍射图谱中,出现了 的明锐衍射峰。
的明锐衍射峰。①
 属于
属于②
 提高了
提高了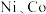 的浸取速率,其原因是
的浸取速率,其原因是(5)①“析晶”过程中通入的酸性气体A为
②由
 可制备
可制备 晶体,其立方晶胞如图。
晶体,其立方晶胞如图。 与O最小间距大于
与O最小间距大于 与O最小间距,x、y为整数,则
与O最小间距,x、y为整数,则 在晶胞中的位置为
在晶胞中的位置为 周围与其最近的O的个数为
周围与其最近的O的个数为
(6)①“结晶纯化”过程中,没有引入新物质。晶体A含6个结晶水,则所得
 溶液中
溶液中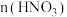 与
与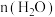 的比值,理论上最高为
的比值,理论上最高为②“热解”对于从矿石提取
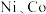 工艺的意义,在于可重复利用
工艺的意义,在于可重复利用 和
和
您最近一年使用:0次
2023-07-04更新
|
9716次组卷
|
6卷引用:2023年广东卷高考真题变式题(工业流程题)
(已下线)2023年广东卷高考真题变式题(工业流程题)2023年高考广东卷化学真题(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题05 盐类的水解-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)湖北省沙市中学2023-2024学年高三下学期3月月考化学试题
名校
解题方法
2 . 以含铅废料(Pb、PbO、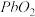 、
、 及炭黑等)制备高纯PbO。其流程如下:
及炭黑等)制备高纯PbO。其流程如下:
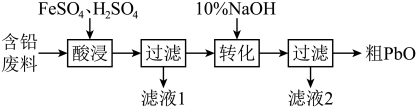
(1)酸浸时,在 催化下Pb和
催化下Pb和 反应生成
反应生成 的离子方程式是
的离子方程式是___________ 。
(2) 催化过程可表示为:
催化过程可表示为:
ⅰ: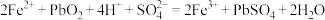 ⅱ:……
ⅱ:……
写出ⅱ的离子方程式:___________ 。
(3)PbO溶解在NaOH溶液中,存在平衡:
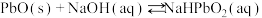 ,其溶解度曲线如图所示。
,其溶解度曲线如图所示。
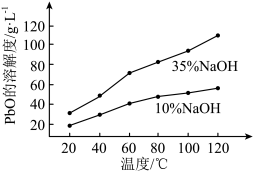
①转化过程中,选用10%NaOH溶液的原因是___________ 。
②滤液2中含有的阴离子有 、
、___________ 。
(4)结合上述溶解度曲线,设计利用粗PbO制备高纯PbO的方案:___________ 。(实验中可选用的试剂:___________ ;10%NaOH溶液、35%NaOH溶液、蒸馏水)
(5)六方氧化铅晶体的结构如图所示。用碳原子代替氧原子和铅原子,即为六方金刚石。请在该图内用粗线框出六方金刚石的一个晶胞,要求框线必须包含图中已有的一段粗线,且框出的晶胞体积最小___________ 。

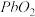 、
、 及炭黑等)制备高纯PbO。其流程如下:
及炭黑等)制备高纯PbO。其流程如下:
(1)酸浸时,在
 催化下Pb和
催化下Pb和 反应生成
反应生成 的离子方程式是
的离子方程式是(2)
 催化过程可表示为:
催化过程可表示为:ⅰ:
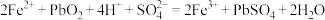 ⅱ:……
ⅱ:……写出ⅱ的离子方程式:
(3)PbO溶解在NaOH溶液中,存在平衡:
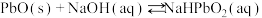 ,其溶解度曲线如图所示。
,其溶解度曲线如图所示。
①转化过程中,选用10%NaOH溶液的原因是
②滤液2中含有的阴离子有
 、
、(4)结合上述溶解度曲线,设计利用粗PbO制备高纯PbO的方案:
(5)六方氧化铅晶体的结构如图所示。用碳原子代替氧原子和铅原子,即为六方金刚石。请在该图内用粗线框出六方金刚石的一个晶胞,要求框线必须包含图中已有的一段粗线,且框出的晶胞体积最小

您最近一年使用:0次
2023-06-03更新
|
396次组卷
|
3卷引用:2023年广东卷高考真题变式题(工业流程题)
3 . 工业上利用黑钨矿(其主要成分是 、
、 ,同时还含有少量
,同时还含有少量 )制备钮的工艺流程如下图所示:
)制备钮的工艺流程如下图所示:

已知:①
②
回答下列问题:
(1)黑钨矿“焙烧”前需充分研磨,目的是___________ 。“焙烧”过程中发生的其他反应的化学方程式为___________ 。
(2)“滤渣1”的成分是___________ (填化学式,下同),“滤渣2”的成分是___________ 。
(3)将 还原成
还原成 单质,使用的还原剂可以用
单质,使用的还原剂可以用 、
、 或
或___________ (填一种常见金属名称)。
(4)钨酸钙( )和氢氧化钙都是微溶电解质。某温度下
)和氢氧化钙都是微溶电解质。某温度下 和
和 的饱和溶液中,
的饱和溶液中, 与
与 (阴离子)的关系如图所示,已知:
(阴离子)的关系如图所示,已知: (离子)
(离子) (离子)。该温度下将
(离子)。该温度下将 溶液加入石灰乳中得到大量钨酸钙,发生反应的离子方程式为
溶液加入石灰乳中得到大量钨酸钙,发生反应的离子方程式为___________ ,该反应的平衡常数
___________ 。

(5)合金具有比金属单质更优越的性能,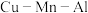 合金为磁性形状记忆合金材料之一,其晶胞结构如图所示。
合金为磁性形状记忆合金材料之一,其晶胞结构如图所示。

①若A原子的坐标参数为 ,则B原子的坐标参数为
,则B原子的坐标参数为___________ 。
②已知该合金晶体的密度为 ,则最近的两个
,则最近的两个 原子间的距离为
原子间的距离为___________  (列出计算式,阿伏加德罗常数的值用
(列出计算式,阿伏加德罗常数的值用 表示)。
表示)。
 、
、 ,同时还含有少量
,同时还含有少量 )制备钮的工艺流程如下图所示:
)制备钮的工艺流程如下图所示:
已知:①

②

回答下列问题:
(1)黑钨矿“焙烧”前需充分研磨,目的是
(2)“滤渣1”的成分是
(3)将
 还原成
还原成 单质,使用的还原剂可以用
单质,使用的还原剂可以用 、
、 或
或(4)钨酸钙(
 )和氢氧化钙都是微溶电解质。某温度下
)和氢氧化钙都是微溶电解质。某温度下 和
和 的饱和溶液中,
的饱和溶液中, 与
与 (阴离子)的关系如图所示,已知:
(阴离子)的关系如图所示,已知: (离子)
(离子) (离子)。该温度下将
(离子)。该温度下将 溶液加入石灰乳中得到大量钨酸钙,发生反应的离子方程式为
溶液加入石灰乳中得到大量钨酸钙,发生反应的离子方程式为

(5)合金具有比金属单质更优越的性能,
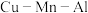 合金为磁性形状记忆合金材料之一,其晶胞结构如图所示。
合金为磁性形状记忆合金材料之一,其晶胞结构如图所示。
①若A原子的坐标参数为
 ,则B原子的坐标参数为
,则B原子的坐标参数为②已知该合金晶体的密度为
 ,则最近的两个
,则最近的两个 原子间的距离为
原子间的距离为 (列出计算式,阿伏加德罗常数的值用
(列出计算式,阿伏加德罗常数的值用 表示)。
表示)。
您最近一年使用:0次
名校
4 . 赤泥是氧化铝生产排放的固体废弃物。由赤泥(主要成分为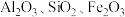 、
、 等)制备一种高效净水剂聚合硫酸铝铁(PAFS)的工艺流程如下:
等)制备一种高效净水剂聚合硫酸铝铁(PAFS)的工艺流程如下:___________ , 的空间构型是
的空间构型是___________ 。
(2)“焙烧”时,需将赤泥粉碎的目的是___________ 。
(3)酸浸渣的主要成分是___________ (填化学式)。
(4)“氧化”时发生反应的离子方程式为___________ 。室温下,向氧化后的溶液中滴加 溶液至
溶液至 时,溶液中的
时,溶液中的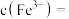
___________  。(已知
。(已知 ,
, 的
的 )
)
(5)为了测试所制得的聚合硫酸铝铁的性能,取某水样在不同 条件下加入PAFS【
条件下加入PAFS【 】并测定其去浊率,结果如图所示。(已知去浊率越高,净水效果越好)由图可知在设定的偏酸性和偏碱性条件下,水样的去浊率均不高。试分析
】并测定其去浊率,结果如图所示。(已知去浊率越高,净水效果越好)由图可知在设定的偏酸性和偏碱性条件下,水样的去浊率均不高。试分析 时,去浊率较低的可能原因为
时,去浊率较低的可能原因为___________ 。___________ ,若晶体密度为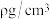 ,则晶胞中最近的两个碳原子的距离为
,则晶胞中最近的两个碳原子的距离为___________  (阿伏加德罗常数的值用
(阿伏加德罗常数的值用 表示,写出计算式即可)。
表示,写出计算式即可)。
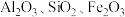 、
、 等)制备一种高效净水剂聚合硫酸铝铁(PAFS)的工艺流程如下:
等)制备一种高效净水剂聚合硫酸铝铁(PAFS)的工艺流程如下:
 的空间构型是
的空间构型是(2)“焙烧”时,需将赤泥粉碎的目的是
(3)酸浸渣的主要成分是
(4)“氧化”时发生反应的离子方程式为
 溶液至
溶液至 时,溶液中的
时,溶液中的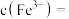
 。(已知
。(已知 ,
, 的
的 )
)(5)为了测试所制得的聚合硫酸铝铁的性能,取某水样在不同
 条件下加入PAFS【
条件下加入PAFS【 】并测定其去浊率,结果如图所示。(已知去浊率越高,净水效果越好)由图可知在设定的偏酸性和偏碱性条件下,水样的去浊率均不高。试分析
】并测定其去浊率,结果如图所示。(已知去浊率越高,净水效果越好)由图可知在设定的偏酸性和偏碱性条件下,水样的去浊率均不高。试分析 时,去浊率较低的可能原因为
时,去浊率较低的可能原因为
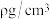 ,则晶胞中最近的两个碳原子的距离为
,则晶胞中最近的两个碳原子的距离为 (阿伏加德罗常数的值用
(阿伏加德罗常数的值用 表示,写出计算式即可)。
表示,写出计算式即可)。
您最近一年使用:0次
2023-05-29更新
|
589次组卷
|
4卷引用:2023年广东卷高考真题变式题(工业流程题)
(已下线)2023年广东卷高考真题变式题(工业流程题)广东省华南师范大学附属中学2023届高三下学期第三次模拟考试化学试题广东省广州市天河外国语学校2024届高三1月校考化学试题广东省汕头市潮南区科利园实验学校2024届高三下学期第三次模拟考试化学
5 . 优化的NaFePO4复合材料作钠离子电池的正极材料时表现出优异的循环稳定性。以黄铁矿(主要成分是FeS2,含少量SiO2等杂质)为原料制备NaFePO4的流程如图所示。
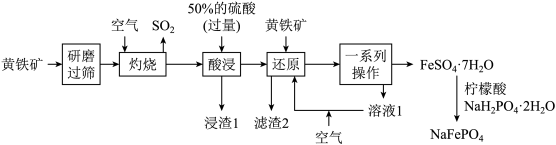
已知:“滤渣2”中不含硫单质。涉及离子的氢氧化物常温下的溶度积常数如表。(当离子的物质的量浓度≤10-5mol·L-1时,认为沉淀完全,lg4=0.6)
回答下列问题:
(1)“研磨”的目的是_______ 。
(2)“灼烧”时的大量尾气直接排放,会引起的主要环境问题为_______ (填一种)。
(3)常温下,“酸浸”时,加入过量50%的硫酸的目的为_______ (答一条即可)。
(4)“浸渣1”的主要成分是_______ (填化学式) 。
(5)“还原”中FeS2与Fe3+反应的离子方程式为_______ ;通入空气的条件下, “溶液1”可在“还原”步骤中循环利用,则通入空气的目的是_______ 。
(6)“一系列操作”包括_______ 、_______ 、过滤、 洗涤和低温干燥。
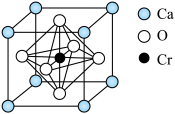
(7)铬与铁为同周期元素,某含铬化合物立方晶胞如图所示。晶体的化学式为_______ ;与Cr最近的氧原子的个数为_______ ;Ca 和Cr的最近距离为a nm,设NA为阿伏加德常数的值,则该晶体密度为_______ (填含 a、NA的表达式)g· cm-3。

已知:“滤渣2”中不含硫单质。涉及离子的氢氧化物常温下的溶度积常数如表。(当离子的物质的量浓度≤10-5mol·L-1时,认为沉淀完全,lg4=0.6)
| 离子 | Fe2+ | Fe3+ |
| Ksp | 8×10-16 | 4×0-38 |
(1)“研磨”的目的是
(2)“灼烧”时的大量尾气直接排放,会引起的主要环境问题为
(3)常温下,“酸浸”时,加入过量50%的硫酸的目的为
(4)“浸渣1”的主要成分是
(5)“还原”中FeS2与Fe3+反应的离子方程式为
(6)“一系列操作”包括
(7)铬与铁为同周期元素,某含铬化合物立方晶胞如图所示。晶体的化学式为

您最近一年使用:0次
6 . 钠离子电池有望代替锂离子电池,其正极材料可再生利用。某钠离子电池正极材料有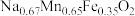 、石墨烯和少量镁等。充电时,钠离子从正极脱嵌经盐离子导体向负极移动。现欲利用以下工艺流程回收正极材料中的某些金属资源(部分条件未给出)。
、石墨烯和少量镁等。充电时,钠离子从正极脱嵌经盐离子导体向负极移动。现欲利用以下工艺流程回收正极材料中的某些金属资源(部分条件未给出)。
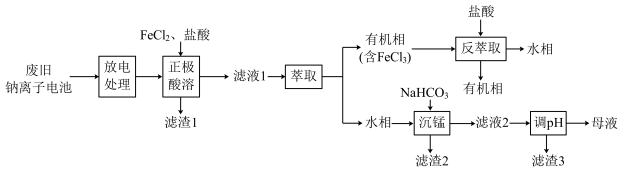
已知:溶液中离子浓度小于等于 时,认为该离子沉淀完全;部分物质的溶度积常数如表所示。
时,认为该离子沉淀完全;部分物质的溶度积常数如表所示。
回答下列问题:
(1)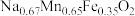 中
中 为+4价,则其中Fe(Ⅱ)与Fe(Ⅲ)的数目之比为
为+4价,则其中Fe(Ⅱ)与Fe(Ⅲ)的数目之比为___________ (其中的Ⅱ、Ⅲ表示化合价的数值)
(2)“放电处理”的主要目的为___________ ;“正极酸溶”反应的离子方程式为___________ 。
(3)“萃取”时,几种萃取剂对铁的萃取率与盐酸浓度的关系如图所示。则适合选用的萃取剂为___________ (填字母),理由为___________ 。

(4)由“反萃取”所得水相制备 的操作为
的操作为___________ 。
(5)“沉锰”时,若 沉淀完全而
沉淀完全而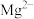 不形成沉淀,则“萃取”所得水相中
不形成沉淀,则“萃取”所得水相中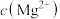 不超过
不超过___________ (保留2位有效数字);该工序不采用调 的方法的原因为
的方法的原因为___________ 。
(6)母液中提取所得晶体的部分立方结构如图所示。
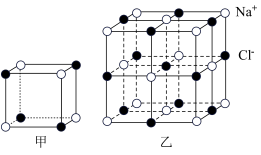
①图甲所示单元结构不是 的晶胞单元的理由为
的晶胞单元的理由为___________ 。
② 晶体中,由最近
晶体中,由最近 围成的正八面体与最近
围成的正八面体与最近 围成的正四面体的数目之比为
围成的正四面体的数目之比为___________ 。
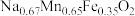 、石墨烯和少量镁等。充电时,钠离子从正极脱嵌经盐离子导体向负极移动。现欲利用以下工艺流程回收正极材料中的某些金属资源(部分条件未给出)。
、石墨烯和少量镁等。充电时,钠离子从正极脱嵌经盐离子导体向负极移动。现欲利用以下工艺流程回收正极材料中的某些金属资源(部分条件未给出)。
已知:溶液中离子浓度小于等于
 时,认为该离子沉淀完全;部分物质的溶度积常数如表所示。
时,认为该离子沉淀完全;部分物质的溶度积常数如表所示。| 物质 |  |  |  |  |
溶度积常数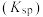 | 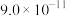 |  | 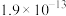 | 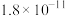 |
(1)
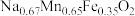 中
中 为+4价,则其中Fe(Ⅱ)与Fe(Ⅲ)的数目之比为
为+4价,则其中Fe(Ⅱ)与Fe(Ⅲ)的数目之比为(2)“放电处理”的主要目的为
(3)“萃取”时,几种萃取剂对铁的萃取率与盐酸浓度的关系如图所示。则适合选用的萃取剂为

(4)由“反萃取”所得水相制备
 的操作为
的操作为(5)“沉锰”时,若
 沉淀完全而
沉淀完全而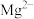 不形成沉淀,则“萃取”所得水相中
不形成沉淀,则“萃取”所得水相中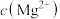 不超过
不超过 的方法的原因为
的方法的原因为(6)母液中提取所得晶体的部分立方结构如图所示。

①图甲所示单元结构不是
 的晶胞单元的理由为
的晶胞单元的理由为②
 晶体中,由最近
晶体中,由最近 围成的正八面体与最近
围成的正八面体与最近 围成的正四面体的数目之比为
围成的正四面体的数目之比为
您最近一年使用:0次
7 . 分铜液净化渣主要含铜、碲(Te)、锑(Sb)、砷(As)等元素的化合物,一种回收工艺流程如图所示:
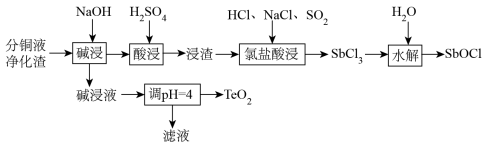
已知:①“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有 、
、 。
。
②“酸浸”时,锑元素反应生成难溶的 浸渣。
浸渣。
回答下列问题:
(1)As位于第四周期VA族,基态As的价层电子排布式为___________ 。
(2)“碱浸”时, 与NaOH反应的离子方程式为
与NaOH反应的离子方程式为___________ 。
(3)向碱浸液加入盐酸调节pH=4,有 析出,分离出
析出,分离出 的操作是
的操作是___________ 。滤液中As元素最主要的存在形式为___________ (常温下, 的各级电离常数为:
的各级电离常数为: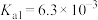 、
、 、
、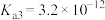 )。
)。
A. B.
B.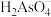 C.
C. D.
D.
(4)① 中,Sb的化合价为
中,Sb的化合价为___________ 。
②“氯盐酸浸”时,通入 的目的是
的目的是___________ 。
(5)“水解”时,生成SbOCl的化学方程式为___________ 。
(6) 可用作电子元件材料,熔点为733℃,其熔点远高于
可用作电子元件材料,熔点为733℃,其熔点远高于 的原因为
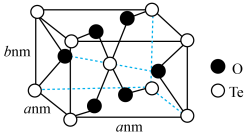
的原因为___________ 。 晶胞是长方体结构(如图所示),碲的配位数为
晶胞是长方体结构(如图所示),碲的配位数为___________ 。已知 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为___________  (列出计算表达式)
(列出计算表达式)

已知:①“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有
 、
、 。
。②“酸浸”时,锑元素反应生成难溶的
 浸渣。
浸渣。回答下列问题:
(1)As位于第四周期VA族,基态As的价层电子排布式为
(2)“碱浸”时,
 与NaOH反应的离子方程式为
与NaOH反应的离子方程式为(3)向碱浸液加入盐酸调节pH=4,有
 析出,分离出
析出,分离出 的操作是
的操作是 的各级电离常数为:
的各级电离常数为: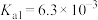 、
、 、
、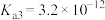 )。
)。A.
 B.
B.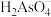 C.
C. D.
D.
(4)①
 中,Sb的化合价为
中,Sb的化合价为②“氯盐酸浸”时,通入
 的目的是
的目的是(5)“水解”时,生成SbOCl的化学方程式为
(6)
 可用作电子元件材料,熔点为733℃,其熔点远高于
可用作电子元件材料,熔点为733℃,其熔点远高于 的原因为
的原因为 晶胞是长方体结构(如图所示),碲的配位数为
晶胞是长方体结构(如图所示),碲的配位数为 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为 (列出计算表达式)
(列出计算表达式)
您最近一年使用:0次
2023-04-20更新
|
1069次组卷
|
3卷引用:广东省广州市天河区2023届高三二模化学试题变式题(工业流程题)
8 . (氧化铬(Cr2O3)可用作着色剂、分析试剂、催化剂等。以含铬废料(含FeCr2O4、MgO、SiO2、Al2O3等)为原料制备氧化铬的一种流程如图所示。
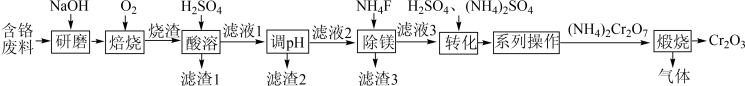
已知:烧渣的成分为Na2CrO4、NaAlO2、Na2SiO3、Fe2O3、MgO;25℃时,Ksp[Fe(OH)3]=4×10-38、Ksp[Al(OH)3]=1×l0-33、Ksp[Mg(OH)2]=2×10-11,溶液中离子浓度≤10-5mol·L-1时,认为该离子沉淀完全。回答下列问题:
(1)“研磨”的目的是_________ ;“焙烧”过程发生的氧化还原反应中,氧化剂与还原剂的物质的量之比是_________ 。
(2)25℃时,若滤液l中金属离子的浓度均为0.2mol·L-1,则“调pH”的最小值为_________ 。(保留两位有效数字)。
(3)“除镁”工序不能在陶瓷容器中进行的原因是_________ 。
(4)“转化”时加入适量H2SO4的作用是_________ 。
(5)“煅烧”反应生成的气体中含有一种单质,该反应的化学方程式_________ 。
(6)已知MgO具有NaCl型晶体结构,其结构如图所示。
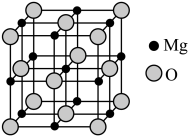
则每个Mg2+周围距离最近的Mg2+个数为_________ 。已知MgO晶胞边长为0.4nm,则MgO的密度为_________ g/cm3(设NA为阿伏加德罗常数的值,只需列出算式)。

已知:烧渣的成分为Na2CrO4、NaAlO2、Na2SiO3、Fe2O3、MgO;25℃时,Ksp[Fe(OH)3]=4×10-38、Ksp[Al(OH)3]=1×l0-33、Ksp[Mg(OH)2]=2×10-11,溶液中离子浓度≤10-5mol·L-1时,认为该离子沉淀完全。回答下列问题:
(1)“研磨”的目的是
(2)25℃时,若滤液l中金属离子的浓度均为0.2mol·L-1,则“调pH”的最小值为
(3)“除镁”工序不能在陶瓷容器中进行的原因是
(4)“转化”时加入适量H2SO4的作用是
(5)“煅烧”反应生成的气体中含有一种单质,该反应的化学方程式
(6)已知MgO具有NaCl型晶体结构,其结构如图所示。

则每个Mg2+周围距离最近的Mg2+个数为
您最近一年使用:0次
9 . 钼酸铋作为新型半导体光催化材料,因其具有优异的离子导电性、介电性、气体传感性和催化性而广泛应用于生产生活中。以氧化铋渣(主要成分是 、
、 、还含有
、还含有 、ZnO、
、ZnO、 和
和 等杂质)为原料制备钼酸铋(
等杂质)为原料制备钼酸铋( ,其中Mo为+6价)的工艺流程如下:
,其中Mo为+6价)的工艺流程如下:

回答下列问题:
(1)基态 的价电子排布式为
的价电子排布式为___________ 。
(2)“浸渣”的主要成分为___________ (填化学式)。
(3)“除锑”过程中发生反应的化学方程式为______ ;该过程需要加热的原因为_______ 。
(4)已知:硫代乙酰胺(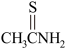 )在酸性溶液中会水解为乙酰胺(
)在酸性溶液中会水解为乙酰胺(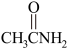 )和硫化氢;
)和硫化氢; 的
的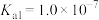 ,
,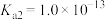 ;
; 。
。
①硫化氢会进一步发生反应 ,计算该反应的平衡常数K=
,计算该反应的平衡常数K=___________ 。
②硫代乙酰胺比乙酰胺的沸点低,解释其原因为___________ 。
(5)“酸溶”时会有NO逸出,此过程中氧化剂与还原剂的物质的量之比为___________ 。
(6)已知钼酸铋在空气中放置会变质,生成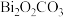 和
和 ,该过程中的化学方程式为
,该过程中的化学方程式为___________ 。
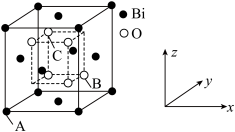
(7) 的立方晶胞结构如图所示,以A点为原点建立分数坐标,已知A点坐标为(0,0,0),B点坐标为
的立方晶胞结构如图所示,以A点为原点建立分数坐标,已知A点坐标为(0,0,0),B点坐标为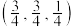 ,则C点坐标为
,则C点坐标为___________ 。
 、
、 、还含有
、还含有 、ZnO、
、ZnO、 和
和 等杂质)为原料制备钼酸铋(
等杂质)为原料制备钼酸铋( ,其中Mo为+6价)的工艺流程如下:
,其中Mo为+6价)的工艺流程如下:
回答下列问题:
(1)基态
 的价电子排布式为
的价电子排布式为(2)“浸渣”的主要成分为
(3)“除锑”过程中发生反应的化学方程式为
(4)已知:硫代乙酰胺(
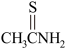 )在酸性溶液中会水解为乙酰胺(
)在酸性溶液中会水解为乙酰胺(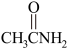 )和硫化氢;
)和硫化氢; 的
的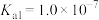 ,
,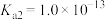 ;
; 。
。①硫化氢会进一步发生反应
 ,计算该反应的平衡常数K=
,计算该反应的平衡常数K=②硫代乙酰胺比乙酰胺的沸点低,解释其原因为
(5)“酸溶”时会有NO逸出,此过程中氧化剂与还原剂的物质的量之比为
(6)已知钼酸铋在空气中放置会变质,生成
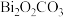 和
和 ,该过程中的化学方程式为
,该过程中的化学方程式为(7)
 的立方晶胞结构如图所示,以A点为原点建立分数坐标,已知A点坐标为(0,0,0),B点坐标为
的立方晶胞结构如图所示,以A点为原点建立分数坐标,已知A点坐标为(0,0,0),B点坐标为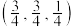 ,则C点坐标为
,则C点坐标为
您最近一年使用:0次
2023-04-10更新
|
978次组卷
|
4卷引用:2023年广东卷高考真题变式题(工业流程题)
(已下线)2023年广东卷高考真题变式题(工业流程题)(已下线)专题18 工艺流程题河北省石家庄市部分学校2023届高中毕业年级教学质量检测(二)(一模)化学试题河北省邢台市2022-2023学年高三下学期4月第一次模拟考试化学试题
10 . 一种锂的氧化物的晶胞结构如图所示(晶胞参数a=b=c=0.4665nm,晶胞棱边夹角均为90°)。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。下列有关说法不正确的是
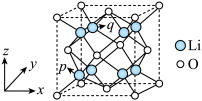
| A.该氧化物的化学式为Li2O |
B.O原子之间的最短距离为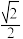 ×466.5pm ×466.5pm |
| C.与Li距离最近且相等的O有8个 |
D.若p原子的分数坐标为( , , , , ),则q原子的分数坐标为( ),则q原子的分数坐标为( , , , , ) ) |
您最近一年使用:0次
2023-03-31更新
|
1508次组卷
|
10卷引用:专题06 物质结构与性质



