名校
解题方法
1 . BTCu是荧光增强型Cu2+荧光分子探针,可对环境和生物体内的微量Cu2+进行有效检测。BTCu识别Cu2+机理如下图:

回答下列问题:
(1)基态Cu原子的价电子排布式为___________ 。
(2)BTCu中所含第二周期元素的第一电离能由小到大的顺序为___________ (用元素符号表示)。
(3)探针BTCu与Cu2+的识别过程既有氧化脱氢反应,也有配合形式的参与。1molBTCu-Cu+中,Cu+形成的配位键有___________ mol,B原子的杂化轨道类型是___________ 。
(4)某晶体的晶胞结构如下图所示。已知:a=b=0.524 nm,c-1.032 nm,晶胞棱边夹角均为90°,NA为阿伏加德罗常数的值。(1nm=1×10-7cm)

①距离Fe最近且等距的S有___________ 个。
②该晶体的化学式是___________ 。
③该晶体的密度是___________ g/cm3 (列出计算式)。

回答下列问题:
(1)基态Cu原子的价电子排布式为
(2)BTCu中所含第二周期元素的第一电离能由小到大的顺序为
(3)探针BTCu与Cu2+的识别过程既有氧化脱氢反应,也有配合形式的参与。1molBTCu-Cu+中,Cu+形成的配位键有
(4)某晶体的晶胞结构如下图所示。已知:a=b=0.524 nm,c-1.032 nm,晶胞棱边夹角均为90°,NA为阿伏加德罗常数的值。(1nm=1×10-7cm)

①距离Fe最近且等距的S有
②该晶体的化学式是
③该晶体的密度是
您最近一年使用:0次
2022高三·全国·专题练习
2 . 硫铁化合物( 、
、 等)应用广泛。
等)应用广泛。
(1)纳米 可去除水中微量六价铬
可去除水中微量六价铬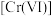 。在
。在 的水溶液中,纳米
的水溶液中,纳米 颗粒表面带正电荷,
颗粒表面带正电荷, 主要以
主要以 、
、 、
、 等形式存在,纳米
等形式存在,纳米 去除水中
去除水中 主要经过“吸附→反应→沉淀”的过程。
主要经过“吸附→反应→沉淀”的过程。
已知: ,
,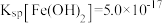 ;
; 电离常数分别为
电离常数分别为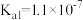 、
、 。
。
①在弱碱性溶液中, 与
与 反应生成
反应生成 、
、 和单质S,其离子方程式为
和单质S,其离子方程式为_______ 。
②在弱酸性溶液中,反应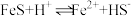 的平衡常数K的数值为
的平衡常数K的数值为_______ 。
③在 溶液中,pH越大,
溶液中,pH越大, 去除水中
去除水中 的速率越慢,原因是
的速率越慢,原因是_______ 。
(2) 具有良好半导体性能。
具有良好半导体性能。 的一种晶体与
的一种晶体与 晶体的结构相似,该
晶体的结构相似,该 晶体的一个晶胞中
晶体的一个晶胞中 的数目为
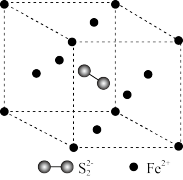
的数目为_______ ,在 晶体中,每个S原子与三个
晶体中,每个S原子与三个 紧邻,且
紧邻,且 间距相等,如图给出了
间距相等,如图给出了 晶胞中的
晶胞中的 和位于晶胞体心的
和位于晶胞体心的 (
( 中的
中的 键位于晶胞体对角线上,晶胞中的其他
键位于晶胞体对角线上,晶胞中的其他 已省略)。如图中用“-”将其中一个S原子与紧邻的
已省略)。如图中用“-”将其中一个S原子与紧邻的 连接起来
连接起来_______ 。
(3) 、
、 在空气中易被氧化,将
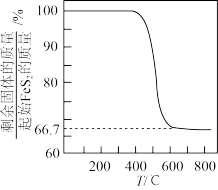
在空气中易被氧化,将 在空气中氧化,测得氧化过程中剩余固体的质量与起始
在空气中氧化,测得氧化过程中剩余固体的质量与起始 的质量的比值随温度变化的曲线如图所示。
的质量的比值随温度变化的曲线如图所示。 时,
时, 氧化成含有两种元素的固体产物为
氧化成含有两种元素的固体产物为_______ (填化学式,写出计算过程)。
 、
、 等)应用广泛。
等)应用广泛。(1)纳米
 可去除水中微量六价铬
可去除水中微量六价铬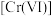 。在
。在 的水溶液中,纳米
的水溶液中,纳米 颗粒表面带正电荷,
颗粒表面带正电荷, 主要以
主要以 、
、 、
、 等形式存在,纳米
等形式存在,纳米 去除水中
去除水中 主要经过“吸附→反应→沉淀”的过程。
主要经过“吸附→反应→沉淀”的过程。已知:
 ,
,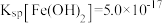 ;
; 电离常数分别为
电离常数分别为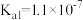 、
、 。
。①在弱碱性溶液中,
 与
与 反应生成
反应生成 、
、 和单质S,其离子方程式为
和单质S,其离子方程式为②在弱酸性溶液中,反应
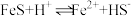 的平衡常数K的数值为
的平衡常数K的数值为③在
 溶液中,pH越大,
溶液中,pH越大, 去除水中
去除水中 的速率越慢,原因是
的速率越慢,原因是(2)
 具有良好半导体性能。
具有良好半导体性能。 的一种晶体与
的一种晶体与 晶体的结构相似,该
晶体的结构相似,该 晶体的一个晶胞中
晶体的一个晶胞中 的数目为
的数目为 晶体中,每个S原子与三个
晶体中,每个S原子与三个 紧邻,且
紧邻,且 间距相等,如图给出了
间距相等,如图给出了 晶胞中的
晶胞中的 和位于晶胞体心的
和位于晶胞体心的 (
( 中的
中的 键位于晶胞体对角线上,晶胞中的其他
键位于晶胞体对角线上,晶胞中的其他 已省略)。如图中用“-”将其中一个S原子与紧邻的
已省略)。如图中用“-”将其中一个S原子与紧邻的 连接起来
连接起来
(3)
 、
、 在空气中易被氧化,将
在空气中易被氧化,将 在空气中氧化,测得氧化过程中剩余固体的质量与起始
在空气中氧化,测得氧化过程中剩余固体的质量与起始 的质量的比值随温度变化的曲线如图所示。
的质量的比值随温度变化的曲线如图所示。 时,
时, 氧化成含有两种元素的固体产物为
氧化成含有两种元素的固体产物为
您最近一年使用:0次
2022-07-21更新
|
8791次组卷
|
13卷引用:北京市第二中学2022-2023学年高三下学期2月开学测试化学试题
北京市第二中学2022-2023学年高三下学期2月开学测试化学试题北京市第二中学2023-2024学年高三下学期开学考化学试卷(已下线)专题17 物质结构与性质(综合题)-2022年高考真题模拟题分项汇编江苏省2022年普通高中学业水平选择性考试(已下线)2022年江苏卷高考真题变式题14-17(已下线)易错点26 沉淀溶解平衡-备战2023年高考化学考试易错题(已下线)热点情景汇编-专题十四 结构性质中的新材料(已下线)专题三 离子反应-实战高考·二轮复习核心突破江苏省南京市金陵中学河西分校2022-2023学年高二上学期期末检测化学试题(已下线)江苏省2022年普通高中学业水平选择性考试变式题(结构与性质)(已下线)2022年北京高考真题化学试题变式题(结构与性质)(已下线)专题20 结构与性质(已下线)专题20 结构与性质
3 . MnO2可作氨选择性催化还原法脱除NOx的催化剂。
(1)基态Mn的价层电子排布的轨道表示式是____ 。
(2)MnO2可由(NH4)2S2O8与MnSO4反应制得。S2O 的结构如图。
的结构如图。

①S2O 中S—O—O
中S—O—O____ (填“是”或“不是”)在一条直线上。
②S2O 中的O—O比H2O2中的更
中的O—O比H2O2中的更____ (填“难”或“易”)断裂。
(3)一种MnO2晶体的晶胞示意图如图,该长方体晶胞的长和宽均为anm,高为bnm。

①图中“●”代表的是____ (填“Mn”或“O”)。
②NA为阿伏加德罗常数,该晶体的密度为____ g·cm-3。
③MnO2作催化剂,氨催化还原脱除NO的一种催化机理示意图如图。

从化学键的角度解释MnO2能结合NH3的原因:____ 。该催化过程的总反应的化学方程式是____ 。
(1)基态Mn的价层电子排布的轨道表示式是
(2)MnO2可由(NH4)2S2O8与MnSO4反应制得。S2O
 的结构如图。
的结构如图。
①S2O
 中S—O—O
中S—O—O②S2O
 中的O—O比H2O2中的更
中的O—O比H2O2中的更(3)一种MnO2晶体的晶胞示意图如图,该长方体晶胞的长和宽均为anm,高为bnm。

①图中“●”代表的是
②NA为阿伏加德罗常数,该晶体的密度为
③MnO2作催化剂,氨催化还原脱除NO的一种催化机理示意图如图。

从化学键的角度解释MnO2能结合NH3的原因:
您最近一年使用:0次
2022-05-08更新
|
639次组卷
|
4卷引用:北京市广渠门中学2023-2024学年高三上学期开学考试化学试题
名校
解题方法
4 . 铁的多种化合物均为磁性材料,氮化铁(FexNy)是其中一种,某FexNy的制备需铁、氮气、丙酮和乙醇参与。
(1)Fe在元素周期表中的位置______ 。
(2)丙酮(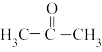 )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是______ ,1mol丙酮分子中含有σ键的数目为______ mol。
(3)乙醇的晶体类型为______ ,乙醇分子中C、O、H三种元素中电负性最大的元素是______ 。
(4)乙醇的沸点(78.3℃)高于丙酮的沸点(56.5℃),原因是______ 。
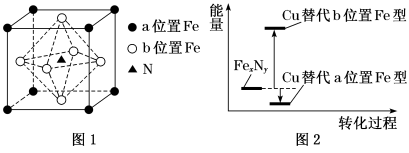
(5)某FexNy的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x−n)CunNy。由FexNy转化为两种Cu替代型产物的能量变化如图2所示,其中更稳定的Cu替代型产物的化学式为______ 。基态Cu原子的价电子轨道表示式为______ 。
(1)Fe在元素周期表中的位置
(2)丙酮(
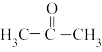 )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是(3)乙醇的晶体类型为
(4)乙醇的沸点(78.3℃)高于丙酮的沸点(56.5℃),原因是
(5)某FexNy的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x−n)CunNy。由FexNy转化为两种Cu替代型产物的能量变化如图2所示,其中更稳定的Cu替代型产物的化学式为

您最近一年使用:0次
2022-01-18更新
|
496次组卷
|
3卷引用:北京市第一七一中学2021-2022学年高三下学期开学考试化学试卷



