名校
解题方法
1 . 周期表中ⅢA族单质及其化合物应用广泛。BF3极易水解生成HBF4(HBF4在水中完全电离为H+和BF )和硼酸(H3BO3),硼酸是一元弱酸,能溶于水。硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯[B(OCH3)3],硼酸甲酯主要用作热稳定剂、木材防腐剂等。GaN的结构与晶体硅类似,是第三代半导体研究的热点。
)和硼酸(H3BO3),硼酸是一元弱酸,能溶于水。硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯[B(OCH3)3],硼酸甲酯主要用作热稳定剂、木材防腐剂等。GaN的结构与晶体硅类似,是第三代半导体研究的热点。
(1)Ga原子基态外围电子排布式为_____ 。
(2)在第二周期里,第一电离能介于B、N之间的元素有_____ 种;B(OCH3)3分子间_____ (填“能”或“不能”)能形成氢键,GaN属于_____ 晶体。
(3)硼酸是一元弱酸,它的水溶液之所以呈弱酸性并非本身能电离出H+,而是它结合了一个OH-,这种电离方式可表示为B(OH)3+H2O H++
H++_____ 。
(4)硼酸是一种片层状结构的白色晶体,层内的H3BO3分子通过氢键相连(如图)。下列有关说法正确的是_____(填字母)。

(5)Al2O3的熔点(2054℃)很高,工业冶炼铝时要加入冰晶石(化学式为Na3AlF6)来降低生产成本,如图所示为冰晶石的晶胞。图中“ ”位于大立方体顶点和面心,“
”位于大立方体顶点和面心,“ ”位于大立方体的12条棱的中点和8个小立方体的体心。则大立方体的体心处△代表的微粒是
”位于大立方体的12条棱的中点和8个小立方体的体心。则大立方体的体心处△代表的微粒是______ (填“Na+”或“AlF63-”),与Na+距离相等且最近的Na+有_____ 个。

 )和硼酸(H3BO3),硼酸是一元弱酸,能溶于水。硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯[B(OCH3)3],硼酸甲酯主要用作热稳定剂、木材防腐剂等。GaN的结构与晶体硅类似,是第三代半导体研究的热点。
)和硼酸(H3BO3),硼酸是一元弱酸,能溶于水。硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯[B(OCH3)3],硼酸甲酯主要用作热稳定剂、木材防腐剂等。GaN的结构与晶体硅类似,是第三代半导体研究的热点。(1)Ga原子基态外围电子排布式为
(2)在第二周期里,第一电离能介于B、N之间的元素有
(3)硼酸是一元弱酸,它的水溶液之所以呈弱酸性并非本身能电离出H+,而是它结合了一个OH-,这种电离方式可表示为B(OH)3+H2O
 H++
H++(4)硼酸是一种片层状结构的白色晶体,层内的H3BO3分子通过氢键相连(如图)。下列有关说法正确的是_____(填字母)。

| A.硼酸晶体的熔点比NaBF4低 |
| B.H3BO3分子的热稳定性与氢键有关 |
| C.含1molH3BO3的晶体中有3mol氢键 |
| D.BF3分子中每个原子最外层均满足8电子结构 |
(5)Al2O3的熔点(2054℃)很高,工业冶炼铝时要加入冰晶石(化学式为Na3AlF6)来降低生产成本,如图所示为冰晶石的晶胞。图中“
 ”位于大立方体顶点和面心,“
”位于大立方体顶点和面心,“ ”位于大立方体的12条棱的中点和8个小立方体的体心。则大立方体的体心处△代表的微粒是
”位于大立方体的12条棱的中点和8个小立方体的体心。则大立方体的体心处△代表的微粒是
您最近一年使用:0次
2023-12-11更新
|
198次组卷
|
2卷引用:重庆市万州二中2023-2024学年高二下学期开学考试 化学
名校
解题方法
2 . 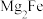 是目前储氢密度最高的材料之一,其晶胞结构如图所示,晶胞边长为
是目前储氢密度最高的材料之一,其晶胞结构如图所示,晶胞边长为 。
。 原子占据
原子占据 形成的所有四面体空隙,储氢后,
形成的所有四面体空隙,储氢后, 分子占据
分子占据 形成的八面体空隙,化学式为
形成的八面体空隙,化学式为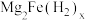

下列说法正确的是
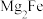 是目前储氢密度最高的材料之一,其晶胞结构如图所示,晶胞边长为
是目前储氢密度最高的材料之一,其晶胞结构如图所示,晶胞边长为 。
。 原子占据
原子占据 形成的所有四面体空隙,储氢后,
形成的所有四面体空隙,储氢后, 分子占据
分子占据 形成的八面体空隙,化学式为
形成的八面体空隙,化学式为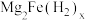

下列说法正确的是
A.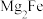 晶胞中, 晶胞中, 的配位数为4 的配位数为4 |
B.储氢时,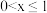 |
C.氢气储满后, 和 和 的最短距离为 的最短距离为 |
D.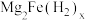 单位体积中含氢的质量的计算公式为 单位体积中含氢的质量的计算公式为 |
您最近一年使用:0次
2023-12-08更新
|
393次组卷
|
3卷引用:湖北省恩施土家族苗族自治州利川市第一中学2023-2024学年高二下学期开学化学试题
真题
名校
3 . 锆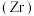 是重要的战略金属,可从其氧化物中提取。下图是某种锆的氧化物晶体的立方晶胞,
是重要的战略金属,可从其氧化物中提取。下图是某种锆的氧化物晶体的立方晶胞, 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是
 是重要的战略金属,可从其氧化物中提取。下图是某种锆的氧化物晶体的立方晶胞,
是重要的战略金属,可从其氧化物中提取。下图是某种锆的氧化物晶体的立方晶胞, 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是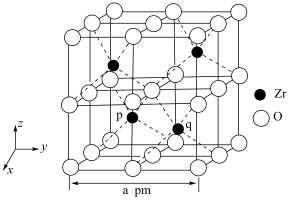
A.该氧化物的化学式为 |
B.该氧化物的密度为 |
C. 原子之间的最短距离为 原子之间的最短距离为 |
D.若坐标取向不变,将p点 原子平移至原点,则q点 原子平移至原点,则q点 原子位于晶胞 原子位于晶胞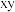 面的面心 面的面心 |
您最近一年使用:0次
2023-11-29更新
|
5022次组卷
|
10卷引用:山东省东营市第一中学2023-2024学年高二下学期开学收心考试化学试题
山东省东营市第一中学2023-2024学年高二下学期开学收心考试化学试题江西省宜春市高安市灰埠中学2023-2024学年高三上学期11月期中化学试题(已下线)选择题11-14(已下线)微题型02 晶体结构及相关计算-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)题型20 物质结构与性质基础-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)河北省石家庄市第十七中学2023-2024高二上学期期末考试化学试题湖北省沙市中学2023-2024学年高三下学期3月月考化学试题2023年河北省高考化学试卷四川省成都市石室中学2023-2024学年高二下学期4月月考化学试卷(已下线)选择题11-14
名校
解题方法
4 . 完成下列问题
(1)氨硼烷(NH3BH3)含氢量高、热稳定性好,是一种有潜力的固体储氢材料,回答问题:
①画出B的价电子轨道表示式___________ ;H、B、N中,原子半径最大的是___________ 。
② 分子中
分子中___________ (填“存在”或“不存在”)配位键。
③氨硼烷在一定条件下和水发生如下反应: ,
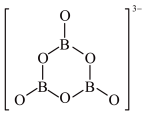
, 的结构如图,在该反应中,B原子的杂化轨道类型由
的结构如图,在该反应中,B原子的杂化轨道类型由___________ 变为___________ ;反应涉及的N、B、O三种元素的第一电离能从大到小的顺序为___________ 。
(2) 是碳元素的一种单质,因为其特殊的结构和性质而受到科学家的关注。如图是
是碳元素的一种单质,因为其特殊的结构和性质而受到科学家的关注。如图是 分子结构图和
分子结构图和 立方晶胞图。
立方晶胞图。
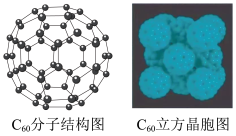
① 晶体属于
晶体属于___________ 晶体,每个 分子周围紧邻的分子数目为
分子周围紧邻的分子数目为___________ 个;
②凸多面体中有欧拉定理:顶点+面-棱边=2,则 分子中的五边形数目为
分子中的五边形数目为___________ ,六边形的数目为___________ ;
(3)许多气体可以在深海低温、高压的状态下,与水形成水合物晶体,其中可燃冰因为其良好的应用前景而备受关注,如图是天然气分子藏在水分子笼中的示意图。

天然气分子藏在水分子笼内
甲烷等分子是装在通过氢键相连的几个水分子构成的笼内。假设天然气水合物的化学式为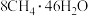 ,其密度为
,其密度为 ,把甲烷水合物从海底提升到海平面,
,把甲烷水合物从海底提升到海平面,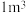 的固体理论上最多可释放标准状况下
的固体理论上最多可释放标准状况下___________  甲烷气体(列出计算式)。
甲烷气体(列出计算式)。
(1)氨硼烷(NH3BH3)含氢量高、热稳定性好,是一种有潜力的固体储氢材料,回答问题:
①画出B的价电子轨道表示式
②
 分子中
分子中③氨硼烷在一定条件下和水发生如下反应:
 ,
, 的结构如图,在该反应中,B原子的杂化轨道类型由
的结构如图,在该反应中,B原子的杂化轨道类型由
(2)
 是碳元素的一种单质,因为其特殊的结构和性质而受到科学家的关注。如图是
是碳元素的一种单质,因为其特殊的结构和性质而受到科学家的关注。如图是 分子结构图和
分子结构图和 立方晶胞图。
立方晶胞图。
①
 晶体属于
晶体属于 分子周围紧邻的分子数目为
分子周围紧邻的分子数目为②凸多面体中有欧拉定理:顶点+面-棱边=2,则
 分子中的五边形数目为
分子中的五边形数目为(3)许多气体可以在深海低温、高压的状态下,与水形成水合物晶体,其中可燃冰因为其良好的应用前景而备受关注,如图是天然气分子藏在水分子笼中的示意图。

天然气分子藏在水分子笼内
甲烷等分子是装在通过氢键相连的几个水分子构成的笼内。假设天然气水合物的化学式为
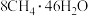 ,其密度为
,其密度为 ,把甲烷水合物从海底提升到海平面,
,把甲烷水合物从海底提升到海平面,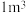 的固体理论上最多可释放标准状况下
的固体理论上最多可释放标准状况下 甲烷气体(列出计算式)。
甲烷气体(列出计算式)。
您最近一年使用:0次
名校
解题方法
5 . Ti和P的化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)Ti的四卤化物熔点如下表所示, 熔点高于其他三种卤化物,自
熔点高于其他三种卤化物,自 至
至 熔点依次升高,四种卤化物熔点变化的原因是
熔点依次升高,四种卤化物熔点变化的原因是___________ 。(已知:电负性:Ti 1.5;F 4.0;Cl 3.0;Br 2.8;I 2.5)
(2)钙钛矿(CaTiO3)型化合物是一类可用于生产太阳能电池、传感器等的功能材料。
①基态 原子的核外电子排布式为
原子的核外电子排布式为___________ 。
② 的晶胞如图甲所示,金属离子与氧离子间的作用力为
的晶胞如图甲所示,金属离子与氧离子间的作用力为___________ 。 的配位数是
的配位数是___________ 。 、
、 和有机碱离子
和有机碱离子 ,晶胞如图乙所示(与甲晶胞取法不同)。其中
,晶胞如图乙所示(与甲晶胞取法不同)。其中 与图甲中
与图甲中___________ 的空间位置相同。 的立体结构为
的立体结构为___________ 。
②磷酸通过分子间脱水缩合形成多磷酸,如:___________ 。
(1)Ti的四卤化物熔点如下表所示,
 熔点高于其他三种卤化物,自
熔点高于其他三种卤化物,自 至
至 熔点依次升高,四种卤化物熔点变化的原因是
熔点依次升高,四种卤化物熔点变化的原因是| 化合物 |  |  |  |  |
| 熔点/℃ | 377 | 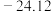 | 38.3 | 155 |
(2)钙钛矿(CaTiO3)型化合物是一类可用于生产太阳能电池、传感器等的功能材料。
①基态
 原子的核外电子排布式为
原子的核外电子排布式为②
 的晶胞如图甲所示,金属离子与氧离子间的作用力为
的晶胞如图甲所示,金属离子与氧离子间的作用力为 的配位数是
的配位数是
 、
、 和有机碱离子
和有机碱离子 ,晶胞如图乙所示(与甲晶胞取法不同)。其中
,晶胞如图乙所示(与甲晶胞取法不同)。其中 与图甲中
与图甲中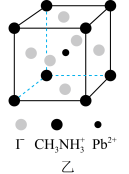
 的立体结构为
的立体结构为②磷酸通过分子间脱水缩合形成多磷酸,如:
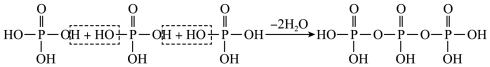
您最近一年使用:0次
名校
解题方法
6 . 回答下列问题
(1)下图为几种晶体或晶胞的示意图。
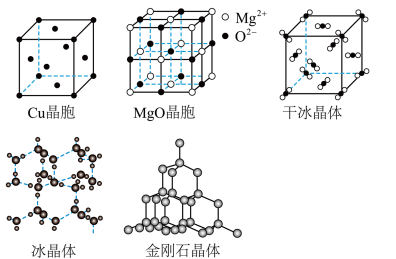
请回答下列问题:
① 上述晶体中,粒子之间以共价键结合形成的晶体是___________ 。
② 冰、金刚石、MgO、干冰4种晶体的熔点由高到低的顺序为___________ 。
③ MgO晶胞与NaCl晶胞相同,每个MgO晶胞中平均占有___________ 个Mg2+,由与Mg2+最近的O2-围成的空间几何构型为___________ 。
④ 干冰晶体中原子堆积方式如上图所示,每个CO2分子与___________ 个CO2分子紧邻。
(2)氯化亚铜(CuCl)广泛应用于冶金工业,也用作催化剂和杀菌剂。CuCl晶胞如图1所示,图2为晶胞沿y轴的投影1∶1平面图,注:a pm表示两个原子在投影平面上的核间距离,而非实际距离。
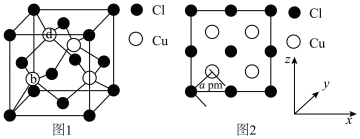
① 晶胞中Cl原子的配位数为___________ 。
②从核外电子排布角度解释高温下CuCl比CuCl2更稳定的原因___________ 。
③ 原子坐标参数表示晶胞内部各原子的相对位置,图中b位置原子的坐标参数为( ,
, ,
, ),则d位置原子的坐标参数为
),则d位置原子的坐标参数为___________ 。
④ 晶胞中最近的两个Cu原子之间的距离为___________ pm(用a来表示)。
(1)下图为几种晶体或晶胞的示意图。

请回答下列问题:
① 上述晶体中,粒子之间以共价键结合形成的晶体是
② 冰、金刚石、MgO、干冰4种晶体的熔点由高到低的顺序为
③ MgO晶胞与NaCl晶胞相同,每个MgO晶胞中平均占有
④ 干冰晶体中原子堆积方式如上图所示,每个CO2分子与
(2)氯化亚铜(CuCl)广泛应用于冶金工业,也用作催化剂和杀菌剂。CuCl晶胞如图1所示,图2为晶胞沿y轴的投影1∶1平面图,注:a pm表示两个原子在投影平面上的核间距离,而非实际距离。

① 晶胞中Cl原子的配位数为
②从核外电子排布角度解释高温下CuCl比CuCl2更稳定的原因
③ 原子坐标参数表示晶胞内部各原子的相对位置,图中b位置原子的坐标参数为(
 ,
, ,
, ),则d位置原子的坐标参数为
),则d位置原子的坐标参数为④ 晶胞中最近的两个Cu原子之间的距离为
您最近一年使用:0次
名校
解题方法
7 . 硒(Se)是一种有抗癌、抗氧化作用的元素,可形成多种化合物。某化合物是潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。

A.Se的基态原子价电子排布式为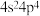 |
| B.该化合物的晶体类型是离子晶体 |
C.该化合物的化学式为 |
D.距离K最近的 八面体有4个 八面体有4个 |
您最近一年使用:0次
2023-11-06更新
|
791次组卷
|
8卷引用:黑龙江省大庆市大庆中学2023-2024学年高三下学期开学化学试题
8 . 2023年6月27日,我国工业与信息化部办公下达了2023年度国家工业节能监察任务的通知,其监察的重点为企业节能减排的落实情况。
(1)利用反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H,可减少CO2排放,并介成清洁能源。该反应一般认为可通过以下两步来实现:
CH3OH(g)+H2O(g) △H,可减少CO2排放,并介成清洁能源。该反应一般认为可通过以下两步来实现:
①CO2(g)+H2(g) H2O(g)+CO(g) △H1=+41kJ•mol-1
H2O(g)+CO(g) △H1=+41kJ•mol-1
②CO2(g)+2H2(g) CH3OH(g) △H2=-90kJ•mol-1
CH3OH(g) △H2=-90kJ•mol-1
则合成反应的△H=______ kJ•mol-1;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是______ (填标号)。
A. B.
B.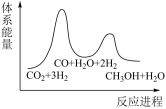
C. D.
D.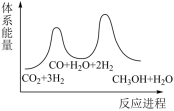
(2)500℃时,在2L的密闭容器中充入3molCO2和8molH2,发生CO2(g)+3H2(g) CH3OH(g)+H2O(g)。下列现象可以说明反应达到平衡的是
CH3OH(g)+H2O(g)。下列现象可以说明反应达到平衡的是______ 。
A.3 正(H2)=
正(H2)= 逆(H2O) B.气体平均相对分子质量不再改变
逆(H2O) B.气体平均相对分子质量不再改变
C.气体密度不再改变 D.CO2与H2的物质的量之比不再改变
测得t=5min时,反应达到平衡,此时c(CO2)=0.5mol/L,则从反应开始到平衡,CO2的平均反应速率 (CO2)=
(CO2)= ______ 。
(3)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为ZnO/ZrO2固溶体。已知ZrO2的熔点高达2700℃,四方ZrO2的晶胞如图所示:

ZrO2属于______ 晶体(选填“分子”或“离子”),若四方ZrO2的晶胞参数为apm,该晶体的密度为______ g•cm-3(写表达式,用NA表示阿伏加德罗常数)。在ZrO2中掺杂少量ZnO后形成的催化剂,化学式可表示为ZnxZr1-xOy,则y=______ (用含x的代数式表示)。
(1)利用反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H,可减少CO2排放,并介成清洁能源。该反应一般认为可通过以下两步来实现:
CH3OH(g)+H2O(g) △H,可减少CO2排放,并介成清洁能源。该反应一般认为可通过以下两步来实现:①CO2(g)+H2(g)
 H2O(g)+CO(g) △H1=+41kJ•mol-1
H2O(g)+CO(g) △H1=+41kJ•mol-1②CO2(g)+2H2(g)
 CH3OH(g) △H2=-90kJ•mol-1
CH3OH(g) △H2=-90kJ•mol-1则合成反应的△H=
A.
 B.
B.
C.
 D.
D.
(2)500℃时,在2L的密闭容器中充入3molCO2和8molH2,发生CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。下列现象可以说明反应达到平衡的是
CH3OH(g)+H2O(g)。下列现象可以说明反应达到平衡的是A.3
 正(H2)=
正(H2)= 逆(H2O) B.气体平均相对分子质量不再改变
逆(H2O) B.气体平均相对分子质量不再改变C.气体密度不再改变 D.CO2与H2的物质的量之比不再改变
测得t=5min时,反应达到平衡,此时c(CO2)=0.5mol/L,则从反应开始到平衡,CO2的平均反应速率
 (CO2)=
(CO2)= (3)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为ZnO/ZrO2固溶体。已知ZrO2的熔点高达2700℃,四方ZrO2的晶胞如图所示:

ZrO2属于
您最近一年使用:0次
解题方法
9 . 某离子晶体的晶胞是由M、N两种离子组成的正方体结构,晶胞参数为apm。该晶胞沿x轴在yz平面的投影如图2所示,沿体对角线方向的投影如图3所示(注:M离子用 表示,N离子用
表示,N离子用 表示,两种离子投影重合时用
表示,两种离子投影重合时用 表示)。下列说法错误的是
表示)。下列说法错误的是

 表示,N离子用
表示,N离子用 表示,两种离子投影重合时用
表示,两种离子投影重合时用 表示)。下列说法错误的是
表示)。下列说法错误的是
| A.该晶体的化学式可表示为MN |
| B.与N离子距离最近的N离子有8个 |
C.M离子与N离子之间的最近距离为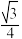 apm apm |
D.晶胞中其中一个N离子的分数坐标可能为( , , , , ) ) |
您最近一年使用:0次
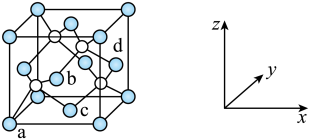
10 . ZnS晶体的晶胞如图所示(黑球代表 ,白球代表
,白球代表 )。原子坐标参数可表示晶胞内部各原子的相对位置,如图晶胞中,原子坐标参数a为
)。原子坐标参数可表示晶胞内部各原子的相对位置,如图晶胞中,原子坐标参数a为 ;b为
;b为 ;c为
;c为 。已知该晶体的密度为
。已知该晶体的密度为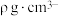 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。下列说法错误的是
。下列说法错误的是
 ,白球代表
,白球代表 )。原子坐标参数可表示晶胞内部各原子的相对位置,如图晶胞中,原子坐标参数a为
)。原子坐标参数可表示晶胞内部各原子的相对位置,如图晶胞中,原子坐标参数a为 ;b为
;b为 ;c为
;c为 。已知该晶体的密度为
。已知该晶体的密度为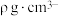 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。下列说法错误的是
。下列说法错误的是
| A.Zn位于元素周期表ds区 |
B. 在晶胞中的配位数是4 在晶胞中的配位数是4 |
C.d的坐标参数为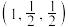 |
D.晶胞中最近的两个 之间的距离为 之间的距离为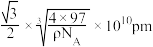 |
您最近一年使用:0次



