1 . 下列物质性质的比较,不正确的是
| A.微粒的半径:Al3+<Cl- | B.元素的电负性:P<S<Cl |
| C.共价晶体的硬度:晶体硅>金刚石 | D.离子晶体的熔点:NaCl>CsCl |
您最近一年使用:0次
解题方法
2 . 下面排序不正确的是
A.晶体的熔点由高到低排列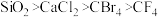 |
B.硬度由大到小:金刚石 碳化硅 碳化硅 晶体硅 晶体硅 |
C.熔点由高到低: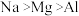 |
D.熔点由高到低: 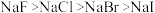 |
您最近一年使用:0次
解题方法
3 . CrSi、Ge—GaAs、ZnGeAs2和碳化硅都是重要的半导体化合物,下列说法错误的是
| A.基态铬原子的价电子排布式为3d54s1 |
| B.Ge—GaAs中元素Ge、Ga、As的第一电离能由大到小的顺序为As>Ga>Ge |
| C.ZnGeAs2中元素Zn、Ge、As的电负性由大到小的顺序为As>Ge>Zn |
| D.碳化硅属于原子晶体,其熔沸点均大于晶体硅 |
您最近一年使用:0次
2021-09-11更新
|
799次组卷
|
4卷引用:湖北省新高考联考协作体2021-2022学年高三上学期起点考试化学试题
4 . 碳化硅(SiC)俗称金刚砂,与金刚石具有相似的晶体结构,硬度为9.5,熔点为2700℃,其晶胞结构如图所示。下列说法错误的是


A.SiC晶体中碳原子和硅原子均采用 杂化 杂化 |
| B.距离硅原子最近的硅原子数为12 |
| C.金刚石的熔点低于2700℃ |
D.若晶胞参数为apm,则该晶体的密度为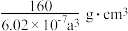 |
您最近一年使用:0次
2021-07-04更新
|
429次组卷
|
3卷引用:湖北省新高考联考协作体2020-2021高二下学期期末考试化学试题
5 . 开发新型储氢材料是氢能利用的重要研究方向。
(1) 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。
反应制得。
①基态原子Ti有_______ 种能量不同的电子,基态 的未成对电子有
的未成对电子有_______ 个。
② 由
由 和
和 构成,
构成, 的立体构型是
的立体构型是_______ 。
③Li、B、H元素的电负性由大到小排列顺序为_______ 。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径
_______ (填“ ”、“
”、“ ”或:“
”或:“ ”)
”) 。
。
②某储氢材料是短周期金属元素M的氢化物,M的部分电离能如下表所示:
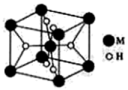
该储氢材料的化学式为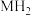 ,其晶胞结构如图所示。已知该晶体的密度
,其晶胞结构如图所示。已知该晶体的密度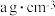 ,则该晶胞的体积为
,则该晶胞的体积为_______  [用a、
[用a、 表示(
表示( 为阿伏加德罗常数的值)]。
为阿伏加德罗常数的值)]。
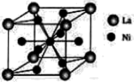
(3)氨硼烷与镧镍合金( )都是优良的储氢材料。
)都是优良的储氢材料。
①镧镍合金的晶胞结构示意图如下图所示(只有1个原子位于晶胞内部),则
_______ 。
②氦硼烷(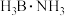 )在高温下释放氢后生成的立方氮化硼晶体,具有类似金刚石的结构,硬度略小于金刚石。则在下列各项中,立方氮化硼晶体不可用作
)在高温下释放氢后生成的立方氮化硼晶体,具有类似金刚石的结构,硬度略小于金刚石。则在下列各项中,立方氮化硼晶体不可用作_______ (填字母)。
a.耐磨材料 b.切削工具 c.导电材料 d.钻探钻头
(1)
 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。
反应制得。①基态原子Ti有
 的未成对电子有
的未成对电子有②
 由
由 和
和 构成,
构成, 的立体构型是
的立体构型是③Li、B、H元素的电负性由大到小排列顺序为
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径

 ”、“
”、“ ”或:“
”或:“ ”)
”) 。
。②某储氢材料是短周期金属元素M的氢化物,M的部分电离能如下表所示:
 |  |  |  | 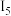 | |
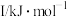 | 738 | 1451 | 7733 | 10540 | 13630 |
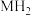 ,其晶胞结构如图所示。已知该晶体的密度
,其晶胞结构如图所示。已知该晶体的密度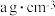 ,则该晶胞的体积为
,则该晶胞的体积为 [用a、
[用a、 表示(
表示( 为阿伏加德罗常数的值)]。
为阿伏加德罗常数的值)]。
(3)氨硼烷与镧镍合金(
 )都是优良的储氢材料。
)都是优良的储氢材料。①镧镍合金的晶胞结构示意图如下图所示(只有1个原子位于晶胞内部),则


②氦硼烷(
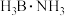 )在高温下释放氢后生成的立方氮化硼晶体,具有类似金刚石的结构,硬度略小于金刚石。则在下列各项中,立方氮化硼晶体不可用作
)在高温下释放氢后生成的立方氮化硼晶体,具有类似金刚石的结构,硬度略小于金刚石。则在下列各项中,立方氮化硼晶体不可用作a.耐磨材料 b.切削工具 c.导电材料 d.钻探钻头
您最近一年使用:0次
名校
解题方法
6 . 镓(Ga)、锗(Ge)、硅(Si)、硒(Se)的单质及某些化合物如砷化镓、磷化镓等都是常用的半导体材料,应用于航空航天测控、光纤通讯等领域。回答下列问题:
(1)硒常用作光敏材料,基态硒原子的核外电子排布式为_______ ;与硒同周期的p区元素中第一电离能大于硒的元素有_______ 种; 的空间构型是
的空间构型是_______ 。
(2)水晶的主要成分是二氧化硅,在水晶中硅原子的配位数是_______ 。硅与氢结合能形成一系列的二元化合物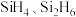 等,与氯、溴结合能形成
等,与氯、溴结合能形成 ,上述四种物质沸点由高到低顺序为
,上述四种物质沸点由高到低顺序为_______ ,丁硅烯 中
中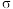 键与
键与 键个数之比为
键个数之比为_______ 。
(3)GaN、GaP、GaAs都是原子晶体,熔点如表所示,分析其熔点变化的原因_______ 。
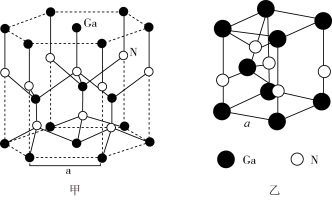
(4)GaN晶胞结构如图甲所示。已知六棱柱底边边长为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。从GaN晶体中分割出的平行六面体如图乙,该平行六面体的高为
。从GaN晶体中分割出的平行六面体如图乙,该平行六面体的高为 ,GaN晶体的密度为
,GaN晶体的密度为_______  (用
(用 表示)。
表示)。
(1)硒常用作光敏材料,基态硒原子的核外电子排布式为
 的空间构型是
的空间构型是(2)水晶的主要成分是二氧化硅,在水晶中硅原子的配位数是
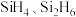 等,与氯、溴结合能形成
等,与氯、溴结合能形成 ,上述四种物质沸点由高到低顺序为
,上述四种物质沸点由高到低顺序为 中
中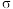 键与
键与 键个数之比为
键个数之比为(3)GaN、GaP、GaAs都是原子晶体,熔点如表所示,分析其熔点变化的原因
| GaN | GaP | GaAs | |
| 熔点 | 1700℃ | 1480℃ | 1238℃ |
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。从GaN晶体中分割出的平行六面体如图乙,该平行六面体的高为
。从GaN晶体中分割出的平行六面体如图乙,该平行六面体的高为 ,GaN晶体的密度为
,GaN晶体的密度为 (用
(用 表示)。
表示)。
您最近一年使用:0次
2021-03-08更新
|
904次组卷
|
4卷引用:湖北省罗田县第一中学2021-2022学年高二下学期3月月考化学试题
名校
7 . 下列有关金刚石晶体和二氧化硅晶体(如图所示)的叙述正确的是
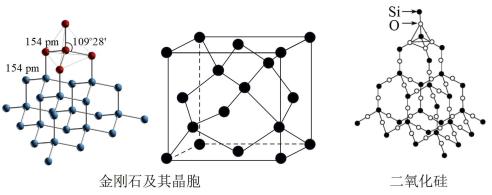

| A.金刚石晶体和二氧化硅晶体均属于原子晶体 |
| B.金刚石晶胞中含有6个碳原子 |
C.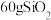 晶体中所含共价键数目为 晶体中所含共价键数目为 ( ( 是阿伏加德罗常数的值) 是阿伏加德罗常数的值) |
| D.金刚石晶体熔化时破坏共价键,二氧化硅晶体熔化时破坏分子间作用力 |
您最近一年使用:0次
2021-03-05更新
|
903次组卷
|
7卷引用:2021年高考化学押题预测卷(湖北卷)03(含考试版、答题卡、参考答案、全解全析)
(已下线)2021年高考化学押题预测卷(湖北卷)03(含考试版、答题卡、参考答案、全解全析)湖北省武汉市洪山高级中学2022-2023学年高二下学期2月考试化学试题辽宁省名校联盟2021届高三下学期开学考试(新高考)化学试题江苏省常州市礼嘉中学2020-2021学年高二下学期第二次阶段质量调研化学试题专题3 微粒间作用力与物质性质 第三单元 共价键共价晶体 第2课时 共价键的键能与化学反应的反应热 共价晶体(已下线)3.2.2 共价晶体-同步学习必备知识3.3.2共价晶体 课后
解题方法
8 . 下列有关比较,正确的是
A.在水中的溶解度: | B.沸点: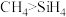 |
| C.熔点:晶体硅>金刚石 | D.键角: |
您最近一年使用:0次
2021-02-23更新
|
320次组卷
|
2卷引用:湖北省武汉市部分重点中学2020-2021学年高二下学期期中考试化学试题
解题方法
9 . 回答下列问题。
(1)SO2与O3互为等电子体。SO2的VSEPR模型名称是_____ ,与O3分子互为等电子体的一种阴离子为(写化学式)______ 。
(2)氯化钠和氯化铯是两种不同类型的晶体结构。晶体结构不同的主要原因是______ 。
(3)SiO2 和GeO2具有类似的晶体结构,其中熔点较高的是______ (写化学式),原因是_____ 。
(4)向盛有氯化银的试管中加入氨水,沉淀溶解。请写出反应的化学方程式:______ 。
(1)SO2与O3互为等电子体。SO2的VSEPR模型名称是
(2)氯化钠和氯化铯是两种不同类型的晶体结构。晶体结构不同的主要原因是
(3)SiO2 和GeO2具有类似的晶体结构,其中熔点较高的是
(4)向盛有氯化银的试管中加入氨水,沉淀溶解。请写出反应的化学方程式:
您最近一年使用:0次
10 . 下列物质之间的关系与微粒半径大小无关的是
A.熔点: | B.熔点:金刚石>硅单质 |
| C.沸点:水晶>氯化锂 | D.热分解所需温度: |
您最近一年使用:0次



