名校
解题方法
1 . 某研究小组以硫化铜精矿(含 、
、 元素的杂质)为主要原料制备
元素的杂质)为主要原料制备 粉,其流程如下:
粉,其流程如下: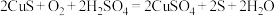 。
。
②金属氢氧化物开始沉淀和沉淀完全的 如下表所示。
如下表所示。
回答下列问题:
(1)步骤I中通入 采用高压的原因是
采用高压的原因是___________ 。
(2)下列说法正确的是___________(填字母)。
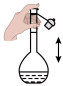
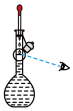
(3)步骤I、Ⅲ需要使用高压反应釜装置(如图)。步骤Ⅲ中,首先关闭出气口,向高压反应釜中通入固定流速的 ,然后通过控制气阀
,然后通过控制气阀 或
或 ,维持反应釜中的压强为
,维持反应釜中的压强为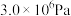 。请给出反应过程中的操作排序:
。请给出反应过程中的操作排序:___________ 。
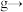 _____
_____ _____
_____ _____
_____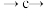 _____。
_____。 b.开启气阀
b.开启气阀 ,通入高压
,通入高压 c.关闭气阀
c.关闭气阀
d.开启气阀 e.开启气阀
e.开启气阀 ,通入高压
,通入高压 f.关闭气阀
f.关闭气阀
g.开启搅拌器 h.拆下罐体
(4)步骤Ⅲ中高压 可以从滤液中置换出金属
可以从滤液中置换出金属 ,而无法置换出金属
,而无法置换出金属 。请结合方程式说明其原因:
。请结合方程式说明其原因:___________ 。
(5)现取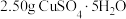 样品,加热分解,分解过程的热重曲线(样品质量随温度变化的曲线)如图所示。生成
样品,加热分解,分解过程的热重曲线(样品质量随温度变化的曲线)如图所示。生成 的温度范围为
的温度范围为___________ , 时发生反应的化学方程式为
时发生反应的化学方程式为___________ 。
 、
、 元素的杂质)为主要原料制备
元素的杂质)为主要原料制备 粉,其流程如下:
粉,其流程如下:
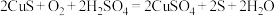 。
。②金属氢氧化物开始沉淀和沉淀完全的
 如下表所示。
如下表所示。| 金属氢氧化物 |  |  |  |
开始沉淀的 | 1.9 | 4.2 | 6.2 |
沉淀完全的 | 3.2 | 6.7 | 8.2 |
(1)步骤I中通入
 采用高压的原因是
采用高压的原因是(2)下列说法正确的是___________(填字母)。
| A.步骤I中过滤得到的滤渣中含有S |
B.步骤Ⅱ中用 调节 调节 约至4,使 约至4,使 、 、 沉淀完全 沉淀完全 |
C.步骤Ⅲ中增大溶液的酸度不利于 生成 生成 |
| D.为加快过滤速率,需用玻璃棒对漏斗中的沉淀进行充分搅拌 |
(3)步骤I、Ⅲ需要使用高压反应釜装置(如图)。步骤Ⅲ中,首先关闭出气口,向高压反应釜中通入固定流速的
 ,然后通过控制气阀
,然后通过控制气阀 或
或 ,维持反应釜中的压强为
,维持反应釜中的压强为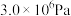 。请给出反应过程中的操作排序:
。请给出反应过程中的操作排序: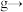 _____
_____ _____
_____ _____
_____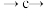 _____。
_____。
 b.开启气阀
b.开启气阀 ,通入高压
,通入高压 c.关闭气阀
c.关闭气阀
d.开启气阀
 e.开启气阀
e.开启气阀 ,通入高压
,通入高压 f.关闭气阀
f.关闭气阀
g.开启搅拌器 h.拆下罐体
(4)步骤Ⅲ中高压
 可以从滤液中置换出金属
可以从滤液中置换出金属 ,而无法置换出金属
,而无法置换出金属 。请结合方程式说明其原因:
。请结合方程式说明其原因:(5)现取
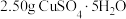 样品,加热分解,分解过程的热重曲线(样品质量随温度变化的曲线)如图所示。生成
样品,加热分解,分解过程的热重曲线(样品质量随温度变化的曲线)如图所示。生成 的温度范围为
的温度范围为 时发生反应的化学方程式为
时发生反应的化学方程式为
您最近一年使用:0次
2024-06-02更新
|
200次组卷
|
3卷引用:广东省华南师范大学附属中学2024届高三下学期高考适应性练习(4月)化学试题
广东省华南师范大学附属中学2024届高三下学期高考适应性练习(4月)化学试题(已下线)江苏省南京市第十三中学2024届高三下学期适应性考试化学试题甘肃省陇南市部分学校2023-2024学年高三下学期化学押题考试(三模)化学试题
名校
解题方法
2 . 催化裂化(FCC)是石油精炼中最重要的转化之一、FCC催化剂中含有多种金属元素,一种针对FCC废催化剂(含较多的CeO2、铁铝的氧化物和少量其他可溶于酸的物质,固载在玻璃纤维上)综合回收利用的工艺流程如下:
回答下列问题:
(1)已知基态Ce原子价层电子排布式为4f15d16s2,它有___________ 个未成对电子,它的最高正化合价为___________ 。
(2)物质X为___________ ,若利用pH传感器监测反应2,当pH=___________ 时,Fe3+已沉淀完全(c(Fe3+)≤1×10-5时视为沉淀完全)。
(3)反应3的化学反应方程式为___________ ,其中H2O2的作用与反应1中的H2O2作用___________ (填“相同”或“不相同”)。H2O2中O的杂化方式为___________ 杂化。
(4)从溶液中获得NH4Al(SO4)2·H2O晶体的“一系列操作”包括___________ 、过滤、洗涤、常温晾干。
(5)氧化铈(CeO2)是一种重要的光催化材料,光催化过程中立方晶胞的组成变化如图所示,则每个CeO2-x晶胞中Ce4+个数为___________ 。

回答下列问题:
(1)已知基态Ce原子价层电子排布式为4f15d16s2,它有
(2)物质X为
(3)反应3的化学反应方程式为
(4)从溶液中获得NH4Al(SO4)2·H2O晶体的“一系列操作”包括
(5)氧化铈(CeO2)是一种重要的光催化材料,光催化过程中立方晶胞的组成变化如图所示,则每个CeO2-x晶胞中Ce4+个数为

您最近一年使用:0次
3 . 实现废钨-镍型加氢催化剂(主要成分为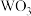 、
、 、
、 ,还含有
,还含有 、
、 和少量含S有机物)中有价值金属回收的工艺流程如下。
和少量含S有机物)中有价值金属回收的工艺流程如下。
(1) ,纯碱不与
,纯碱不与 、
、 反应。
反应。
(2)相关金属离子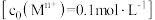 形成氢氧化物沉淀的
形成氢氧化物沉淀的 范围如下:
范围如下:
回答下列问题:
(1)基态 的价层电子排布式为
的价层电子排布式为___________ 。
(2)“氧化”的目的为___________ 和将金属单质氧化至相应的价态。
(3)“钠化焙烧”中生成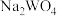 的化学方程式为
的化学方程式为___________ 。
(4)“酸化沉钨”后过滤,所得滤饼的主要成分为___________ (填化学式)。
(5)“调 除铁和铝,溶液的
除铁和铝,溶液的 范围应调节为
范围应调节为___________ 。
(6)资料显示,硫酸镍结晶水合物的形态与温度有如表关系。
“一系列操作”依次是___________ 、及时过滤、洗涤、干燥。
(7)强碱溶液中 氧化
氧化 ,可沉淀出用作电池正极材料的
,可沉淀出用作电池正极材料的 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(8)某笼形络合物 结构中,镍离子与
结构中,镍离子与 连接形成平面层,两个平面层通过
连接形成平面层,两个平面层通过 分子连接,所有N原子均参与形成配位键,中间的空隙填充大小合适的分子(如
分子连接,所有N原子均参与形成配位键,中间的空隙填充大小合适的分子(如 ), 其基本结构如图H原子未画出)。
), 其基本结构如图H原子未画出)。
①
___________ 。
②晶胞的密度为___________  (用代数式表示)。
(用代数式表示)。
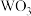 、
、 、
、 ,还含有
,还含有 、
、 和少量含S有机物)中有价值金属回收的工艺流程如下。
和少量含S有机物)中有价值金属回收的工艺流程如下。
(1)
 ,纯碱不与
,纯碱不与 、
、 反应。
反应。(2)相关金属离子
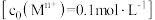 形成氢氧化物沉淀的
形成氢氧化物沉淀的 范围如下:
范围如下:| 金属离子 |  |  |  |
开始沉淀时的 | 6.9 | 3.4 | 1.5 |
沉淀完全时的 | 8.9 | 4.7 | 2.8 |
(1)基态
 的价层电子排布式为
的价层电子排布式为(2)“氧化”的目的为
(3)“钠化焙烧”中生成
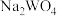 的化学方程式为
的化学方程式为(4)“酸化沉钨”后过滤,所得滤饼的主要成分为
(5)“调
 除铁和铝,溶液的
除铁和铝,溶液的 范围应调节为
范围应调节为(6)资料显示,硫酸镍结晶水合物的形态与温度有如表关系。
| 温度 | 低于 |  |  | 高于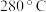 |
| 晶体形态 |  | 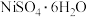 | 多种结晶水合物 |  |
(7)强碱溶液中
 氧化
氧化 ,可沉淀出用作电池正极材料的
,可沉淀出用作电池正极材料的 ,该反应的离子方程式为
,该反应的离子方程式为(8)某笼形络合物
 结构中,镍离子与
结构中,镍离子与 连接形成平面层,两个平面层通过
连接形成平面层,两个平面层通过 分子连接,所有N原子均参与形成配位键,中间的空隙填充大小合适的分子(如
分子连接,所有N原子均参与形成配位键,中间的空隙填充大小合适的分子(如 ), 其基本结构如图H原子未画出)。
), 其基本结构如图H原子未画出)。
①

②晶胞的密度为
 (用代数式表示)。
(用代数式表示)。
您最近一年使用:0次
4 . 工业上用红土镍矿(主要成分为NiO,含CoO、FeO、 、
、 、MgO、CaO和
、MgO、CaO和 )制备
)制备 。工艺流程如图所示,回答下列问题:
。工艺流程如图所示,回答下列问题: 在高压下进行酸浸。充分浸取后过滤出的酸浸渣的主要成分为
在高压下进行酸浸。充分浸取后过滤出的酸浸渣的主要成分为______ (填化学式)。
(2)由 溶液获取
溶液获取 的操作是
的操作是______ 、______ 、过滤、洗涤。
(3)沉镁沉钙加入NaF溶液,生成 和
和 若沉淀前溶液中
若沉淀前溶液中 ,当沉淀完全后滤液中
,当沉淀完全后滤液中 时,除钙率为
时,除钙率为______ (忽略沉淀前后溶液体积变化)。(已知: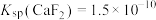 、
、 )
)
(4)“萃取”可将金属离子进行富集与分离,原理如下:
 。工业上用
。工业上用 磺化煤油做萃取剂,萃取时,Co、Ni的浸出率和Co/Ni分离因素随pH的关系如图所示:
磺化煤油做萃取剂,萃取时,Co、Ni的浸出率和Co/Ni分离因素随pH的关系如图所示:______ 左右。
②反萃取的试剂为______ 。
(5)氧化、沉铁沉铝时,需加入NaClO溶液起氧化作用。写出 与NaClO在碱性条件下发生反应的离子方程式:
与NaClO在碱性条件下发生反应的离子方程式:______ 。
(6) 中阴离子的空间构型为
中阴离子的空间构型为______ 。
 、
、 、MgO、CaO和
、MgO、CaO和 )制备
)制备 。工艺流程如图所示,回答下列问题:
。工艺流程如图所示,回答下列问题:
 在高压下进行酸浸。充分浸取后过滤出的酸浸渣的主要成分为
在高压下进行酸浸。充分浸取后过滤出的酸浸渣的主要成分为(2)由
 溶液获取
溶液获取 的操作是
的操作是(3)沉镁沉钙加入NaF溶液,生成
 和
和 若沉淀前溶液中
若沉淀前溶液中 ,当沉淀完全后滤液中
,当沉淀完全后滤液中 时,除钙率为
时,除钙率为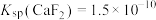 、
、 )
)(4)“萃取”可将金属离子进行富集与分离,原理如下:

 。工业上用
。工业上用 磺化煤油做萃取剂,萃取时,Co、Ni的浸出率和Co/Ni分离因素随pH的关系如图所示:
磺化煤油做萃取剂,萃取时,Co、Ni的浸出率和Co/Ni分离因素随pH的关系如图所示: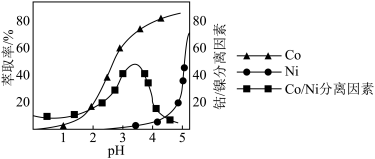
②反萃取的试剂为
(5)氧化、沉铁沉铝时,需加入NaClO溶液起氧化作用。写出
 与NaClO在碱性条件下发生反应的离子方程式:
与NaClO在碱性条件下发生反应的离子方程式:(6)
 中阴离子的空间构型为
中阴离子的空间构型为
您最近一年使用:0次
5 . 一种从工业锌置换渣(主要含 等)中回收锗、铅的工艺流程如图:
等)中回收锗、铅的工艺流程如图: 能溶于强酸的浓溶液或强碱溶液;
能溶于强酸的浓溶液或强碱溶液; 可溶于热盐酸中:
可溶于热盐酸中: ;常温下,
;常温下,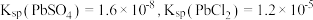 。
。
(1)“还原浸出”时, 的存在可促进
的存在可促进 浸出。
浸出。
① 的空间结构为
的空间结构为___________ 。
②该反应中氧化剂与还原剂的物质的量之比为___________ 。
(2)“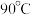 酸浸”所用盐酸的浓度不宜过大或过小,浓度不宜过大的主要原因是
酸浸”所用盐酸的浓度不宜过大或过小,浓度不宜过大的主要原因是___________ 。
(3)“碱溶”时, 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(4)“降温析铅”过程中,体系温度冷却至常温,且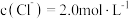 。为防止
。为防止 中混有
中混有 杂质,应控制溶液中
杂质,应控制溶液中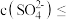
___________ 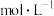 (保留两位有效数字)。
(保留两位有效数字)。
(5)“转化”的意义在于可重复利用___________ (填物质名称)。
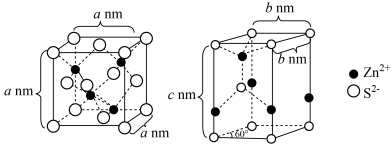
(6)通过掺杂硅可将锗单质转化为不同掺杂比例的硅锗合金,锗及硅锗合金的立方晶胞如图所示。 周围与其最近的
周围与其最近的 的个数为
的个数为___________ 。
②若硅锗合金i的晶胞边长为 ,设
,设 为阿伏加德罗常数的值,则硅锗合金i晶体的密度为
为阿伏加德罗常数的值,则硅锗合金i晶体的密度为___________  (列计算式)。
(列计算式)。
③硅锗合金ii沿晶胞对角面取得的截图为___________ (填标号)。
 等)中回收锗、铅的工艺流程如图:
等)中回收锗、铅的工艺流程如图: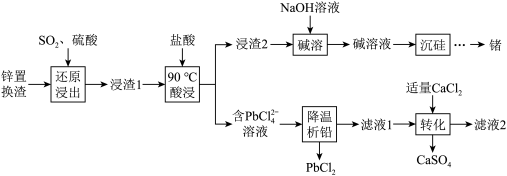
 能溶于强酸的浓溶液或强碱溶液;
能溶于强酸的浓溶液或强碱溶液; 可溶于热盐酸中:
可溶于热盐酸中: ;常温下,
;常温下,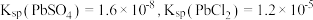 。
。(1)“还原浸出”时,
 的存在可促进
的存在可促进 浸出。
浸出。①
 的空间结构为
的空间结构为②该反应中氧化剂与还原剂的物质的量之比为
(2)“
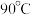 酸浸”所用盐酸的浓度不宜过大或过小,浓度不宜过大的主要原因是
酸浸”所用盐酸的浓度不宜过大或过小,浓度不宜过大的主要原因是(3)“碱溶”时,
 发生反应的离子方程式为
发生反应的离子方程式为(4)“降温析铅”过程中,体系温度冷却至常温,且
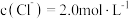 。为防止
。为防止 中混有
中混有 杂质,应控制溶液中
杂质,应控制溶液中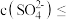
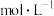 (保留两位有效数字)。
(保留两位有效数字)。(5)“转化”的意义在于可重复利用
(6)通过掺杂硅可将锗单质转化为不同掺杂比例的硅锗合金,锗及硅锗合金的立方晶胞如图所示。
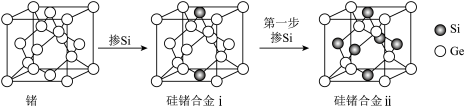
 周围与其最近的
周围与其最近的 的个数为
的个数为②若硅锗合金i的晶胞边长为
 ,设
,设 为阿伏加德罗常数的值,则硅锗合金i晶体的密度为
为阿伏加德罗常数的值,则硅锗合金i晶体的密度为 (列计算式)。
(列计算式)。③硅锗合金ii沿晶胞对角面取得的截图为
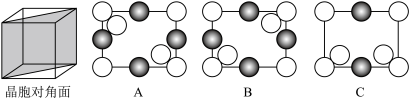
您最近一年使用:0次
解题方法
6 . 金属铼广泛用于航空航天等领域。以钼精矿(主要成分为钼的硫化物和少量铼的硫化物)制取高铼酸铵晶体的流程如下图所示。回答下列问题:___________ 。
(2)①“焙烧”常采用高压空气、逆流操作(空气从培烧炉下部通入,矿粉从中上部加入),其目的是___________ 。
②“焙烧”过程中 转化为
转化为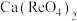 ,反应方程式
,反应方程式
___________ 。
(3)“萃取”机理为: ,则“反萃取”对应的离子方程式为
,则“反萃取”对应的离子方程式为___________ ;常温下,“反萃取”得到高铼酸铵溶液的 ,则溶液中
,则溶液中
___________ 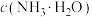 (填“>”“<”或“=”)。(已知:常温下
(填“>”“<”或“=”)。(已知:常温下 )
)
(4)下图是 的X射线衍射图谱,则
的X射线衍射图谱,则 属于
属于___________ 。(填“晶体”或“非晶体”)___________ 。
(6)三氧化铼是简单立方晶胞,晶胞结构如下图所示,摩尔质量为Mg/mol,晶胞密度为 。铼原子填在氧原子围成的
。铼原子填在氧原子围成的___________ (填“四面体”“立方体”或“八面体”)空隙中,该晶胞中两个相距最近的O原子间的距离为___________ cm。(列出计算式)

(2)①“焙烧”常采用高压空气、逆流操作(空气从培烧炉下部通入,矿粉从中上部加入),其目的是
②“焙烧”过程中
 转化为
转化为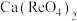 ,反应方程式
,反应方程式
(3)“萃取”机理为:
 ,则“反萃取”对应的离子方程式为
,则“反萃取”对应的离子方程式为 ,则溶液中
,则溶液中
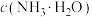 (填“>”“<”或“=”)。(已知:常温下
(填“>”“<”或“=”)。(已知:常温下 )
)(4)下图是
 的X射线衍射图谱,则
的X射线衍射图谱,则 属于
属于

表1 | ||
| 物质 | 熔点(℃) | 沸点(℃) |
 | 3180 | 5900 |
| C | 3652 | 4827 |
 | 1535 | 2750 |
(6)三氧化铼是简单立方晶胞,晶胞结构如下图所示,摩尔质量为Mg/mol,晶胞密度为
 。铼原子填在氧原子围成的
。铼原子填在氧原子围成的
您最近一年使用:0次
7 . 铼(Re)用于制造高效能火箭引擎。从辉钼矿氧化焙烧后的烟道灰(主要成分有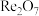 、
、 、
、 、CuO、
、CuO、 )中提取铼粉的一种工艺流程如图所示。
)中提取铼粉的一种工艺流程如图所示。
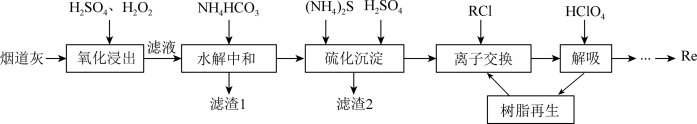
已知:
回答下列问题:
(1)“氧化浸出”时, 被氧化为
被氧化为 ,
, 被氧化的离子方程式为
被氧化的离子方程式为___________ 。
(2)“水解中和”时,加 调节溶液pH=6。
调节溶液pH=6。
① 溶液中
溶液中
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
②除钼的化合物外,滤渣1中还有___________ (填化学式)。
③计算此时溶液中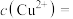
___________  。
。
(3)“硫化沉淀”时,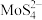 与
与 反应生成难溶的
反应生成难溶的 ,离子方程式为
,离子方程式为___________ 。
(4)“离子交换”“解吸”“树脂再生”一系列步骤中物质转化关系如图所示。
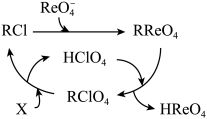
①树脂再生时需加入的试剂X为___________ (填化学式)。
②“解吸”所用 中的阴离子的空间构型为
中的阴离子的空间构型为___________ 。
(5)铼的某种氧化物的晶胞如图所示,该物质的化学式为___________ 。铼原子填在氧原子围成的___________ (填“四面体”、“立方体”或“八面体”)空隙中。

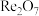 、
、 、
、 、CuO、
、CuO、 )中提取铼粉的一种工艺流程如图所示。
)中提取铼粉的一种工艺流程如图所示。
已知:
 |  |  | |
| 开始沉淀pH | 2.5 | 7.0 | 5.7 |
| 完全沉淀pH | 3.2 | 9.0 | 6.7 |
(1)“氧化浸出”时,
 被氧化为
被氧化为 ,
, 被氧化的离子方程式为
被氧化的离子方程式为(2)“水解中和”时,加
 调节溶液pH=6。
调节溶液pH=6。①
 溶液中
溶液中
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。②除钼的化合物外,滤渣1中还有
③计算此时溶液中
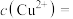
 。
。(3)“硫化沉淀”时,
 与
与 反应生成难溶的
反应生成难溶的 ,离子方程式为
,离子方程式为(4)“离子交换”“解吸”“树脂再生”一系列步骤中物质转化关系如图所示。

①树脂再生时需加入的试剂X为
②“解吸”所用
 中的阴离子的空间构型为
中的阴离子的空间构型为(5)铼的某种氧化物的晶胞如图所示,该物质的化学式为

您最近一年使用:0次
解题方法
8 . 硫代乙醇酸( )可用作毛毯整理剂及冷烫液的原料,工业上可利用反应
)可用作毛毯整理剂及冷烫液的原料,工业上可利用反应 制备,实验室设计如图装置进行相关模拟实验(夹持装置省略)。
制备,实验室设计如图装置进行相关模拟实验(夹持装置省略)。 (熔点-16.5℃、沸点123℃)在空气中迅速被氧化,在较高温度下受热分解产生有毒的硫化物烟气。
(熔点-16.5℃、沸点123℃)在空气中迅速被氧化,在较高温度下受热分解产生有毒的硫化物烟气。
回答下列问题:
(1) 可通过以下反应制备:
可通过以下反应制备: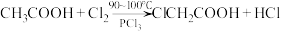 。
。
①简述 小于
小于 的原因:
的原因:___________ 。
② 属于
属于___________ (填“极性”或“非极性”)分子。
(2)该实验需要250mL 10mol/L NaOH溶液,配制该溶液时,下列操作正确的是___________ (填标号)。
(3)检查完气密性后,关闭 、
、 、
、 ,添加实验药品,先制备NaHS。
,添加实验药品,先制备NaHS。
①制备 时,打开
时,打开 ,使25%磷酸缓缓滴入
,使25%磷酸缓缓滴入 浓溶液中,缓缓滴加的优点是
浓溶液中,缓缓滴加的优点是___________ 。
②实验时不能用25%硝酸代替装置A中25%磷酸的原因是___________ 。
③装置C的作用是___________ 。
④装置D中多孔球泡的作用是___________ ;写出装置D中刚开始反应的离子方程式:___________ 。
⑤经过一系列分离提纯可获得 粗品,提纯
粗品,提纯 需要采取减压精馏的原因是
需要采取减压精馏的原因是___________ 。
 )可用作毛毯整理剂及冷烫液的原料,工业上可利用反应
)可用作毛毯整理剂及冷烫液的原料,工业上可利用反应 制备,实验室设计如图装置进行相关模拟实验(夹持装置省略)。
制备,实验室设计如图装置进行相关模拟实验(夹持装置省略)。
 (熔点-16.5℃、沸点123℃)在空气中迅速被氧化,在较高温度下受热分解产生有毒的硫化物烟气。
(熔点-16.5℃、沸点123℃)在空气中迅速被氧化,在较高温度下受热分解产生有毒的硫化物烟气。回答下列问题:
(1)
 可通过以下反应制备:
可通过以下反应制备: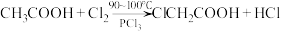 。
。①简述
 小于
小于 的原因:
的原因:②
 属于
属于(2)该实验需要250mL 10mol/L NaOH溶液,配制该溶液时,下列操作正确的是
| 操作 |
|
|
|
|
| 选项 | a | b | c | d |
(3)检查完气密性后,关闭
 、
、 、
、 ,添加实验药品,先制备NaHS。
,添加实验药品,先制备NaHS。①制备
 时,打开
时,打开 ,使25%磷酸缓缓滴入
,使25%磷酸缓缓滴入 浓溶液中,缓缓滴加的优点是
浓溶液中,缓缓滴加的优点是②实验时不能用25%硝酸代替装置A中25%磷酸的原因是
③装置C的作用是
④装置D中多孔球泡的作用是
⑤经过一系列分离提纯可获得
 粗品,提纯
粗品,提纯 需要采取减压精馏的原因是
需要采取减压精馏的原因是
您最近一年使用:0次
解题方法
9 . 碘是生物必需的一种微量元素,海带、海藻等食物含碘量最为丰富.某小组通过实验提取并测定干海带中碘的含量.回答下列问题:
Ⅰ.从海带中提取碘.该小组同学按如图实验流程进行实验:______ (填仪器名称)。______ (用离子方程式表示)。
Ⅱ.滴定法测海带中碘的含量。
用 滴定
滴定 的水溶液,淀粉溶液作指示剂。原理为:
的水溶液,淀粉溶液作指示剂。原理为: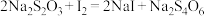 ,
,
(3)用酸式滴定管量取 的水溶液时常需要排出气泡,操作是
的水溶液时常需要排出气泡,操作是__________ 。
(4)小组同学进行了实验测定,在滴定终点附近,反复变回蓝色,一直测不到终点。
猜想1:碘离子被______ 氧化;
猜想2:碘离子被步骤iii中过量的 氧化;
氧化;
②验证猜想
③查阅资料 小组同学认为可能是反应速率不同造成的, 氧化
氧化 的速率
的速率______ (填“快于”或“慢于”) 还原
还原 的速率,导致待测液反复变为蓝色。
的速率,导致待测液反复变为蓝色。
④优化设计 鉴于反应终点无法到达的问题,请提出合理的修正方案____________ 。
⑤完成实验 小组同学修正方案后,取5.000 g干海带进行测定,消耗15.75 mL
 溶液,则干海带中碘的含量为
溶液,则干海带中碘的含量为______ mg/g(保留2位有效数字)。
Ⅰ.从海带中提取碘.该小组同学按如图实验流程进行实验:

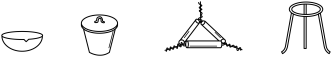
Ⅱ.滴定法测海带中碘的含量。
用
 滴定
滴定 的水溶液,淀粉溶液作指示剂。原理为:
的水溶液,淀粉溶液作指示剂。原理为: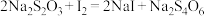 ,
,(3)用酸式滴定管量取
 的水溶液时常需要排出气泡,操作是
的水溶液时常需要排出气泡,操作是(4)小组同学进行了实验测定,在滴定终点附近,反复变回蓝色,一直测不到终点。

猜想1:碘离子被
猜想2:碘离子被步骤iii中过量的
 氧化;
氧化;②验证猜想
| 序号 | 实验操作 | 实验现象 | 结论 |
| 1 | 取少量原海带浸出液,加入硫酸酸化,再滴加几滴淀粉溶液,鼓入空气 | 待测液始终保持无色 | 猜想1不成立 |
| 2 | 将2mL KI溶液、2滴 KI溶液、2滴  溶液、2滴淀粉溶液和1滴 溶液、2滴淀粉溶液和1滴  溶液混合配制待测液,用 溶液混合配制待测液,用 溶液滴定 溶液滴定 | 猜想2不成立 |
 氧化
氧化 的速率
的速率 还原
还原 的速率,导致待测液反复变为蓝色。
的速率,导致待测液反复变为蓝色。④优化设计 鉴于反应终点无法到达的问题,请提出合理的修正方案
⑤完成实验 小组同学修正方案后,取5.000 g干海带进行测定,消耗15.75 mL

 溶液,则干海带中碘的含量为
溶液,则干海带中碘的含量为
您最近一年使用:0次
2024-04-16更新
|
667次组卷
|
2卷引用:广东省佛山市2024届高三教学质量检测(一)化学试题
解题方法
10 .  是制造锌钡白和锌盐的主要原料,也可用作印染媒染剂,木材和皮革的保存剂。由菱锌矿(主要成分为
是制造锌钡白和锌盐的主要原料,也可用作印染媒染剂,木材和皮革的保存剂。由菱锌矿(主要成分为 ,还含有少量:
,还含有少量: 、
、 、
、 、
、 、
、 、PbO,
、PbO, 、CdO和
、CdO和 )制备
)制备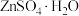 流程如下:
流程如下:
回答下列问题:
(1)加硫酸浸取后再调节pH=5,过滤获得的滤渣①的主要成分为 、
、 、
、 、
、___________ 和___________ 。
(2)加入 溶液后过滤可以得到
溶液后过滤可以得到 和
和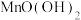 两种沉淀,
两种沉淀, 发生反应的离子方程式为
发生反应的离子方程式为___________ ,常温下,此时溶液pH仍为5,则溶液残留的微量 的浓度约为
的浓度约为___________ mol/L⋅,根据“转化过滤”过程,推测若Zn、稀硫酸、Cd形成原电池,则电势较高的一极为___________ 。
(3)“脱钙镁”后“过滤”所得的滤渣还可以和浓硫酸反应制备HF以循环使用,则该反应可以发生的原因是___________ 。
(4)脱完钙和镁之后的 滤液中含有少量的
滤液中含有少量的 ,
, 的溶解度曲线如图。由滤液④获得
的溶解度曲线如图。由滤液④获得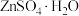 的具体操作为
的具体操作为___________ 。___________ (用含a、b、c的代数式表示)。
 是制造锌钡白和锌盐的主要原料,也可用作印染媒染剂,木材和皮革的保存剂。由菱锌矿(主要成分为
是制造锌钡白和锌盐的主要原料,也可用作印染媒染剂,木材和皮革的保存剂。由菱锌矿(主要成分为 ,还含有少量:
,还含有少量: 、
、 、
、 、
、 、
、 、PbO,
、PbO, 、CdO和
、CdO和 )制备
)制备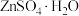 流程如下:
流程如下: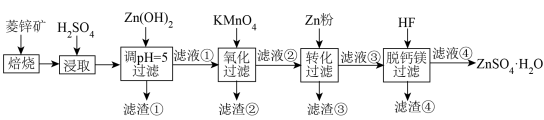
| 金属阳离子 |  |  |  | 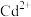 |  |  |  |
| 开始沉淀pH | 6.2 | 7.4 | 2.2 | 7.7 | 9.1 | 8.1 | 3.4 |
| 沉淀完全pH | 8.2 | 8.9 | 3.2 | 9.7 | 11.1 | 10.1 | 4.7 |
(1)加硫酸浸取后再调节pH=5,过滤获得的滤渣①的主要成分为
 、
、 、
、 、
、(2)加入
 溶液后过滤可以得到
溶液后过滤可以得到 和
和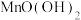 两种沉淀,
两种沉淀, 发生反应的离子方程式为
发生反应的离子方程式为 的浓度约为
的浓度约为(3)“脱钙镁”后“过滤”所得的滤渣还可以和浓硫酸反应制备HF以循环使用,则该反应可以发生的原因是
(4)脱完钙和镁之后的
 滤液中含有少量的
滤液中含有少量的 ,
, 的溶解度曲线如图。由滤液④获得
的溶解度曲线如图。由滤液④获得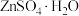 的具体操作为
的具体操作为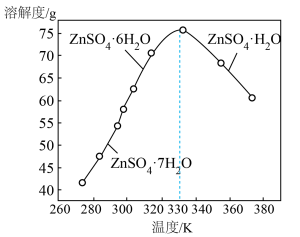
您最近一年使用:0次