解题方法
1 . 室温下,工业上用含少量Mg2+的MnSO4溶液制备MnCO3的过程如图所示,下列说法正确的是
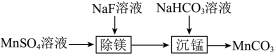
| A.“除镁”步骤中,进行过滤操作需要用到的玻璃仪器仅有漏斗和烧杯 |
| B.“除镁”步骤中,所用的NaF溶液为强电解质 |
C.“沉锰"步骤中的离子方程式为2 +Mn2+=MnCO3↓+H2O+CO2↑ +Mn2+=MnCO3↓+H2O+CO2↑ |
D.“沉锰”后的滤液中: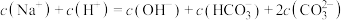 |
您最近一年使用:0次
2 . 三草酸合铁( )酸钾晶体
)酸钾晶体 是制备负载型活性铁催化剂的主要原料。实验室欲制备少量三草酸合铁(
是制备负载型活性铁催化剂的主要原料。实验室欲制备少量三草酸合铁( )酸钾晶体。
)酸钾晶体。
已知: 为翠绿色晶体,难溶于乙醇;0℃时在水中溶解度为4.7g,100℃时溶解度为117.7g。
为翠绿色晶体,难溶于乙醇;0℃时在水中溶解度为4.7g,100℃时溶解度为117.7g。
 .制备
.制备 :称取2.0g莫尔盐
:称取2.0g莫尔盐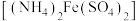 于锥形瓶中,溶于水,滴加足量
于锥形瓶中,溶于水,滴加足量 ,加热并搅拌。当变成红褐色后,再煮沸十分钟,冷却后,过滤、洗涤。
,加热并搅拌。当变成红褐色后,再煮沸十分钟,冷却后,过滤、洗涤。
 .制备草酸氢钾:称取
.制备草酸氢钾:称取 溶于20mL水中,加入
溶于20mL水中,加入 ,反应生成
,反应生成 。
。
 .制备三草酸合铁(
.制备三草酸合铁( )酸钾晶体。步骤如图:
)酸钾晶体。步骤如图:
(1) 中制备
中制备 的离子反应方程式为
的离子反应方程式为___________ 。
(2) 中制备三草酸合铁(
中制备三草酸合铁( )酸钾晶体
)酸钾晶体
①步骤1装置中仪器a的名称为___________ 。
②步骤2的操作名称是___________ ,步骤3采用冰水冷却的目的为___________ 。
③过滤后需要用乙醇溶液洗涤,其优点是___________ 。
(3)三草酸合铁( )酸钾晶体具有光敏性,在强光下分解生成
)酸钾晶体具有光敏性,在强光下分解生成 、
、 和
和 等,该反应的化学方程式为
等,该反应的化学方程式为___________ 。
(4)产品纯度的测定
称取ag晶体粗品溶于100mL水中配成溶液,取20mL溶液于锥形瓶中,用 的酸性
的酸性 ,标准溶液进行滴定(已知
,标准溶液进行滴定(已知 被还原为
被还原为 且粗品中的杂质不参与反应),进行了三次平行实验,达到滴定终点时平均消枆标准溶液VmL。
且粗品中的杂质不参与反应),进行了三次平行实验,达到滴定终点时平均消枆标准溶液VmL。
①所得粗品的纯度为___________ %(用含V、c、a的代数式表示)。
②下列情况会导致产品纯度测定结果偏高的有___________ 。
A.产品中含有
B.滴定终点读数时滴定管尖嘴有气泡(滴定前无气泡)
C.盛装酸性 溶液的滴定管未润洗
溶液的滴定管未润洗
D.产品干燥不充分
 )酸钾晶体
)酸钾晶体 是制备负载型活性铁催化剂的主要原料。实验室欲制备少量三草酸合铁(
是制备负载型活性铁催化剂的主要原料。实验室欲制备少量三草酸合铁( )酸钾晶体。
)酸钾晶体。已知:
 为翠绿色晶体,难溶于乙醇;0℃时在水中溶解度为4.7g,100℃时溶解度为117.7g。
为翠绿色晶体,难溶于乙醇;0℃时在水中溶解度为4.7g,100℃时溶解度为117.7g。 .制备
.制备 :称取2.0g莫尔盐
:称取2.0g莫尔盐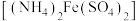 于锥形瓶中,溶于水,滴加足量
于锥形瓶中,溶于水,滴加足量 ,加热并搅拌。当变成红褐色后,再煮沸十分钟,冷却后,过滤、洗涤。
,加热并搅拌。当变成红褐色后,再煮沸十分钟,冷却后,过滤、洗涤。 .制备草酸氢钾:称取
.制备草酸氢钾:称取 溶于20mL水中,加入
溶于20mL水中,加入 ,反应生成
,反应生成 。
。 .制备三草酸合铁(
.制备三草酸合铁( )酸钾晶体。步骤如图:
)酸钾晶体。步骤如图:
(1)
 中制备
中制备 的离子反应方程式为
的离子反应方程式为(2)
 中制备三草酸合铁(
中制备三草酸合铁( )酸钾晶体
)酸钾晶体①步骤1装置中仪器a的名称为
②步骤2的操作名称是
③过滤后需要用乙醇溶液洗涤,其优点是
(3)三草酸合铁(
 )酸钾晶体具有光敏性,在强光下分解生成
)酸钾晶体具有光敏性,在强光下分解生成 、
、 和
和 等,该反应的化学方程式为
等,该反应的化学方程式为(4)产品纯度的测定
称取ag晶体粗品溶于100mL水中配成溶液,取20mL溶液于锥形瓶中,用
 的酸性
的酸性 ,标准溶液进行滴定(已知
,标准溶液进行滴定(已知 被还原为
被还原为 且粗品中的杂质不参与反应),进行了三次平行实验,达到滴定终点时平均消枆标准溶液VmL。
且粗品中的杂质不参与反应),进行了三次平行实验,达到滴定终点时平均消枆标准溶液VmL。①所得粗品的纯度为
②下列情况会导致产品纯度测定结果偏高的有
A.产品中含有

B.滴定终点读数时滴定管尖嘴有气泡(滴定前无气泡)
C.盛装酸性
 溶液的滴定管未润洗
溶液的滴定管未润洗D.产品干燥不充分
您最近一年使用:0次
3 . 钨是国防及高新技术应用中极为重要的功能材料之一,由黑钨矿[主要成分是钨酸亚铁( )、钨酸锰(
)、钨酸锰( ),以及少量的Si、As元素]冶炼钨的流程如下:
),以及少量的Si、As元素]冶炼钨的流程如下:
①钨酸( )酸性很弱,难溶于水。
)酸性很弱,难溶于水。
②水浸液中含有 、
、 、
、 、
、 等阴离子。
等阴离子。
回答下列问题:
(1)“焙烧”前,需将黑钨矿粉碎,目的是_______ 。
(2)“焙烧”过程中,生成 的化学方程式为
的化学方程式为_______ 。
(3)“净化”过程中, 的作用是
的作用是_______ 。
(4)“酸化”过程中,发生反应的离子方程式为_______ 。
(5)“高温还原”过程中,被还原的物质与被氧化的物质的物质的量之比为_______ 。
(6)硬质合金刀具中含碳化钨(WC,碳元素为-4价),利用电解法可以从碳化钨废料中回收钨。电解时,用碳化钨做阳极,不锈钢做阴极,HCl溶液为电解液,阳极析出钨酸沉淀并放出 气体,则阳极的电极反应式为
气体,则阳极的电极反应式为_______ 。
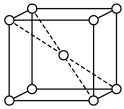
(7)钨晶胞为体心立方晶胞,晶胞结构如图所示(注:晶胞体对角线的W原子相切),则钨晶胞的原子空间利用率为_______(填标号。晶胞的原子空间利用率=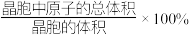 )。
)。
 )、钨酸锰(
)、钨酸锰( ),以及少量的Si、As元素]冶炼钨的流程如下:
),以及少量的Si、As元素]冶炼钨的流程如下:
①钨酸(
 )酸性很弱,难溶于水。
)酸性很弱,难溶于水。②水浸液中含有
 、
、 、
、 、
、 等阴离子。
等阴离子。回答下列问题:
(1)“焙烧”前,需将黑钨矿粉碎,目的是
(2)“焙烧”过程中,生成
 的化学方程式为
的化学方程式为(3)“净化”过程中,
 的作用是
的作用是(4)“酸化”过程中,发生反应的离子方程式为
(5)“高温还原”过程中,被还原的物质与被氧化的物质的物质的量之比为
(6)硬质合金刀具中含碳化钨(WC,碳元素为-4价),利用电解法可以从碳化钨废料中回收钨。电解时,用碳化钨做阳极,不锈钢做阴极,HCl溶液为电解液,阳极析出钨酸沉淀并放出
 气体,则阳极的电极反应式为
气体,则阳极的电极反应式为(7)钨晶胞为体心立方晶胞,晶胞结构如图所示(注:晶胞体对角线的W原子相切),则钨晶胞的原子空间利用率为_______(填标号。晶胞的原子空间利用率=
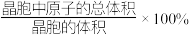 )。
)。
A. | B.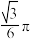 | C. | D. |
您最近一年使用:0次
4 . 一种从某混合物(主要成分为 、
、 、
、 )中提取钒的工艺流程如图所示。已知:P2O4能够萃取溶液中的
)中提取钒的工艺流程如图所示。已知:P2O4能够萃取溶液中的 。下列说法正确的是
。下列说法正确的是
 、
、 、
、 )中提取钒的工艺流程如图所示。已知:P2O4能够萃取溶液中的
)中提取钒的工艺流程如图所示。已知:P2O4能够萃取溶液中的 。下列说法正确的是
。下列说法正确的是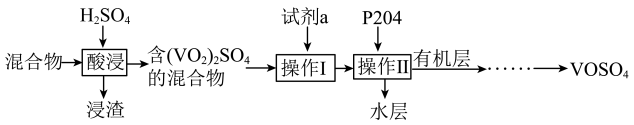
| A.“酸浸”过程中发生了氧化还原反应 |
B.试剂a的作用是氧化 |
| C.操作Ⅱ使用的主要玻璃仪器有漏斗、烧杯、玻璃棒 |
D.水层中可能含有 |
您最近一年使用:0次
解题方法
5 . 盐泥是氯碱工业的废渣,主要含镁、钙、铁、铝、锰的硅酸盐和碳酸盐,可用于提取 ,工艺流程如图所示:
,工艺流程如图所示: .常见氢氧化物的溶度积Ksp如下表:
.常见氢氧化物的溶度积Ksp如下表:
 .物质的溶解度S(g/100g水)
.物质的溶解度S(g/100g水)
(1)基态Fe原子价层电子轨道排布图为___________
(2)滤渣 的主要成分为
的主要成分为___________ (填化学式)。
(3)流程中加NaClO溶液煮沸10min后,立即趁热过滤的原因是___________ 。
(4)滤渣 含有
含有 、写出生成
、写出生成 的离子反应方程式
的离子反应方程式___________ 。
(5)滤液 中
中
___________ 。
(6)从滤液 中获得晶体的实验操作步骤为:①向滤液中加入NaOH,②过滤,得沉淀,③向沉淀中加入稀硫酸,④
中获得晶体的实验操作步骤为:①向滤液中加入NaOH,②过滤,得沉淀,③向沉淀中加入稀硫酸,④___________ ,⑤过滤、洗涤得产品。
(7) 作催化剂、氨催化还原脱除NO的一种催化机理示意图如图。从化学键的角度解释
作催化剂、氨催化还原脱除NO的一种催化机理示意图如图。从化学键的角度解释 能结合
能结合 的原因:
的原因:___________ 。
 ,工艺流程如图所示:
,工艺流程如图所示:
 .常见氢氧化物的溶度积Ksp如下表:
.常见氢氧化物的溶度积Ksp如下表: |  |  |  |  |  |
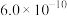 | 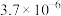 | 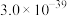 |  | 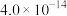 | 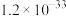 |
 .物质的溶解度S(g/100g水)
.物质的溶解度S(g/100g水)| 温度/℃ | 0 | 10 | 20 | 40 | 60 | 80 | 100 |
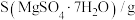 | 20.3 | 23.3 | 25.2 | 30.8 | 35.3 | 35.8 | 33.4 |
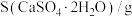 | 0.223 | 0.224 | 0.255 | 0.265 | 0.244 | 0.234 | 0.205 |
(1)基态Fe原子价层电子轨道排布图为
(2)滤渣
 的主要成分为
的主要成分为(3)流程中加NaClO溶液煮沸10min后,立即趁热过滤的原因是
(4)滤渣
 含有
含有 、写出生成
、写出生成 的离子反应方程式
的离子反应方程式(5)滤液
 中
中
(6)从滤液
 中获得晶体的实验操作步骤为:①向滤液中加入NaOH,②过滤,得沉淀,③向沉淀中加入稀硫酸,④
中获得晶体的实验操作步骤为:①向滤液中加入NaOH,②过滤,得沉淀,③向沉淀中加入稀硫酸,④(7)
 作催化剂、氨催化还原脱除NO的一种催化机理示意图如图。从化学键的角度解释
作催化剂、氨催化还原脱除NO的一种催化机理示意图如图。从化学键的角度解释 能结合
能结合 的原因:
的原因: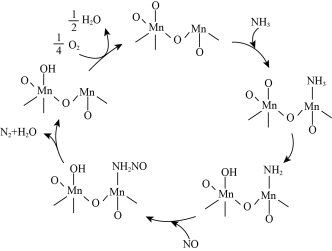
您最近一年使用:0次
6 . 镍、铬、铜及其化合物在工业上有广泛的应用,从电镀污泥[含有 、
、 、
、 、
、 和
和 等]中回收制备
等]中回收制备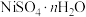 和其它金属及其化合物的工艺流程如图所示。
和其它金属及其化合物的工艺流程如图所示。
 (水相)+2RH(有机相)
(水相)+2RH(有机相)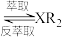 (有机相)
(有机相) (水相)
(水相)
回答下列问题:
(1)与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有________ (填元素符号)。原子核外运动的电子有两种相反的自旋状态,若一种自旋状态用“ ”表示,与之相反的用“
”表示,与之相反的用“ ”表示,“
”表示,“ ”即称为电子的自旋磁量子数。对于基态Ni原子,其价电子自旋磁量子数的代数和为
”即称为电子的自旋磁量子数。对于基态Ni原子,其价电子自旋磁量子数的代数和为________ 。
(2)已知NiO与MgO的晶体结构相同,其中 和
和 的离子半径分别为66pm和69pm。则熔点:NiO
的离子半径分别为66pm和69pm。则熔点:NiO________ MgO(填“>”“<”或“=”),理由是________ 。
(3)滤渣1的主要成分为________ (填化学式)。
(4)电解之后加入碳酸钠调节pH的目的是________ 。
(5)反萃取剂A为________ 。
(6)“反萃取”得到的 溶液,在碱性条件下可被NaClO氧化生成NiOOH沉淀,该反应的离子方程式为
溶液,在碱性条件下可被NaClO氧化生成NiOOH沉淀,该反应的离子方程式为________ 。
(7)资料显示,硫酸镍结晶水合物的形态与温度有如表关系:
由 溶液获得
溶液获得 晶体的操作依次是蒸发浓缩、
晶体的操作依次是蒸发浓缩、________ 、过滤、洗涤、干燥。
 、
、 、
、 、
、 和
和 等]中回收制备
等]中回收制备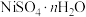 和其它金属及其化合物的工艺流程如图所示。
和其它金属及其化合物的工艺流程如图所示。
 (水相)+2RH(有机相)
(水相)+2RH(有机相)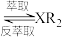 (有机相)
(有机相) (水相)
(水相)回答下列问题:
(1)与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有
 ”表示,与之相反的用“
”表示,与之相反的用“ ”表示,“
”表示,“ ”即称为电子的自旋磁量子数。对于基态Ni原子,其价电子自旋磁量子数的代数和为
”即称为电子的自旋磁量子数。对于基态Ni原子,其价电子自旋磁量子数的代数和为(2)已知NiO与MgO的晶体结构相同,其中
 和
和 的离子半径分别为66pm和69pm。则熔点:NiO
的离子半径分别为66pm和69pm。则熔点:NiO(3)滤渣1的主要成分为
(4)电解之后加入碳酸钠调节pH的目的是
(5)反萃取剂A为
(6)“反萃取”得到的
 溶液,在碱性条件下可被NaClO氧化生成NiOOH沉淀,该反应的离子方程式为
溶液,在碱性条件下可被NaClO氧化生成NiOOH沉淀,该反应的离子方程式为(7)资料显示,硫酸镍结晶水合物的形态与温度有如表关系:
温度 | 低于30.8℃ | 30.8℃~53.8℃ | 53.8℃~280℃ | 高于280℃ |
晶体形态 |
|
| 多种结晶水合物 |
|
 溶液获得
溶液获得 晶体的操作依次是蒸发浓缩、
晶体的操作依次是蒸发浓缩、
您最近一年使用:0次
名校
解题方法
7 . ZnO是一种难溶于水的白色固体,在化学工业中主要用作橡胶和颜料的添加剂,医药上用于制软膏、橡皮膏等。工业上由菱锌矿(主要成分为 、ZnO,还含有少量
、ZnO,还含有少量 、FeO、
、FeO、 、
、 等杂质)制备ZnO的工艺流程如图所示:
等杂质)制备ZnO的工艺流程如图所示: ,
,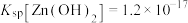 ;
;
②“溶浸”后的溶液所含金属离子主要有: 、
、 、
、 、
、 ;
;
③氧化性顺序: 。
。
回答下列问题:
(1)基态Zn原子的最高能层符号为__________ 。
(2)滤渣1的化学式是__________ ,“溶浸”过程中 发生反应的离子方程式是
发生反应的离子方程式是__________ 。
(3)“氧化”时适当加热,其目的是__________ ,但温度不能过高,其原因是__________ 。
(4)已知“氧化”后溶液中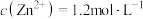 ,“调pH”的pH范围是
,“调pH”的pH范围是__________ (保留两位有效数字)。(已知:溶液中离子浓度小于等于 时,认为该离子沉淀完全。)“还原”时加入锌粉的目的是
时,认为该离子沉淀完全。)“还原”时加入锌粉的目的是__________ 。
(5)有机萃取剂HA与 反应的化学方程式为
反应的化学方程式为 ,则“反萃取”时加入试剂X的化学式是
,则“反萃取”时加入试剂X的化学式是__________ 。
(6)在“沉锌”与“灼烧”之间进行的操作是__________ ,“沉锌”得到碱式碳酸锌[化学式为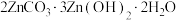 ],碱式碳酸锌升温过程中固体的质量变化如图所示。350℃时,剩余固体中已不含碳元素,则剩余固体的成分是
],碱式碳酸锌升温过程中固体的质量变化如图所示。350℃时,剩余固体中已不含碳元素,则剩余固体的成分是__________ (填化学式)。
 、ZnO,还含有少量
、ZnO,还含有少量 、FeO、
、FeO、 、
、 等杂质)制备ZnO的工艺流程如图所示:
等杂质)制备ZnO的工艺流程如图所示: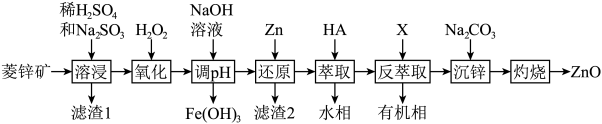
 ,
,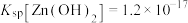 ;
;②“溶浸”后的溶液所含金属离子主要有:
 、
、 、
、 、
、 ;
;③氧化性顺序:
 。
。回答下列问题:
(1)基态Zn原子的最高能层符号为
(2)滤渣1的化学式是
 发生反应的离子方程式是
发生反应的离子方程式是(3)“氧化”时适当加热,其目的是
(4)已知“氧化”后溶液中
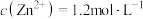 ,“调pH”的pH范围是
,“调pH”的pH范围是 时,认为该离子沉淀完全。)“还原”时加入锌粉的目的是
时,认为该离子沉淀完全。)“还原”时加入锌粉的目的是(5)有机萃取剂HA与
 反应的化学方程式为
反应的化学方程式为 ,则“反萃取”时加入试剂X的化学式是
,则“反萃取”时加入试剂X的化学式是(6)在“沉锌”与“灼烧”之间进行的操作是
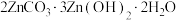 ],碱式碳酸锌升温过程中固体的质量变化如图所示。350℃时,剩余固体中已不含碳元素,则剩余固体的成分是
],碱式碳酸锌升温过程中固体的质量变化如图所示。350℃时,剩余固体中已不含碳元素,则剩余固体的成分是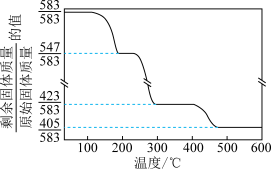
您最近一年使用:0次
2024-04-18更新
|
704次组卷
|
5卷引用:广西壮族自治区部分学校2023-2024学年高三下学期教学质量监测联考(二模)化学试题
广西壮族自治区部分学校2023-2024学年高三下学期教学质量监测联考(二模)化学试题江西省部分地区2023-2024学年高三下学期3月月考化学试题甘肃省酒泉市九师联盟2023-2024学年高三下学期3月月考化学试题(已下线)题型10 工艺流程题(25题)-2024年高考化学常考点必杀300题(新高考通用)湖北省九师联盟2024届高三下学期3月质量检测(W-G)化学试卷
解题方法
8 . 氯氧化铋(BiOCl)广泛用于彩釉调料、塑料助剂、油漆调色等。工业上常用辉铋矿(主要成分是 ,还含有少量
,还含有少量 、铁的氧化物等杂质)为原料制备氯氧化铋。
、铁的氧化物等杂质)为原料制备氯氧化铋。 在
在 时开始水解,
时开始水解,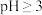 时几乎完全水解为白色的BiOCl沉淀;
时几乎完全水解为白色的BiOCl沉淀;
②该工艺下,有关金属离子开始沉淀和沉淀完全的pH见下表。
(1)铋与氮同主族,且位于元素周期表的第六周期,基态Bi的价电子排布式为___________ 。
(2)“浸渣”的主要成分是S和___________ ,“浸取”时生成S的离子方程式为___________ 。
(3)“充分搅拌”时加入盐酸羟胺的目的是___________ 。
(4)加入碳酸钠粉末制取BiOCl时,溶液pH值需控制的合理范围为___________ ,发生反应的化学方程式为___________ 。
(5)氯氧化铋(BiOCl)可用作钾离子电池(有机物作离子导体)的负极材料,充电时嵌入 ,BiOCl被还原为Bi,则阴极的电极反应式是
,BiOCl被还原为Bi,则阴极的电极反应式是___________ 。
(6)铋的一种氧化物的立方晶胞结构如图所示,已知最近的两个铋离子之间的距离为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该晶体的密度为
,则该晶体的密度为___________  (列出计算式即可)。
(列出计算式即可)。
 ,还含有少量
,还含有少量 、铁的氧化物等杂质)为原料制备氯氧化铋。
、铁的氧化物等杂质)为原料制备氯氧化铋。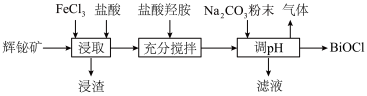
 在
在 时开始水解,
时开始水解,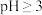 时几乎完全水解为白色的BiOCl沉淀;
时几乎完全水解为白色的BiOCl沉淀;②该工艺下,有关金属离子开始沉淀和沉淀完全的pH见下表。
| 金属离子 |  |  |
| 开始沉淀的pH | 1.9 | 7.2 |
| 沉淀完全的pH | 2.9 | 8.2 |
(1)铋与氮同主族,且位于元素周期表的第六周期,基态Bi的价电子排布式为
(2)“浸渣”的主要成分是S和
(3)“充分搅拌”时加入盐酸羟胺的目的是
(4)加入碳酸钠粉末制取BiOCl时,溶液pH值需控制的合理范围为
(5)氯氧化铋(BiOCl)可用作钾离子电池(有机物作离子导体)的负极材料,充电时嵌入
 ,BiOCl被还原为Bi,则阴极的电极反应式是
,BiOCl被还原为Bi,则阴极的电极反应式是(6)铋的一种氧化物的立方晶胞结构如图所示,已知最近的两个铋离子之间的距离为
 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该晶体的密度为
,则该晶体的密度为 (列出计算式即可)。
(列出计算式即可)。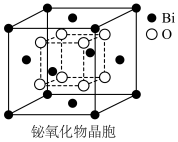
您最近一年使用:0次
2024-04-01更新
|
554次组卷
|
3卷引用:广西壮族自治区柳州市2024届高三第三次模拟考试化学试题
广西壮族自治区柳州市2024届高三第三次模拟考试化学试题广西柳州市2024届高三下学期第三次模拟考试(三模)化学试题(已下线)题型10 工艺流程题(25题)-2024年高考化学常考点必杀300题(新高考通用)
9 . 用FeCl3溶液腐蚀覆铜板产生的腐蚀废液可回收利用,实验流程如下。下列有关说法错误的是
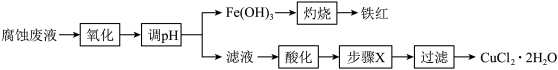

| A.“氧化”步骤中可用的试剂为氯气 |
| B.“调pH”后,检验Fe3+是否沉淀完全的操作为:取少量上层清液于试管中,滴加几滴酸性KMnO4溶液,观察溶液紫色是否褪去 |
| C.进行“灼烧”操作时需用到的仪器有坩埚和酒精灯 |
| D.“步骤X”包含的操作有蒸发浓缩、冷却结晶 |
您最近一年使用:0次
名校
解题方法
10 . 对某溶液中部分离子的定性检测流程如下。相关分析正确的是

| A.步骤①所加试剂可以是浓KOH溶液 |
| B.可以用湿润的蓝色石蕊试纸检验生成的无色气体 |
C.步骤②发生的反应为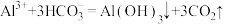 |
D. 遇铁氰化钾会生成蓝色溶液 遇铁氰化钾会生成蓝色溶液 |
您最近一年使用:0次
2024-03-06更新
|
581次组卷
|
15卷引用:【全国百强校】广西柳州高级中学2018届高三5月冲刺模拟理科综合化学试题
【全国百强校】广西柳州高级中学2018届高三5月冲刺模拟理科综合化学试题四川省成都市2018届高三第二次诊断性检测理综化学试题2024届四川省成都市第七中学高三下学期二模诊断考试理综试题-高中化学 2024届四川省成都市第七中学高三下学期二诊模拟考试理综试卷-高中化学2024届四川省仁寿第一中学校(北校区)二模理综试题-高中化学(已下线)化学(山东卷02)-2024年高考押题预测卷2024届山东省邹城市北大新世纪高级中学高三下学期第三次模拟考试化学试题四川省成都外国语学校2017-2018学年高二6月(零诊模拟)月考化学试题山东省泰安第一中学2020届高三上学期期中模拟联合考试化学试题宁夏固原市五原中学补习部2021届高三上学期期中考试化学试题陕西省宝鸡市金台区2021届高三11月检测理综化学试题辽宁省沈阳市郊联体2021届高三上学期期末考试化学试题(已下线)专题04 离子反应(缺项配平、离子检验、离子推断、共存)-2021年高考化学必做热点专题(已下线)小题07 描述型实验选择题(侧重物质检验、定量实验) ——备战2021年高考化学经典小题考前必刷(全国通用)黑龙江省哈尔滨市第九中学2020-2021学年高二下学期6月月考化学试题




