名校
1 . 硫酸锌广泛应用于工农业生产中。工业上以粗氧化锌(含 等杂质)为原料生产
等杂质)为原料生产 的一种流程的部分过程如下(各过程需控制适宜条件)。
的一种流程的部分过程如下(各过程需控制适宜条件)。
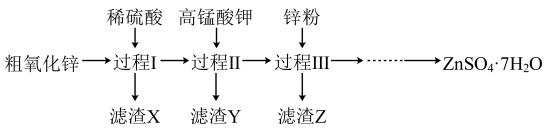
(1)过程Ⅰ、Ⅱ、Ⅲ中,分离出X、Y、Z的实验操作是_______ 。
(2)过程Ⅰ,能与稀硫酸反应的物质有________ 。写出生成氢气的离子方程式:_______ ,因此过程Ⅰ需要持续强制通风,原因是生成的氢气具有______ 性。
(3)过程Ⅱ中,滤渣Y含有 。加入高锰酸钾的主要目的是
。加入高锰酸钾的主要目的是_______ 。
(4)过程Ⅲ中,滤渣Z含铜,生成铜的离子方程式为________ 。
 等杂质)为原料生产
等杂质)为原料生产 的一种流程的部分过程如下(各过程需控制适宜条件)。
的一种流程的部分过程如下(各过程需控制适宜条件)。
(1)过程Ⅰ、Ⅱ、Ⅲ中,分离出X、Y、Z的实验操作是
(2)过程Ⅰ,能与稀硫酸反应的物质有
(3)过程Ⅱ中,滤渣Y含有
 。加入高锰酸钾的主要目的是
。加入高锰酸钾的主要目的是(4)过程Ⅲ中,滤渣Z含铜,生成铜的离子方程式为
您最近一年使用:0次
名校
2 . 铁及其化合物在日常生产生活中应用广泛,研究铁及其化合物的应用意义重大。
(1)所含铁元素只有还原性的物质是___________。
(2)当人体缺铁时,往往需要吃补铁保健品。人体能够吸收的是+2价的铁,但是+2价的铁很容易被氧化。
①如何检验某固体补铁剂中铁元素已被氧化?写出操作过程、现象及结论。
答:研细后用盐酸溶解,___________ 。
②服用维生素C,可使食物中的三价铁离子转化为二价铁离子。由此可推知,维生素C具有___________ (填化学性质)。
(3)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、C1O-、OH-、FeO 、Cl-、H2O。写出并配平湿法制高铁酸钾的离子反应方程式:
、Cl-、H2O。写出并配平湿法制高铁酸钾的离子反应方程式:___________
______Fe(OH)3+_______ClO-+_______=_______FeO +_______Cl-+_______
+_______Cl-+_______
(4)工业上用氯化铁腐蚀铜箔、制造电路板。某工程师为了从使用过的腐蚀废液中回收铜,并获得氯化铁晶体,准备采用下列步骤:

回答下列问题:
①试剂a是___________ ,操作I用到的玻璃仪器有烧杯、玻璃棒和___________ 。
②滤液X、Z中都有同一种溶质,它们转化为溶液W的离子方程式为___________ 。
③上述流程中操作Ⅲ包括:蒸发浓缩、___________ 、过滤、洗涤。
(1)所含铁元素只有还原性的物质是___________。
| A.Fe | B.FeCl2 | C.FeCl3 | D.Fe2O3 |
(2)当人体缺铁时,往往需要吃补铁保健品。人体能够吸收的是+2价的铁,但是+2价的铁很容易被氧化。
①如何检验某固体补铁剂中铁元素已被氧化?写出操作过程、现象及结论。
答:研细后用盐酸溶解,
②服用维生素C,可使食物中的三价铁离子转化为二价铁离子。由此可推知,维生素C具有
(3)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、C1O-、OH-、FeO
 、Cl-、H2O。写出并配平湿法制高铁酸钾的离子反应方程式:
、Cl-、H2O。写出并配平湿法制高铁酸钾的离子反应方程式:______Fe(OH)3+_______ClO-+_______=_______FeO
 +_______Cl-+_______
+_______Cl-+_______(4)工业上用氯化铁腐蚀铜箔、制造电路板。某工程师为了从使用过的腐蚀废液中回收铜,并获得氯化铁晶体,准备采用下列步骤:

回答下列问题:
①试剂a是
②滤液X、Z中都有同一种溶质,它们转化为溶液W的离子方程式为
③上述流程中操作Ⅲ包括:蒸发浓缩、
您最近一年使用:0次
名校
3 . 回答下列问题:
(1)从海水中得到的粗盐中常含 、
、 、
、 等杂质离子,可依次加入
等杂质离子,可依次加入_______ 、_______ 、_______ 、稀盐酸来进行提纯。加入适量盐酸的目的是_______ 。
(2)用上述方法得到氯化钠,配制氯化钠饱和溶液进行如下图所示电解实验。
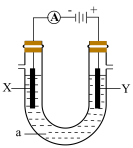
①写出该电解反应的化学方程式_______ 。
②简述检测Y极附近产生的气体的实验方案:_______
(3)下列方法可用于海水淡化的是_______ (填字母)。
A.蒸馏法 B.萃取法 C.过滤法
(4)①“84”消毒液是生活中常见的消毒剂, 与
与 溶液反应制取“84”消毒液的化学方程式为
溶液反应制取“84”消毒液的化学方程式为_______ 。
②“84”消毒液的稀溶液在浸泡餐具过程中,因吸收空气中 使消毒杀菌能力增强,产物中有小苏打,请用化学方程式说明原因:
使消毒杀菌能力增强,产物中有小苏打,请用化学方程式说明原因:_______ 。
(5)目前很多自来水厂使用 来消毒、杀菌。工业制取
来消毒、杀菌。工业制取 的反应:
的反应: ,请用双线桥表示反应中电子转移情况
,请用双线桥表示反应中电子转移情况_______ 。
(6)物质的制备是化学学科的基本研究方向。
①室温下,将氨水和 溶液混合,可制得
溶液混合,可制得 溶液。离子方程式为
溶液。离子方程式为_______ 。
②软锰矿(主要成分 )的水悬浊液可吸收烟气中的
)的水悬浊液可吸收烟气中的 并同时制备
并同时制备 。制备
。制备 反应的化学方程式为
反应的化学方程式为_______ 。
(1)从海水中得到的粗盐中常含
 、
、 、
、 等杂质离子,可依次加入
等杂质离子,可依次加入(2)用上述方法得到氯化钠,配制氯化钠饱和溶液进行如下图所示电解实验。

①写出该电解反应的化学方程式
②简述检测Y极附近产生的气体的实验方案:
(3)下列方法可用于海水淡化的是
A.蒸馏法 B.萃取法 C.过滤法
(4)①“84”消毒液是生活中常见的消毒剂,
 与
与 溶液反应制取“84”消毒液的化学方程式为
溶液反应制取“84”消毒液的化学方程式为②“84”消毒液的稀溶液在浸泡餐具过程中,因吸收空气中
 使消毒杀菌能力增强,产物中有小苏打,请用化学方程式说明原因:
使消毒杀菌能力增强,产物中有小苏打,请用化学方程式说明原因:(5)目前很多自来水厂使用
 来消毒、杀菌。工业制取
来消毒、杀菌。工业制取 的反应:
的反应: ,请用双线桥表示反应中电子转移情况
,请用双线桥表示反应中电子转移情况(6)物质的制备是化学学科的基本研究方向。
①室温下,将氨水和
 溶液混合,可制得
溶液混合,可制得 溶液。离子方程式为
溶液。离子方程式为②软锰矿(主要成分
 )的水悬浊液可吸收烟气中的
)的水悬浊液可吸收烟气中的 并同时制备
并同时制备 。制备
。制备 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次
4 . 废旧锂离子电池的回收利用意义重大,其正极废料的主要成分是 、铝、炭黑及其他微量杂质,回收利用的流程如下:
、铝、炭黑及其他微量杂质,回收利用的流程如下:
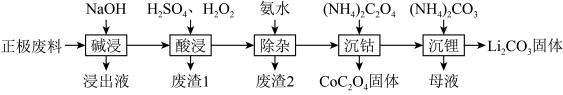
(1)“碱浸”步骤中铝溶解的离子方程式为________ ,“废渣1”的主要成分是_______ 。
(2)已知Li在化合物中显 价,
价, 中Co的化合价为
中Co的化合价为_____ ,“酸浸”步骤中 固体溶解的化学方程式为
固体溶解的化学方程式为_______ ,反应中 的作用为
的作用为_______ 。
(3)“酸浸”后的溶液中含有少量 、
、 、
、 ,滤渣2的主要成分是
,滤渣2的主要成分是______ 。
(4)沉钴过程发生的反应属于______ (填反应类型)。
(5)“母液”中的溶质成分是_______ ,生成 固体的离子方程式为
固体的离子方程式为________ 。
 、铝、炭黑及其他微量杂质,回收利用的流程如下:
、铝、炭黑及其他微量杂质,回收利用的流程如下:
(1)“碱浸”步骤中铝溶解的离子方程式为
(2)已知Li在化合物中显
 价,
价, 中Co的化合价为
中Co的化合价为 固体溶解的化学方程式为
固体溶解的化学方程式为 的作用为
的作用为(3)“酸浸”后的溶液中含有少量
 、
、 、
、 ,滤渣2的主要成分是
,滤渣2的主要成分是(4)沉钴过程发生的反应属于
(5)“母液”中的溶质成分是
 固体的离子方程式为
固体的离子方程式为
您最近一年使用:0次
5 . 某化工厂欲以工业生产废料(金属铁、铝及其氧化物)为原料制取PAFC(聚合氯化铁铝)[AlFe(OH)nCl6-n]m,设计生产流程如下,请回答下列问题:

(1)用10mol/L的浓盐酸配制2mol/L的稀盐酸500mL, 所取浓盐酸的体积________ mL,所用玻璃仪器除量筒、玻璃棒和胶头滴管外,还有_______ 。
A.500mL容量瓶 B.蒸发皿 C.烧瓶
(2)写出Fe2O3粉末与盐酸反应的离子方程式:_______________ 。
(3)取少量酸性溶液滴加几滴KSCN试剂,溶液变为______ 色,证明含有Fe3+。
(4)通入氯气的目的是___________________ 。
(5)加入NaOH调节pH时,氢氧化钠不宜过多,生成一种红褐色沉淀,写出溶液中Fe3+与过量NaOH反应的离子方程式:______________________ 。

(1)用10mol/L的浓盐酸配制2mol/L的稀盐酸500mL, 所取浓盐酸的体积
A.500mL容量瓶 B.蒸发皿 C.烧瓶
(2)写出Fe2O3粉末与盐酸反应的离子方程式:
(3)取少量酸性溶液滴加几滴KSCN试剂,溶液变为
(4)通入氯气的目的是
(5)加入NaOH调节pH时,氢氧化钠不宜过多,生成一种红褐色沉淀,写出溶液中Fe3+与过量NaOH反应的离子方程式:
您最近一年使用:0次
解题方法
6 . 我国拥有很长的海岸线,具有丰富的海洋资源。
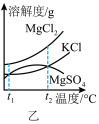
Ⅰ.盐卤是海水晒盐后的富含镁盐的溶液,其中除含镁盐外,还含有其他盐类(如图甲所示)。
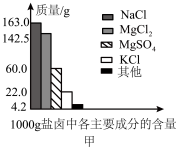
(1)根据图甲所示,写出盐卤中含量最多的盐为___________ (填化学式)其电子式为___________
(2)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到 ℃以上,根据溶解度曲线,首先析出的晶体应是
℃以上,根据溶解度曲线,首先析出的晶体应是___________ 。(填化学式)
(3)如图是常用于混合物的分离和提纯的装置:
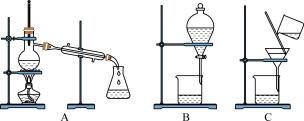
粗盐的提纯应选择图___________ (填字母,下同)装置,若实验中为了除去粗盐中的 、
、 、
、 等杂质离子加入试剂的顺序可以是
等杂质离子加入试剂的顺序可以是___________ 。
A.NaOH、Na2CO3、BaCl2、HCl B.NaOH、BaCl2、Na2CO3、HCl
C.Na2CO3、BaCl2、NaOH、HCl D.BaCl2、NaOH、Na2CO3、HCl
Ⅱ.海带是一种含碘量很高的海藻,从中提取的碘广泛应用于医药、食品和化工。实验室里从海带中提取碘的流程如图。
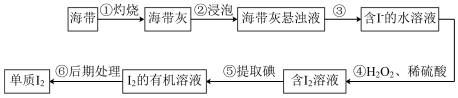
(4)实验步骤①会用到下列仪器中的___________ (填字母)
a.酒精灯 b.蒸发皿 c.坩埚 d.泥三角
(5)设计实验证明第③步操作后滤液中K+的存在,___________ 。
(6)“提取碘”存在以下两种方案。
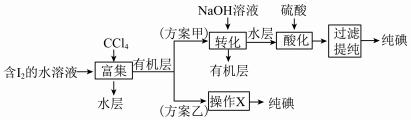
①方案乙中“操作X”的名称是___________ 。
②该流程可循环利用的物质是___________ 。
③采用方案乙得到纯碘的产率较低,原因是___________ 。
Ⅰ.盐卤是海水晒盐后的富含镁盐的溶液,其中除含镁盐外,还含有其他盐类(如图甲所示)。

(1)根据图甲所示,写出盐卤中含量最多的盐为
(2)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到
 ℃以上,根据溶解度曲线,首先析出的晶体应是
℃以上,根据溶解度曲线,首先析出的晶体应是
(3)如图是常用于混合物的分离和提纯的装置:

粗盐的提纯应选择图
 、
、 、
、 等杂质离子加入试剂的顺序可以是
等杂质离子加入试剂的顺序可以是A.NaOH、Na2CO3、BaCl2、HCl B.NaOH、BaCl2、Na2CO3、HCl
C.Na2CO3、BaCl2、NaOH、HCl D.BaCl2、NaOH、Na2CO3、HCl
Ⅱ.海带是一种含碘量很高的海藻,从中提取的碘广泛应用于医药、食品和化工。实验室里从海带中提取碘的流程如图。

(4)实验步骤①会用到下列仪器中的
a.酒精灯 b.蒸发皿 c.坩埚 d.泥三角
(5)设计实验证明第③步操作后滤液中K+的存在,
(6)“提取碘”存在以下两种方案。

①方案乙中“操作X”的名称是
②该流程可循环利用的物质是
③采用方案乙得到纯碘的产率较低,原因是
您最近一年使用:0次
名校
7 . 硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:

请回答下列问题:
(1)向操作①的滤液中滴加_______ 溶液后变为红色,则该滤液中含有________ (填离子符号)。
(2)操作②中反应的离子方程式:________________ ,若向操作②得到的溶液中加入足量的铁粉,反应的离子方程式为:________________ 。
(3)操作③中反应的离子方程式:________________ 。
(4)操作④中一系列处理的操作步骤:过滤、________ 、干燥、灼烧、________ 、称量。
(5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为_______ g。(用含a的代数式表示)。

请回答下列问题:
(1)向操作①的滤液中滴加
(2)操作②中反应的离子方程式:
(3)操作③中反应的离子方程式:
(4)操作④中一系列处理的操作步骤:过滤、
(5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为
您最近一年使用:0次
名校
8 . 社会要可持续发展,“绿色化学”要渗透到生产生活中。某同学以“从印刷电路板废液中回收铜,并再生FeCl3溶液”为实验主题设计的实验方案。根据该同学试设计的流程,回答下列问题:
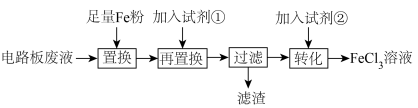
(1)“滤渣”的化学式为___________ 。
(2)根据上面流程:“转化”时,加入的试剂符合条件的是___________。
(3)为了检验是否生成了Fe3+溶液,请写出检验方法:___________ 。
(4)利用FeCl3溶液为原料还可以生成高铁酸钾 ,高铁酸钾是一种新型的净水剂,可以通过下述反应制取:
,高铁酸钾是一种新型的净水剂,可以通过下述反应制取: 。
。
①该反应中还原剂是___________ (填化学式,下同),还原产物为___________ 。
②通过发生的反应可知,物质氧化性:KClO___________ K2FeO4(填“>”或“<”)。
③当反应中有 生成,转移电子的物质的量为
生成,转移电子的物质的量为___________  。
。

(1)“滤渣”的化学式为
(2)根据上面流程:“转化”时,加入的试剂符合条件的是___________。
| A.铁粉 | B.氯水 | C.KMnO4溶液 | D.H2O2溶液 |
(3)为了检验是否生成了Fe3+溶液,请写出检验方法:
(4)利用FeCl3溶液为原料还可以生成高铁酸钾
 ,高铁酸钾是一种新型的净水剂,可以通过下述反应制取:
,高铁酸钾是一种新型的净水剂,可以通过下述反应制取: 。
。①该反应中还原剂是
②通过发生的反应可知,物质氧化性:KClO
③当反应中有
 生成,转移电子的物质的量为
生成,转移电子的物质的量为 。
。
您最近一年使用:0次
名校
9 . Na元素相关的物质有很多且具有广泛的用途。
(1)氯化钠(NaCl)是生活中常用的化学品,也是重要的化工生产原料。粗盐中一般含有CaCl2、MgCl2、CaSO4和MgSO4杂质。从粗盐制得精盐的过程如下:

①试剂Ⅰ是_____ 。
②加入试剂Ⅱ所发生的离子方程式为:_____
③操作a中,未用到的实验仪器是_____
A.蒸发皿 B.玻璃棒 C.漏斗 D.烧杯
④用到操作c的名称为_____ ,操作b不能省略,理由是_____ 。
(2)Na2CO3、NaHCO3走进千家万户,在食品加工方面有着广泛的用途。
①下列关于Na2CO3的认识正确的是_____ 。
A.受热易分解 B.俗称纯碱、苏打 C.可用于制皂 D.可与酸反应
②传统蒸馒头常采用酵头发面,再用Na2CO3调节面团酸度。查阅资料得知,酵头可使面团在微生物作用下产生CO2气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。等质量的碳酸钠和碳酸氢钠,消耗酸更多的是_____ 。
③若面团发得不好,面团内的气孔少,略有酸味。可不用Na2CO3而用NaHCO3,继续揉面,上锅蒸后也能蒸出松软的馒头。解释NaHCO3的作用_____ 。
(3)某品牌复合膨松剂的说明书如下图所示。其中葡萄糖酸-δ-内酯和淀粉是助剂,其作用是防止膨松剂吸潮结块而失效。焦磷酸二氢二钠的作用是_____ 。

(1)氯化钠(NaCl)是生活中常用的化学品,也是重要的化工生产原料。粗盐中一般含有CaCl2、MgCl2、CaSO4和MgSO4杂质。从粗盐制得精盐的过程如下:

①试剂Ⅰ是
②加入试剂Ⅱ所发生的离子方程式为:
③操作a中,未用到的实验仪器是
A.蒸发皿 B.玻璃棒 C.漏斗 D.烧杯
④用到操作c的名称为
(2)Na2CO3、NaHCO3走进千家万户,在食品加工方面有着广泛的用途。
①下列关于Na2CO3的认识正确的是
A.受热易分解 B.俗称纯碱、苏打 C.可用于制皂 D.可与酸反应
②传统蒸馒头常采用酵头发面,再用Na2CO3调节面团酸度。查阅资料得知,酵头可使面团在微生物作用下产生CO2气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。等质量的碳酸钠和碳酸氢钠,消耗酸更多的是
③若面团发得不好,面团内的气孔少,略有酸味。可不用Na2CO3而用NaHCO3,继续揉面,上锅蒸后也能蒸出松软的馒头。解释NaHCO3的作用
(3)某品牌复合膨松剂的说明书如下图所示。其中葡萄糖酸-δ-内酯和淀粉是助剂,其作用是防止膨松剂吸潮结块而失效。焦磷酸二氢二钠的作用是

您最近一年使用:0次
名校
解题方法
10 . 物质的分离和提纯都是利用物质状态(相)的不同进行操作的,固体与液体、液体与气体、气体与固体的分离都是比较容易,相对的固固分离、液液分离、气气分离都比较困难。因此我们在进行物质的分离与提纯时经常会使用物质的状态不同进行分离。
(1)HCl中含有少量水蒸气选用的试剂为:___________ 。
(2)酒精和水分离的操作名称为:___________ 。
(3)除去CO2中的CO可采取的操作是:___________ 。
(4)氯化钠、硝酸钾的混合物中去除氯化钠的操作名称为___________ 。
(5)上述实验操作的具体操作为:___________ 。
(6)上述操作如果除不干净,可以采用的操作为___________ 。
(1)HCl中含有少量水蒸气选用的试剂为:
(2)酒精和水分离的操作名称为:
(3)除去CO2中的CO可采取的操作是:
(4)氯化钠、硝酸钾的混合物中去除氯化钠的操作名称为
(5)上述实验操作的具体操作为:
(6)上述操作如果除不干净,可以采用的操作为
您最近一年使用:0次



