名校
解题方法
1 . 过氧化钠可在呼吸面具和潜水艇中作供氧剂,实验室可用如图装置进行验证(A是实验室中制取CO2的装置,C中盛放的是过氧化钠)。下列说法不正确的是
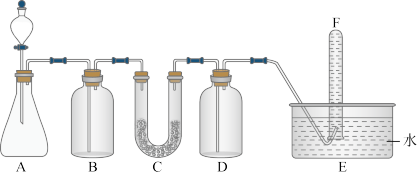

A.A中发生的反应离子方程式为: +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
| B.B中盛放饱和NaHCO3溶液,目的是除去CO2中的HCl气体 |
| C.C中每转移0.2mol电子,产生O2 0.1mol |
| D.D装置是安全瓶,防止E中水倒流进入C中 |
您最近一年使用:0次
2022-03-22更新
|
760次组卷
|
3卷引用:江西省宜春市奉新县第一中学2021-2022学年高一下学期第一次月考化学试题
名校
2 . Ⅰ.滴定实验是化学学科中最重要的定量实验之一、葡萄酒中抗氧化剂残留量的测定,常采用氧化还原滴定法。葡萄酒常用 作抗氧化剂,测定某葡萄酒中抗氧化剂的残留量(以游离
作抗氧化剂,测定某葡萄酒中抗氧化剂的残留量(以游离 计算)的方案如下:
计算)的方案如下:

往实验中加入盐酸的目的是将 转化成
转化成 ;滴定过程中发生的反应是:
;滴定过程中发生的反应是:
(1)滴定时,该滴定过程的指示剂是___________ ,滴定终点的判断方法___________ 。
(2)实验消耗标准 溶液50.00ml,所测样品中抗氧化剂的残留量(以游离
溶液50.00ml,所测样品中抗氧化剂的残留量(以游离 计算)为
计算)为___________  。
。
(3)下列情形会造成测定结果偏高的是___________(填序号)。
Ⅱ.回答下列问题
(4) 随意排放会造成严重的大气污染。某小组同学利用
随意排放会造成严重的大气污染。某小组同学利用 溶液氧化吸收烟气中
溶液氧化吸收烟气中
①该反应的离子方程式___________ (反应a)。
为验证该反应,同学们将 通入0.05mol/L
通入0.05mol/L 溶液中,溶液很快由黄色变为红褐色;将溶液长时间放置后,最终变为浅绿色。关于红褐色液体,以下是同学们的分析推测与实验。
溶液中,溶液很快由黄色变为红褐色;将溶液长时间放置后,最终变为浅绿色。关于红褐色液体,以下是同学们的分析推测与实验。
②利用胶体的___________ (填性质)可以检验步骤Ⅰ中是否得到了 胶体。
胶体。
③根据反应b说明步骤II中液体颜色变化的原因是___________ (用离子方程式及必要的文字说明)。
④经讨论后得出结论: 溶液和
溶液和 反应过程中,反应a、b在体系中共存。请从化学反应速率和反应限度的角度分析,
反应过程中,反应a、b在体系中共存。请从化学反应速率和反应限度的角度分析, 通入
通入 溶液产生上述现象的原因
溶液产生上述现象的原因___________ 。
 作抗氧化剂,测定某葡萄酒中抗氧化剂的残留量(以游离
作抗氧化剂,测定某葡萄酒中抗氧化剂的残留量(以游离 计算)的方案如下:
计算)的方案如下:
往实验中加入盐酸的目的是将
 转化成
转化成 ;滴定过程中发生的反应是:
;滴定过程中发生的反应是:
(1)滴定时,该滴定过程的指示剂是
(2)实验消耗标准
 溶液50.00ml,所测样品中抗氧化剂的残留量(以游离
溶液50.00ml,所测样品中抗氧化剂的残留量(以游离 计算)为
计算)为 。
。(3)下列情形会造成测定结果偏高的是___________(填序号)。
| A.滴定持续时间稍长,溶液中部分HI被空气氧化 |
B.盛装标准 溶液的滴定管用蒸馏水洗净后,未润洗 溶液的滴定管用蒸馏水洗净后,未润洗 |
| C.滴定前平视,滴定后俯视 |
| D.滴定前滴定管尖嘴有气泡滴定后气泡消失 |
Ⅱ.回答下列问题
(4)
 随意排放会造成严重的大气污染。某小组同学利用
随意排放会造成严重的大气污染。某小组同学利用 溶液氧化吸收烟气中
溶液氧化吸收烟气中
①该反应的离子方程式
为验证该反应,同学们将
 通入0.05mol/L
通入0.05mol/L 溶液中,溶液很快由黄色变为红褐色;将溶液长时间放置后,最终变为浅绿色。关于红褐色液体,以下是同学们的分析推测与实验。
溶液中,溶液很快由黄色变为红褐色;将溶液长时间放置后,最终变为浅绿色。关于红褐色液体,以下是同学们的分析推测与实验。| 分析推测 | 实验步骤及现象 |
甲:生成了 胶体 胶体乙:经查阅资料,可能发生反应: 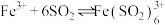 (反应b)(红褐色) (反应b)(红褐色) | Ⅰ.制备 胶体并检验 胶体并检验Ⅱ.分别向  胶体和该红褐色液体中加入适量铁粉,振荡后前者不变色,后者变为浅绿色 胶体和该红褐色液体中加入适量铁粉,振荡后前者不变色,后者变为浅绿色 |
 胶体。
胶体。③根据反应b说明步骤II中液体颜色变化的原因是
④经讨论后得出结论:
 溶液和
溶液和 反应过程中,反应a、b在体系中共存。请从化学反应速率和反应限度的角度分析,
反应过程中,反应a、b在体系中共存。请从化学反应速率和反应限度的角度分析, 通入
通入 溶液产生上述现象的原因
溶液产生上述现象的原因
您最近一年使用:0次
名校
解题方法
3 . 氯化铁主要用作饮水的净水剂和废水处理的沉淀剂,还可在印染工业用作靛蓝染料染色时的氧化剂和印染媒染剂。
Ⅰ.利用硫铁矿烧渣(主要成分为FeO、 、
、 )生产三氯化铁晶体(
)生产三氯化铁晶体( )的工艺流程示意图如图。此法具有工艺条件温和,操作方法简单,容易形成规模生产等优点。
)的工艺流程示意图如图。此法具有工艺条件温和,操作方法简单,容易形成规模生产等优点。
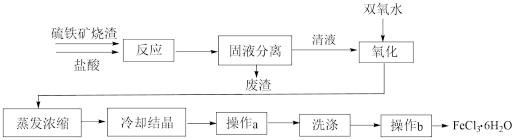
(1)硫铁矿烧渣与盐酸发生反应的化学方程式有_____ 、_____ 、_____ 。
Ⅱ.学习小组对 催化
催化 分解实验进行探究。
分解实验进行探究。
实验操作与现象如下表:
(2) 分解的反应中氧化剂与还原剂的物质的量之比为
分解的反应中氧化剂与还原剂的物质的量之比为___________ 。
(3)上述实验证明了 的催化作用,其催化机理可表示为
的催化作用,其催化机理可表示为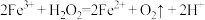 和
和___________ 。
Ⅲ.为了验证反应中 和
和 之间转化关系的存在,再另取a、b两支试管,进一步实验。
之间转化关系的存在,再另取a、b两支试管,进一步实验。
已知:实验中所用的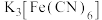 溶液放置了两周以上,其中杂质不影响
溶液放置了两周以上,其中杂质不影响 的检验,且此
的检验,且此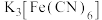 溶液遇
溶液遇 会出现蓝色沉淀、遇
会出现蓝色沉淀、遇 呈绿色。
呈绿色。
(4)试管a中盛有10% 溶液,向其中滴加3滴
溶液,向其中滴加3滴 溶液,反应开始后立即滴入
溶液,反应开始后立即滴入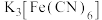 溶液,出现蓝色沉淀,说明有
溶液,出现蓝色沉淀,说明有___________ 生成。
(5)试管b中盛有蒸馏水,向其中滴加3滴 溶液后,再滴加某
溶液后,再滴加某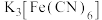 溶液,试管内溶液变为绿色,设置该实验的目的为
溶液,试管内溶液变为绿色,设置该实验的目的为___________ 。
Ⅰ.利用硫铁矿烧渣(主要成分为FeO、
 、
、 )生产三氯化铁晶体(
)生产三氯化铁晶体( )的工艺流程示意图如图。此法具有工艺条件温和,操作方法简单,容易形成规模生产等优点。
)的工艺流程示意图如图。此法具有工艺条件温和,操作方法简单,容易形成规模生产等优点。
(1)硫铁矿烧渣与盐酸发生反应的化学方程式有
Ⅱ.学习小组对
 催化
催化 分解实验进行探究。
分解实验进行探究。实验操作与现象如下表:
| 操作 | 现象 |
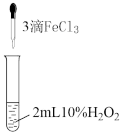 | 溶液颜色迅速变深后又变回原色,并产生较多气泡 |
 分解的反应中氧化剂与还原剂的物质的量之比为
分解的反应中氧化剂与还原剂的物质的量之比为(3)上述实验证明了
 的催化作用,其催化机理可表示为
的催化作用,其催化机理可表示为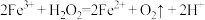 和
和Ⅲ.为了验证反应中
 和
和 之间转化关系的存在,再另取a、b两支试管,进一步实验。
之间转化关系的存在,再另取a、b两支试管,进一步实验。已知:实验中所用的
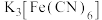 溶液放置了两周以上,其中杂质不影响
溶液放置了两周以上,其中杂质不影响 的检验,且此
的检验,且此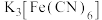 溶液遇
溶液遇 会出现蓝色沉淀、遇
会出现蓝色沉淀、遇 呈绿色。
呈绿色。(4)试管a中盛有10%
 溶液,向其中滴加3滴
溶液,向其中滴加3滴 溶液,反应开始后立即滴入
溶液,反应开始后立即滴入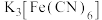 溶液,出现蓝色沉淀,说明有
溶液,出现蓝色沉淀,说明有(5)试管b中盛有蒸馏水,向其中滴加3滴
 溶液后,再滴加某
溶液后,再滴加某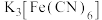 溶液,试管内溶液变为绿色,设置该实验的目的为
溶液,试管内溶液变为绿色,设置该实验的目的为
您最近一年使用:0次
名校
4 . 下列实验的操作、现象和结论都正确的是
| 选项 | 实验目的 | 操作 | 现象和结论 |
| A | 探究苯酚与钠是否反应 | 取1.5g苯酚溶于适量乙醇中,再加入绿豆大小的吸干煤油的金属钠 | 有连续的气泡产生,则钠与苯酚反应生成氢气 |
| B | 探究某无色溶液中是否含有HSO | 取少量该溶液于试管中,加入足量稀盐酸,将产生的气体通入品红溶液中 | 品红溶液褪色,则该溶液中含有HSO |
| C | 探究铁、铜金属活泼性的强弱 | 将适量的金属铜置于一定浓度的氯化铁溶液中 | 金属Cu溶解,则铁比铜活泼 |
| D | 探究CH3CH2Br在NaOH溶液中是否发生水解 | 将CH3CH2Br与NaOH溶液共热,冷却后,取出上层水溶液用稀HNO3酸化加入AgNO3溶液 | 产生淡黄色沉淀,则CH3CH2Br发生了水解反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-12-25更新
|
785次组卷
|
6卷引用:江西省重点校联盟2022-2023学年高三上学期10月联考化学试题
江西省重点校联盟2022-2023学年高三上学期10月联考化学试题山东省淄博市2021-2022学年高三12月教学质量摸底检测化学试题(已下线)解密11 化学实验(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)3.2.2 酚-2021-2022学年高二化学课后培优练(人教版2019选择性必修3)(已下线)查补易混易错点08 化学实验基础-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)查补易混易错点08 化学实验基础-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)
名校
5 .  在生产和生活中有着广泛用途,某化学小组在实验室制备
在生产和生活中有着广泛用途,某化学小组在实验室制备 并探究其性质。请回答:
并探究其性质。请回答:
(一) 的制备,分步骤Ⅰ、Ⅱ两步进行。
的制备,分步骤Ⅰ、Ⅱ两步进行。
步骤Ⅰ.先利用下图所示装置制备
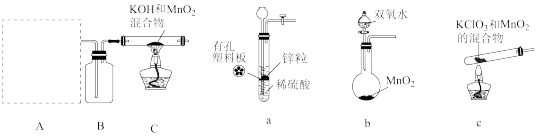
(1)装置A应选用___________ (填a、b或c)。
(2)装置B中所盛试剂的名称为___________ 。
(3)装置C处反应生成 的化学方程式为
的化学方程式为___________ 。
步骤Ⅱ.由 制备
制备 。已知:
。已知: 易溶于水,水溶液呈墨绿色。主要过程如下:
易溶于水,水溶液呈墨绿色。主要过程如下:
①充分反应后,将装置C处所得固体加水溶解,过滤;
②向滤液中通入足量CO2,过滤出生成的 ;
;
⑧将滤液蒸发浓缩、降温结晶、过滤、洗涤、干燥,得 晶体。
晶体。
(4)过程②向滤液中通入足量 ,可观察到的现象为
,可观察到的现象为___________ ;该步反应中氧化剂与还原剂的物质的量之比为___________ 。
(二)KMnO4的性质
已知:KMnO4具有强氧化性,可与草酸 反应。
反应。
(5)写出 酸性溶液与草酸反应的离子方程式
酸性溶液与草酸反应的离子方程式___________ 。
(6)基于(5)的反应原理,选择适当试剂探究浓度对化学反应速率的影响。
可供选择的试剂有:①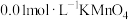 酸性溶液;②
酸性溶液;②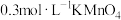 酸性溶液;③
酸性溶液;③ 溶液;④
溶液;④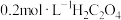 溶液,为了更好的观察现象,应选择的试剂为
溶液,为了更好的观察现象,应选择的试剂为___________ (填序号)。
 在生产和生活中有着广泛用途,某化学小组在实验室制备
在生产和生活中有着广泛用途,某化学小组在实验室制备 并探究其性质。请回答:
并探究其性质。请回答:(一)
 的制备,分步骤Ⅰ、Ⅱ两步进行。
的制备,分步骤Ⅰ、Ⅱ两步进行。步骤Ⅰ.先利用下图所示装置制备


(1)装置A应选用
(2)装置B中所盛试剂的名称为
(3)装置C处反应生成
 的化学方程式为
的化学方程式为步骤Ⅱ.由
 制备
制备 。已知:
。已知: 易溶于水,水溶液呈墨绿色。主要过程如下:
易溶于水,水溶液呈墨绿色。主要过程如下:①充分反应后,将装置C处所得固体加水溶解,过滤;
②向滤液中通入足量CO2,过滤出生成的
 ;
;⑧将滤液蒸发浓缩、降温结晶、过滤、洗涤、干燥,得
 晶体。
晶体。(4)过程②向滤液中通入足量
 ,可观察到的现象为
,可观察到的现象为(二)KMnO4的性质
已知:KMnO4具有强氧化性,可与草酸
 反应。
反应。(5)写出
 酸性溶液与草酸反应的离子方程式
酸性溶液与草酸反应的离子方程式(6)基于(5)的反应原理,选择适当试剂探究浓度对化学反应速率的影响。
可供选择的试剂有:①
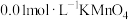 酸性溶液;②
酸性溶液;②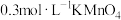 酸性溶液;③
酸性溶液;③ 溶液;④
溶液;④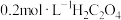 溶液,为了更好的观察现象,应选择的试剂为
溶液,为了更好的观察现象,应选择的试剂为
您最近一年使用:0次
2021-12-07更新
|
646次组卷
|
7卷引用:江西省临川一中暨临川一中实验学校2021-2022学年高二下学期第二次月考化学试题
江西省临川一中暨临川一中实验学校2021-2022学年高二下学期第二次月考化学试题河北省邢台市四校联盟2021-2022学年高三12月联考化学试题湖南省隆回县第二中学2021-2022学年高三上学期第四次月考化学试题(已下线)解密11 化学实验(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题11 物质制备类综合实验-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)回归教材重难点10 综合实验方案的设计与评价-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)回归教材重难点10 实验方案的设计与评价-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)
名校
解题方法
6 . 为检验淀粉水解的情况,进行如下图所示的实验,试管甲和丙均用60~80 ℃的水浴加热5~6 min,试管乙不加热。待试管甲、丙中的溶液冷却后再进行后续实验。
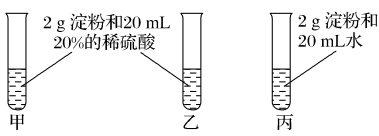
实验1:取少量甲中溶液,加入新制氢氧化铜,加热,没有红色沉淀出现。
实验2:取少量乙中溶液,滴加几滴碘水,溶液变为蓝色,但取少量甲中溶液做此实验时,溶液不变蓝色。
实验3:取少量丙中溶液加入NaOH溶液调节至碱性,再滴加碘水,溶液颜色无明显变化。
(1)写出淀粉水解的化学方程式:___________ 。
(2)设计甲和乙是为了探究___________ 对淀粉水解的影响,设计甲和丙是为了探究___________ 对淀粉水解的影响。
(3)实验1失败的原因是___________ 。
(4)实验3中溶液的颜色无明显变化的原因是___________ 。
(5)下列结论合理的是___________(填字母)。

实验1:取少量甲中溶液,加入新制氢氧化铜,加热,没有红色沉淀出现。
实验2:取少量乙中溶液,滴加几滴碘水,溶液变为蓝色,但取少量甲中溶液做此实验时,溶液不变蓝色。
实验3:取少量丙中溶液加入NaOH溶液调节至碱性,再滴加碘水,溶液颜色无明显变化。
(1)写出淀粉水解的化学方程式:
(2)设计甲和乙是为了探究
(3)实验1失败的原因是
(4)实验3中溶液的颜色无明显变化的原因是
(5)下列结论合理的是___________(填字母)。
| A.淀粉水解需要在催化剂和一定温度下进行 |
| B.欲检验淀粉是否完全水解,最好在冷却后的水解液中直接加碘 |
| C.欲检验淀粉的水解产物具有还原性,应先在水解液中加入氢氧化钠中和稀硫酸至溶液呈碱性,再加入新制氢氧化铜并加热 |
| D.若用唾液代替稀硫酸,则实验1可能出现预期的现象 |
您最近一年使用:0次
2021-11-30更新
|
723次组卷
|
15卷引用:江西省高安中学2017-2018学年高二1月月考化学试题
江西省高安中学2017-2018学年高二1月月考化学试题广东省蕉岭县蕉岭中学2018-2019学年高二下学期第三次月考化学试题福建省莆田市2020-2021学年高二下学期第二次月考化学(B卷) 试题河北省石家庄市藁城新冀明中学2020-2021学年高二下学期5月月考化学试题2015届北京市海淀区高三4月模拟练习化学试卷(已下线)2018年5月29日 淀粉水解程度的判断及水解产物的检验——《每日一题》2017-2018学年高二化学人教选修5(已下线)2019年5月14日 《每日一题》人教选修5—— 淀粉水解程度的判断及水解产物的检验(已下线)2019年10月30日 《每日一题》2020年高考一轮复习-淀粉水解程度的判断及水解产物的检验高二选择性必修3(人教版2019)第四章 生物大分子 第一节 糖类(已下线)专题09 常见有机物及其应用——备战2021年高考化学纠错笔记(已下线)4.1 糖类(C级检测练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修3)(已下线)4.2 糖类(C级检测练)-2020-2021学年高二化学章节分层检测ABC(人教版选修5)(已下线)专题08 常见有机物及其应用-备战2022年高考化学学霸纠错(全国通用)专题6 生命活动的物质基础——糖类、油脂、蛋白质 第一单元 糖类和油脂 第1课时 糖类6.1.1糖类 课后
名校
7 . 下图是实验室制备氯气并进行一系列相关实验的装置(部分夹持装置已略):

回答下列问题:
(1)装置A中是用MnO2和浓盐酸反应制备Cl2,请写出其反应的化学方程式:___________ 。
(2)装置B有安全瓶作用,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:___________ 。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ应依次放入:湿润的有色布条、___________ 、干燥的有色布条。
(4)装置E中潮湿的Cl2与Na2CO3反应,生成NaHCO3、Cl2O气体和另一种盐,试写出该反应的化学方程式:___________
(5)装置F的作用是:___________ 。
(6)反应G中的离子方程式为___________ 。
(7)设计最简单的实验方案验证E中生成的固体中存在HCO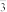 :
:___________ 。

回答下列问题:
(1)装置A中是用MnO2和浓盐酸反应制备Cl2,请写出其反应的化学方程式:
(2)装置B有安全瓶作用,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ应依次放入:湿润的有色布条、
(4)装置E中潮湿的Cl2与Na2CO3反应,生成NaHCO3、Cl2O气体和另一种盐,试写出该反应的化学方程式:
(5)装置F的作用是:
(6)反应G中的离子方程式为
(7)设计最简单的实验方案验证E中生成的固体中存在HCO
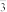 :
:
您最近一年使用:0次
2021-11-27更新
|
139次组卷
|
2卷引用:江西省赣州市赣县第三中学2021-2022学年高一上学期12月月考化学试卷
名校
解题方法
8 . 为了探究 溶液与
溶液与 溶液的反应产物,某化学兴趣小组利用如图装置进行如下实验:
溶液的反应产物,某化学兴趣小组利用如图装置进行如下实验:
Ⅰ.向盛有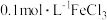 溶液的三颈瓶中,滴加一定量
溶液的三颈瓶中,滴加一定量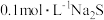 溶液,搅拌,能闻到臭鸡蛋气味,产生沉淀A。
溶液,搅拌,能闻到臭鸡蛋气味,产生沉淀A。
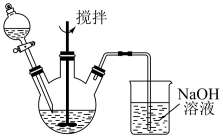
Ⅱ.向盛有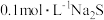 溶液的三颈瓶中,滴加少量
溶液的三颈瓶中,滴加少量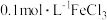 溶液,搅拌,产生沉淀B。
溶液,搅拌,产生沉淀B。
已知:① 为黑色固体,且不溶于水和盐酸。
为黑色固体,且不溶于水和盐酸。
②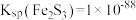 ,
, ,
,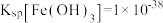 ,
, 。
。
③硫不溶于水,微溶于酒精,易溶于二硫化碳。
回答下列问题:
(1)装置中NaOH溶液的作用是___________ 。
小组同学猜测,沉淀A、B可能为S、硫化物或它们的混合物。他们设计如下实验进行探究:
实验一、探究A的成分
取沉淀A于小烧杯中,进行如下实验:
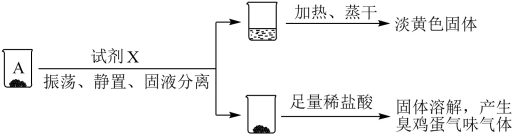
(2)试剂X是___________ 。由此推断A的成分是___________ (填化学式)。
实验二、探究B的成分
取沉淀B于小烧杯中,进行如下实验:

(3)向试管a中加入试剂Y,观察到明显现象,证明溶液中存在 。试剂Y是NaOH溶液,明显现象是
。试剂Y是NaOH溶液,明显现象是___________ 。由此推断B的成分是___________ (填化学式)。
(4)请分析Ⅱ中实验未得到 的原因是
的原因是___________ 。
 溶液与
溶液与 溶液的反应产物,某化学兴趣小组利用如图装置进行如下实验:
溶液的反应产物,某化学兴趣小组利用如图装置进行如下实验:Ⅰ.向盛有
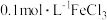 溶液的三颈瓶中,滴加一定量
溶液的三颈瓶中,滴加一定量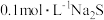 溶液,搅拌,能闻到臭鸡蛋气味,产生沉淀A。
溶液,搅拌,能闻到臭鸡蛋气味,产生沉淀A。
Ⅱ.向盛有
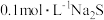 溶液的三颈瓶中,滴加少量
溶液的三颈瓶中,滴加少量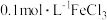 溶液,搅拌,产生沉淀B。
溶液,搅拌,产生沉淀B。已知:①
 为黑色固体,且不溶于水和盐酸。
为黑色固体,且不溶于水和盐酸。②
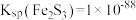 ,
, ,
,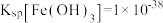 ,
, 。
。③硫不溶于水,微溶于酒精,易溶于二硫化碳。
回答下列问题:
(1)装置中NaOH溶液的作用是
小组同学猜测,沉淀A、B可能为S、硫化物或它们的混合物。他们设计如下实验进行探究:
实验一、探究A的成分
取沉淀A于小烧杯中,进行如下实验:

(2)试剂X是
实验二、探究B的成分
取沉淀B于小烧杯中,进行如下实验:

(3)向试管a中加入试剂Y,观察到明显现象,证明溶液中存在
 。试剂Y是NaOH溶液,明显现象是
。试剂Y是NaOH溶液,明显现象是(4)请分析Ⅱ中实验未得到
 的原因是
的原因是
您最近一年使用:0次
2021-11-20更新
|
480次组卷
|
9卷引用:江西省丰城中学2021-2022学年上学期高三创新实验班第四次月考化学试题
江西省丰城中学2021-2022学年上学期高三创新实验班第四次月考化学试题湖南省长沙市雅礼中学2021-2022学年高三上学期月考卷(三)化学试题山东省潍坊市2020届高三上学期期末考试化学试题(已下线)考点21 物质制备型综合实验-2020年高考化学命题预测与模拟试题分类精编山东省东营第一中学2020届高三上学期期末考试化学试题广东省省名校联盟2021届高三下学期开学考试(新高考)化学试题(已下线)小题26 探究性实验——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)2021年高考化学押题预测卷(福建卷)(03)(含考试版、答题卡、参考答案、全解全析)(已下线)第十单元 化学实验基础(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)
9 . 某研究小组将纯净的SO2气体通入0.1 mol·L-1的Ba(NO3)2溶液中,得到了BaSO4沉淀,为探究上述溶液中何种微粒能氧化通入的SO2,该小组提出了如下假设:
假设一:溶液中的NO
假设二:溶液中溶解的O2
(1)验证假设一
该小组设计实验验证了假设一,请在表格空白处填写相关实验现象。
(2)为深入研究该反应,该小组还测得上述两个实验中溶液pH随通入SO2体积的变化曲线如图:
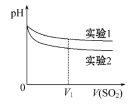
实验1中溶液pH变小的原因是_______ ;V1时,实验2中溶液pH小于实验1的原因是(用离子方程式表示)_______ 。
(3)验证假设二
请设计实验验证假设二,写出实验步骤、预期现象和结论。
(4)若假设二成立,请预测:在相同条件下,分别用足量的O2和KNO3氧化相同的H2SO3溶液(溶液体积变化忽略不计),充分反应后两溶液的pH前者_______ (填“大于”或“小于”)后者,理由略。
假设一:溶液中的NO

假设二:溶液中溶解的O2
(1)验证假设一
该小组设计实验验证了假设一,请在表格空白处填写相关实验现象。
| 实验步骤 | 实验现象 | 结论 |
| 实验1:在盛有不含O2的25 mL 0.1 mol·L-1BaCl2溶液的烧杯中,缓慢通入纯净的SO2气体 | 假设一成立 | |
| 实验2:在盛有不含O2的25 mL 0.1 mol·L-1Ba(NO3)2溶液的烧杯中,缓慢通入纯净的SO2气体 |

实验1中溶液pH变小的原因是
(3)验证假设二
请设计实验验证假设二,写出实验步骤、预期现象和结论。
| 实验步骤、预期现象和结论(不要求写具体操作过程) |
您最近一年使用:0次
名校
解题方法
10 . 将SO2分别通入无氧、有氧的浓度均为0.1mol•L-1的BaCl2溶液和Ba(NO3)2溶液中,除BaCl2溶液(无氧)外,都产生白色沉淀。实验测得各溶液pH变化曲线如图。下列说法不正确的是
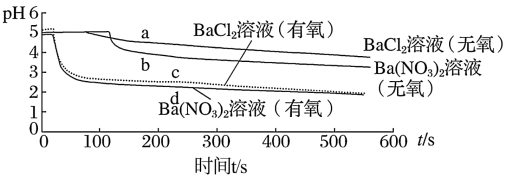
A.曲线a所示溶液pH降低的原因:SO2+H2O H2SO3 H2SO3 H++HSO H++HSO |
| B.依据曲线b可推知0.2mol•L-1KNO3溶液(无氧)能氧化SO2 |
| C.曲线c所示溶液中发生反应的离子方程式为:2Ba2++2SO2+O2+2H2O=2BaSO4↓+4H+ |
D.曲线d所表示的过程中NO 是氧化SO2的主要微粒 是氧化SO2的主要微粒 |
您最近一年使用:0次
2021-11-07更新
|
1148次组卷
|
6卷引用:江西省安福中学2023-2024学年高一下学期第一次学科练习化学试题
江西省安福中学2023-2024学年高一下学期第一次学科练习化学试题福建省龙岩第一中学2020-2021学年高三上学期第三次月考化学试题湖北省武汉市第二中学2023-2024学年高一下学期化学周练A卷(1)试卷 (已下线)必刷卷03-2022年高考化学考前信息必刷卷(河北专用)(已下线)第13讲 硫及其化合物(练)-2023年高考化学一轮复习讲练测(全国通用)山东省滨州市沾化区、阳信县2022-2023学年高一下学期期中联考化学(B)试题



