解题方法
1 . 过硫酸钠(Na2S2O8)具有极强的氧化性,且不稳定,某化学兴趣小组探究过硫酸钠的相关性质,实验如下。已知SO3是无色易挥发的固体,熔点16.8℃,沸点44.8℃。
(1)稳定性探究(装置如图):
分解原理:2Na2S2O8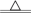 2Na2SO4+2SO3↑+O2↑。
2Na2SO4+2SO3↑+O2↑。
此装置有明显错误之处,请改正:______________________ ,水槽冰水浴的目的是____________________ ;带火星的木条的现象_______________ 。

(2)过硫酸钠在酸性环境下,在Ag+的催化作用下可以把Mn2+氧化为紫红色的离子,所得溶液加入BaCl2可以产生白色沉淀,该反应的离子方程式为______________________ ,该反应的氧化剂是______________ ,氧化产物是________ 。
(3)向上述溶液中加入足量的BaCl2,过滤后对沉淀进行洗涤的操作是___________________________ 。
(4)可用H2C2O4溶液滴定产生的紫红色离子,取20mL待测液,消耗0.1mol·L-1的H2C2O4溶液30mL,则上述溶液中紫红色离子的浓度为______ mol·L-1,若Na2S2O8有剩余,则测得的紫红色离子浓度将________ (填“偏高”“偏低”或“不变”)。
(1)稳定性探究(装置如图):
分解原理:2Na2S2O8
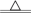 2Na2SO4+2SO3↑+O2↑。
2Na2SO4+2SO3↑+O2↑。此装置有明显错误之处,请改正:

(2)过硫酸钠在酸性环境下,在Ag+的催化作用下可以把Mn2+氧化为紫红色的离子,所得溶液加入BaCl2可以产生白色沉淀,该反应的离子方程式为
(3)向上述溶液中加入足量的BaCl2,过滤后对沉淀进行洗涤的操作是
(4)可用H2C2O4溶液滴定产生的紫红色离子,取20mL待测液,消耗0.1mol·L-1的H2C2O4溶液30mL,则上述溶液中紫红色离子的浓度为
您最近一年使用:0次
2020-04-25更新
|
296次组卷
|
3卷引用:江西省都昌蔡岭慈济中学2020届高三5月月考理综化学试题
江西省都昌蔡岭慈济中学2020届高三5月月考理综化学试题辽宁省丹东市2020届高三第一次模拟考试理科综合化学试题(已下线)专题40 硫的含氧酸盐-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)
解题方法
2 . “84消毒液”(主要成分为NaClO)能有效杀灭新型冠状病毒,某化学小组对“84消毒液”的制备和性质进行研究。请回答下列问题:
I.甲同学查阅资料知道可以利用氯气与氢氧化钠溶液反应制取“84消毒液”,同时发现“在加热情况下卤素与碱液发生如下反应:3X2+6OH-→5X-+XO3-+3H2O”。由此设计了如下装置。

(1)仪器a的名称为__________ ,B中所用试剂为__________ 。
(2)A中发生反应的离子方程式为________ 。
(3)有同学认为该实验存在明显的缺陷,如何改进:________ 。
II.乙同学阅读某“84消毒液”的包装说明得到以下信息:
严禁与洁厕灵(主要成分盐酸)同时使用。
有效氯含量在5%以上。
有效氯含量用“单位质量的含氯消毒液在酸性条件下所能释放出氯气的质量”进行表征。
(1)“84消毒液”与洁厕灵同时使用会产生有毒的氯气,写出反应的离子方程式___ 。
(2)乙同学进行如下实验测定有效氯:
步骤一:取C中大试管溶液5 g于锥形瓶,加入20 mL 0.5 mol·L-1 KI溶液,10 mL 2 mol·L-1的硫酸溶液。
步骤二:用0.1000 mol·L-1 Na2S2O3标准溶液滴定锥形瓶中的溶液,指示剂显示终点时共用去20.00 mL Na2S2O3溶液。(I2+2S2O32-=2I-+S4O62-)
步骤一反应的离子方程式为________ 。通常选用__________ 作指示剂,滴定至终点的现象________ 。此消毒液有效氯含量为__________ %(保留二位有效数字)。
I.甲同学查阅资料知道可以利用氯气与氢氧化钠溶液反应制取“84消毒液”,同时发现“在加热情况下卤素与碱液发生如下反应:3X2+6OH-→5X-+XO3-+3H2O”。由此设计了如下装置。

(1)仪器a的名称为
(2)A中发生反应的离子方程式为
(3)有同学认为该实验存在明显的缺陷,如何改进:
II.乙同学阅读某“84消毒液”的包装说明得到以下信息:
严禁与洁厕灵(主要成分盐酸)同时使用。
有效氯含量在5%以上。
有效氯含量用“单位质量的含氯消毒液在酸性条件下所能释放出氯气的质量”进行表征。
(1)“84消毒液”与洁厕灵同时使用会产生有毒的氯气,写出反应的离子方程式
(2)乙同学进行如下实验测定有效氯:
步骤一:取C中大试管溶液5 g于锥形瓶,加入20 mL 0.5 mol·L-1 KI溶液,10 mL 2 mol·L-1的硫酸溶液。
步骤二:用0.1000 mol·L-1 Na2S2O3标准溶液滴定锥形瓶中的溶液,指示剂显示终点时共用去20.00 mL Na2S2O3溶液。(I2+2S2O32-=2I-+S4O62-)
步骤一反应的离子方程式为
您最近一年使用:0次
2020-04-21更新
|
130次组卷
|
2卷引用:江西省宜春市奉新县冶城职业学校(奉新县第三中学)2020-2021学年高三上学期第五次月考化学试题
19-20高一·全国·期末
名校
解题方法
3 . 铝是一种应用广泛的金属。某兴趣小组对金属铝展开了系列研究。
I. 研究铝的化学性质
(1)铝和酸、碱、盐溶液的反应
实验一的现象为______________________ 。
实验二查阅资料:铝和氢氧化钠、水反应生成偏铝酸钠(NaAlO2)和氢气,反应的化学方程式为__________________________________ 。
实验三表明,铝的金属活动性______ (填“大于“或”小于“)铜。
(2)小组同学将实验一中的稀盐酸换成等质量、氢离子浓度相同的稀硫酸,相同时间内发现铝片表面产生的气泡较少,反应较慢。对比上述两组实验产生猜想。 猜想①:稀盐酸中的氯离子对反应可能有促进作用。 猜想②:________________ 。为验证猜想①是否合理,应在铝和稀硫酸中加入_______________ (填字母),观察现象。
A.Na2SO4 B.Na2CO3 C.NaCl
II. 测定某铝样品中金属铝的质量分数
【资料1】氢氧化铝能与氢氧化钠溶液反应,但不与氨水反应。
【资料2】AlCl3+3NaOH=Al(OH)3↓+3NaCl
AlCl3+3NH3·H2O=Al(OH)3↓+3NH4Cl。
(3)小组同学称取4.62g某金属铝样品(样品中杂质仅为氧化铝),置于图一烧瓶中,加入足量稀盐酸至完全反应。将反应后的液体分成溶液1和溶液2两等份,设计两种实验方案(如图三),通过沉淀质量测定样品中金属铝的质量分数。

①选择正确的一种实验方案,计算样品中金属铝的质量分数______ (保留3位有效数字).
②小组同学组合图一和图二装置测氢气体积,烧瓶中反应停止即读出量筒内水的体积, 计算后发现金属铝的质量分数偏大,可能的原因是______________________ 。
I. 研究铝的化学性质
(1)铝和酸、碱、盐溶液的反应
| 实验 | 操作 | 现象 | 结论 |
| 一 | 将铝片放入稀盐酸中 | ,试管变烫 | 铝能与盐酸发生反应,反应放热 |
| 二 | 将铝片放入氢氧化钠溶液中 | 铝表面有气泡产生,试管变烫 | 铝能与氢氧化钠溶液反应,反应放热 |
| 三 | 将铝放入硫酸铜溶液中 | 铝表面有红色物质产生,溶液逐渐变成无色 | 金属活动性:铝 铜 |
实验一的现象为
实验二查阅资料:铝和氢氧化钠、水反应生成偏铝酸钠(NaAlO2)和氢气,反应的化学方程式为
实验三表明,铝的金属活动性
(2)小组同学将实验一中的稀盐酸换成等质量、氢离子浓度相同的稀硫酸,相同时间内发现铝片表面产生的气泡较少,反应较慢。对比上述两组实验产生猜想。 猜想①:稀盐酸中的氯离子对反应可能有促进作用。 猜想②:
A.Na2SO4 B.Na2CO3 C.NaCl
II. 测定某铝样品中金属铝的质量分数
【资料1】氢氧化铝能与氢氧化钠溶液反应,但不与氨水反应。
【资料2】AlCl3+3NaOH=Al(OH)3↓+3NaCl
AlCl3+3NH3·H2O=Al(OH)3↓+3NH4Cl。
(3)小组同学称取4.62g某金属铝样品(样品中杂质仅为氧化铝),置于图一烧瓶中,加入足量稀盐酸至完全反应。将反应后的液体分成溶液1和溶液2两等份,设计两种实验方案(如图三),通过沉淀质量测定样品中金属铝的质量分数。

①选择正确的一种实验方案,计算样品中金属铝的质量分数
②小组同学组合图一和图二装置测氢气体积,烧瓶中反应停止即读出量筒内水的体积, 计算后发现金属铝的质量分数偏大,可能的原因是
您最近一年使用:0次
4 . “84消毒液”(主要溶质为次氯酸钠和氯化钠)与硫酸溶液加热反应可以制取氯气。为探究氯气的性质,某同学设计了如下所示的实验装置。(已知:氧化性Cl2>I2)
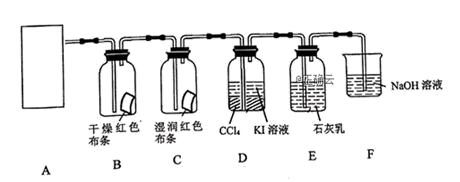
请回答:
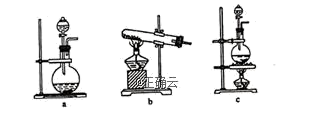
(1)在该实验中,用“84消毒液制取氯气的离子方程式为____ 。A方框中应选用以下装置中的 ____ (填字母)
(2)装置B、C中依次放的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中的布条也褪色,分析原因并提出改进方法____ 。
(3)将装置D中的混合物,充分振荡静置后观察到的现象是____ 。
(4)E中通入氯气后,得到的混合物可用于杀消毒,其有效成分为____ (化学式)但该物质敞口放置在空气中会失效,用化学方程式解释其原因 ____ 。
(5)F的作用为____ 。

请回答:
(1)在该实验中,用“84消毒液制取氯气的离子方程式为

(2)装置B、C中依次放的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中的布条也褪色,分析原因并提出改进方法
(3)将装置D中的混合物,充分振荡静置后观察到的现象是
(4)E中通入氯气后,得到的混合物可用于杀消毒,其有效成分为
(5)F的作用为
您最近一年使用:0次
18-19高一下·江西南昌·阶段练习
名校
5 . 某化学兴趣小组用下图装置制取并探究氯气的性质。
(A装置中发生反应的化学方程式:2KMnO4+16HCl(浓)=2KCl+2MnCl2+ 5Cl2↑+ 8H2O)

(1)制取氯气反应中氯气是_______ (填“氧化产物”或“还原产物”);
(2)实验进行一段时间后,可观察到_____ (填“B”或“C”)装置中有色布条褪色。
(3)E装置中发生的化学反应的化学方程式___________________ 。
(4)用31.6 g KMnO4固体与足量的浓盐酸反应,最多可生成标准状况下____ L氯气。
(A装置中发生反应的化学方程式:2KMnO4+16HCl(浓)=2KCl+2MnCl2+ 5Cl2↑+ 8H2O)

(1)制取氯气反应中氯气是
(2)实验进行一段时间后,可观察到
(3)E装置中发生的化学反应的化学方程式
(4)用31.6 g KMnO4固体与足量的浓盐酸反应,最多可生成标准状况下
您最近一年使用:0次
18-19高一下·江西南昌·阶段练习
名校
6 . 硫酸是化工行业广泛应用的基础原料,某化学兴趣小组为探究浓硫酸所具有的一些特殊性质,进行如下有关实验.
实验一:浓硫酸和铜反应

(1)装置A中发生反应的化学方程式为______________________
(2)装置D中试管口放置的棉花中浸有NaOH浓溶液,其作用是_________________
(3)装置B的作用是贮存多余的气体.当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中由于气压增大引发的现象是_____________________ B中应放置的液体是_________ (填字母).
A.水 B.酸性KMnO4溶液 C.浓溴水 D.饱和NaHSO3溶液
实验二:浓硫酸与碳反应并验证反应生成的气体产物

(4)冯同学认为按照甲、丙、丁、乙的装置顺序,即可验证产物为二氧化硫和二氧化碳,那么丁中酸性KMnO4溶液的作用是____________________ ;
(5)陈同学认为丙装置要使用两次才能确保检验气体产物的准确性,如按该同学所说,气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):A——____________________________ ——B,能证明有CO2生成的现象:① ________________________ ;②_____________________
实验一:浓硫酸和铜反应

(1)装置A中发生反应的化学方程式为
(2)装置D中试管口放置的棉花中浸有NaOH浓溶液,其作用是
(3)装置B的作用是贮存多余的气体.当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中由于气压增大引发的现象是
A.水 B.酸性KMnO4溶液 C.浓溴水 D.饱和NaHSO3溶液
实验二:浓硫酸与碳反应并验证反应生成的气体产物

(4)冯同学认为按照甲、丙、丁、乙的装置顺序,即可验证产物为二氧化硫和二氧化碳,那么丁中酸性KMnO4溶液的作用是
(5)陈同学认为丙装置要使用两次才能确保检验气体产物的准确性,如按该同学所说,气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):A——
您最近一年使用:0次
18-19高一下·江西南昌·期中
解题方法
7 . X、Y、Z、W为原子序数依次递增的短周期元素。已知:X是空气中含量最高的元素,Y和Z同主族,Z和W的氢化物具有相同的电子数,X的核外电子总数等于W的最外层电子数,在中学范围内Y的单质只有氧化性,且是空气的主要成分之一。
(1)写出实验室制取W2反应的离子方程式:_____________________ ;
(2)某小组设计如图所示的装置,分别研究ZY2和W2的性质.
①分别通入ZY2和W2,在装置A中观察到的现象是否相同__________ (填“相同”或“不相同”);若装置D中装的是Fe粉,当通入足量W2时观察到的现象为__________ ;若装置D中装的是五氧化二钒(催化剂),当通入足量ZY2时,打开K通入适量Y2,化学反应方程式为______________ ;
②若装置B中装有0.05mol的碘水,当通入足量W2完全反应后,转移了0.5mol电子,则该反应的氧化产物的化学式为_______________ ;
(3)某同学将足量的ZY2通入一支装有氯化钡溶液的试管,未见沉淀生成,再向该试管中加入过量的下列溶液也无沉淀生成的是______________ (填字母)。
A.氨水 B.稀盐酸 C.稀硝酸 D. 双氧水 E.硝酸银
(4)一定量的Mg溶于一定浓度的X的最高价氧化物对应的水化物中充分反应,产生标况下的X2Y气体11.2L,在所得溶液中加入过量NaOH溶液完全反应后,过滤出沉淀,经洗涤、蒸干并充分灼烧,最后得到固体物质的质量为___________ 。
(1)写出实验室制取W2反应的离子方程式:
(2)某小组设计如图所示的装置,分别研究ZY2和W2的性质.
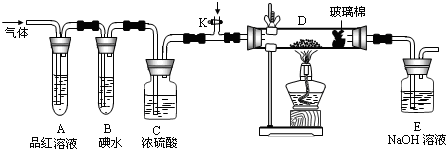
①分别通入ZY2和W2,在装置A中观察到的现象是否相同
②若装置B中装有0.05mol的碘水,当通入足量W2完全反应后,转移了0.5mol电子,则该反应的氧化产物的化学式为
(3)某同学将足量的ZY2通入一支装有氯化钡溶液的试管,未见沉淀生成,再向该试管中加入过量的下列溶液也无沉淀生成的是
A.氨水 B.稀盐酸 C.稀硝酸 D. 双氧水 E.硝酸银
(4)一定量的Mg溶于一定浓度的X的最高价氧化物对应的水化物中充分反应,产生标况下的X2Y气体11.2L,在所得溶液中加入过量NaOH溶液完全反应后,过滤出沉淀,经洗涤、蒸干并充分灼烧,最后得到固体物质的质量为
您最近一年使用:0次
18-19高一下·江西南昌·阶段练习
解题方法
8 . 实验室为探究铁与足量浓硫酸反应,并验证SO2的性质,设计如图装置进行实验。下列说法错误的是
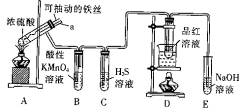

| A.装置B中酸性KMnO4溶液逐渐褪色,体现SO2的还原性 |
| B.装置C中出现淡黄色浑浊,体现了SO2的氧化性 |
| C.装置D中品红溶液褪色可以验证SO2的漂白性 |
| D.实验结束后可向装置A的溶液中滴加KSCN溶液检验是否有Fe2+ |
您最近一年使用:0次
解题方法
9 . 为探究乙烯与溴的加成反应,甲同学设计并进行如下实验:先取一定量的工业用乙烯气体(在储气瓶中),使气体通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应;乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊物质,推测在工业上制得的乙烯中还可能含有少量还原性气体杂质,由此他提出必须先除去杂质,再让乙烯与溴水反应。请回答下列问题:
(1)甲同学设计的实验________ (填“能”或“不能”)验证乙烯与溴发生了加成反应,其理由是________ (填序号)。
①使溴水褪色的反应不一定是加成反应
②使溴水褪色的反应就是加成反应
③使溴水褪色的物质不一定是乙烯
④使溴水褪色的物质就是乙烯
(2)乙同学推测此乙烯中一定含有的一种杂质气体是________ ,它与溴水反应的化学方程式是________________ 。在实验前必须全部除去,除去该杂质的试剂可用________ 。
(3)为验证乙烯与溴发生的反应是加成反应而不是取代反应,丙同学提出可用 试纸来测试反应后溶液的酸性,理由是
试纸来测试反应后溶液的酸性,理由是_____________________________________________________________________________ 。
(1)甲同学设计的实验
①使溴水褪色的反应不一定是加成反应
②使溴水褪色的反应就是加成反应
③使溴水褪色的物质不一定是乙烯
④使溴水褪色的物质就是乙烯
(2)乙同学推测此乙烯中一定含有的一种杂质气体是
(3)为验证乙烯与溴发生的反应是加成反应而不是取代反应,丙同学提出可用
 试纸来测试反应后溶液的酸性,理由是
试纸来测试反应后溶液的酸性,理由是
您最近一年使用:0次
2020-04-15更新
|
215次组卷
|
3卷引用:江西省九江市都昌县第三中学2019?2020学年高一下学期五月教学检测化学试题
名校
解题方法
10 . 欲进行下列实验,其方案设计合理的是( )
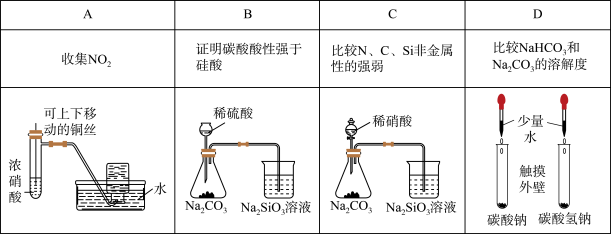

| A.A | B.B | C.C | D.D |
您最近一年使用:0次



