1 . 某研究性学习小组根据反应 ,进行SO2的制备及性质探究实验。请回答下列问题:
,进行SO2的制备及性质探究实验。请回答下列问题:
(1)将SO2气体分别通入下列溶液中:
①品红溶液,现象是___________
②氢硫酸(H2S水溶液),反应的化学方程式___________
③SO2与澄清石灰水反应方程式___________
(2)有一小组在实验中发现,SO2气体产生缓慢(不考虑SO2在溶液中的溶解),实验中不存在漏气、反应温度等装置和操作上的问题,请你推测可能的原因:___________ 。
 ,进行SO2的制备及性质探究实验。请回答下列问题:
,进行SO2的制备及性质探究实验。请回答下列问题:(1)将SO2气体分别通入下列溶液中:
①品红溶液,现象是
②氢硫酸(H2S水溶液),反应的化学方程式
③SO2与澄清石灰水反应方程式
(2)有一小组在实验中发现,SO2气体产生缓慢(不考虑SO2在溶液中的溶解),实验中不存在漏气、反应温度等装置和操作上的问题,请你推测可能的原因:
您最近一年使用:0次
2 . 某小组在实验室中探究金属钠与二氧化碳的反应。回答下列问题:
(1)选用如图所示装置及药品制取CO2。打开弹簧夹,制取CO2。反应结束后,关闭弹簧夹,球形干燥管内可观察到的现象是_______ 。不能用稀硫酸代替稀盐酸,其原因是_______ 。

(2)产生的气体经过饱和NaHCO3溶液、浓H2SO4洗气干燥后,得到质量为13.2g的CO2,在标准状况下的体积为_______ L。
(3)金属钠与二氧化碳反应的实验步骤及现象如下表:
①为检验集气瓶瓶壁上白色物质的成分,取适量滤液于2支试管中,向一支试管中滴加1滴酚酞溶液,溶液变红:向第二支试管中滴加澄清石灰水,溶液变浑浊。据此推断,白色物质的主要成分是_______ (填标号)。
A.Na2O B.Na2O2 C.NaOH D.Na2CO3
②为检验黑色固体的成分,将其与CuO共热,生成红色固体。据此推断黑色固体是_______ 。
③本实验中金属钠与二氧化碳反应的化学方程式为_______ 。
(1)选用如图所示装置及药品制取CO2。打开弹簧夹,制取CO2。反应结束后,关闭弹簧夹,球形干燥管内可观察到的现象是

(2)产生的气体经过饱和NaHCO3溶液、浓H2SO4洗气干燥后,得到质量为13.2g的CO2,在标准状况下的体积为
(3)金属钠与二氧化碳反应的实验步骤及现象如下表:
| 步骤 | 现象 |
| 将一小块金属钠在燃烧匙中加热融化,迅速伸入盛有CO2的集气瓶中。充分反应,放置冷却 | 产生大量白烟,集气瓶底部有黑色固体产生,瓶壁上有白色物质产生 |
| 在集气瓶中加入适量蒸馏水,振荡。过滤 | 滤纸上留下黑色固体,滤液为无色溶液 |
A.Na2O B.Na2O2 C.NaOH D.Na2CO3
②为检验黑色固体的成分,将其与CuO共热,生成红色固体。据此推断黑色固体是
③本实验中金属钠与二氧化碳反应的化学方程式为
您最近一年使用:0次
名校
3 . 实验小组探究 和
和 的性质。
的性质。
【进行实验】
(1)写出实验1中 与盐酸反应的离子方程式
与盐酸反应的离子方程式___________ 。
(2)①实验2中,试剂a是___________ ,此实验得出的结论是___________ 。
②称量 固体168g,加热一段时间之后,剩余固体的质量为137g,则剩余固体中
固体168g,加热一段时间之后,剩余固体的质量为137g,则剩余固体中 与
与 的物质的量之比为
的物质的量之比为___________ 。
已知: 易溶于水。
易溶于水。
(3) 溶液与
溶液与 溶液混合的现象中,有些只观察到浑浊但没有观察到气体,可能原因是
溶液混合的现象中,有些只观察到浑浊但没有观察到气体,可能原因是___________ 。
(4)写出溶液中 与
与 反应的离子方程式
反应的离子方程式___________ 。
【反思评价】
(5)根据实验3,鉴别浓度均为0.50 的
的 和
和 的方法是:分别取等量溶液置于两试管中,
的方法是:分别取等量溶液置于两试管中,___________ 。
 和
和 的性质。
的性质。【进行实验】
| 序号 | 实验装置 | 主要实验步骤 | 实验现象 |
| 实验1 |  | 向2支试管中分别加入少量 和 和 溶液,再分别滴加盐酸 溶液,再分别滴加盐酸 | 2支试管中均有气泡产生 |
| 实验2 | 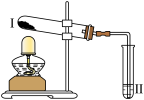 | 向Ⅱ中加入试剂a,向Ⅰ中加入少量 或 或 固体,分别加热一段时间 固体,分别加热一段时间 |  受热时Ⅱ中无明显现象, 受热时Ⅱ中无明显现象, 受热时Ⅱ出现浑浊 受热时Ⅱ出现浑浊 |
(1)写出实验1中
 与盐酸反应的离子方程式
与盐酸反应的离子方程式(2)①实验2中,试剂a是
②称量
 固体168g,加热一段时间之后,剩余固体的质量为137g,则剩余固体中
固体168g,加热一段时间之后,剩余固体的质量为137g,则剩余固体中 与
与 的物质的量之比为
的物质的量之比为| 实验3 |  |  | |||
浓度/ | 0.01 | 0.10 | 0.50 | 0.01 | |
 | 0.01 | 无明显现象 | 有浑浊 | 有浑浊 | 有浑浊 |
| 0.10 | 无明显现象 | 有浑浊 | 有浑浊,有微小气泡 | 有沉淀 | |
| 0.50 | 无明显现象 | 有浑浊 | 有浑浊,有大量气泡 | 有沉淀 | |
已知:
 易溶于水。
易溶于水。(3)
 溶液与
溶液与 溶液混合的现象中,有些只观察到浑浊但没有观察到气体,可能原因是
溶液混合的现象中,有些只观察到浑浊但没有观察到气体,可能原因是(4)写出溶液中
 与
与 反应的离子方程式
反应的离子方程式【反思评价】
(5)根据实验3,鉴别浓度均为0.50
 的
的 和
和 的方法是:分别取等量溶液置于两试管中,
的方法是:分别取等量溶液置于两试管中,
您最近一年使用:0次
2023-11-29更新
|
296次组卷
|
2卷引用:江苏省天一中学2023-2024学年高一上学期期中考试化学试卷(强化班)
4 . 某实验室利用 和
和 反应合成硫酰氯(
反应合成硫酰氯( ),并对
),并对 和HClO的酸性强弱进行探究。已知
和HClO的酸性强弱进行探究。已知 的熔点为-54.1℃,沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量HCl白雾,100℃以上分解生成
的熔点为-54.1℃,沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量HCl白雾,100℃以上分解生成 和
和 。实验室合成
。实验室合成 的原理:
的原理: ,且反应会放出大量的热。实验装置如图所示(夹持仪器已省略),请回答下列问题:
,且反应会放出大量的热。实验装置如图所示(夹持仪器已省略),请回答下列问题:
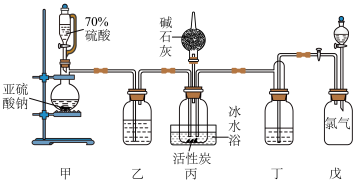
(1)写出碱石灰起作用的化学方程式:_______ 。(写一个即可)
(2)装置戊上方分液漏斗中最好选用_______ (填字母)。
a.蒸馏水 b.饱和食盐水 c.浓氢氧化钠溶液 d. 盐酸
盐酸
(3)装置乙和丁盛放的试剂均是_______ 。
(4)装置丙放置在冰水浴中的原因是_______ 。
(5) 和水反应的化学方程式为
和水反应的化学方程式为_______ 。
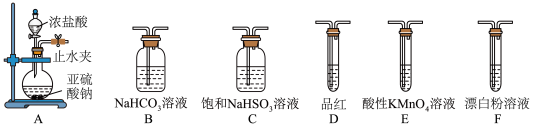
(6)选用下面的装置探究酸性: ,溶液均足量,其连接顺序为A→
,溶液均足量,其连接顺序为A→_______ 。能证明 的酸性强于HClO的实验现象为
的酸性强于HClO的实验现象为_______ 。信息: 可以使品红褪色,通常用来检验;
可以使品红褪色,通常用来检验; 难溶于饱和的
难溶于饱和的 ;
; 酸性大于
酸性大于
 和
和 反应合成硫酰氯(
反应合成硫酰氯( ),并对
),并对 和HClO的酸性强弱进行探究。已知
和HClO的酸性强弱进行探究。已知 的熔点为-54.1℃,沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量HCl白雾,100℃以上分解生成
的熔点为-54.1℃,沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量HCl白雾,100℃以上分解生成 和
和 。实验室合成
。实验室合成 的原理:
的原理: ,且反应会放出大量的热。实验装置如图所示(夹持仪器已省略),请回答下列问题:
,且反应会放出大量的热。实验装置如图所示(夹持仪器已省略),请回答下列问题:
(1)写出碱石灰起作用的化学方程式:
(2)装置戊上方分液漏斗中最好选用
a.蒸馏水 b.饱和食盐水 c.浓氢氧化钠溶液 d.
 盐酸
盐酸(3)装置乙和丁盛放的试剂均是
(4)装置丙放置在冰水浴中的原因是
(5)
 和水反应的化学方程式为
和水反应的化学方程式为(6)选用下面的装置探究酸性:
 ,溶液均足量,其连接顺序为A→
,溶液均足量,其连接顺序为A→ 的酸性强于HClO的实验现象为
的酸性强于HClO的实验现象为 可以使品红褪色,通常用来检验;
可以使品红褪色,通常用来检验; 难溶于饱和的
难溶于饱和的 ;
; 酸性大于
酸性大于

您最近一年使用:0次
2023-11-29更新
|
346次组卷
|
2卷引用:江苏省天一中学2023-2024学年高一上学期期中考试化学试卷(强化班)
5 . 某学习小组探究潮湿的 与
与 反应的产物,进行如下实验:
反应的产物,进行如下实验:
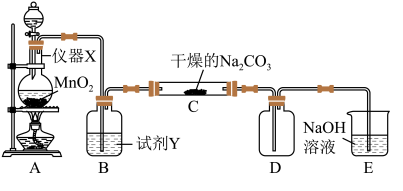
请回答:
(1)试剂Y是______ 。
(2)请写出装置A中的化学方程式______ 。
(3)装置C中潮湿的 与
与 以等物质的量反应,生成
以等物质的量反应,生成 、气体
、气体 和另一种盐,试写出该反应化学方程式
和另一种盐,试写出该反应化学方程式______ 。
(4)若将上述装置中的C、D、E部分换成下图所述装置,其中Ⅰ与Ⅲ是干燥的有色布条,E中盛装 溶液,请回答下列问题:
溶液,请回答下列问题:
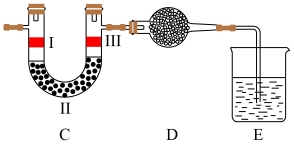
①装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅱ的作用是______ 。
②E中化学方程式______ 。
 与
与 反应的产物,进行如下实验:
反应的产物,进行如下实验:
请回答:
(1)试剂Y是
(2)请写出装置A中的化学方程式
(3)装置C中潮湿的
 与
与 以等物质的量反应,生成
以等物质的量反应,生成 、气体
、气体 和另一种盐,试写出该反应化学方程式
和另一种盐,试写出该反应化学方程式(4)若将上述装置中的C、D、E部分换成下图所述装置,其中Ⅰ与Ⅲ是干燥的有色布条,E中盛装
 溶液,请回答下列问题:
溶液,请回答下列问题:
①装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅱ的作用是
②E中化学方程式
您最近一年使用:0次
解题方法
6 . 如图所示,根据实验室制取氯气的原理制备氯气并进行性质验证,回答下列问题:

(1)装置A的名称为___________ 。
(2)利用装置丙制取饱和氯水并测其pH。
①证明氯水已饱和的现象是___________ 。
②若撤去装置乙,直接将装置甲和丙相连,这样做对实验测定结果的影响是___________ 。
(3)在装有20mL饱和氯水试管中加入过量的块状碳酸钙,过滤,将滤液滴在有色布条上,发现其褪色速度比用饱和氯水更快(已知酸性:HCl>H2CO3>HClO),产生这一现象的原因是___________ 。
(4)制备HClO溶液,可将氯气和空气(空气中所有成分不参与反应)按体积比1:3混合后通入含水8%的Na2CO3悬浊液中制备Cl2O,并用水吸收Cl2O制备HClO溶液,实验过程如图所示(夹持装置未画出)。
已知:①Cl2O极易溶于水并与水反应生成HClO;
②Cl2O的沸点为3.8℃,42℃以上分解为Cl2和O2。
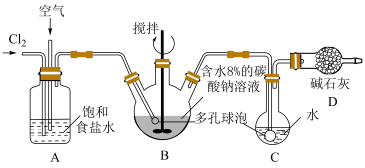
①A瓶中通入的是纯净的Cl2,写出装置A的两个作用___________ 。
②装置B中每生成1molCl2O转移的电子为___________ mol。
③有同学提出B装置外围最好加一个水浴加热装置,控制温度范围在_______ 之间,则效果会更好。
④装置C中发生的化学反应方程式为___________ 。

(1)装置A的名称为
(2)利用装置丙制取饱和氯水并测其pH。
①证明氯水已饱和的现象是
②若撤去装置乙,直接将装置甲和丙相连,这样做对实验测定结果的影响是
(3)在装有20mL饱和氯水试管中加入过量的块状碳酸钙,过滤,将滤液滴在有色布条上,发现其褪色速度比用饱和氯水更快(已知酸性:HCl>H2CO3>HClO),产生这一现象的原因是
(4)制备HClO溶液,可将氯气和空气(空气中所有成分不参与反应)按体积比1:3混合后通入含水8%的Na2CO3悬浊液中制备Cl2O,并用水吸收Cl2O制备HClO溶液,实验过程如图所示(夹持装置未画出)。
已知:①Cl2O极易溶于水并与水反应生成HClO;
②Cl2O的沸点为3.8℃,42℃以上分解为Cl2和O2。

①A瓶中通入的是纯净的Cl2,写出装置A的两个作用
②装置B中每生成1molCl2O转移的电子为
③有同学提出B装置外围最好加一个水浴加热装置,控制温度范围在
④装置C中发生的化学反应方程式为
您最近一年使用:0次
7 . 2021年在四川广汉三星堆新发现大量青铜器,如青铜面具、青铜神树等等。如图中的文物是三星堆出土的青铜面具之一,由于时间久远,表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、O2、CO2作用产生的,其化学式为Cu2(OH)2CO3,请用学过的方法对其展开探究。___________ 、___________ (选取其中两点)。
(2)从不同的物质分类标准的角度分析,“铜绿”不属于___________ 。
A.铜盐 B.碳酸盐 C.碱式盐 D.碱 E.含氧酸盐 F.碱
(3)从“铜绿”的组成、类别和性质的关联角度,预测它可能具有的化学性质,并用化学方程式加以表达(注:选写两个你认为可以实现的反应方程式,并且尽可能使得到的产物形态不同)
①___________ ,②___________ 。
(4)以“铜绿”为反应物可以实现以下物质转化:

反应④使用的是气体还原剂,且得到的产物之一,可以使澄清石灰水变浑浊。请写出反应④的化学方程式___________ 。

(2)从不同的物质分类标准的角度分析,“铜绿”不属于
A.铜盐 B.碳酸盐 C.碱式盐 D.碱 E.含氧酸盐 F.碱
(3)从“铜绿”的组成、类别和性质的关联角度,预测它可能具有的化学性质,并用化学方程式加以表达(注:选写两个你认为可以实现的反应方程式,并且尽可能使得到的产物形态不同)
①
(4)以“铜绿”为反应物可以实现以下物质转化:

反应④使用的是气体还原剂,且得到的产物之一,可以使澄清石灰水变浑浊。请写出反应④的化学方程式
您最近一年使用:0次
2023-11-02更新
|
611次组卷
|
4卷引用:江苏省南京市金陵中学2023-2024学年高一上学期10月调研化学试题
江苏省南京市金陵中学2023-2024学年高一上学期10月调研化学试题江苏省江都区大桥中学2023-2024学年高一上学期期末复习模拟测试化学试题卷一 物质及其变化 2023-2024学年高一上学期化学人教版(2019)必修第一册 期末复习检测卷 (已下线)专题突破卷01 化学物质及其变化-2025年高考化学一轮复习考点通关卷(新高考通用)
8 . 下图是实验室研究潜水艇中供氧体系反应原理的装置图(夹持仪器略)。(提示:供氧剂能提供O2)
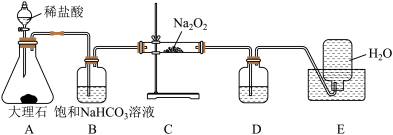
已知:①Na2O2是淡黄色固体
②2Na2O2+2H2O=4NaOH+O2↑、2Na2O2+2CO2=2Na2CO3+O2
(1)B装置的作用是_______ ,B装置中反应的化学方程式_______ 。
(2)D装置中盛放的试剂是_______ ,装置D的作用是_______ 。
(3)当装置内气流平稳后开始收集气体,该气体能_______ ,证明过氧化钠可做供氧剂。
(4)C装置中固体由淡黄色完全变为白色,检验固体成分的实验方案为:取少量C装置中反应后的固体溶于水,向溶液中滴入过量_______ 溶液,若有白色沉淀生成,则证明固体中含有_______ ;过滤,向滤液中滴入几滴酚酞试液,若_______ ,则证明固体中含有_______ 。
(5)若反应后生成氧气2240mL(已折合成标准状况),则参与反应的过氧化钠的质量为_______ g。(请写出计算过程)

已知:①Na2O2是淡黄色固体
②2Na2O2+2H2O=4NaOH+O2↑、2Na2O2+2CO2=2Na2CO3+O2
(1)B装置的作用是
(2)D装置中盛放的试剂是
(3)当装置内气流平稳后开始收集气体,该气体能
(4)C装置中固体由淡黄色完全变为白色,检验固体成分的实验方案为:取少量C装置中反应后的固体溶于水,向溶液中滴入过量
(5)若反应后生成氧气2240mL(已折合成标准状况),则参与反应的过氧化钠的质量为
您最近一年使用:0次
9 . 下列实验方案能达到探究目的的是
| 选项 | 实验方案 | 探究目的 |
| A | 向2mL5%H2O2溶液中滴加几滴FeSO4溶液,观察气泡产生情况 | Fe2+能否催化H2O2分解 |
| B | 用铂丝蘸取某溶液进行焰色试验,观察火焰颜色 | 溶液中是否存在钠盐 |
| C | 向某溶液中加入氢氧化钠溶液并加热 观察产生的气体能否使蓝色石蕊试纸变色 | 溶液中是否存在NH4+ |
| D | 向盛有SO2水溶液的试管中滴加石蕊,观察颜色变化 | SO2水溶液是否具有酸性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 在炽热条件下,将石蜡油分解产生的乙烯通入下列各试管里,装置如图所示。
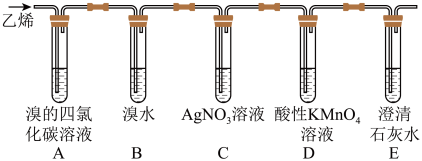
根据上述装置,回答下列问题:
(1)已知:1,2-二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。
预测:A装置中的现象是_____ ,B装置中的现象是_____ 。
(2)D装置中溶液由紫色变无色,D装置中发生反应的类型为_____ 。教材中用溴的四氯化碳溶液替代溴水与乙烯反应,其目的是_____ 。
(3)写出A装置中发生反应的化学方程式_____ ,反应类型为_____ 。E装置的作用是_____ ,当观察到_____ 现象时能验证E装置功能。
(4)丙烯( )与乙烯具有相似的化学性质(写结构简式)。
)与乙烯具有相似的化学性质(写结构简式)。
①丙烯与溴的加成反应产物为_____ 。
②在一定条件下丙烯与 的加成产物可能为
的加成产物可能为_____ 。

根据上述装置,回答下列问题:
(1)已知:1,2-二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。
预测:A装置中的现象是
(2)D装置中溶液由紫色变无色,D装置中发生反应的类型为
(3)写出A装置中发生反应的化学方程式
(4)丙烯(
 )与乙烯具有相似的化学性质(写结构简式)。
)与乙烯具有相似的化学性质(写结构简式)。①丙烯与溴的加成反应产物为
②在一定条件下丙烯与
 的加成产物可能为
的加成产物可能为
您最近一年使用:0次



