18. (1)第四周期元素中价层成对电子数与基态Mg价层成对电子数相等的元素有
_________种。
(2)吡咯(平面形结构,结构式为
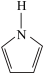
),N原子杂化方式为
______。多原子分子中的大π键可用符号

表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为
_______。
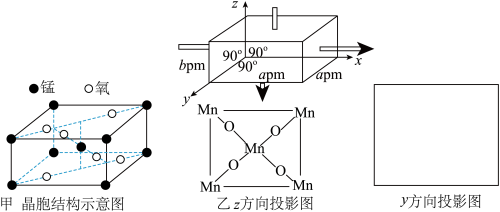
(3)一种锰的氧化物的晶胞如图甲,请写出该氧化物的化学式
______。若沿z轴方向观察该晶胞,可得投影图如图乙,请画出沿y轴方向的投影图
______。
(4)某含Mg储氢晶体储氢后转化为MgH
2,MgH
2晶体的结构如图丙,晶胞参数a=b=450pm,c=301pm,原子分数坐标为A(0,0,0)、B(0.305,0.305,0)、C(1,1,1)、D(0.195,0.805,0.5)。
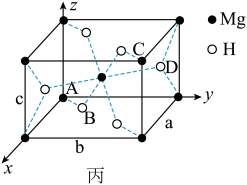
①该晶体中Mg的配位数是
__________。
②Mg
2+的半径为72pm,则H
-的半径为
____________pm(列出计算表达式)
③用N
A表示阿伏加 德罗常数,则MgH
2晶体中氢的密度是标准状况下氢气密度的
_______倍(列出计算表达式,氢气密度为0.089g·L
-1)