宁夏回族自治区中宁县中宁中学2019-2020学年高一上学期期末考试化学试题
宁夏
高一
期末
2020-07-05
391次
整体难度:
容易
考查范围:
常见无机物及其应用、认识化学科学、化学实验基础
一、单选题 添加题型下试题
| A.水 | B.煤油 | C.沙子 | D.泡沫灭火剂 |
【知识点】 钠及其化合物
| A.1molN2的质量是14g | B.H2SO4的摩尔质量是98g |
| C.H2O的摩尔质量是18 g /mol | D.1mol HCl的质量是36.5g/mol |
【知识点】 摩尔质量 摩尔质量与相对原子质量区别与联系解读 物质的量有关计算
| A.CO32-. H + . Na + . NO3- | B.H + . Ag+ . Cl-. SO42- |
| C.K+ . Na + . OH- .NO 3- | D.Ba2+ .Ca 2+ .SO42- . OH- |
【知识点】 离子共存 无附加条件的离子共存解读
| A.铁与稀硫酸反应 Fe+2H+=Fe3++H2↑ |
| B.二氧化碳与水反应 CO2+H2O=2H++CO32- |
| C.碳酸钡与盐酸反应 CO32—+2H+=H2O+CO2↑+Ba2+ |
| D.氢氧化钠溶液与硫酸铜溶液反应 2OH—+Cu2+=Cu(OH)2↓ |
【知识点】 离子反应的发生及书写 离子方程式的书写解读 离子方程式的正误判断解读
| A.石墨、醋酸溶液、食盐晶体 | B.熔融状态的KOH、熔融状态的NaCl |
| C.稀H2SO4、NaOH溶液、纯HNO3 | D.液氨、石灰水、水银 |
【知识点】 非电解质、电解质物质类别判断解读
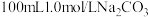 溶液,下列操作正确的是
溶液,下列操作正确的是A.称取10.6g无水碳酸钠,加入 容量瓶中,加水溶解定容 容量瓶中,加水溶解定容 |
B.称取10.6g无水碳酸钠,加入 蒸馏水,搅拌、溶解 蒸馏水,搅拌、溶解 |
C.转移 溶液时,未用玻璃棒引流,直接倒入容量瓶中 溶液时,未用玻璃棒引流,直接倒入容量瓶中 |
| D.定容后,塞好瓶塞,反复倒转、摇匀 |
【知识点】 配制一定物质的量浓度的溶液的步骤、操作解读
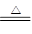 MnCl2+Cl2↑+2H2O,下列说法正确的是
MnCl2+Cl2↑+2H2O,下列说法正确的是| A.MnO2是还原剂 | B.MnCl2是氧化产物 |
| C.Cl2是氧化产物 | D.H2O是还原产物 |
【知识点】 氧化还原反应基本概念 氧化还原反应的几组概念解读
| A.分液、萃取、蒸馏 | B.萃取、蒸馏、分液 |
| C.分液、蒸馏、萃取 | D.蒸馏、萃取、分液 |
| A.溶液的导电性与溶液中离子的浓度有关 |
| B.溶液的导电性与溶液中离子数目的多少有关 |
| C.灯泡最暗时溶液中无任何电解质 |
| D.往氢氧化钡溶液中滴加盐酸与滴加硫酸时现象相同 |
| A.等浓度的溶液中滴入稀盐酸,放出气体的快慢Na2CO3<NaHCO3 | B.热稳定性Na2CO3<NaHCO3 |
| C.常温时水溶性Na2CO3<NaHCO3 | D.相对分子质量Na2CO3<NaHCO3 |
| A.+2 | B.+3 | C.+4 | D.+5 |
【知识点】 基于氧化还原反应守恒规律的计算解读
①加入足量氯水 ②观察到无现象 ③加入少量KSCN溶液
| A.①③② | B.③①② | C.③②① | D.①②③ |
【知识点】 Fe2+的鉴别及其应用解读
| A.Ba(OH)2 | B.H2SO4 | C.NaOH | D.AgNO3 |
| A.1:1 | B.2:3 | C.3:2 | D.1:6 |
| A. Fe3+→Fe2+ | B.Mn2+→MnO4- | C.Cl-→Cl2 | D.N2O3→HNO2 |
| A.3.8g | B.4.8g | C.5.4g | D.6.6g |
| A.溶液呈橙色 | B.溶液呈无色 |
| C.上层液体呈橙色,下层液体几乎无色 | D.上层液体呈紫红色,下层液体几乎无色 |
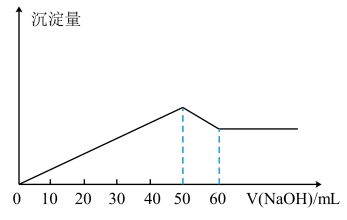
| A.1:1 | B.1:2 | C.2:3 | D.3:2 |
二、填空题 添加题型下试题
(2)已知4.8g某混合气体含分子数为0.15NA,该气体的平均摩尔质量为
(3)等物质的量的SO2和SO3含有的氧原子个数比为
(4)12gCH4和O2的混合气体在标准状况下的体积为11.2L,则混合气体中CH4与O2的物质的量之比为
(1)其化学方程式为
(2)浓硫酸在反应中表现出来的性质是
(3)产生0.1molCO2,转移电子的物质的量为
(4)若在反应中共转移了4mol电子,则标况下生成气体的总体积为
三、解答题 添加题型下试题
A.把制得的溶液小心地转移至容量瓶中。
B.在天平上称取 g的氢氧化钠钠固体,把它放在烧杯中,用适量的蒸馏水将它完全溶解并冷却至室温。
C.继续向容量瓶中加蒸馏水至 ,改用胶头滴管小心滴加蒸馏水至溶液凹液面底部与刻度线相切。
D.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心注入容量瓶,并轻轻振荡。
E.将容量瓶塞塞紧,充分摇匀。
请填写下列空白:
(1)操作步骤的正确顺序为
(2)题目B、C项空白处填入。
(3)本实验用到的基本仪器已有烧杯、天平(砝码、镊子)、玻璃棒,还缺少的必要仪器是
(4)下列情况中,会使所配溶液浓度偏高的是
A.没有冷却直接移液
B.没有进行上述的操作步骤D
C.加蒸馏水时,不慎超过了刻度线
D.容量瓶使用前内壁沾有水珠
四、填空题 添加题型下试题
(1)若铁粉有剩余,则容器中不可能有的离子是
(2)若氯化铜有剩余,则容器中还可能有的离子为
(3)若氯化铁和氯化铜都剩余,则容器中不可能有的单质是
【知识点】 Fe、Cu与Fe3+反应几种情况分析及判断
五、解答题 添加题型下试题

(1)写出F、G的化学式。F:
(2)检验D中阳离子的方法
(3)保存C溶液时为什么要加固体A
(4)写出下列转化的离子方程式或化学方程式。
①A→C:
②C→D:
【知识点】 铁盐的检验解读 与“铁三角”有关的推断解读
六、计算题 添加题型下试题
(1)原混合物中Na2SO4的物质的量
(2)碳酸钠的质量分数
七、解答题 添加题型下试题
 +OH-
+OH- NH3↑+H2O;有一混合物水溶液,可能含有以下离子中的若干种:K+、
NH3↑+H2O;有一混合物水溶液,可能含有以下离子中的若干种:K+、 、Cl-、Mg2+、Fe3+、
、Cl-、Mg2+、Fe3+、 、
、 ,现各取100mL溶液二份进行实验。
,现各取100mL溶液二份进行实验。(1)向第一份加入足量NaOH溶液后加热,收集气体0.896L(标准状况);
(2)向第二份加入足量的BaCl2溶液,得到沉淀6.27g,沉淀经足量盐酸洗涤后,剩余2.33g。
试回答下列问题:(少填,错填都不得分)
(1)肯定存在的离子有
(2)试分别确定下列离子在原溶液中各自的物质的量浓度。
 :
: :
: :
:试卷分析
导出试卷题型(共 27题)
试卷难度
知识点分析
细目表分析
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 钠及其化合物 | |
| 2 | 0.85 | 钠 镁 铝 | |
| 3 | 0.85 | 摩尔质量 摩尔质量与相对原子质量区别与联系 物质的量有关计算 | |
| 4 | 0.85 | 离子共存 无附加条件的离子共存 | |
| 5 | 0.94 | 离子反应的发生及书写 离子方程式的书写 离子方程式的正误判断 | |
| 6 | 0.94 | 非电解质、电解质物质类别判断 | |
| 7 | 0.85 | 胶体 渗析 | |
| 8 | 0.94 | 配制一定物质的量浓度的溶液的步骤、操作 | |
| 9 | 0.94 | 氧化还原反应基本概念 氧化还原反应的几组概念 | |
| 10 | 0.65 | 蒸馏与分馏 萃取和分液 | |
| 11 | 0.85 | 物质水溶液的导电性 | |
| 12 | 0.65 | 氢氧化钠、碳酸钠混合溶液与盐酸反应相关考查 碳酸钠与碳酸氢钠性质的比较 | |
| 13 | 0.65 | 基于氧化还原反应守恒规律的计算 | |
| 14 | 0.85 | Fe2+的鉴别及其应用 | |
| 15 | 0.85 | 离子反应在化合物组成的分析、鉴定的应用 物质的检验 常见阳离子的检验 常见阴离子的检验 | |
| 16 | 0.85 | 化学方程式中物质的量的运用 铝与酸溶液反应 铝与强碱溶液反应 | |
| 17 | 0.85 | 氧化还原反应基本概念 氧化还原反应的几组概念 常见氧化剂与还原剂 氧化还原反应的规律 | |
| 18 | 0.65 | 化学方程式中物质的量的运用 过氧化钠的相关计算 探究物质组成或测量物质的含量 | |
| 19 | 0.85 | 氯气 其他含卤化合物 萃取和分液 | |
| 20 | 0.85 | 氢氧化铝与强碱反应 | |
| 二、填空题 | |||
| 21 | 0.94 | 根据n=N/NA进行相关计算 根据n=m/M进行相关计算 以N=m·NA/M为中心的有关基本粒子的推算 | |
| 22 | 0.85 | 化学方程式计算中物质的量的运用 氧化还原反应的几组概念 电子转移计算 | |
| 24 | 0.4 | Fe、Cu与Fe3+反应几种情况分析及判断 | |
| 三、解答题 | |||
| 23 | 0.85 | 配制一定物质的量浓度的溶液的步骤、操作 配制一定物质的量浓度的溶液实验的误差分析 配制一定物质的量浓度的溶液实验的仪器 | 实验探究题 |
| 25 | 0.65 | 铁盐的检验 与“铁三角”有关的推断 | 无机推断题 |
| 27 | 0.65 | 离子反应的实际应用 铵根离子的检验 硫酸根离子的检验 探究物质组成或测量物质的含量 | 无机推断题 |
| 四、计算题 | |||
| 26 | 0.85 | 化学方程式计算中物质的量的运用 常见硫酸盐的性质 碳酸钠 探究物质组成或测量物质的含量 | |



