10. 甲烷是最简单的烃,可用来作为燃料,也是一种重要的化工原料。
(1)A.CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-Q1kJ/mol
B.CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-Q2kJ/mol
C.CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=+Q2kJ/mol
D. CH4(g)+O2(g)=
CH4(g)+O2(g)= CO2(g)+H2O(l) ΔH=
CO2(g)+H2O(l) ΔH= Q2kJ/mol
Q2kJ/mol
上述热化学方程式中的反应热能正确表示甲烷燃烧热的是___,水的汽化热ΔH=___kJ/mol。
(2)以甲烷为原料通过以下反应可以合成甲醇:2CH4(g)+O2(g) CH3OH(g) ΔH=-251.0kJ/mol
CH3OH(g) ΔH=-251.0kJ/mol
现将2molCH4(g)和1molO2(g)充入密闭容器中,在不同温度和压强下进行上述反应。实验测得平衡时甲醇的物质的量随温度、压强的变化如图所示:
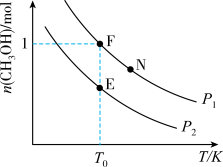
①P1时升高温度,n(CH3OH)__(填“增大”、“减小”或“不变”);P1___P2(填“>"、“<”或“=”);
②E、F、N点对应的化学反应速率由大到小的顺序为____(用v(E)、v(F)、v(N)表示);
③下列能提高CH4平衡转化率的措施是___(填序号);
a.选择高效催化剂b.增大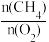 投料比
投料比
c.及时分离产物
④若F点,n(CH3OH)=1mol,总压强为2.5MPa,则T0时F点用分压强代替浓度表示的平衡常数Kp=___。
⑤在温度为T0,压强为P2时,各物质以下列量进行投料反应,达到平衡时,混合气体各组分的百分含量与E点相同的是___。
A.4molCH4(g)和2molO2(g)
B.2molCH4(g)、1molO2(g)和2molCH3OH(g)
C.1molCH3OH(g)
D.1molCH4(g)、1molO2(g)和1molCH3OH(g)
E.1molCH4(g)、0.5molO2(g)和1molCH3OH(g)