23. 碳酸钠与工农业生产、日常生活紧密相关。工业碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少量NaCl,现欲测定样品中Na
2CO
3的质量分数,某探究性学习小组分别设计了如下实验方案。请回答下列有关问题:
方案一:沉淀分析法
(1)把一定质量的样品溶解后加入过量的CaCl
2溶液,根据所得沉淀的质量进行计算,对应的离子方程式为
________________________________方案二:气体分析法
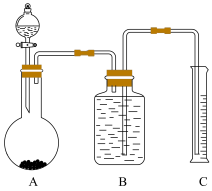
(2)把一定量的样品与足量盐酸反应后,用如图装置测定产生CO
2气体的体积,为了测定结果准确,B中的溶液最好采用
________,但选用该溶液后实验结果仍然不够准确,其原因是
________________(用化学方程式表示)。
a.饱和碳酸钠溶液
b.饱和碳酸氢钠溶液
c.饱和氢氧化钠溶液
d.氯化钠溶液
方案三:质量差分析法
(3)把一定质量的样品和足量的稀硫酸反应,采用如图所示装置,通过称量反应前后盛有碱石灰的干燥管质量,利用其质量差求算样品的纯度。
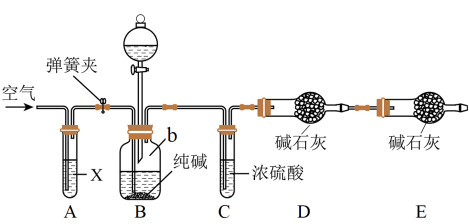
①按图组装仪器,并检查装置气密性
②准确称得6.0g纯碱试样放入装置B的广口瓶中
③称得盛有碱石灰的干燥管D的质量为183.4g
④从A中导管缓缓通入空气一段时间后,
⑤从分液漏斗中滴入足量的试剂至不再产生气泡
⑥再从A中导管缓慢通入空气一段时间
⑦再次称量干燥管D的总质量为185.6g
分液漏斗中所装的药品是
__________________(写名称),E 装置的作用是
__________________(4)A中试剂X为
__________________,其作用是
__________________(5)试样中纯碱的质量分数为
__________________(6)若省略步骤⑥,对实验结果的影响是
__________________;若去掉装置E,对实验结果的影响是
__(填偏大,偏小或无影响)