15. 化工原料水合肼(N
2H
4·H
2O)是一种强还原性的碱性液体。
Ⅰ.实验室用下图装置制备水合肼(N
2H
4·H
2O)。
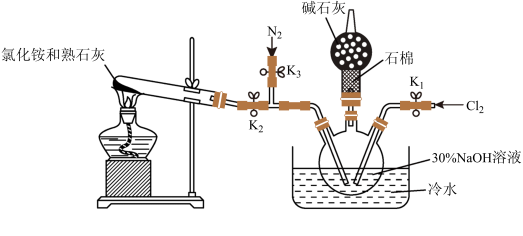
实验步骤:关闭K
2、K
3,打开K
1,制备 NaClO;关闭K
1、K
2,打开K
3,通入N
2一段时间;关闭K
3,打开K
2,点燃酒精灯。回答下列问题:
(1)盛放碱石灰的仪器的名称为
___________________。
(2)配制30%NaOH溶液时,所需玻璃仪器有烧杯、玻璃棒、胶头滴管和
_________。
(3)步骤2中通入N
2一段时间的原因是
____________________________________。
(4)水槽中放入冷水的目的是
_____________________________________________。
(5)NH
3与 NaClO反应生成N
2H
4·H
2O的化学方程式为
_______________________。
Ⅱ.已知:N
2H
4·H
2O+2I
2=N
2↑+4HI+H
2O,测定水合肼粗产品的纯度步骤如下:
a.称取N
2H
4·H
2O粗产品(其它杂质不与I
2反应)2.000g。
b.加水配成250.00mL溶液。
c.移出25.00mL置于锥形瓶中,滴加几滴淀粉溶液。
d.用0.3000mol·L
-1的碘标准溶液进行滴定。
e.重复上述操作两次。三次测定数据如下表:
| 实验序号 | 1 | 2 | 3 |
| 消耗碘标准溶体积/mL | 20.24 | 20.02 | 19.98 |
f.数据处理。
(6)碘标准溶液盛放在
____________(填“酸式”或“碱式”)滴定管中。在滴定管中装入碘标准溶的前一步,应进行的操作为
_________,达到终点的现象是
__________。
(7)消耗的碘标准溶平均体积为
______mL,粗产品中水合肼的质量分数为
______。
(8)判断下列操作对测定结果的影响(填“偏高”、“偏低”或“无影响”)。
①若在配制碘标准溶液时,烧杯中的溶液有少量溅出,则测定结果
___________。
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果
___________。