10. 甲醇是一种重要的有机化工原料,在工业上有着重要的用途。
(1)已知:①C
2H
4(g)+H
2O(g)=C
2H
5OH(g)
△H
1=-akJ·mol
-l②2CH
3OH(g)=CH
3OCH
3(g)+H
2O(g)
△H
2=-bkJ·mol
-1③C
2H
5OH(g)=CH
3OCH
3(g)
△H
3=+ckJ·mol
-1则1mol乙烯和水蒸气在上述条件下化合生成甲醇气体的热化学方程式的
△H=
_______。
(2)若在体积为1.0L的恒容密闭容器中充入1molCO
2和3molH
2模拟工业合成甲醇的反应:CO
2(g)+3H
2(g)

CH
3OH(g)+H
2O(g),二氧化碳的平衡转化率和温度的关系如下图A曲线所示。
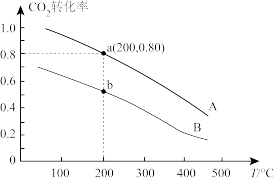
①下列有关说法正确的是
_______。
A该反应为放热反应
B.若加倍投料,曲线A可变为曲线B
C.当v
正(CO
2)=3v
逆(H
2),该反应达到平衡状态
D.容器内压强和混合气体平均相对分子质量不变,均可以说明该反应达到平衡状态
E.CO
2和H
2质量之比不变时,说明已达平衡状态
②计算a点该反应的化学平衡常数K=
_______L
2/mol
2(计算结果保留一位小数)。其他条件不变,向a点平衡体系中再充入0.4molCO
2和0.4molH
2O,则平衡
_______(填“正向”、“逆向”、或“不”)移动。
(3)一定条件下,往一密闭恒容容器中两次通入等量CO和H
2的混和气合成甲醇[其中n(CO):n(H
2)=1:2],其反应为:CO(g)+2H
2(g)

CH
3OH(g),测得容器内总压强(p)、温度(T)与反应时间(t)的关系如图所示。
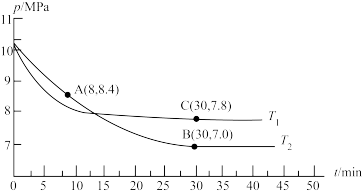
①T
1_______T
2(填“>”、“<”或“=”)。C点的正反应速率v
C(正)与A点的逆反应速率v
A(逆)的大小关系:v
C(正)
________v
A(逆)(填“>”、“<”或“=”)。
②图中达平衡的B点(其起始压强为10Mpa)的压强平衡常数K
p=
_______(Mpa)
-2(只列出计算式即可)(K
p为压强平衡常数,用各气体物质平衡分压代替此物质平衡浓度计算,某气体物质分压=总压×此物质物质的量分数)。