河南省新乡市2020-2021学年高二下学期期末考试化学试题
河南
高二
期末
2021-08-31
301次
整体难度:
适中
考查范围:
常见无机物及其应用、化学反应原理、物质结构与性质、化学与STSE、认识化学科学、化学实验基础、有机化学基础
河南省新乡市2020-2021学年高二下学期期末考试化学试题
河南
高二
期末
2021-08-31
301次
整体难度:
适中
考查范围:
常见无机物及其应用、化学反应原理、物质结构与性质、化学与STSE、认识化学科学、化学实验基础、有机化学基础
一、单选题 添加题型下试题
单选题
|
适中(0.65)
1. “长征五号”B遥二运载火箭搭载我国空间站“天宫”的组成部分天和核心舱成功发射并进入预定轨道,该火箭推进剂为液氧煤油和液氧液氢。天和核心舱配置了光电转换效率最高的三价砷化镓太阳能电池。下列说法不正确的是
| A.煤油为混合物 |
| B.砷化镓的化学式为GaAs |
| C.该推进剂在反应时化学能只转化为热能 |
| D.相对于推进剂四氧化二氮/偏二甲基肼,该推进剂具有毒性低且更环保的特点 |
您最近一年使用:0次
单选题
|
较易(0.85)
2. 反应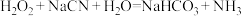 中涉及的相关化学用语表示正确的是
中涉及的相关化学用语表示正确的是
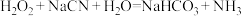 中涉及的相关化学用语表示正确的是
中涉及的相关化学用语表示正确的是A. 的结构示意图: 的结构示意图: |
B. 的结构式: 的结构式: |
C. 的电子式: 的电子式: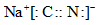 |
D. 水解的离子方程式: 水解的离子方程式: |
【知识点】 共价型分子结构式、电子式解读 盐类水解的原理解读
您最近一年使用:0次
2021-07-19更新
|
103次组卷
|
2卷引用:贵州省黔西南州2020-2021学年高二下学期期末检测理科化学试题
单选题
|
适中(0.65)
4. 用图中所示装置进行实验,不能达到相应实验目的的是
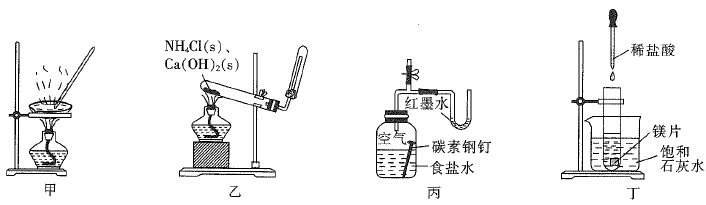

| A.甲装置可用于分解FeSO4·7H2O制取铁红 |
| B.乙装置可用于制取并收集少量NH3 |
| C.丙装置可用于验证铁的吸氧腐蚀 |
| D.丁装置可用于验证镁与盐酸的反应是放热反应 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
5. 下列各组离子在指定的溶液中能大量共存的是
A.c(OH-)=0.1 mol·L-1的溶液中:Na+、Ba2+、Cl-、HCO |
B.c(H+)=0.1 mol·L-1的溶液中:Fe2+、NO 、NH 、NH 、SO 、SO |
C.c(Na2S)=0.1 mol·L-1的溶液中:H+、K+、Cl-、CO |
D.c(KI)=0.1 mol·L-1的溶液中:Na+、NH 、Cl-、SO 、Cl-、SO |
【知识点】 限定条件下的离子共存解读 硝酸的强氧化性解读
您最近一年使用:0次
单选题
|
适中(0.65)
6. Cyrneine A对治疗神经系统疾病有着很好的疗效。可用香芹酮经过多步反应合成。下列说法正确的是


| A.香芹酮的分子式为C10H16O | B.香芹酮的一氯代物有7种 |
| C.香芹酮和Cyrneine A均能发生酯化反应 | D.Cyrneine A中含有4种官能团 |
您最近一年使用:0次
单选题
|
适中(0.65)
7. 下列实验操作规范且能达到实验目的的是
| 实验目的 | 实验操作 | |
| A | 洗涤分解氯酸钾的试管 | 先用水洗涤,若洗不干净,再加入热的草酸溶液洗涤 |
| B | 取20.00mLKI溶液 | 向20mL量筒中加入溶液至凹液面与刻度20处齐平 |
| C | 检验加碘食盐中的碘元素 | 将食盐溶于水,然后加入淀粉溶液 |
| D | 分离乙酸乙酯与饱和Na2CO3溶液 | 先从分液漏斗下端放出Na2CO3溶液,再放出乙酸乙酯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
8. a、b、c、d是原子序数依次增大的短周期主族元素。a与b位于不同周期,且两者的最外层电子数之和与c的最外层电子数相等,b的原子序数等于d的一半,d的最高正价与最低负价的代数和为0。下列说法正确的是
| A.原子半径:a<b<c<d |
| B.最简单氢化物的热稳定性:d<b |
| C.a、b、c三种元素形成的化合物的水溶液均呈碱性 |
| D.c与其他三种元素形成二元化合物时,其化合价均为-2价 |
您最近一年使用:0次
单选题
|
适中(0.65)
9. “长征2F”运载火箭推进剂工作时发生反应:(CH3)2NNH2+2N2O4=2CO2+4H2O+3N2。设NA为阿伏加德罗常数的值,下列说法正确的是
| A.常温常压下,CO2的密度比N2的小 |
| B.1 mol (CH3)2NNH2中含共用电子对的数目为11 NA |
| C.每生成22.4 L CO2时,转移的电子数目为8 NA |
| D.火箭启动初期逸出的红棕色气体是N2O4蒸气 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
10. 下列由已知得到的类推结论正确的是
选项 | 已知 | 类推 |
A | 金属钠可保存在煤油中 | 金属锂也可保存在煤油中 |
B |
|
|
C | 向 | 向 |
D |
|
|
| A.A | B.B | C.C | D.D |
【知识点】 盐类水解规律理解及应用解读
您最近一年使用:0次
2021-07-19更新
|
84次组卷
|
2卷引用:贵州省黔西南州2020-2021学年高二下学期期末检测理科化学试题
单选题
|
适中(0.65)
名校
解题方法
11. 含氯苯的废水可通过加入适量乙酸钠设计成微生物电池,该微生物电池可将氯苯转化为苯而除去,其原理如图所示。下列说法不正确的是
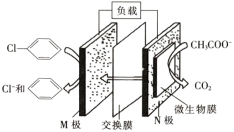

| A.交换膜为阳离子交换膜 |
B.N极的电极反应式: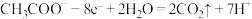 |
C.处理后的废水 变大 变大 |
| D.M极为正极,发生还原反应 |
您最近一年使用:0次
2021-07-19更新
|
288次组卷
|
3卷引用:贵州省黔西南州2020-2021学年高二下学期期末检测理科化学试题
单选题
|
适中(0.65)
解题方法
12. 在10 L的恒容密闭容器中通入X(g)和Y(g),发生反应X(g)+Y(g) M(g)+N(g),所得实验数据如下表所示:
M(g)+N(g),所得实验数据如下表所示:
下列说法正确的是
 M(g)+N(g),所得实验数据如下表所示:
M(g)+N(g),所得实验数据如下表所示:实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(X) | n(Y) | n(M) | ||
① | 700 | 0.40 | 0.10 | 0.090 |
② | 800 | 0.10 | 0.40 | 0.080 |
③ | 800 | 0.20 | 0.30 | a |
④ | 900 | 0.15 | 0.20 | b |
A.实验①中,该反应的平衡常数K=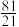 |
| B.实验②中,若5 min时测得n(N)=0.050 mol,则0~5 min内,用X表示的平均反应速率v(X)=7×10-3 mol·L-1·min-1 |
| C.实验③中,反应达到平衡时,Y的转化率为40% |
D.实验④中,反应达到平衡时,b>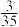 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
13. 实验:①将0.1 mol·L-1的AgNO3溶液和0.1 mol·L-1的NaCl溶液等体积混合,得到浊液a,过滤,得到滤液b和白色沉淀c;
②取一部分沉淀c,向其中滴加0.1 mol·L-1的 KI溶液,沉淀变为黄色(AgI);
KI溶液,沉淀变为黄色(AgI);
③往剩余的沉淀c中滴加0.1 mol·L-1的KBr溶液,沉淀变为淡黄色(AgBr)。
通过以上实验进行分析,下列有关结论不正确的是
②取一部分沉淀c,向其中滴加0.1 mol·L-1的
 KI溶液,沉淀变为黄色(AgI);
KI溶液,沉淀变为黄色(AgI);③往剩余的沉淀c中滴加0.1 mol·L-1的KBr溶液,沉淀变为淡黄色(AgBr)。
通过以上实验进行分析,下列有关结论不正确的是
A.滤液b中:c(Na+)=c(NO ) ) |
B.实验②中反应达到平衡时,平衡常数表达式为K= |
C.实验③中发生反应的化学方程式为AgCl(s)+Br-(aq) AgBr(s)+Cl-(aq) AgBr(s)+Cl-(aq) |
| D.根据实验②③可得出:Ksp(AgCl)>Ksp(AgBr)>Ksp(AgI) |
您最近一年使用:0次
2021-08-30更新
|
561次组卷
|
4卷引用:河南省新乡市2020-2021学年高二下学期期末考试化学试题
河南省新乡市2020-2021学年高二下学期期末考试化学试题(已下线)高中化学《新教材变化解读与考法剖析》第三章 水溶液中的离子反应与平衡(人教版2019选择性必修1)(已下线)3.4.2 沉淀溶解平衡的应用-2021-2022学年高二化学课后培优练(人教版选修4)内蒙古自治区包头市第九中学2022-2023学年高二上学期期末考试化学试题
单选题
|
适中(0.65)
名校
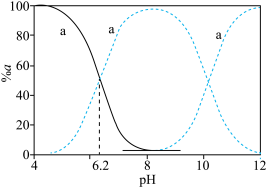
14. 常温下,H2CO3溶液中微粒的物质的量百分数α与pH的关系如图所示。人体血浆中最重要的缓冲体系是碳酸氢盐,正常人的血液的pH在7.35~7.45,由Henderson-Hasselbalch方程可知:pH=6.1+lg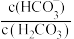 。下列说法不正确的是
。下列说法不正确的是
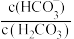 。下列说法不正确的是
。下列说法不正确的是
A.曲线c表示c(CO )随溶液pH变化的曲线 )随溶液pH变化的曲线 |
| B.H2CO3的Ka1的数量级为10-7 |
C.当血浆中c(HCO )增大时,pH一定增大 )增大时,pH一定增大 |
D.当血浆的pH=7.1时,则发生酸中毒,此时c(HCO )是c(H2CO3)的10倍 )是c(H2CO3)的10倍 |
您最近一年使用:0次
2021-08-30更新
|
861次组卷
|
9卷引用:河南省新乡市2020-2021学年高二下学期期末考试化学试题
河南省新乡市2020-2021学年高二下学期期末考试化学试题(已下线)专题3.2.1 水的电离和溶液的酸碱性(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)(已下线)3.1 电离平衡-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)必考点05 电离平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)江西省宁冈中学2020-2021学年高二上学期期中考试化学试题山东省2021-2022学年高二12月“山东学情”联考(人教版)化学试题广东省佛山市第一中学2021-2022学年高二上学期期中考试化学(选考) 试题黑龙江省大庆实验中学2021-2022学年高二上学期期中考试化学试题广东省广州市第二中学2023-2024学年高二上学期期中考试化学试题
二、解答题 添加题型下试题
解答题-原理综合题
|
适中(0.65)
15. 氨气及其相关产品在化工领域中具有重要作用。回答下列问题:
(1)以NH3和CO2为原料生产尿素[CO(NH2)2],发生反应的化学方程式为2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) △H。
CO(NH2)2(s)+H2O(g) △H。
①该反应每消耗1 mol NH3,放出174kJ热量,则△H=___________ kJ·mol-1。
②为了提高尿素的产率,下列措施可行的是___________ (填标号)。
A.升高温度 B.增大压强 C.加入合适的催化剂 D.及时移除部分H2O(g)
(2)某温度下,向恒容密闭容器中通入1 mol NH3、0.5 mol CO2两种原料气,使之发生上述反应。5 min后,反应达到平衡,此时得到的尿素质量为15 g,容器内的压强(p)随时间(t)的变化如图1所示。
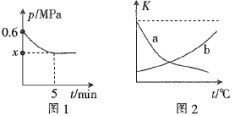
①保持其他条件不变,图2中能正确反映平衡常数K随温度的变化关系的曲线是___________ (填标号)。
②反应达到平衡后,CO2的转化率为___________ ,x=___________ ,平衡常数Kp=___________ (kPa)-2(以分压表示,分压=总压×物质的量分数)。
(3)NH3-O2燃料电池的结构如图所示。
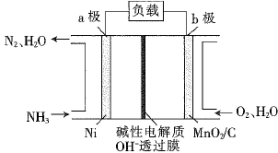
①a极的电极反应式为___________ 。
②每消耗标准状况下5.6 L O2,电路中转移的电子数为___________ NA。
(1)以NH3和CO2为原料生产尿素[CO(NH2)2],发生反应的化学方程式为2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g) △H。
CO(NH2)2(s)+H2O(g) △H。①该反应每消耗1 mol NH3,放出174kJ热量,则△H=
②为了提高尿素的产率,下列措施可行的是
A.升高温度 B.增大压强 C.加入合适的催化剂 D.及时移除部分H2O(g)
(2)某温度下,向恒容密闭容器中通入1 mol NH3、0.5 mol CO2两种原料气,使之发生上述反应。5 min后,反应达到平衡,此时得到的尿素质量为15 g,容器内的压强(p)随时间(t)的变化如图1所示。

①保持其他条件不变,图2中能正确反映平衡常数K随温度的变化关系的曲线是
②反应达到平衡后,CO2的转化率为
(3)NH3-O2燃料电池的结构如图所示。

①a极的电极反应式为
②每消耗标准状况下5.6 L O2,电路中转移的电子数为
【知识点】 热化学方程式 化学平衡的有关计算 化学平衡图像分析 原电池电极反应式书写解读
您最近一年使用:0次
解答题-实验探究题
|
较难(0.4)
解题方法
16. 氮化铝(AIN)是一种新型无机非金属材料,将氧化铝与活性炭按一定比例混合,高温下在纯氮气流中反应: 。
。
I.氮化铝的制备
某同学设计如图1所示装置制备氮化铝(各装置盛装足量试剂),所使用的氮气样品中可能含有少量CO、CO2、O2等气体杂质。
已知:醋酸二氨合亚铜{CH3COO[Cu(NH3)2]}溶液能定量吸收CO,但易被O2氧化,失去吸收CO的能力;连苯三酚碱性溶液能定量吸收O2。

(1)装置A中发生反应的离子方程式为___________ 。
(2)装置B、C、D盛装的试剂分别是___________ (填标号)。
a.连苯三酚碱性溶液
b.浓硫酸
c.醋酸二氨合亚铜溶液
(3)该装置设计存在缺陷,提出改进方案:___________ 。
II.产品纯度的测定
已知:氮化铝遇水分解为氢氧化铝和氨,反应为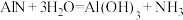 ,产品中仅含有Al2O3杂质。为测定AIN的含量,设计如图2(图中夹持装置略)所示装置,称取6.0g I中所得产品,加入干燥的三颈烧瓶中,然后用恒压漏斗加入NaOH溶液,通入水蒸气,将产生的氨全部蒸出,用
,产品中仅含有Al2O3杂质。为测定AIN的含量,设计如图2(图中夹持装置略)所示装置,称取6.0g I中所得产品,加入干燥的三颈烧瓶中,然后用恒压漏斗加入NaOH溶液,通入水蒸气,将产生的氨全部蒸出,用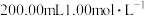 盐酸标准溶液完全吸收(吸收液体积变化忽略不计)。从烧杯中量取20.00mL的吸收液,用
盐酸标准溶液完全吸收(吸收液体积变化忽略不计)。从烧杯中量取20.00mL的吸收液,用 NaOH标准溶液滴定过剩的HCl,到滴定终点时消耗10.00mLNaOH溶液。
NaOH标准溶液滴定过剩的HCl,到滴定终点时消耗10.00mLNaOH溶液。
(4)三颈烧瓶中AIN发生反应的化学方程式为___________ 。
(5)装置中长玻璃管的作用原理是___________ 。
(6)产品纯度为___________ (保留三位有效数字)。
(7)下列实验操作可能使氮化铝测定结果偏低的是___________ (填标号)。
a.滴定前碱式滴定管未排气泡,滴定后气泡消失
b.滴定后,碱式滴定管尖嘴外还悬着一滴液体
c.读数时,滴定前平视,滴定后俯视
 。
。I.氮化铝的制备
某同学设计如图1所示装置制备氮化铝(各装置盛装足量试剂),所使用的氮气样品中可能含有少量CO、CO2、O2等气体杂质。
已知:醋酸二氨合亚铜{CH3COO[Cu(NH3)2]}溶液能定量吸收CO,但易被O2氧化,失去吸收CO的能力;连苯三酚碱性溶液能定量吸收O2。

(1)装置A中发生反应的离子方程式为
(2)装置B、C、D盛装的试剂分别是
a.连苯三酚碱性溶液
b.浓硫酸
c.醋酸二氨合亚铜溶液
(3)该装置设计存在缺陷,提出改进方案:
II.产品纯度的测定
已知:氮化铝遇水分解为氢氧化铝和氨,反应为
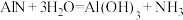 ,产品中仅含有Al2O3杂质。为测定AIN的含量,设计如图2(图中夹持装置略)所示装置,称取6.0g I中所得产品,加入干燥的三颈烧瓶中,然后用恒压漏斗加入NaOH溶液,通入水蒸气,将产生的氨全部蒸出,用
,产品中仅含有Al2O3杂质。为测定AIN的含量,设计如图2(图中夹持装置略)所示装置,称取6.0g I中所得产品,加入干燥的三颈烧瓶中,然后用恒压漏斗加入NaOH溶液,通入水蒸气,将产生的氨全部蒸出,用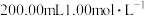 盐酸标准溶液完全吸收(吸收液体积变化忽略不计)。从烧杯中量取20.00mL的吸收液,用
盐酸标准溶液完全吸收(吸收液体积变化忽略不计)。从烧杯中量取20.00mL的吸收液,用 NaOH标准溶液滴定过剩的HCl,到滴定终点时消耗10.00mLNaOH溶液。
NaOH标准溶液滴定过剩的HCl,到滴定终点时消耗10.00mLNaOH溶液。(4)三颈烧瓶中AIN发生反应的化学方程式为
(5)装置中长玻璃管的作用原理是
(6)产品纯度为
(7)下列实验操作可能使氮化铝测定结果偏低的是
a.滴定前碱式滴定管未排气泡,滴定后气泡消失
b.滴定后,碱式滴定管尖嘴外还悬着一滴液体
c.读数时,滴定前平视,滴定后俯视
您最近一年使用:0次
2021-07-23更新
|
260次组卷
|
2卷引用:河北省部分名校2020-2021学年高二下学期期末联考化学试题
解答题-工业流程题
|
适中(0.65)
解题方法
17. 氢化铝钠(NaAlH4)是重要的还原剂。以铝土矿(主要成分为Al2O3,含少量SiO2、Fe2O3)为原料制备NaAlH4的流程如图。已知:“碱浸”时,SiO2转化成难溶的Na2Al2Si2O8。

回答下列问题:
(1)加快“碱浸”速率的措施是___________ 。(写一条)
(2)“反应1”中,HCO 与AlO
与AlO 反应的离子方程式为
反应的离子方程式为___________ 。
(3)为避免铝元素在“碱浸”过程中的损失,请提出一条合理化建议:___________ 。
(4)“电解2”生成的NaHCO3和NaOH可循环使用,阴极产生的物质是___________ (填化学式)。
(5)“反应3”___________ (填“是”或“不是”)氧化还原反应。
(6)氢化铝钠遇水发生剧烈反应并产生大量气泡,当产生标准状况下8.96L气体时,该反应中转移电子的物质的量为___________ mol。
(7)Al与LiBH4反应制备的复合材料是重要的制氢材料,对Al-LiBH4体系与水反应产氢的特性进行下列研究:
①请解释Al-LiBH4体系与水反应产氢比纯Al产氢具有的优势:___________ 。
②25℃和75℃时,Al-LiBH4复合材料[ω(LiBH4)=25%]与水反应一定时间后产物的X-射线衍射图谱(X-射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)如图所示。

分析图中信息可知,25℃与75℃时,Al-LiBH4复合材料中与水未完全反应的物质是___________ (填化学式)。

回答下列问题:
(1)加快“碱浸”速率的措施是
(2)“反应1”中,HCO
 与AlO
与AlO 反应的离子方程式为
反应的离子方程式为(3)为避免铝元素在“碱浸”过程中的损失,请提出一条合理化建议:
(4)“电解2”生成的NaHCO3和NaOH可循环使用,阴极产生的物质是
(5)“反应3”
(6)氢化铝钠遇水发生剧烈反应并产生大量气泡,当产生标准状况下8.96L气体时,该反应中转移电子的物质的量为
(7)Al与LiBH4反应制备的复合材料是重要的制氢材料,对Al-LiBH4体系与水反应产氢的特性进行下列研究:
①请解释Al-LiBH4体系与水反应产氢比纯Al产氢具有的优势:
②25℃和75℃时,Al-LiBH4复合材料[ω(LiBH4)=25%]与水反应一定时间后产物的X-射线衍射图谱(X-射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)如图所示。

分析图中信息可知,25℃与75℃时,Al-LiBH4复合材料中与水未完全反应的物质是
您最近一年使用:0次
解答题-结构与性质
|
适中(0.65)
18. 光州科学技术院Jaeyoung Lee等首次报道在富含磷的Cu电极(CuP2)上进行电催化,可将CO2还原为丁醇。基于反应生成甲酸、乙醛中间体确定该反应的反应机理,展示了一种新型合成多碳物种的过程。回答下列问题:
(1)基态Cu原子成为阳离子时,首先失去___________ 轨道电子;基态P原子价层电子的轨道表示式(电子排布图)为___________ 。
(2)CO2、HCOOH、CH3CHO和CH3CH2CH2CH2OH四种化合物中,C原子的杂化方式中含sp3杂化的是___________ (填结构简式);HCOOH的沸点比CO2的高得多的主要原因是___________ 。
(3)CuP2水解可生成PH3,同主族的氢化物NH3、PH3、AsH3中键角最大的是___________ 。H3PO4及HNO3所含四种元素中电负性最大的是___________ ,第一电离能最大的是___________ 。
(4)配合物[CH3NH2CH3][Cu(HCOO)3](如图甲)中Cu元素的化合价为___________ ,配位键中提供孤电子对的原子是___________ (填元素符号)。

(5)铜氧化物超导体LaSr·CuO的四方晶胞结构如图乙所示,该超导体的密度ρ=___________ g·cm-3(列出计算式,设NA为阿伏加德罗常数的值)。

(1)基态Cu原子成为阳离子时,首先失去
(2)CO2、HCOOH、CH3CHO和CH3CH2CH2CH2OH四种化合物中,C原子的杂化方式中含sp3杂化的是
(3)CuP2水解可生成PH3,同主族的氢化物NH3、PH3、AsH3中键角最大的是
(4)配合物[CH3NH2CH3][Cu(HCOO)3](如图甲)中Cu元素的化合价为

(5)铜氧化物超导体LaSr·CuO的四方晶胞结构如图乙所示,该超导体的密度ρ=

您最近一年使用:0次
解答题-有机推断题
|
适中(0.65)
名校
解题方法
19. 攻克癌症是人类不懈的追求,有机物I是合成某种抗癌药物黄酮醋酸的中间体,其合成路线如图所示:

已知: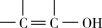 →
→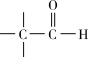 。
。
回答下列问题:
(1)C的化学名称为___________ ,A→B的反应类型为___________ ,G中含有的官能团的名称为___________ 。
(2)写出C→D的化学方程式:___________ 。
(3)RCN在酸性条件下发生水解反应:RCN RCOOH。I在酸性条件下发生水解反应后得到有机物M,M的结构简式为
RCOOH。I在酸性条件下发生水解反应后得到有机物M,M的结构简式为___________ ,其核磁共振氢谱显示有___________ 组信号峰。
(4)有机物K与F互为同分异构体,则满足下列条件的K有___________ 种。
a.能与三氯化铁溶液发生显色反应
b.能与新制的氢氧化铜发生反应
c.苯环上只有两个取代基
(5)结合所学知识并参考上述合成路线,设计以苯和一氯甲烷为原料合成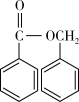 的路线,无机试剂任选。
的路线,无机试剂任选。___________

已知:
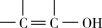 →
→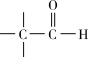 。
。回答下列问题:
(1)C的化学名称为
(2)写出C→D的化学方程式:
(3)RCN在酸性条件下发生水解反应:RCN
 RCOOH。I在酸性条件下发生水解反应后得到有机物M,M的结构简式为
RCOOH。I在酸性条件下发生水解反应后得到有机物M,M的结构简式为(4)有机物K与F互为同分异构体,则满足下列条件的K有
a.能与三氯化铁溶液发生显色反应
b.能与新制的氢氧化铜发生反应
c.苯环上只有两个取代基
(5)结合所学知识并参考上述合成路线,设计以苯和一氯甲烷为原料合成
 的路线,无机试剂任选。
的路线,无机试剂任选。
您最近一年使用:0次
2021-08-30更新
|
143次组卷
|
2卷引用:河南省新乡市2020-2021学年高二下学期期末考试化学试题
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、化学反应原理、物质结构与性质、化学与STSE、认识化学科学、化学实验基础、有机化学基础
试卷题型(共 19题)
题型
数量
单选题
14
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 二氧化氮 常见能量转化形式 预测元素的性质 石油能源现状及其产品的利用 | |
| 2 | 0.85 | 共价型分子结构式、电子式 盐类水解的原理 | |
| 3 | 0.65 | 高分子材料 传统硅酸盐材料 新型无机非金属材料 | |
| 4 | 0.65 | 氨气的实验室制法 吸氧腐蚀 化学实验基础操作 综合实验设计与评价 | |
| 5 | 0.65 | 限定条件下的离子共存 硝酸的强氧化性 | |
| 6 | 0.65 | 根据元素种类、原子个数、有机物类别确定分子式 常见官能团名称、组成及结构 羧酸酯化反应 多官能团有机物的结构与性质 | |
| 7 | 0.65 | 常用仪器及使用 萃取和分液 物质检验和鉴别的实验方案设计 | |
| 8 | 0.65 | 元素周期律、元素周期表的推断 元素周期律的应用 微粒半径大小的比较方法 根据原子结构进行元素种类推断 | |
| 9 | 0.65 | 阿伏加德罗常数的求算 22.4L/mol适用条件 阿伏加德罗定律及其推论 二氧化氮 | |
| 10 | 0.65 | 盐类水解规律理解及应用 | |
| 11 | 0.65 | 原电池原理的应用 原电池正负极判断 原电池电极反应式书写 新型电池 | |
| 12 | 0.65 | 化学反应速率计算 化学平衡常数的影响因素及应用 转化率的相关计算及判断 化学平衡题中基于图表数据的相关计算 | |
| 13 | 0.65 | 化学平衡常数的概念及表达方式 沉淀的溶解与生成 沉淀转化 溶度积规则及其应用 | |
| 14 | 0.65 | 弱电解质在水溶液中的电离平衡 电离平衡常数及影响因素 | |
| 二、解答题 | |||
| 15 | 0.65 | 热化学方程式 化学平衡的有关计算 化学平衡图像分析 原电池电极反应式书写 | 原理综合题 |
| 16 | 0.4 | 离子方程式的书写 酸碱中和滴定的误差分析 常见无机物的制备 探究物质组成或测量物质的含量 | 实验探究题 |
| 17 | 0.65 | 氧化还原反应有关计算 含氧化铝的混合物的提纯 电解池电极反应式及化学方程式的书写与判断 物质分离、提纯综合应用 | 工业流程题 |
| 18 | 0.65 | 电离能变化规律 利用杂化轨道理论判断化学键杂化类型 简单配合物的成键 晶胞的有关计算 | 结构与性质 |
| 19 | 0.65 | 有机反应类型 同分异构体的数目的确定 逆合成分析法 根据题给物质选择合适合成路线 | 有机推断题 |

 通入
通入 溶液中无沉淀生成
溶液中无沉淀生成 溶液中也无沉淀生成
溶液中也无沉淀生成 表面滴加盐酸无明显现象
表面滴加盐酸无明显现象 能溶于
能溶于 浓溶液
浓溶液 浓溶液
浓溶液

