10. I.(1)浙江大学用甲醇、CO、O
2在常压、某温度和催化剂的条件下合成碳酸二甲酯(DMC)的研究开发。
已知:ⅰ. CO的燃烧热:△H=-283.0kJ•mol
-1;
ⅱ.1mol H
2O(l)完全蒸发变成H
2O(g)需吸收44 kJ的热量;
ⅲ.2CH
3OH(g)+CO
2(g)

CH
3OCOOCH
3(g)+H
2O(g) △H=-15.5 kJ•mol
-1则2CH
3OH(g)+CO(g)+ 1/2O
2(g)

CH
3OCOOCH
3(g)+H
2O(l) △H=
_________。该反应平衡常数K的表达式为:
____________。
(2)甲醇也是制备甲酸的一种重要原料。某温度时,将10mol甲酸钠溶于水,溶液显碱性,向该溶液中滴加1L某浓度的甲酸,使溶液呈中性,则滴加甲酸的过程中水的电离平衡将
_____________(填“正向”、“逆向”或“不”) 移动, 此中性溶液中离子浓度由大到小的顺序为:
_____________。
Ⅱ.甲醇和CO
2可直接合成DMC:2CH
3OH(g)+CO
2(g)

CH
3OCOOCH
3(g)+ H
2O(g),但甲醇转化率通常不会超过1%,制约该反应走向工业化生产。
(1)在恒容密闭容器中发生上述反应,能说明反应达到平衡状态的是
___(选填编号)。
A.2v
正(CH
3OH)=v
逆(CO
2)
B.CH
3OH与H
2O的物质的量之比保持不变
C.容器内气体的密度不变
D.容器内压强不变
(2)某研究小组在某温度下,在100mL恒容密闭容器中投入2.5 mol CH
3OH(g)、适量CO
2和6×10
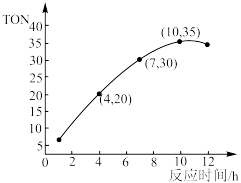
-5mol催化剂,研究反应时间对甲醇转化数(TON)的影响,其变化曲线如图所示。计算公式为:TON = 转化的甲醇的物质的量/催化剂的物质的量。在该温度下,最佳反应时间是
______;4~10 h内碳酸二甲酯的平均反应速率是
________。