Ⅰ.含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶液。向其中加入少量酸或碱时,溶液的酸碱性变化不大。
(1)向该溶液中加入少量盐酸时,发生反应的离子方程式是____________________ ;向其中加入少量KOH溶液时,发生反应的离子方程式是________________ 。
(2)现将0.04mol·L−1HA 溶液和0.02mol·L−1NaOH 溶液等体积混合,得到缓冲溶液。
①若 HA为HCN,该溶液显碱性,则溶液中c(Na+)____ c(CN−)(填“<”“=”或“>”)。
②若 HA为CH3COOH,该溶液显酸性,溶液中所有的离子按浓度由大到小排列的顺序是_____________________ 。
Ⅱ.(3)常温下,将NH3·H2O与盐酸等体积混合,实验数据如下:
针对甲、乙、丙三组实验,回答下列问题:
①甲组反应后,溶液中离子浓度的大小顺序为__________________ ;
②乙组b_____ 7(填“>”、“<”或“=”);
③丙组溶液混合后c=7,A___ 0.1mol·L−1(填“>”、“<”或“=”);
④甲中a=6,混合溶液中c(Cl−)−c(NH4+)=____________ mol·L−1 (列式表示结果,不能做近似计算)。
(1)向该溶液中加入少量盐酸时,发生反应的离子方程式是
(2)现将0.04mol·L−1HA 溶液和0.02mol·L−1NaOH 溶液等体积混合,得到缓冲溶液。
①若 HA为HCN,该溶液显碱性,则溶液中c(Na+)
②若 HA为CH3COOH,该溶液显酸性,溶液中所有的离子按浓度由大到小排列的顺序是
Ⅱ.(3)常温下,将NH3·H2O与盐酸等体积混合,实验数据如下:
| 组别 | NH3·H2O | HCl | 混合溶液的pH |
| 甲 | c(NH3·H2O)=0.1mol·L−1 | c(HCl)=0.1mol·L−1 | pH=a |
| 乙 | NH3·H2O的pH=12 | HCl的pH=2 | pH=b |
| 丙 | c(NH3·H2O)=A mol·L−1 | c(HCl)=0.1mol·L−1 | pH=c |
针对甲、乙、丙三组实验,回答下列问题:
①甲组反应后,溶液中离子浓度的大小顺序为
②乙组b
③丙组溶液混合后c=7,A
④甲中a=6,混合溶液中c(Cl−)−c(NH4+)=
更新时间:2020-09-04 19:48:27
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】已知室温下浓度均为0.1mol·L-1的各溶液PH如下表所示:
(1)若要配制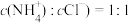 的溶液,可向NH4Cl溶液中加入适量的
的溶液,可向NH4Cl溶液中加入适量的________
A、浓氨水B、浓盐酸C、KCl固体D、KOH固体
(2)0.1mol·L-1的NaHSO3溶液中各离子浓度由大到小的顺序是________________________
(3)根据上述可知,室温下,同浓度同体积的HClO与HCN,与相同浓度的氢氧化钠溶液反应至中性时,消耗碱的量前者________ 后者(请填“<”“<”或“=”)。
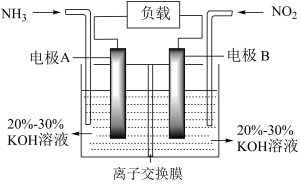
(4)已知NO2与NH3在一定条件下反应可以生成N2,该原理能有效消除氮氧化物的排放,写出该反应的化学方程式________________________
(5)利用上述(4)中原理设计成如图所示装置,即可减轻环境污染,又能充分利用化学能,请写出电极A的电极反应式________________________ ,当有4.48LNO2(标况)被处理时,转移电子为________ mol。
| 序号 | ① | ② | ③ | ④ |
| 溶液 | NH4Cl | NaHSO3 | NaClO | NaCN |
| PH值 | 5.1 | 5.2 | 10.3 | 11.0 |
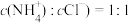 的溶液,可向NH4Cl溶液中加入适量的
的溶液,可向NH4Cl溶液中加入适量的A、浓氨水B、浓盐酸C、KCl固体D、KOH固体
(2)0.1mol·L-1的NaHSO3溶液中各离子浓度由大到小的顺序是
(3)根据上述可知,室温下,同浓度同体积的HClO与HCN,与相同浓度的氢氧化钠溶液反应至中性时,消耗碱的量前者
(4)已知NO2与NH3在一定条件下反应可以生成N2,该原理能有效消除氮氧化物的排放,写出该反应的化学方程式
(5)利用上述(4)中原理设计成如图所示装置,即可减轻环境污染,又能充分利用化学能,请写出电极A的电极反应式

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】用所学知识填写下列空白:(填代号)
(1)下列物质:①金属铜 ②固态NaCl ③O2 ④盐酸 ⑤石墨 ⑥酒精水溶液 ⑦KOH水溶液 ⑧熔融状态的KNO3 ⑨葡萄糖。属于电解质的是_________ ;属于非电解质是_________ ;能导电的是_________ 。
(2)已知t℃时,Kw=1×10-12,则在t℃时将pH=11Ba(OH)2溶液a L与pH=1的HCl溶液b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a:b=_________ 。
(3)现有三种一元酸HA、HB、HC在相同温度下他们的电离平衡常数依次为K1=3.53×10-4,K2=2.95×10-8,K3=4.93×10-10。那么1 mol/L的HA、HB、HC的水溶液的pH由小到大的顺序是_________ 。
(4)常温下,在pH都等于9的NaOH和CH3COONa两种溶液中,设由水电离产生的c(OHˉ)分别为a mol·L-1与b mol·L-1,则a与b的比值为_________ 。
(1)下列物质:①金属铜 ②固态NaCl ③O2 ④盐酸 ⑤石墨 ⑥酒精水溶液 ⑦KOH水溶液 ⑧熔融状态的KNO3 ⑨葡萄糖。属于电解质的是
(2)已知t℃时,Kw=1×10-12,则在t℃时将pH=11Ba(OH)2溶液a L与pH=1的HCl溶液b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a:b=
(3)现有三种一元酸HA、HB、HC在相同温度下他们的电离平衡常数依次为K1=3.53×10-4,K2=2.95×10-8,K3=4.93×10-10。那么1 mol/L的HA、HB、HC的水溶液的pH由小到大的顺序是
(4)常温下,在pH都等于9的NaOH和CH3COONa两种溶液中,设由水电离产生的c(OHˉ)分别为a mol·L-1与b mol·L-1,则a与b的比值为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】自然界是各类物质相互依存、各种变化相互制约的复杂平衡体系,水溶液中的离子平衡是其中一个重要方面。请根据所学知识,回答下列问题。
(1)某温度下, 的盐酸中水电离出的
的盐酸中水电离出的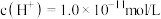 ,该温度下将
,该温度下将 的
的 溶液与
溶液与 的
的 溶液等体积混合,混合后溶液的
溶液等体积混合,混合后溶液的
_______ 。
(2)常温下将pH均为3,体积均为 的
的 和
和 溶液,分别加水稀释至体积V,pH随
溶液,分别加水稀释至体积V,pH随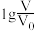 的变化如图所示。
的变化如图所示。
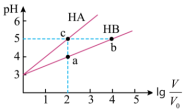
①a、b、c三点水的电离程度由大到小的顺序_______
②常温下,取上述pH均为3的 和
和 溶液各
溶液各 ,向其中分别加入足量的Zn粒,反应结束时
,向其中分别加入足量的Zn粒,反应结束时 中产生氢气的物质的量为
中产生氢气的物质的量为 ,HB溶液中产生氢气的物质的量为
,HB溶液中产生氢气的物质的量为 ,则
,则
_______  (用“>”、“=”、“<”填空)。
(用“>”、“=”、“<”填空)。
(3)以 溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是_______ 。
a.利用阳极泥可回收Ag、Pt、Au等金属 b.粗铜接电源正极,发生氧化反应
c.溶液中 向阳极移动 d.电能全部转化为化学能
向阳极移动 d.电能全部转化为化学能
(4)人工肾脏可采用间接电化学方法除去代谢产物中的尿素 ,原理如图。
,原理如图。
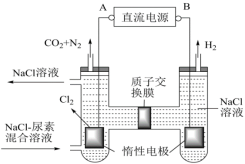
①电源的正极为_______ (填“A”或“B”)。
②电解结束后,阴极室溶液的pH与电解前相比将_______ (填“增大”、“减小”、“不变”);若两极共收集到气体 (标准状况),则除去的尿素为
(标准状况),则除去的尿素为_______ g(忽略气体的溶解)。
(1)某温度下,
 的盐酸中水电离出的
的盐酸中水电离出的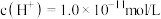 ,该温度下将
,该温度下将 的
的 溶液与
溶液与 的
的 溶液等体积混合,混合后溶液的
溶液等体积混合,混合后溶液的
(2)常温下将pH均为3,体积均为
 的
的 和
和 溶液,分别加水稀释至体积V,pH随
溶液,分别加水稀释至体积V,pH随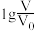 的变化如图所示。
的变化如图所示。
①a、b、c三点水的电离程度由大到小的顺序
②常温下,取上述pH均为3的
 和
和 溶液各
溶液各 ,向其中分别加入足量的Zn粒,反应结束时
,向其中分别加入足量的Zn粒,反应结束时 中产生氢气的物质的量为
中产生氢气的物质的量为 ,HB溶液中产生氢气的物质的量为
,HB溶液中产生氢气的物质的量为 ,则
,则
 (用“>”、“=”、“<”填空)。
(用“>”、“=”、“<”填空)。(3)以
 溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是a.利用阳极泥可回收Ag、Pt、Au等金属 b.粗铜接电源正极,发生氧化反应
c.溶液中
 向阳极移动 d.电能全部转化为化学能
向阳极移动 d.电能全部转化为化学能(4)人工肾脏可采用间接电化学方法除去代谢产物中的尿素
 ,原理如图。
,原理如图。
①电源的正极为
②电解结束后,阴极室溶液的pH与电解前相比将
 (标准状况),则除去的尿素为
(标准状况),则除去的尿素为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.CH3COOH为常见的弱酸,在工业生产和生活中有广泛应用。
(1)中和100 mL pH=3的CH3COOH溶液和1 L pH=4的CH3COOH溶液,需要等物质的量浓度的NaOH溶液的体积分别为V1和V2,则V1____ (填“>”、“=”或“<”)V2。
(2)常温下,用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL某未知浓度的CH3COOH溶液,滴定曲线如图所示。其中A点所示溶液中c(CH3COO-)=2c(CH3COOH),C点所示溶液中存在:c(CH3COO-)+c(CH3COOH)=c(Na+)。则CH3COOH的电离常数Ka=____ ,CH3COOH的实际浓度为_____ 。

Ⅱ.将0.23 mol二氧化硫气体和0.11 mol氧气混合放入容积为1 L的恒容密闭容器中,发生反应生成三氧化硫气体,反应达到平衡时,得到0.12 mol三氧化硫气体。若温度保持不变,向其中再加入0.50 mol氧气后重新达到平衡,则氧气的转化率____ (填“增大”、“不变”或“减小”,下同),混合气体的密度____ ,该温度下反应的平衡常数K____ ;若温度保持不变,向其中再加入0.12 mol氦气后重新达到平衡,则二氧化硫的转化率___ 。
Ⅲ.向BaCl2溶液中先后滴加AgNO3溶液和KBr溶液,当两种沉淀共存时, =
=______ 。[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=1.8×10-10]
(1)中和100 mL pH=3的CH3COOH溶液和1 L pH=4的CH3COOH溶液,需要等物质的量浓度的NaOH溶液的体积分别为V1和V2,则V1
(2)常温下,用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL某未知浓度的CH3COOH溶液,滴定曲线如图所示。其中A点所示溶液中c(CH3COO-)=2c(CH3COOH),C点所示溶液中存在:c(CH3COO-)+c(CH3COOH)=c(Na+)。则CH3COOH的电离常数Ka=

Ⅱ.将0.23 mol二氧化硫气体和0.11 mol氧气混合放入容积为1 L的恒容密闭容器中,发生反应生成三氧化硫气体,反应达到平衡时,得到0.12 mol三氧化硫气体。若温度保持不变,向其中再加入0.50 mol氧气后重新达到平衡,则氧气的转化率
Ⅲ.向BaCl2溶液中先后滴加AgNO3溶液和KBr溶液,当两种沉淀共存时,
 =
=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】I.人类使用能源经历了三个时期。
(1)柴草时期
从能量转化的角度看,木材燃烧时化学能主要转化成_______ 能和光能。
(2)化石能源时期
迄今为止,煤、石油、天然气仍是人类使用的主要能源。煤的综合利用有_______ 、煤的气化和煤的液化等:石油经分馏可以获得汽油、煤油、柴油等轻质油,通过催化裂化和裂解可以得到乙烯、丙烯等,通过结构的重新调整可得到芳香烃类化合物。
(3)多能源结构时期
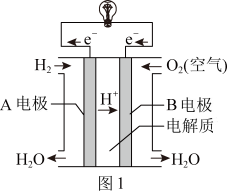
基于环保理念,天津市将逐步减少传统燃油汽车的使用,燃料电池汽车将有更广阔的发展前景。如图1所示为氢氧燃料电池的示意图,其基本工作原理与铜锌原电池的相同。根据图中电子流动方向判断,A电极的电极反应方程式为_______ ,氢氧燃料电池的优点是_______ (写一条即可)。
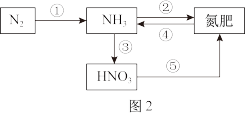
II.氮的循环对人类的生产和生活具有重要意义,图2为氮的部分循环过程:
(4)上述转化中,属于氮的固定的是_______ (填标号)。
(5)步骤②,以氨气为原料制备两种常见氮肥的反应如下:
a.NH3+H2O+CO2=NH4HCO3
b.2NH3(g)+CO2(g)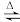 H2O(g)+CO(NH2)2(s) ΔH<0
H2O(g)+CO(NH2)2(s) ΔH<0
其中原子利用率为100%的反应是_______ (填字母)。既能加快反应b的化学反应速率,又能使该平衡正向移动的外界因素是_______ (任写一项)
III.(6)用0.1mol·L-1NaOH标准溶液滴定20mL等浓度的三元酸H3A,得到pH与V(NaOH)、lgX[X=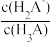 或
或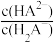 或
或 的关系分别如图3、图4所示。
的关系分别如图3、图4所示。

结合图3信息,当滴入20mLNaOH溶液时,请补全溶液中的离子浓度大小排序:c(Na+)>___ >___ c(HA2-)>c(OH-),结合图4中的II,当溶液中的 =101.8,此时溶液的pH=
=101.8,此时溶液的pH=____ 。
(1)柴草时期
从能量转化的角度看,木材燃烧时化学能主要转化成
(2)化石能源时期
迄今为止,煤、石油、天然气仍是人类使用的主要能源。煤的综合利用有
(3)多能源结构时期
基于环保理念,天津市将逐步减少传统燃油汽车的使用,燃料电池汽车将有更广阔的发展前景。如图1所示为氢氧燃料电池的示意图,其基本工作原理与铜锌原电池的相同。根据图中电子流动方向判断,A电极的电极反应方程式为


II.氮的循环对人类的生产和生活具有重要意义,图2为氮的部分循环过程:
(4)上述转化中,属于氮的固定的是
(5)步骤②,以氨气为原料制备两种常见氮肥的反应如下:
a.NH3+H2O+CO2=NH4HCO3
b.2NH3(g)+CO2(g)
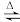 H2O(g)+CO(NH2)2(s) ΔH<0
H2O(g)+CO(NH2)2(s) ΔH<0其中原子利用率为100%的反应是
III.(6)用0.1mol·L-1NaOH标准溶液滴定20mL等浓度的三元酸H3A,得到pH与V(NaOH)、lgX[X=
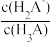 或
或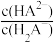 或
或 的关系分别如图3、图4所示。
的关系分别如图3、图4所示。
结合图3信息,当滴入20mLNaOH溶液时,请补全溶液中的离子浓度大小排序:c(Na+)>
 =101.8,此时溶液的pH=
=101.8,此时溶液的pH=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】 与人类息息相关。近年来,为了缓解温室效应,
与人类息息相关。近年来,为了缓解温室效应, 的资源化利用是化学研究热点之一。科学家提出了多种回收和利用
的资源化利用是化学研究热点之一。科学家提出了多种回收和利用 的方案。
的方案。
(1)人体血液中存在平衡 ,当人呼吸过快或过深,体内失去二氧化碳太多,引发呼吸性碱中毒,导致手脚发麻、头晕。试用平衡移动原理解释上述现象:
,当人呼吸过快或过深,体内失去二氧化碳太多,引发呼吸性碱中毒,导致手脚发麻、头晕。试用平衡移动原理解释上述现象:_______ 。
(2)利用 制备
制备 可以实现变废为宝,300℃时,向2L恒容密闭容器中充入2mol
可以实现变废为宝,300℃时,向2L恒容密闭容器中充入2mol 和8mol
和8mol 发生反应:
发生反应:
 ,混合气体中
,混合气体中 的浓度与反应时间的关系如图所示,回答下列问题:
的浓度与反应时间的关系如图所示,回答下列问题:
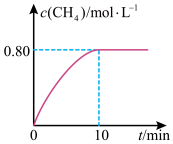
①下列说法正确的是_______ 。
A.容器内密度不变,说明反应达到平衡状态
B.容器内压强不变,说明反应达到平衡状态
C.断开2mol C=O键的同时断开4mol C-H键,说明反应达到平衡状态
D.300℃时,向平衡后的容器中再充入2mol 和8mol
和8mol ,重新达到平衡时
,重新达到平衡时 的浓度小于1.6mol/L
的浓度小于1.6mol/L
②从反应开始到10min, 的平均反应速率
的平均反应速率
_______ 。
③300℃时,反应的平衡常数K=_______ 。
④500℃该反应达到平衡时,上述容器中有1.6mol 、2.0mol
、2.0mol 、5.6mol
、5.6mol 、4.0mol
、4.0mol 。
。
则
_______ 0(填“>”“<”或“=”)
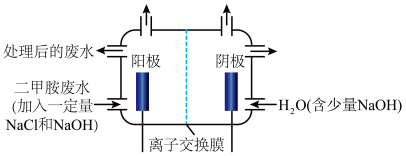
(3)化工废水中常常含有以二甲胺(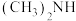 )为代表的含氮有机物,可以通过电解法将二甲胺转化为无毒无害的气体排放,装置如图所示。
)为代表的含氮有机物,可以通过电解法将二甲胺转化为无毒无害的气体排放,装置如图所示。
反应原理是:(i) 在阳极转化为
在阳极转化为 ;
;
(ii) 在碱性溶液中歧化为
在碱性溶液中歧化为 ;
;
(iii) 将二甲胺氧化为
将二甲胺氧化为 ,
, 和
和 。
。
①写出电解池中阴极发生反应的方程式_______ 。
②电解池中选择阴离子交换膜而不选择阳离子交换膜的原因是_______ 。
③当阴极区收集到6.72L(标况下) 时,阳极区收集到
时,阳极区收集到 的体积(标况下)是
的体积(标况下)是_______ L。
 与人类息息相关。近年来,为了缓解温室效应,
与人类息息相关。近年来,为了缓解温室效应, 的资源化利用是化学研究热点之一。科学家提出了多种回收和利用
的资源化利用是化学研究热点之一。科学家提出了多种回收和利用 的方案。
的方案。(1)人体血液中存在平衡
 ,当人呼吸过快或过深,体内失去二氧化碳太多,引发呼吸性碱中毒,导致手脚发麻、头晕。试用平衡移动原理解释上述现象:
,当人呼吸过快或过深,体内失去二氧化碳太多,引发呼吸性碱中毒,导致手脚发麻、头晕。试用平衡移动原理解释上述现象:(2)利用
 制备
制备 可以实现变废为宝,300℃时,向2L恒容密闭容器中充入2mol
可以实现变废为宝,300℃时,向2L恒容密闭容器中充入2mol 和8mol
和8mol 发生反应:
发生反应:
 ,混合气体中
,混合气体中 的浓度与反应时间的关系如图所示,回答下列问题:
的浓度与反应时间的关系如图所示,回答下列问题:
①下列说法正确的是
A.容器内密度不变,说明反应达到平衡状态
B.容器内压强不变,说明反应达到平衡状态
C.断开2mol C=O键的同时断开4mol C-H键,说明反应达到平衡状态
D.300℃时,向平衡后的容器中再充入2mol
 和8mol
和8mol ,重新达到平衡时
,重新达到平衡时 的浓度小于1.6mol/L
的浓度小于1.6mol/L②从反应开始到10min,
 的平均反应速率
的平均反应速率
③300℃时,反应的平衡常数K=
④500℃该反应达到平衡时,上述容器中有1.6mol
 、2.0mol
、2.0mol 、5.6mol
、5.6mol 、4.0mol
、4.0mol 。
。则

(3)化工废水中常常含有以二甲胺(
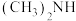 )为代表的含氮有机物,可以通过电解法将二甲胺转化为无毒无害的气体排放,装置如图所示。
)为代表的含氮有机物,可以通过电解法将二甲胺转化为无毒无害的气体排放,装置如图所示。
反应原理是:(i)
 在阳极转化为
在阳极转化为 ;
;(ii)
 在碱性溶液中歧化为
在碱性溶液中歧化为 ;
;(iii)
 将二甲胺氧化为
将二甲胺氧化为 ,
, 和
和 。
。①写出电解池中阴极发生反应的方程式
②电解池中选择阴离子交换膜而不选择阳离子交换膜的原因是
③当阴极区收集到6.72L(标况下)
 时,阳极区收集到
时,阳极区收集到 的体积(标况下)是
的体积(标况下)是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】磷是重要的元素,能形成多种含氧酸和含氧酸盐。回答下列问题:
(1)次磷酸(H3PO2)是一种精细化工产品,向10mL H3PO2溶液中加入30mL等物质的量浓度的NaOH溶液后,所得的溶液中只有 、OH-两种阴离子。则NaH2PO2属于
、OH-两种阴离子。则NaH2PO2属于_______ (填“正盐”或“酸式盐”)。
(2)亚磷酸(H3PO3)溶液存在电离平衡:H3PO3⇌H++ ,
, ⇌H++
⇌H++
①已知25C时,1mol•L-1的H3PO3溶液中,H3PO3的电离度为α,H3PO3的一级电离平衡常数Ka1=_______ (用含α的计算式表示,H3PO3第二步电离忽略不计,忽略水的电离)。
②常温下,将NaOH溶液滴加到亚磷酸(H3PO3)溶液中,混合溶液的pH与离子浓度变化的关系如图所示,则表示 的是曲线
的是曲线_______ (填“I”或“II”),亚磷酸(H3PO3)的Ka2=_______ 。
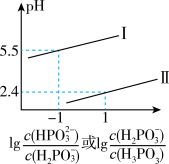
③请结合相关平衡常数判断NaH2PO3溶液显_______ 性(填“酸”、“中”或“碱”),其溶液中离子浓度大到小的顺序是_______ ,c(H+)- c(OH-)_______ c( )- c(H3PO3) (填“>”、“=”或“<”)。
)- c(H3PO3) (填“>”、“=”或“<”)。
(3)25℃时,HF 的电离常数为K=3.6×10-4;H3PO4的电离常数为K1=7.5×10 -3,K2=6.2×10 -8,K3=4.4×10 -13。足量 NaF溶液和 H3PO4溶液反应的离子方程式为:_______ 。
(1)次磷酸(H3PO2)是一种精细化工产品,向10mL H3PO2溶液中加入30mL等物质的量浓度的NaOH溶液后,所得的溶液中只有
 、OH-两种阴离子。则NaH2PO2属于
、OH-两种阴离子。则NaH2PO2属于(2)亚磷酸(H3PO3)溶液存在电离平衡:H3PO3⇌H++
 ,
, ⇌H++
⇌H++
①已知25C时,1mol•L-1的H3PO3溶液中,H3PO3的电离度为α,H3PO3的一级电离平衡常数Ka1=
②常温下,将NaOH溶液滴加到亚磷酸(H3PO3)溶液中,混合溶液的pH与离子浓度变化的关系如图所示,则表示
 的是曲线
的是曲线
③请结合相关平衡常数判断NaH2PO3溶液显
 )- c(H3PO3) (填“>”、“=”或“<”)。
)- c(H3PO3) (填“>”、“=”或“<”)。(3)25℃时,HF 的电离常数为K=3.6×10-4;H3PO4的电离常数为K1=7.5×10 -3,K2=6.2×10 -8,K3=4.4×10 -13。足量 NaF溶液和 H3PO4溶液反应的离子方程式为:
您最近一年使用:0次
【推荐2】研究碳、氮、硫等元素化合物的性质或转化对建设生态文明、美丽中国具有重要意义。
(1)海水中无机碳的存在形式及分布如下图所示:用离子方程式表示海水呈弱碱性的原因_________ 。已知春季海水pH=8.1,预测夏季海水碱性将会_________ (填写“增强”或“减弱”),理由是________ (写出1条即可)
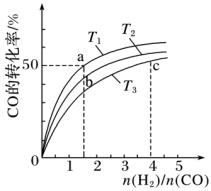
(2)工业上以CO和H2为原料合成甲醇的反应:CO(g)+2H2(g) CH3OH(g)△H<0,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇。如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为lmol)与CO平衡转化率的关系。下列说法正确的是
CH3OH(g)△H<0,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇。如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为lmol)与CO平衡转化率的关系。下列说法正确的是_________ (a、b点横坐标相同,a在曲线T1上,b在曲线T2上)
A.a、b、c三点H2转化率:c>a>b
B.上述三种温度之间关系为T1>T2>T3
C.a点(1.5,50)状态下再通入0.5 mol CO和0.5 mol CH3OH,平衡不移动
D.c点状态下再通入1 molCO和4molH2,新平衡中H2的体积分数增大
(3)NO加速臭氧层被破坏,其反应过程如图所示:
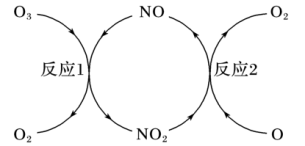
①NO的作用是__________________ 。
②已知:O3(g)+O(g)=2O2(g)△H =-143kJ·mol-1
反应1: O3(g)+NO(g) NO2(g)+O2(g)△H1=-200.2kJ·mol-1
NO2(g)+O2(g)△H1=-200.2kJ·mol-1
反应2:热化学方程式为______________________ 。
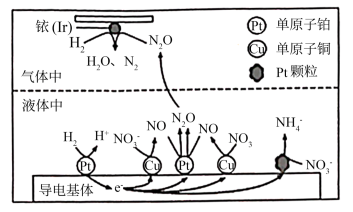
(4)近年来,地下水中的氮污染已成为一个世界性的环境问题。在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的硝态氮(NO3-)从而降低水体中的氮含量,其工作原理如下图所示
①Ir表面发生反应的方程式为__________________________ 。
②若导电基体上的Pt颗粒增多,造成的后果是__________________________ 。
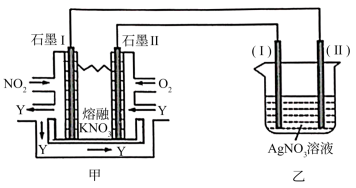
(5)利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,模拟工业电解法来精炼银,装置如图所示,甲池工作时,NO2转变成绿色硝化剂Y,Y是N2O5,可循环使用,则石墨II附近发生的电极反应式为__________________________ 。
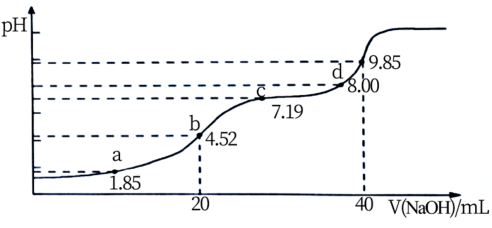
(6)大气污染物SO2可用NaOH吸收。已知pKa=-lgKa,25℃时,H2SO3的pKa1=1.85,pKa2=7.19。该温度下用0.1mol·L-1NaOH溶液滴定20mL0.1mol·L-1H2SO3溶液的滴定曲线如下图所示。b点所得溶液中各离子浓度由大到小的顺序是__________________________ ;c点所得溶液中:c(Na+)__________ 3c(HSO3-)(填“>”、“<”或“=”)
(1)海水中无机碳的存在形式及分布如下图所示:用离子方程式表示海水呈弱碱性的原因
| 无机碳 | HCO3- | 90% |
| CO32- | 9% | |
| CO2 | 1% | |
| H2CO3 | ||
| 其中H2CO3仅为CO2的0.2% | ||

(2)工业上以CO和H2为原料合成甲醇的反应:CO(g)+2H2(g)
 CH3OH(g)△H<0,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇。如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为lmol)与CO平衡转化率的关系。下列说法正确的是
CH3OH(g)△H<0,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇。如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为lmol)与CO平衡转化率的关系。下列说法正确的是A.a、b、c三点H2转化率:c>a>b
B.上述三种温度之间关系为T1>T2>T3
C.a点(1.5,50)状态下再通入0.5 mol CO和0.5 mol CH3OH,平衡不移动
D.c点状态下再通入1 molCO和4molH2,新平衡中H2的体积分数增大
(3)NO加速臭氧层被破坏,其反应过程如图所示:

①NO的作用是
②已知:O3(g)+O(g)=2O2(g)△H =-143kJ·mol-1
反应1: O3(g)+NO(g)
 NO2(g)+O2(g)△H1=-200.2kJ·mol-1
NO2(g)+O2(g)△H1=-200.2kJ·mol-1反应2:热化学方程式为
(4)近年来,地下水中的氮污染已成为一个世界性的环境问题。在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的硝态氮(NO3-)从而降低水体中的氮含量,其工作原理如下图所示
①Ir表面发生反应的方程式为
②若导电基体上的Pt颗粒增多,造成的后果是


(5)利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,模拟工业电解法来精炼银,装置如图所示,甲池工作时,NO2转变成绿色硝化剂Y,Y是N2O5,可循环使用,则石墨II附近发生的电极反应式为
(6)大气污染物SO2可用NaOH吸收。已知pKa=-lgKa,25℃时,H2SO3的pKa1=1.85,pKa2=7.19。该温度下用0.1mol·L-1NaOH溶液滴定20mL0.1mol·L-1H2SO3溶液的滴定曲线如下图所示。b点所得溶液中各离子浓度由大到小的顺序是

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】为有效控制雾霾,各地积极采取措施改善大气质量,有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要。
(1)在汽车排气管内安装催化转化器可将汽车尾气中主要污染物转化为无毒的大气循环物质。已知:
①N2(g)+O2(g)=2NO(g) △H1=+180.5kJ/mol
②C和CO的燃烧热(△H)分别为-393.5 kJ/mol和-283 kJ/mol
则2NO(g)+2CO(g)=N2(g)+2CO2(g) 的△H=_______ kJ/mol。
(2)将 0.20 mol NO 和 0.10 mol CO充入一 个容 积 为 1L 的密闭容器中,反应过程中物质浓度变化如图所示。
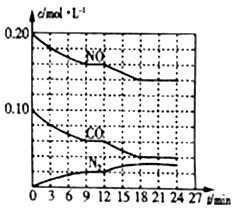
①0~9 min 内 的平均反应速率v(N2)=____ mol/(L ·min) (保留两位有效数字);第12min时改变的反应条件可能为_____ (填字母).
A.升高温度 B.加入NO C.降低温度 D.加催化剂
②该反应在第24min时达到平衡状态,CO的体积分数为____ (保留三位有效数字),化学平衡常数K=_______ (保留两位有效数字)。
(3)烟气中的SO2可用某浓度NaOH溶液吸收得到Na2SO3和NaHSO3混合溶液,且所得溶液呈中性,该溶液中c(Na+)=________ (用含硫微粒浓度的代数式表可)。
(4)通过人工光合作用能将水与燃煤产生的CO2转化成HCOOH和O2。已知常温下0.1mol/LHCOONa溶液的pH=10,则HCOOH 的电离常数Ka=_______ 。
(1)在汽车排气管内安装催化转化器可将汽车尾气中主要污染物转化为无毒的大气循环物质。已知:
①N2(g)+O2(g)=2NO(g) △H1=+180.5kJ/mol
②C和CO的燃烧热(△H)分别为-393.5 kJ/mol和-283 kJ/mol
则2NO(g)+2CO(g)=N2(g)+2CO2(g) 的△H=
(2)将 0.20 mol NO 和 0.10 mol CO充入一 个容 积 为 1L 的密闭容器中,反应过程中物质浓度变化如图所示。

①0~9 min 内 的平均反应速率v(N2)=
A.升高温度 B.加入NO C.降低温度 D.加催化剂
②该反应在第24min时达到平衡状态,CO的体积分数为
(3)烟气中的SO2可用某浓度NaOH溶液吸收得到Na2SO3和NaHSO3混合溶液,且所得溶液呈中性,该溶液中c(Na+)=
(4)通过人工光合作用能将水与燃煤产生的CO2转化成HCOOH和O2。已知常温下0.1mol/LHCOONa溶液的pH=10,则HCOOH 的电离常数Ka=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。试回答下列问题:
(1)元素h的基态原子的价电子排布式为___________ 。
(2)元素g位于元素周期表的___________ 区,基态g+核外电子的空间运动状态有___________ 种。
(3)元素b的第一电离能大于同周期右侧的元素,原因是___________ 。
(4)元素a、c、d以原子个数比1:1:1形成的分子的电子式为___________ 。
(5)某些不同族的元素因电负性相近,其性质也有一定的相似性。如元素b的最高价氧化物对应的水化物和f的最高价氧化物对应的水化物能相互反应,其离子方程式是___________ 。
(6)e是磷元素。已知H3PO3是二元弱酸,常温下向1 L 0.5 mol/L H3PO3溶液中滴加等浓度的NaOH溶液,混合溶液中含P粒子的物质的量分数(δ)与溶液pH的关系如图所示:
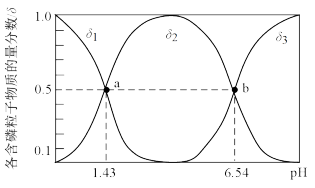
①NaH2PO3溶液中离子浓度由大到小的顺序为___________ (用离子符号表示)。
②反应H3PO3+HPO
 2H2PO
2H2PO 的平衡常数为
的平衡常数为___________ 。
| a | |||||||||||||||||
| b | c | d | |||||||||||||||
| e | |||||||||||||||||
| f | g | h | |||||||||||||||
(2)元素g位于元素周期表的
(3)元素b的第一电离能大于同周期右侧的元素,原因是
(4)元素a、c、d以原子个数比1:1:1形成的分子的电子式为
(5)某些不同族的元素因电负性相近,其性质也有一定的相似性。如元素b的最高价氧化物对应的水化物和f的最高价氧化物对应的水化物能相互反应,其离子方程式是
(6)e是磷元素。已知H3PO3是二元弱酸,常温下向1 L 0.5 mol/L H3PO3溶液中滴加等浓度的NaOH溶液,混合溶液中含P粒子的物质的量分数(δ)与溶液pH的关系如图所示:

①NaH2PO3溶液中离子浓度由大到小的顺序为
②反应H3PO3+HPO

 2H2PO
2H2PO 的平衡常数为
的平衡常数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.葡萄酒中SO2最大使用量为0.25g·L-1,取300.00mL葡萄酒,通过适当的方法使所含SO2全部逸出并用H2O2将其全部氧化为H2SO4,然后用0.0900mol·L-1NaOH标准溶液进行滴定。
①滴定前排气泡时,应选择下图中的___________ (填序号)。

②若用50mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积___________ (填序号)。
A.=10mL B.=40mL C.<10mL D.>40mL
Ⅱ.研究电解质在水溶液中的平衡能了解它的存在形式。
常温下,向100mL0.01mol•L-1HA的溶液中逐滴加入0.02mol•L-1MOH溶液,所得溶液的pH随MOH溶液的体积变化如图所示(溶液体积变化忽略不计)。
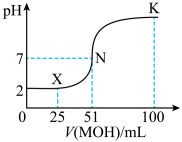
①常温下,0.01mol•L-1HA溶液中由水电离出的c(H+)=___________ mol•L-1
②X点时,溶液中各离子浓度由大到小的顺序是___________ 。
③K点时,溶液中c(H+)+c(M+)–c(OH-)=___________ mol•L-1
①滴定前排气泡时,应选择下图中的

②若用50mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积
A.=10mL B.=40mL C.<10mL D.>40mL
Ⅱ.研究电解质在水溶液中的平衡能了解它的存在形式。
常温下,向100mL0.01mol•L-1HA的溶液中逐滴加入0.02mol•L-1MOH溶液,所得溶液的pH随MOH溶液的体积变化如图所示(溶液体积变化忽略不计)。

①常温下,0.01mol•L-1HA溶液中由水电离出的c(H+)=
②X点时,溶液中各离子浓度由大到小的顺序是
③K点时,溶液中c(H+)+c(M+)–c(OH-)=
您最近一年使用:0次
【推荐3】(1)2017年5月,我国在南海成功开采“可燃冰”(甲烷水合物),标志着在技术方面取得了突破性进展。甲烷是优质的清洁能源,综合开发利用能有效缓解大气污染问题。
已知:CH4(g)+2O2(g)=CO2(g) +2H2O(g) ΔH =- 802 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) ΔH =-566kJ·mol-1
H2O(g)=H2O(l) ΔH =- 44kJ·mol-1
则1mol CH4(g)不完全燃烧生成CO和H2O(l) 的热化学方程式为:___________________________ 。
(2)甲烷转化为CO和H2的反应为:CH4(g)+H2O(g) CO(g)+3H2(g) ΔH>0。
CO(g)+3H2(g) ΔH>0。
①一定条件下,CH4的平衡转化率与温度、压强的关系如下图1所示。则P1________ P2(填“<”、“>”或“=”) ;A、B、C 三点处对应的平衡常数(KA、KB、KC)由大到小的顺序为___________________ 。
②将CH4和H2O(g)按等物质的量混合,一定条件下反应达到平衡,CH4转化率为50%。则反应前与平衡后,混合气体的平均相对分子质量之比为________________ 。


(3)甲烷燃料电池工作原理如上图2所示。a气体是______________ ,b气体通入电极的反应式为__________ 。用该燃料电池作电源、以石墨作电极电解硫酸铜溶液,一段时间后,若将0.1mol Cu2(OH)2CO3溶解于该溶液,恰好使溶液恢复至起始成分和浓度,则燃料电池中理论上消耗CH4的体积(标准状况)为_________________ 。
(4)25℃时,H2CO3的电离常数分别为:Ka1=4.4×10-7mol·L-1;Ka2=5.0×10-11 mol·L-1。在20mL0.1 mol·L-1Na2CO3溶液中逐滴加入0.1 mol·L-1HCl溶液20mL,所得溶液pH=8。此溶液中各阴离子的物质的量浓度大小关系为__________________ ,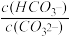 =
=__________________ 。
已知:CH4(g)+2O2(g)=CO2(g) +2H2O(g) ΔH =- 802 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) ΔH =-566kJ·mol-1
H2O(g)=H2O(l) ΔH =- 44kJ·mol-1
则1mol CH4(g)不完全燃烧生成CO和H2O(l) 的热化学方程式为:
(2)甲烷转化为CO和H2的反应为:CH4(g)+H2O(g)
 CO(g)+3H2(g) ΔH>0。
CO(g)+3H2(g) ΔH>0。①一定条件下,CH4的平衡转化率与温度、压强的关系如下图1所示。则P1
②将CH4和H2O(g)按等物质的量混合,一定条件下反应达到平衡,CH4转化率为50%。则反应前与平衡后,混合气体的平均相对分子质量之比为


(3)甲烷燃料电池工作原理如上图2所示。a气体是
(4)25℃时,H2CO3的电离常数分别为:Ka1=4.4×10-7mol·L-1;Ka2=5.0×10-11 mol·L-1。在20mL0.1 mol·L-1Na2CO3溶液中逐滴加入0.1 mol·L-1HCl溶液20mL,所得溶液pH=8。此溶液中各阴离子的物质的量浓度大小关系为
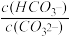 =
=
您最近一年使用:0次



