I.人类使用能源经历了三个时期。
(1)柴草时期
从能量转化的角度看,木材燃烧时化学能主要转化成_______ 能和光能。
(2)化石能源时期
迄今为止,煤、石油、天然气仍是人类使用的主要能源。煤的综合利用有_______ 、煤的气化和煤的液化等:石油经分馏可以获得汽油、煤油、柴油等轻质油,通过催化裂化和裂解可以得到乙烯、丙烯等,通过结构的重新调整可得到芳香烃类化合物。
(3)多能源结构时期
基于环保理念,天津市将逐步减少传统燃油汽车的使用,燃料电池汽车将有更广阔的发展前景。如图1所示为氢氧燃料电池的示意图,其基本工作原理与铜锌原电池的相同。根据图中电子流动方向判断,A电极的电极反应方程式为_______ ,氢氧燃料电池的优点是_______ (写一条即可)。
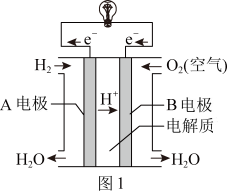
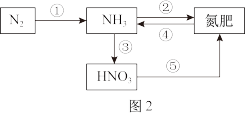
II.氮的循环对人类的生产和生活具有重要意义,图2为氮的部分循环过程:
(4)上述转化中,属于氮的固定的是_______ (填标号)。
(5)步骤②,以氨气为原料制备两种常见氮肥的反应如下:
a.NH3+H2O+CO2=NH4HCO3
b.2NH3(g)+CO2(g)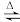 H2O(g)+CO(NH2)2(s) ΔH<0
H2O(g)+CO(NH2)2(s) ΔH<0
其中原子利用率为100%的反应是_______ (填字母)。既能加快反应b的化学反应速率,又能使该平衡正向移动的外界因素是_______ (任写一项)
III.(6)用0.1mol·L-1NaOH标准溶液滴定20mL等浓度的三元酸H3A,得到pH与V(NaOH)、lgX[X=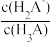 或
或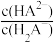 或
或 的关系分别如图3、图4所示。
的关系分别如图3、图4所示。

结合图3信息,当滴入20mLNaOH溶液时,请补全溶液中的离子浓度大小排序:c(Na+)>___ >___ c(HA2-)>c(OH-),结合图4中的II,当溶液中的 =101.8,此时溶液的pH=
=101.8,此时溶液的pH=____ 。
(1)柴草时期
从能量转化的角度看,木材燃烧时化学能主要转化成
(2)化石能源时期
迄今为止,煤、石油、天然气仍是人类使用的主要能源。煤的综合利用有
(3)多能源结构时期
基于环保理念,天津市将逐步减少传统燃油汽车的使用,燃料电池汽车将有更广阔的发展前景。如图1所示为氢氧燃料电池的示意图,其基本工作原理与铜锌原电池的相同。根据图中电子流动方向判断,A电极的电极反应方程式为


II.氮的循环对人类的生产和生活具有重要意义,图2为氮的部分循环过程:
(4)上述转化中,属于氮的固定的是
(5)步骤②,以氨气为原料制备两种常见氮肥的反应如下:
a.NH3+H2O+CO2=NH4HCO3
b.2NH3(g)+CO2(g)
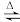 H2O(g)+CO(NH2)2(s) ΔH<0
H2O(g)+CO(NH2)2(s) ΔH<0其中原子利用率为100%的反应是
III.(6)用0.1mol·L-1NaOH标准溶液滴定20mL等浓度的三元酸H3A,得到pH与V(NaOH)、lgX[X=
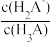 或
或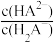 或
或 的关系分别如图3、图4所示。
的关系分别如图3、图4所示。
结合图3信息,当滴入20mLNaOH溶液时,请补全溶液中的离子浓度大小排序:c(Na+)>
 =101.8,此时溶液的pH=
=101.8,此时溶液的pH=
2021·天津南开·三模 查看更多[2]
更新时间:2021-06-12 10:31:14
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。
I.空间站以水为介质将不同形式的能量相互转化,原理如图所示,装置x为电解水,装置y为燃料电池。
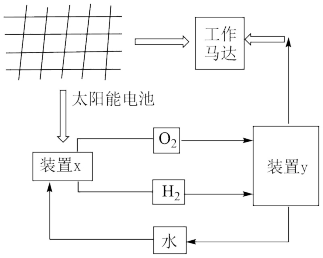
(1)太阳能电池的能量转化形式为_______ (填字母)。
A.化学能转化为电能 B.电能转化为化学能 C.太阳能转化为电能
(2)装置x工作时,产生 的电极为
的电极为_______ 极(填“阳”或“阴”)。
(3)装置y工作时,若电解质溶液为稀硫酸,则正极反应式为_______ 。
II.氢能的利用包括氢的制备、储存和应用三个环节。
(4)氢气直接燃烧的能量转换率远低于燃料电池,写出碱性氢氧燃料电池的负极反应式:_____ 。
(5)化工生产的副产氢也是氢气的来源。电解法制取有广泛用途的 ,同时获得氢气:
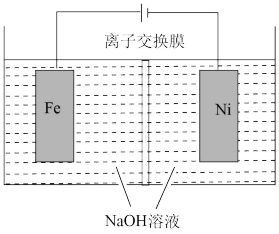
,同时获得氢气: ,工作原理如图所示。装置通电后,铁电极附近生成紫红色的
,工作原理如图所示。装置通电后,铁电极附近生成紫红色的 ,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:
,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知: 只在强碱性条件下稳定,易被
只在强碱性条件下稳定,易被 还原。
还原。
①电解一段时间后, 降低的区域在
降低的区域在_______ (填“阴极室”或“阳极室”)。
②电解过程中,需将阴极产生的气体及时排出,其原因是_______ 。
③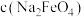 随初始c(NaOH)的变化如图所示,任选M、N两点中的一点,分析
随初始c(NaOH)的变化如图所示,任选M、N两点中的一点,分析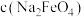 低于最高值的原因:
低于最高值的原因:_______ 。
I.空间站以水为介质将不同形式的能量相互转化,原理如图所示,装置x为电解水,装置y为燃料电池。

(1)太阳能电池的能量转化形式为
A.化学能转化为电能 B.电能转化为化学能 C.太阳能转化为电能
(2)装置x工作时,产生
 的电极为
的电极为(3)装置y工作时,若电解质溶液为稀硫酸,则正极反应式为
II.氢能的利用包括氢的制备、储存和应用三个环节。
(4)氢气直接燃烧的能量转换率远低于燃料电池,写出碱性氢氧燃料电池的负极反应式:
(5)化工生产的副产氢也是氢气的来源。电解法制取有广泛用途的
 ,同时获得氢气:
,同时获得氢气: ,工作原理如图所示。装置通电后,铁电极附近生成紫红色的
,工作原理如图所示。装置通电后,铁电极附近生成紫红色的 ,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:
,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知: 只在强碱性条件下稳定,易被
只在强碱性条件下稳定,易被 还原。
还原。
①电解一段时间后,
 降低的区域在
降低的区域在②电解过程中,需将阴极产生的气体及时排出,其原因是
③
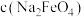 随初始c(NaOH)的变化如图所示,任选M、N两点中的一点,分析
随初始c(NaOH)的变化如图所示,任选M、N两点中的一点,分析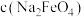 低于最高值的原因:
低于最高值的原因:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】为了探究化学能与热能的转化,某实验小组设计了如图所示三套实验装置:
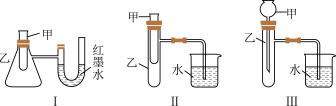
(1)上述3个装置中,不能证明“铜与浓硝酸反应是吸热反应还是放热反应”的是____ 。
(2)某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钡溶液与稀硫酸,U形管中可观察到的现象是________________ ,说明该反应属于____ (填“吸热”或“放热”)反应。
(3)为探究固体M溶于水的热效应,选择装置Ⅱ进行实验(反应在甲中进行)。
①若M为钠,则实验过程中烧杯中可观察到的现象是_______________________
②若观察到烧杯里产生气泡,则说明M溶于水__________ (填“一定是放热反应”“一定是吸热反应”或“可能是放热反应”);
③若观察到烧杯里的玻璃管内形成一段水柱,则M可能是____ 。
(4)至少有两种实验方法能证明超氧化钾与水的反应(4KO2+2H2O 4KOH+3O2↑)是放热反应还是吸热反应。
4KOH+3O2↑)是放热反应还是吸热反应。
方法①:选择上述装置____ (填“I”“Ⅱ”或“Ⅲ”)进行实验;
方法②:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到棉花燃烧,则说明该反应是____ (填“吸热”或“放热”)反应。

(1)上述3个装置中,不能证明“铜与浓硝酸反应是吸热反应还是放热反应”的是
(2)某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钡溶液与稀硫酸,U形管中可观察到的现象是
(3)为探究固体M溶于水的热效应,选择装置Ⅱ进行实验(反应在甲中进行)。
①若M为钠,则实验过程中烧杯中可观察到的现象是
②若观察到烧杯里产生气泡,则说明M溶于水
③若观察到烧杯里的玻璃管内形成一段水柱,则M可能是
(4)至少有两种实验方法能证明超氧化钾与水的反应(4KO2+2H2O
 4KOH+3O2↑)是放热反应还是吸热反应。
4KOH+3O2↑)是放热反应还是吸热反应。方法①:选择上述装置
方法②:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到棉花燃烧,则说明该反应是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】化学在生产生活中无处不在。
(1)某汽车安全气囊的气体发生剂主要含有叠氮化钠( )、
)、 、
、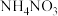 等物质。当汽车发生碰撞时,气体发生剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
等物质。当汽车发生碰撞时,气体发生剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
① 是气体发生剂,是
是气体发生剂,是_______ (填“离子”或“共价”)化合物。
②汽车受到猛烈碰撞时,点火器点火引发 迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是
迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是_______ (填字母)。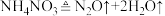 ,推测安全气囊中
,推测安全气囊中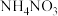 的作用有
的作用有_______ 。
(2)以 为催化剂的光热化学循环分解
为催化剂的光热化学循环分解 反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。_______ 转化为化学能;
②根据数据计算,分解1mol 需
需_______ (填“吸收”或“释放”)_______ kJ的能量。
(3)一定条件下,在2L密闭容器内,反应 ,
,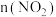 时间变化如表:
时间变化如表:
①0~2s内用 表示该反应的平均速率为
表示该反应的平均速率为_______ 。
②在第5s时, 的转化率为
的转化率为_______ 。(转化率是指某一反应物转化的百分率。)
(4)氮气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和 ,在一定条件下发生反应:
,在一定条件下发生反应: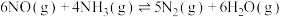 。
。
①能说明该反应已达到平衡状态的标志是_______ (填标号)
A.反应速率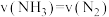
B.容器内压强不再随时间而发生变化
C.容器内 的物质的量分数不再随时间而发生变化
的物质的量分数不再随时间而发生变化
D.容器内
②某次实验中测得容器内NO及 的物质的量随时间变化如图。
的物质的量随时间变化如图。
_______  (填>“<”或“=”),d点对应的速率关系是
(填>“<”或“=”),d点对应的速率关系是
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(1)某汽车安全气囊的气体发生剂主要含有叠氮化钠(
 )、
)、 、
、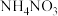 等物质。当汽车发生碰撞时,气体发生剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
等物质。当汽车发生碰撞时,气体发生剂产生大量气体使气囊迅速膨胀,从而起到保护作用。①
 是气体发生剂,是
是气体发生剂,是②汽车受到猛烈碰撞时,点火器点火引发
 迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是
迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是A.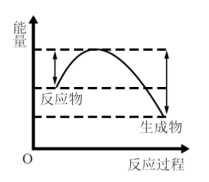 B.
B. C.
C.
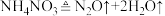 ,推测安全气囊中
,推测安全气囊中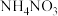 的作用有
的作用有(2)以
 为催化剂的光热化学循环分解
为催化剂的光热化学循环分解 反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。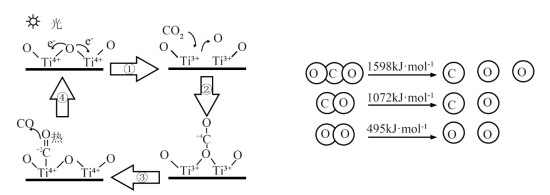
②根据数据计算,分解1mol
 需
需(3)一定条件下,在2L密闭容器内,反应
 ,
,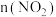 时间变化如表:
时间变化如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
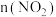 /mol /mol | 0.040 | 0.020 | 0.010 | 0.005 | 0.005 | 0.005 |
 表示该反应的平均速率为
表示该反应的平均速率为②在第5s时,
 的转化率为
的转化率为(4)氮气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和
 ,在一定条件下发生反应:
,在一定条件下发生反应: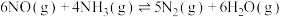 。
。①能说明该反应已达到平衡状态的标志是
A.反应速率
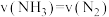
B.容器内压强不再随时间而发生变化
C.容器内
 的物质的量分数不再随时间而发生变化
的物质的量分数不再随时间而发生变化D.容器内

②某次实验中测得容器内NO及
 的物质的量随时间变化如图。
的物质的量随时间变化如图。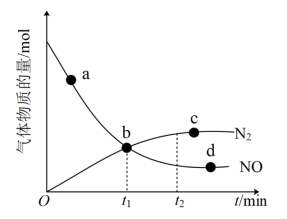

 (填>“<”或“=”),d点对应的速率关系是
(填>“<”或“=”),d点对应的速率关系是
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近一年使用:0次
【推荐1】CO2的利用是国际社会普遍关注的问题。
(1)CO2的电子式是___________ 。
(2)CO2在催化剂作用下可以直接转化为乙二醇和甲醇,但若反应温度过高,乙二醇会深度加氢生成乙醇。
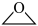 (g)+CO2(g)+3H2(g)→
(g)+CO2(g)+3H2(g)→ (g)+CH3OH(g) ∆H=-131.9kJ∙mol-1
(g)+CH3OH(g) ∆H=-131.9kJ∙mol-1
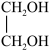 (g)+H2(g)→C2H5OH(g)+H2O(g) ∆H=-94.8kJ∙mol-1
(g)+H2(g)→C2H5OH(g)+H2O(g) ∆H=-94.8kJ∙mol-1
获取乙二醇的反应历程可分为如下2步:
I.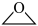 (g)+CO2(g)→
(g)+CO2(g)→ (g) ∆H=-60.3kJ∙mol-1
(g) ∆H=-60.3kJ∙mol-1
II.EC加氢生成乙二醇与甲醇
①步骤II的热化学方程式是___________ 。
②研究反应温度对EC加氢的影响(反应时间均为4小时),实验数据见下表:
由上表可知,温度越高,EC的转化率越高,原因是___________ 。温度升高到220℃时,乙二醇的产率反而降低,原因是___________ 。
(3)用稀硫酸作电解质溶液,电解CO2可制取甲醇,装置如下图所示,电极a接电源___________ 极(填“正”或“负”),生成甲醇的电极反应式是___________ 。

(4)CO2较稳定、能量低。为实现CO2的化学利用,下列研究方向合理的是___________
a.选择高能量的反应物和CO2反应获得低能量的生成物
b.利用电能、光能或热能活化CO2分子
c.选择高效的催化剂
(1)CO2的电子式是
(2)CO2在催化剂作用下可以直接转化为乙二醇和甲醇,但若反应温度过高,乙二醇会深度加氢生成乙醇。
 (g)+CO2(g)+3H2(g)→
(g)+CO2(g)+3H2(g)→ (g)+CH3OH(g) ∆H=-131.9kJ∙mol-1
(g)+CH3OH(g) ∆H=-131.9kJ∙mol-1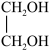 (g)+H2(g)→C2H5OH(g)+H2O(g) ∆H=-94.8kJ∙mol-1
(g)+H2(g)→C2H5OH(g)+H2O(g) ∆H=-94.8kJ∙mol-1获取乙二醇的反应历程可分为如下2步:
I.
 (g)+CO2(g)→
(g)+CO2(g)→ (g) ∆H=-60.3kJ∙mol-1
(g) ∆H=-60.3kJ∙mol-1II.EC加氢生成乙二醇与甲醇
①步骤II的热化学方程式是
②研究反应温度对EC加氢的影响(反应时间均为4小时),实验数据见下表:
| 反应温度/℃ | EC转化率/% | 产率/% | |
| 乙二醇 | 甲醇 | ||
| 160 | 23.8 | 23.2 | 12.9 |
| 180 | 62.1 | 60.9 | 31.5 |
| 200 | 99.9 | 94.7 | 62.3 |
| 220 | 99.9 | 92.4 | 46.1 |
(3)用稀硫酸作电解质溶液,电解CO2可制取甲醇,装置如下图所示,电极a接电源

(4)CO2较稳定、能量低。为实现CO2的化学利用,下列研究方向合理的是
a.选择高能量的反应物和CO2反应获得低能量的生成物
b.利用电能、光能或热能活化CO2分子
c.选择高效的催化剂
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】氨在国防、工农业等领域发挥着重要作用。某实验兴趣小组在实验室模拟工业制氨气,在400℃、2.8MPa时,将一定量N2和H2的混合气体充入一密闭容器中,发生反应 。
。
回答下列问题:
(1)该反应的反应物的键能总和___________ (填“大于”或“小于”)生成物的键能总和。
(2)为了提高 的产率,可采用
的产率,可采用___________ (填一种即可)的方法。
(3)下列说法正确的是___________ (填标号)。
A.升高温度,该反应的反应速率加快,平衡常数减小
B.加入合适的催化剂,N2的转化率保持不变
C. 时,该反应达到平衡状态
时,该反应达到平衡状态
(4)每断裂 键,同时形成
键,同时形成___________  键,转移的电子数为
键,转移的电子数为___________ NA。
 。
。回答下列问题:
(1)该反应的反应物的键能总和
(2)为了提高
 的产率,可采用
的产率,可采用(3)下列说法正确的是
A.升高温度,该反应的反应速率加快,平衡常数减小
B.加入合适的催化剂,N2的转化率保持不变
C.
 时,该反应达到平衡状态
时,该反应达到平衡状态(4)每断裂
 键,同时形成
键,同时形成 键,转移的电子数为
键,转移的电子数为
您最近一年使用:0次
【推荐3】我国力争2030年前实现碳达峰,2060年前实现碳中和。 的综合利用是实现碳中和的措施之一。
的综合利用是实现碳中和的措施之一。
Ⅰ. 和
和 在金属催化剂表面可以合成
在金属催化剂表面可以合成 ,普遍反应路径有三种,其中一种反应路径经历
,普遍反应路径有三种,其中一种反应路径经历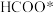 中间体。某小组研究了金属钴的不同晶面【
中间体。某小组研究了金属钴的不同晶面【 、
、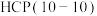 、
、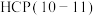 】对
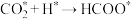
】对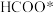 这种反应路径的催化效果,相关基元反应能量变化如下表(*指微粒吸附在催化剂表面):
这种反应路径的催化效果,相关基元反应能量变化如下表(*指微粒吸附在催化剂表面):
(1)写出在 晶面反应的控速步基元反应:
晶面反应的控速步基元反应:______ 。
(2)仅比较表格数据可知, 和
和 在该条件下合成
在该条件下合成 ,
,______ 晶面的催化效果最好。
Ⅱ. 和
和 一定条件下也可以合成甲醇,该过程存在副反应II。
一定条件下也可以合成甲醇,该过程存在副反应II。
反应Ⅰ:
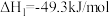
反应Ⅱ:

(3)上述反应中相关物质能量如图1所示。计算
______  。
。
(4)向VL密闭容器中通入
 、
、
 ,在催化剂作用下发生反应。相同时间内温度对
,在催化剂作用下发生反应。相同时间内温度对 转化率及
转化率及 和
和 产率的影响如图2所示。
产率的影响如图2所示。 的转化率随温度升高而增大的原因可能是
的转化率随温度升高而增大的原因可能是______ 。表示 产率随温度变化的曲线是
产率随温度变化的曲线是______ (填“a”或“b”)。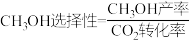 ),则0~tmin内
),则0~tmin内 的反应速率为
的反应速率为______ mol/(L·min),反应Ⅱ的平衡常数为______ (结果保留2位有效数字)。
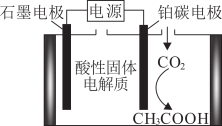
Ⅲ.2021年我国科学家首先实现了从 到淀粉的全人工合成。其中的一个步骤是利用新型电化学催化装置(如图所示)将
到淀粉的全人工合成。其中的一个步骤是利用新型电化学催化装置(如图所示)将 转化为
转化为 。
。______ 。
 的综合利用是实现碳中和的措施之一。
的综合利用是实现碳中和的措施之一。Ⅰ.
 和
和 在金属催化剂表面可以合成
在金属催化剂表面可以合成 ,普遍反应路径有三种,其中一种反应路径经历
,普遍反应路径有三种,其中一种反应路径经历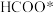 中间体。某小组研究了金属钴的不同晶面【
中间体。某小组研究了金属钴的不同晶面【 、
、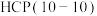 、
、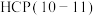 】对
】对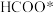 这种反应路径的催化效果,相关基元反应能量变化如下表(*指微粒吸附在催化剂表面):
这种反应路径的催化效果,相关基元反应能量变化如下表(*指微粒吸附在催化剂表面):| 基元反应步骤 |  | 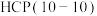 | 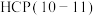 | |||
| 活化能(eV) | 反应热(eV) | 活化能(eV) | 反应热(eV) | 活化能(eV) | 反应热(eV) | |
 | 0.46 | -0.52 | 0.66 | -0.12 | 0.20 | -0.69 |
 | 1.27 | 0.73 | 0.23 | -0.16 | 1.36 | 0.78 |
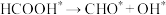 | 0.76 | -0.11 | 0.44 | -0.18 | 0.96 | -0.47 |
 | 0.53 | 0.15 | 0.42 | 0.14 | 0.54 | 0.15 |
 | 0.90 | 0.27 | 0.80 | 0.08 | 1.37 | 0.69 |
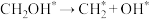 | 0.70 | -0.63 | 0.33 | -0.47 | 0.60 | -1.02 |
 晶面反应的控速步基元反应:
晶面反应的控速步基元反应:(2)仅比较表格数据可知,
 和
和 在该条件下合成
在该条件下合成 ,
,Ⅱ.
 和
和 一定条件下也可以合成甲醇,该过程存在副反应II。
一定条件下也可以合成甲醇,该过程存在副反应II。反应Ⅰ:

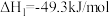
反应Ⅱ:


(3)上述反应中相关物质能量如图1所示。计算

 。
。(4)向VL密闭容器中通入

 、
、
 ,在催化剂作用下发生反应。相同时间内温度对
,在催化剂作用下发生反应。相同时间内温度对 转化率及
转化率及 和
和 产率的影响如图2所示。
产率的影响如图2所示。 的转化率随温度升高而增大的原因可能是
的转化率随温度升高而增大的原因可能是 产率随温度变化的曲线是
产率随温度变化的曲线是
 ),则0~tmin内
),则0~tmin内 的反应速率为
的反应速率为Ⅲ.2021年我国科学家首先实现了从
 到淀粉的全人工合成。其中的一个步骤是利用新型电化学催化装置(如图所示)将
到淀粉的全人工合成。其中的一个步骤是利用新型电化学催化装置(如图所示)将 转化为
转化为 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】Ⅰ、某温度下,HNO2和CH3COOH的电离常数分别为5.0×10-4和1.7×10-5。将pH和体积均相同的两种酸溶液分别加水稀释,其pH随加水体积的变化如图所示。
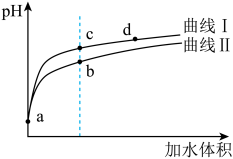
(1)曲线Ⅰ代表____ 溶液(填“HNO2”或“CH3COOH”,下同)。
(2)a点时,物质的量浓度较大的是______ 溶液。相同体积a点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)较少的是_____ 。
(3)b、c两点溶液中水的电离程度较大的是___ (填“b”或“c”)。
(4)CH3COOH的稀释过程中,下列说法正确的是___ (填编号)。
a.CH3COOH的电离常数增大
b.H+的物质的量减小
c. 保持不变
保持不变
d. CH3COOH的电离程度增大,溶液的导电能力增强
Ⅱ、25℃,两种酸的电离平衡常数如表。
(5)HA-的电离平衡常数表达式K =_______ 。
(6)0.10 mol·L-1 NaHB溶液中H+、OH-、Na+、HB-的浓度由大到小的顺序为_______ 。
(7)等浓度的四种溶液:a. Na2A、b. NaHA、c. Na2B、d. NaHB的pH由大到小顺序是_______ (填字母)。

(1)曲线Ⅰ代表
(2)a点时,物质的量浓度较大的是
(3)b、c两点溶液中水的电离程度较大的是
(4)CH3COOH的稀释过程中,下列说法正确的是
a.CH3COOH的电离常数增大
b.H+的物质的量减小
c.
 保持不变
保持不变d. CH3COOH的电离程度增大,溶液的导电能力增强
Ⅱ、25℃,两种酸的电离平衡常数如表。
 |  | |
| H2A | 4.4×10-7 | 4.7×10-11 |
| H2B | 1.3×10-7 | 7.1×10-15 |
(5)HA-的电离平衡常数表达式K =
(6)0.10 mol·L-1 NaHB溶液中H+、OH-、Na+、HB-的浓度由大到小的顺序为
(7)等浓度的四种溶液:a. Na2A、b. NaHA、c. Na2B、d. NaHB的pH由大到小顺序是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】弱电解质在水溶液中的电离状况可以进行定量计算和推测。
(1)25℃时两种酸的电离平衡常数如表所示。
①25℃时,0.100mol·L-1的NaA溶液中H+、OH-、Na+、A-、HA的物质的量浓度由大到小的顺序是:___ 。pH=8的NaA溶液中由水电离出的c(OH-)=___ mol·L-1。
②25℃时,0.100mol·L-1的NaHB溶液pH___ 7,理由是___ 。
③25℃时,向0.100mol·L-1的Na2B溶液中滴加足量0.100mol·L-1的HA溶液,反应的离子方程式为___ 。
(2)已知25℃时,向0.100mol·L-1的H3PO4溶液中滴加NaOH溶液,各含磷微粒的物质的量分数随pH变化的关系如图所示。
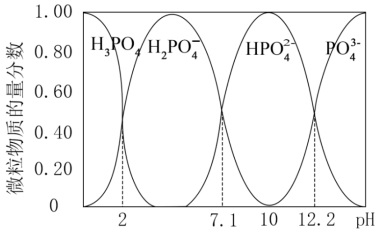
①当溶液pH由11到14时,所发生反应的离子方程式为:___ 。
(1)25℃时两种酸的电离平衡常数如表所示。
| Ka1 | Ka2 | |
| HA | 1×10-4 | |
| H2B | 1×10-2 | 5×10-6 |
①25℃时,0.100mol·L-1的NaA溶液中H+、OH-、Na+、A-、HA的物质的量浓度由大到小的顺序是:
②25℃时,0.100mol·L-1的NaHB溶液pH
③25℃时,向0.100mol·L-1的Na2B溶液中滴加足量0.100mol·L-1的HA溶液,反应的离子方程式为
(2)已知25℃时,向0.100mol·L-1的H3PO4溶液中滴加NaOH溶液,各含磷微粒的物质的量分数随pH变化的关系如图所示。

①当溶液pH由11到14时,所发生反应的离子方程式为:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】油气开采、石油化工、煤化工等行业废气中普遍含有硫化氢,需要回收处理并加以利用。
I.已知下列反应的热化学方程式:
①2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ∆H1
②4H2S(g)+2SO2(g)=3S2(g)+4H2O(g) ∆H2
③2H2(g)+O2(g)=2H2O(g) ∆H3
④2H2S(g)=S2(g)+2H2(g) ∆H4
(1)∆H4=
(2)已知∆H4>0,
A.低温 B.高温
(3)处理H2S普遍采用的方法是克劳斯工艺,即利用反应①和②生成S2;另一种方法是利用反应④分解H2S。相比克劳斯工艺,分解法的优点是
II.在1373K、100 kPa下,分别将n(H2S):n(Ar)为4:1、1:1、1:4、1:9的H2S-Ar混合气体置于密闭容器中发生反应④,反应过程中H2S转化率随时间的变化如下图所示:
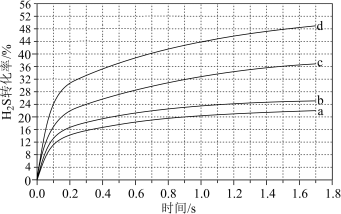
(4)n(H2S):n(Ar)=1:9对应图中曲线
A.a B.b C.c D.d
(5)n(H2S):n(Ar)=1:4的混合气体投料后,若将温度升高至1473K,达到平衡时混合气体中H2S与H2的分压相等,H2S平衡转化率为
III.在真空克劳斯法脱硫中,用K2CO3溶液吸收H2S。
电离平衡常数 | H2CO3 | H2S |
K1 | 4.2×10-7 | 5.6×10-8 |
K2 | 5.6×10-11 | 1.2×10-15 |
(6)下列关于K2CO3溶液中微粒关系正确的是___________。
A.c(OH-)>c(HCO ) ) | B.c(H+)>c(HCO ) ) |
C.c(OH-)=c(H+)+c(HCO )+2c(H2CO3) )+2c(H2CO3) | D.2c(K+)=c(CO )+c(HCO )+c(HCO )+c(H2CO3) )+c(H2CO3) |
(7)K2CO3溶液吸收少量H2S的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】已知Ka、Kb、Kw、Kh、Ksp分别表示弱酸的电离平衡常数、弱碱的电离平衡常数,水的离子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。通过查阅资料获得温度为25℃时以下数据:Kw=1.0×10-14,Ka(CH3COOH)=1.8×10-5,Ka(HSCN)=0.13,Ka(HF)=4.0×10-4,Ksp[Mg(OH)2]=1.8×10-11
(1)有关上述常数的说法正确的是_______ 。
a.它们都能反映一定条件下对应变化进行的程度
b.所有弱电解质的电离常数和难溶电解质的Ksp都随温度的升高而增大
c.常温下,CH3COOH在水中的Ka大于在饱和CH3COONa溶液中的Ka
d.一定温度下,在CH3COONa溶液中,Kw=Ka·Kh
(2)已知CH3COONH4溶液为中性,又知CH3COOH溶液加到Na2CO3溶液中有气体放出,现有25℃时等浓度的四种溶液:A.NH4Cl,B.NH4SCN,C.CH3COONH4,D.NH4HCO3。回答下列问题:
①试推断NH4HCO3溶液的pH_______ 7(填“>”、“<”或“=”);
②将四种溶液按NH4+浓度由大到小的顺序排列是:_______ (填序号)。
③NH4SCN溶液中所有离子浓度由大到小的顺序为_______ 。
(3)为探究Mg(OH)2在酸中的溶解性,利用以上数据可以计算出反应:Mg(OH)2(s)+2CH3COOH(aq) Mg2+(aq)+2CH3COO-(aq)+2H2O(l)在25℃时的平衡常数K=
Mg2+(aq)+2CH3COO-(aq)+2H2O(l)在25℃时的平衡常数K=_______ ,并据此推断Mg(OH)2_______ (填“能”或“不能”)溶解于醋酸。(已知1.83≈5.8)
(1)有关上述常数的说法正确的是
a.它们都能反映一定条件下对应变化进行的程度
b.所有弱电解质的电离常数和难溶电解质的Ksp都随温度的升高而增大
c.常温下,CH3COOH在水中的Ka大于在饱和CH3COONa溶液中的Ka
d.一定温度下,在CH3COONa溶液中,Kw=Ka·Kh
(2)已知CH3COONH4溶液为中性,又知CH3COOH溶液加到Na2CO3溶液中有气体放出,现有25℃时等浓度的四种溶液:A.NH4Cl,B.NH4SCN,C.CH3COONH4,D.NH4HCO3。回答下列问题:
①试推断NH4HCO3溶液的pH
②将四种溶液按NH4+浓度由大到小的顺序排列是:
③NH4SCN溶液中所有离子浓度由大到小的顺序为
(3)为探究Mg(OH)2在酸中的溶解性,利用以上数据可以计算出反应:Mg(OH)2(s)+2CH3COOH(aq)
 Mg2+(aq)+2CH3COO-(aq)+2H2O(l)在25℃时的平衡常数K=
Mg2+(aq)+2CH3COO-(aq)+2H2O(l)在25℃时的平衡常数K=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】已知:①25℃时弱电解质电离平衡数:Ka(CH3COOH)= ,Ka(HSCN)=0.13;难溶电解质的溶度积常数:Ksp(CaF2)=
,Ka(HSCN)=0.13;难溶电解质的溶度积常数:Ksp(CaF2)=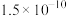
②25℃时, mol·L-1氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系,如下图所示:
mol·L-1氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系,如下图所示:

请根据以下信息回答下列问题:
(1)25℃时,将20mL 0.10 mol·L-1 CH3COOH溶液和20mL 0.10 mol·L-1HSCN溶液分别与20mL 0.10 mol·L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)变化的示意图为图所示:
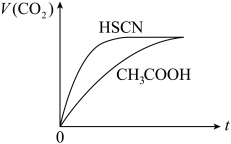
反应初始阶段,两种溶液产生CO2气体的速率存在明显差异的原因是______ ,反应结束后所得两溶液中,c(CH3COO-)______ c(SCN-)(填“>”、“<”或“=”)
(2)25℃时,HF电离平衡常数的数值Ka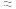
______ ,列式并说明得出该常数的理由______ 。
(3) mol·L-1HF溶液与
mol·L-1HF溶液与 mol·L-1 CaCl2溶液等体积混合,调节混合液pH为4.0(忽略调节混合液体积的变化),通过列式计算说明是否有沉淀产生
mol·L-1 CaCl2溶液等体积混合,调节混合液pH为4.0(忽略调节混合液体积的变化),通过列式计算说明是否有沉淀产生______ 。
 ,Ka(HSCN)=0.13;难溶电解质的溶度积常数:Ksp(CaF2)=
,Ka(HSCN)=0.13;难溶电解质的溶度积常数:Ksp(CaF2)=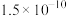
②25℃时,
 mol·L-1氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系,如下图所示:
mol·L-1氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系,如下图所示:
请根据以下信息回答下列问题:
(1)25℃时,将20mL 0.10 mol·L-1 CH3COOH溶液和20mL 0.10 mol·L-1HSCN溶液分别与20mL 0.10 mol·L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)变化的示意图为图所示:

反应初始阶段,两种溶液产生CO2气体的速率存在明显差异的原因是
(2)25℃时,HF电离平衡常数的数值Ka
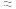
(3)
 mol·L-1HF溶液与
mol·L-1HF溶液与 mol·L-1 CaCl2溶液等体积混合,调节混合液pH为4.0(忽略调节混合液体积的变化),通过列式计算说明是否有沉淀产生
mol·L-1 CaCl2溶液等体积混合,调节混合液pH为4.0(忽略调节混合液体积的变化),通过列式计算说明是否有沉淀产生
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品,工业上常用铝土矿(主要成分为Al2O3和少量的SiO2、Fe2O3杂质)生产铵明矾晶体NH4Al(SO4)2•12H2O,其工艺流程图如图:
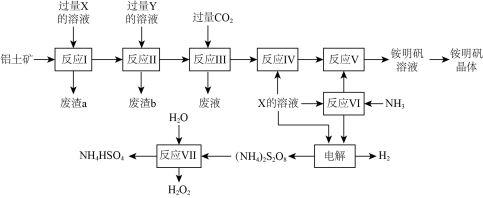
(1)废渣a、b的成分分别是___________ 、___________ (写名称)。
(2)流程图中X的化学式为___________ 。
(3)反应Ⅲ的离子方程式为___________ ;从铵明矾溶液中获得铵明矾晶体的操作依次为(填操作名称)___________ 、冷却结晶、过滤、洗涤。
(4)反应Ⅶ的化学方程式为___________ ;NH4HSO4溶液中离子浓度由大到小顺序为___________ 。

(1)废渣a、b的成分分别是
(2)流程图中X的化学式为
(3)反应Ⅲ的离子方程式为
(4)反应Ⅶ的化学方程式为
您最近一年使用:0次



