一定温度下,在容积为 2 L 的恒容密闭容器中分别充入2.4 mol NO 和 CO, 发 生 可 逆 反 应 如 下 : 2NO(g)+2CO(g)⇌N2(g)+2CO2(g) ΔH<0。反应过程中部分反应物和生成物的物质的量的变化关系如图所示。回答下列问题:
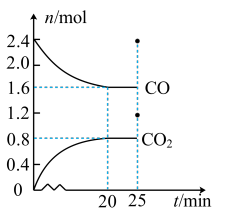
(1)0~20 min 内反应速率 v(N2)=_____ 。
(2)该温度下的平衡常数 K=_____ ,25 min 时,若温度不变,向容器中再分别充入0.4 mol CO 和 N2,则化学平衡将_____ (填“向正反应方向”“ 向逆反应方向”或“不”)移动;再次到达平衡时,NO 的转化率_____ (填“变大”“变小”或“不变”)。
(3)若换用一个恒容、绝热的容器, 使容器内温度迅速升至原来的 2 倍,则平衡将_____ (填“向正反应方向”“ 向逆反应方向”或“不”)移动。达到新平衡后,容器内温度____ (填“大于”“小于”或“等于”)原来的 2 倍。

(1)0~20 min 内反应速率 v(N2)=
(2)该温度下的平衡常数 K=
(3)若换用一个恒容、绝热的容器, 使容器内温度迅速升至原来的 2 倍,则平衡将
20-21高二·重庆沙坪坝·期中 查看更多[2]
更新时间:2020-11-07 16:52:08
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】下列反应在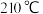 达到平衡:
达到平衡:
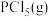

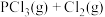
 ①
①



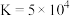 ②
②


 ③
③
(1)根据反应①的平衡常数K表达式,下列等式必定成立的是________ 。
a.
b.
c.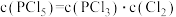
(2)反应②和反应③的K值的乘积是________ 。
(3)降低 浓度,反应③的K值
浓度,反应③的K值________ (填“增大”“减小”或“不变”)。
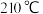 达到平衡:
达到平衡: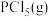

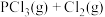
 ①
① 


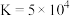 ②
②

 ③
③(1)根据反应①的平衡常数K表达式,下列等式必定成立的是
a.

b.

c.
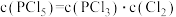
(2)反应②和反应③的K值的乘积是
(3)降低
 浓度,反应③的K值
浓度,反应③的K值
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】完成下列问题
(1)1 mol C与1 mol H2O(g)反应生成1 mol CO(g)和1 mol H2(g),需要吸收131.5 kJ的热量,该反应的反应热为△H=___________ kJ/mol。
(2)已知反应A(g)+3B(g) 2C(g)在一定温度下达到平衡,该反应的平衡常数表达式为
2C(g)在一定温度下达到平衡,该反应的平衡常数表达式为___________
(3)若各物质的平衡浓度分别为c(A)=2.0 mol/L、c(B)=2.0 mol/L、c(C)=1.0 mol/L,则K=___________ 。
(1)1 mol C与1 mol H2O(g)反应生成1 mol CO(g)和1 mol H2(g),需要吸收131.5 kJ的热量,该反应的反应热为△H=
(2)已知反应A(g)+3B(g)
 2C(g)在一定温度下达到平衡,该反应的平衡常数表达式为
2C(g)在一定温度下达到平衡,该反应的平衡常数表达式为(3)若各物质的平衡浓度分别为c(A)=2.0 mol/L、c(B)=2.0 mol/L、c(C)=1.0 mol/L,则K=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】已知:CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH=Q。其平衡常数随温度变化如下表所示:
回答下列问题:
(1)上述反应的化学平衡常数表达式为_______ ,该反应的Q_______ (填“>”或“<”)0。
(2)850 ℃时,在体积为10 L的反应器中,通入一定量的CO和H2O(g),发生上述反应,CO和H2O(g)的浓度变化如下图所示,则0~4 min时,平均反应速率v(CO)=_______ 。
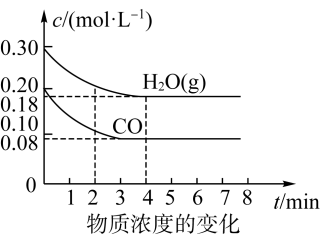
(3)若在500 ℃时进行,且CO、H2O(g)的起始浓度均为0.020 mol·L-1,该条件下,CO的最大转化率为_______ 。(提示:利用平衡常数,三段式计算)
(4)有人提出可以设计反应2CO(g)=2C(s)+O2(g)(ΔH>0)来消除CO的污染。请判断上述反应能否自发进行:_______ (填“能”或“不能”)。理由是_______ 。
| 温度/℃ | 400 | 500 | 850 |
| 平衡常数 | 9.94 | 9 | 1 |
(1)上述反应的化学平衡常数表达式为
(2)850 ℃时,在体积为10 L的反应器中,通入一定量的CO和H2O(g),发生上述反应,CO和H2O(g)的浓度变化如下图所示,则0~4 min时,平均反应速率v(CO)=

(3)若在500 ℃时进行,且CO、H2O(g)的起始浓度均为0.020 mol·L-1,该条件下,CO的最大转化率为
(4)有人提出可以设计反应2CO(g)=2C(s)+O2(g)(ΔH>0)来消除CO的污染。请判断上述反应能否自发进行:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】化学平衡常数
(1)表达式:对于一般的可逆反应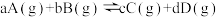 ,当在一定温度下达到化学平衡状态时,平衡常数的表达式为
,当在一定温度下达到化学平衡状态时,平衡常数的表达式为_______ .
(2)意义
①K越大,说明_______ 进行的程度_______ ,反应物的转化率_______ ;反之,K越小,反应进行得越_______ ,反应物的转化率_______ .
②K只受_______ 影响,与反应物或生成物的_______ 变化无关.
(3)应用:判断反应是否达到平衡状态.
对化学反应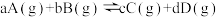 的任意状态有浓度商:
的任意状态有浓度商: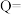
_______ .
若 ,说明反应
,说明反应_______ 进行,此时v正_______ v逆
若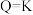 ,说明反应达到
,说明反应达到_______ , 此时v正_______ v逆
若 ,说明反应
,说明反应_______ 进行,此时v正_______ v逆
(1)表达式:对于一般的可逆反应
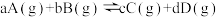 ,当在一定温度下达到化学平衡状态时,平衡常数的表达式为
,当在一定温度下达到化学平衡状态时,平衡常数的表达式为(2)意义
①K越大,说明
②K只受
(3)应用:判断反应是否达到平衡状态.
对化学反应
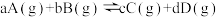 的任意状态有浓度商:
的任意状态有浓度商: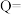
若
 ,说明反应
,说明反应若
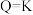 ,说明反应达到
,说明反应达到若
 ,说明反应
,说明反应
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】甲醇是一种重要的化工原料又是一种可再生能源,具有开发和应用的广阔前景。
(1)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2发生反应,CO(g)+2H2(g) CH3OH(g),CO的平衡转化率与温度,压强的关系如图1所示。
CH3OH(g),CO的平衡转化率与温度,压强的关系如图1所示。
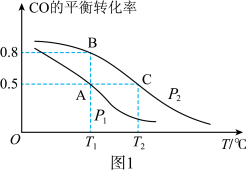
由图可判断△H____ 0,A、B两点对应的平衡常数关系是KA____ KB(填“>、<、=”)。
(2)某温度下,充分反应后,达到平衡时测得c(CO)=0.02mol/L,则此温度下的平衡常数K=____ 。
(3)我国在甲醇燃料电池技术方面获得新突破,组装出自呼吸电池及主动式电池。其工作原理如图2所示。该电池工作时,c口通入的物质为___  (填化学式)
(填化学式) ;电池负极的电极反应式为
;电池负极的电极反应式为____ 。
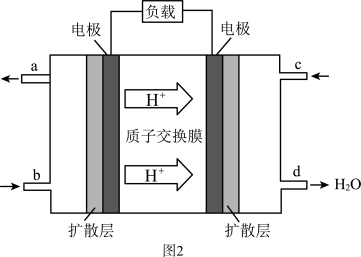
(1)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2发生反应,CO(g)+2H2(g)
 CH3OH(g),CO的平衡转化率与温度,压强的关系如图1所示。
CH3OH(g),CO的平衡转化率与温度,压强的关系如图1所示。
由图可判断△H
(2)某温度下,充分反应后,达到平衡时测得c(CO)=0.02mol/L,则此温度下的平衡常数K=
(3)我国在甲醇燃料电池技术方面获得新突破,组装出自呼吸电池及主动式电池。其工作原理如图2所示。该电池工作时,c口通入的物质为
 (填化学式)
(填化学式) ;电池负极的电极反应式为
;电池负极的电极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】CO可用于合成甲醇,化学方程式为:CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。
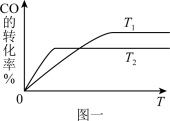
(1)该反应在不同温度下CO的转化率随时间变化如图一所示,则该反应的焓变ΔH___________ 0(填“>”、“<”或“=”)。
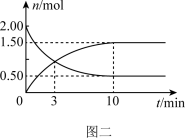
(2)某温度下,在体积为2L的密闭容器中,充入2molCO和4molH2,经测得CO和CH3OH(g)的物质的量随时间的变化如图二所示。则0~10min内v(CH3OH)=___________ ,增加CO平衡转化率的方法有___________ (任写一条)。
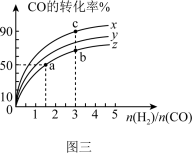
(3)为研究在230℃、250℃和270℃三种温度下合成甲醇的规律,在容积为1L的恒容容器中,测得三种温度下H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系如图三所示,则曲线z对应的温度是___________ ℃;该温度下,对应b点的化学平衡常数为___________ 。
 CH3OH(g)。
CH3OH(g)。(1)该反应在不同温度下CO的转化率随时间变化如图一所示,则该反应的焓变ΔH

(2)某温度下,在体积为2L的密闭容器中,充入2molCO和4molH2,经测得CO和CH3OH(g)的物质的量随时间的变化如图二所示。则0~10min内v(CH3OH)=

(3)为研究在230℃、250℃和270℃三种温度下合成甲醇的规律,在容积为1L的恒容容器中,测得三种温度下H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系如图三所示,则曲线z对应的温度是

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】高炉炼铁中发生的基本反应之一如下:FeO(s)+CO(g) Fe(s)+CO2(g) △H>0,其平衡常数表达式为K=
Fe(s)+CO2(g) △H>0,其平衡常数表达式为K=__ ,又知1100℃时,K=0.28。
(1)温度升高,化学平衡移动后达到新的平衡,平衡常数__ (填“变大”、“变小”或“不变”)。
(2)1100℃时测得高炉中c(CO2)=0.013mol/L,c(CO)=0.05mol/L,在这种情况下,该反应是否处于化学平衡状态:__ (填“是”或“否”),此时,化学反应速率是v正__ v逆(填“大于”、“小于”或“等于”),其原因__ 。
 Fe(s)+CO2(g) △H>0,其平衡常数表达式为K=
Fe(s)+CO2(g) △H>0,其平衡常数表达式为K=(1)温度升高,化学平衡移动后达到新的平衡,平衡常数
(2)1100℃时测得高炉中c(CO2)=0.013mol/L,c(CO)=0.05mol/L,在这种情况下,该反应是否处于化学平衡状态:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:
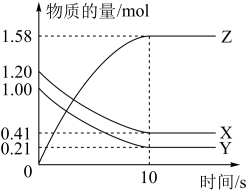
(1)反应的化学方程式为:___________ 。
(2)反应开始到10s,用Z表示的反应速率为___________ 。
(3)反应开始到10s,X的转化率为___________ 。
(4)下列条件的改变能减缓上述反应的反应速率的是___________
A.降低温度
B.补加一定量的X
C.保持压强不变,充入He使容器的体积增大
D.保持体积不变,充入He使容器的压强增大

(1)反应的化学方程式为:
(2)反应开始到10s,用Z表示的反应速率为
(3)反应开始到10s,X的转化率为
(4)下列条件的改变能减缓上述反应的反应速率的是
A.降低温度
B.补加一定量的X
C.保持压强不变,充入He使容器的体积增大
D.保持体积不变,充入He使容器的压强增大
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】(1)在2L的密闭容器中放入4molN2O5,发生如下反应:2N2O5(g) 4NO2(g)+O2(g)。反应至5min时,测得N2O5转化了20%,则v(NO2)为
4NO2(g)+O2(g)。反应至5min时,测得N2O5转化了20%,则v(NO2)为___ ,c(N2O5)为___ ,O2的物质的量浓度为___ 。
(2)某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示。根据图中数据填空:
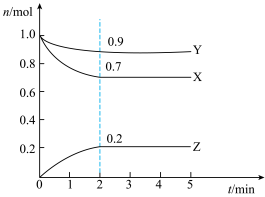
①该反应的化学方程式为___ 。
②反应至平衡时,v(X)为___ ,c(Z)为___ 。
③若X、Y、Z均为气体,则达平衡时,容器内混合气体的平均相对分子质量比起始投料时___ (填“增大”“减小”或“相等”)。
 4NO2(g)+O2(g)。反应至5min时,测得N2O5转化了20%,则v(NO2)为
4NO2(g)+O2(g)。反应至5min时,测得N2O5转化了20%,则v(NO2)为(2)某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示。根据图中数据填空:

①该反应的化学方程式为
②反应至平衡时,v(X)为
③若X、Y、Z均为气体,则达平衡时,容器内混合气体的平均相对分子质量比起始投料时
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】在体积为2L的恒容密闭容器内,充入一定量的NO和O2,800°C时发生反应2NO(g)+O2(g) 2NO2(g),容器中n(NO)随时间的变化如表所示:
2NO2(g),容器中n(NO)随时间的变化如表所示:
(1)反应在1~2s内,O2的物质的量减少__ mol。该反应在第3s___ (填“达到”或“未达到”)平衡状态。
(2)如图所示,表示NO2浓度变化曲线的是___ (填字母)。用O2表示0~2s内该反应的平均速率v=___ mol·L-1·s-1。
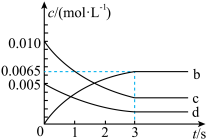
(3)能说明该反应已达到平衡状态的是___ (填字母)。
a.容器内气体颜色不再变化
b.O2的物质的量保持不变
c.容器内混合气体的密度保持不变
 2NO2(g),容器中n(NO)随时间的变化如表所示:
2NO2(g),容器中n(NO)随时间的变化如表所示:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)如图所示,表示NO2浓度变化曲线的是

(3)能说明该反应已达到平衡状态的是
a.容器内气体颜色不再变化
b.O2的物质的量保持不变
c.容器内混合气体的密度保持不变
您最近一年使用:0次

 S2(g),在恒温密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为cmol/L,测定H2S的转化率,H2S的平衡转化率与温度关系如图所示。据图可知:温度升高平衡常数K
S2(g),在恒温密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为cmol/L,测定H2S的转化率,H2S的平衡转化率与温度关系如图所示。据图可知:温度升高平衡常数K


